Stachys Sieboldii MIQ의 성분인 Acteoside는 유망한 항신염제일 수 있습니다: 쥐의 초승달형 항-GBM 신염에 대한 Acteoside의 효과
Mar 08, 2022
자세한 내용은:ali.ma@wecistanche.com
하야시 카즈미, 나가마츠 타다시, 이토 미키오, 핫토리 토모히사, 스즈키 요시오
일본 나고야 텐파쿠구 야고토야마 150 메이조대학 약학부 약리학과
요약
의 효과악티오사이드(ACT) 초승달형 anti-GBM에 대한신장증쥐에서 조사되었습니다. 쥐를 치료했을 때악티오사이드항-GBM 혈청을 정맥내 주사한 후 1일째부터,악티오사이드단백질이 소변으로 배설되는 것을 억제합니다. 에서악티오사이드- 처리된 쥐, 콜레스테롤 및 크레아티닌 함량 및 혈장 내 토끼 r-글로불린에 대한 항체 생산은 신염 대조군 쥐보다 낮았습니다. 조직학적 관찰은 이 약제가 과세포성 및 초승달 형성의 발생, 보우만낭에 대한 모세혈관벽의 유착 및 사구체의 섬유소성 괴사를 억제한다는 것을 보여주었다. 더욱이, GBM에 대한 rat-IgG 및 C3 침착은악티오사이드대조 신염 그룹보다 처리 그룹. 질병이 발병한 항-GBM 혈청을 정맥 주사한 후 20일째부터 치료를 시작한 경우,악티오사이드에 비슷한 영향을 미쳤다.신염위에서 언급한 쥐. 이러한 결과는 Acteoside가 확산 초승달 모양의 심각한 사구체 병변을 특징으로 하는 빠르게 진행하는 사구체신염에 대한 유용한 약이 될 수 있음을 시사합니다.
키워드: 초승달형 anti-GBM신장증,악티오사이드, 쥐-IgG, 쥐-C3

Click to Cistanche는 Acteoside와 함께 사용합니다.
Chyorogi Stachys sieboldii MIQ(Labiatae)는 많은 질병에 처방되며 이 괴경은 중국, 러시아, 일본에서 음식으로 사용됩니다. 최근 조사에 따르면 카이로기는 항산소증 작용(1), 히알루로니다제 활성 억제 작용(2), 면역억제 작용(3)이 있는 것으로 나타났습니다.
한편, 면역반응이 신염의 발병에 관여한다고 언급되어 왔다. 더 구체적으로 말하면 사구체 손상은 사구체의 면역 복합체 침착에 의해 매개되고, 그 다음 보체 활성화 및 다른 염증 매개체의 방출을 포함한 면역 염증 반응이 뒤따릅니다. 최근 연구에서 사구체신염의 발병에서 세포 매개 면역 반응의 기여에 많은 관심을 기울였습니다(4, 5). 또한 Neild et al. (6)은 사이클로스포린 A(CyA)에 의한 T 세포 기능의 억제가 급성 신염에서 사구체 병변의 후속 발달을 차단한다고 보고했습니다. 우리는 mizoribine(7), azathioprine(7), CyA(8), methylprednisolone(9) 및 일부 식물 성분(10)이 항-GBM 신염에 대한 유익한 효과를 나타내는 면역 억제 작용이 있다고 보고했습니다. 이러한 면역억제제는 항신증 작용을 하지만 부작용으로 인해 임상에서 사용하기 어렵다(11). 따라서 임상 단계의 신염 치료를 위한 새로운 면역억제제의 개발이 기대된다.
를 밝히는 것이 본 연구의 목적이었다.Acteoside의 항신염 효과, 쥐의 초승달형 항-GBM 신염에 대한 chyorogi의 성분.

재료 및 방법
동물
수컷 Sprague-Dawley 계통 쥐, 무게 약. 160g(Nihon SLC, Hamamatsu)을 모든 실험에 사용했습니다. 이 동물들은 실험 기간 동안 23 ± 1 C의 에어컨이 설치된 방에 수용되었습니다.
약제
액테오사이드(ACT)(Tsumura Co., Ltd., Tokyo)의 화학 구조는 Fig. 1에 나타내었다. 이 성분은 chyorogi(Stachys sieboldii MIQ)의 기단부에서 추출하였다. ACT의 순도는 HPLC(컬럼: TSK gel ODS{1}}TM(4.{3}} id x 25{9}} mm)로 확인했습니다. 이동상: 20% CH3CN/H2O, 10 AcOH, 유속: 0.7 ml/min, 온도: 실온, 검출기: UV 254 nm) (주) Tsumura Co., Ltd. 이 실험에 사용된 ACT는 9970 이상의 순도를 가졌습니다. ACT는 증류수에 용해되었습니다. Dipyridamole (Dip) (Boehringer Ingelheim, Germany) 및 azathioprine (Aza) (Sigma, St. Louis, MO, USA)도 사용되었습니다. 이 약물은 1070 아라비아 고무에 현탁되었습니다.

초승달형 항GBM 신염 유도
Crescentic-type anti-GBM 신염은 이전에 보고된 방법( 12). 이 실험에서 쥐의 무게는 약. 꼬리 정맥에 항-GBM 혈청 0.6ml/동물을 16{8}}g 투여했습니다.

항GBM 혈청 주사 후 1일째(이종기) 또는 항GBM 혈청 주사 후 20일째(자가기)부터 시험약을 투여하여 시험약의 효과를 추정하였다. 실험에서 24-시간 소변 샘플을 수집한 다음, 쥐를 8마리씩 5~6개 그룹으로 나누어 각 그룹의 24-시간 소변의 평균 단백질 함량이 비슷한 수준.
시험약의 항신염 효과 평가
이종 단계의 약물 치료 실험에서 4개 그룹에는 100g당 1ml의 부피로 각각 3, 10 또는 30mg/kg/day의 ACT 또는 100mg/kg/day의 Dip을 경구 투여했습니다. 항-GBM 혈청을 정맥 주사한 후 1일째 또는 다음 날부터 40일째까지 매일 체중. 자가 단계의 약물 치료 실험에서 3개 또는 4개 그룹에 3, 10 또는 30mg/kg ACT(A) 또는 30mg/kg/day ACT, 100mg/kg/day 경구 투여했습니다. 항GBM 혈청 정맥주사 후 20일째부터 40일(A) 또는 45일까지 Aza(B)를 각각 체중 100g당 1ml의 부피로 1일 50mg/kg/day 담그십시오. (나) 날. 나머지 군은 시험약 대신 비히클(증류수)을 경구 투여하고 신염 대조군으로 삼았다. 또한, 신염군과의 비교를 위해 무처리(정상)군을 사용하였다.
소변 및 혈액 수집
{0}}시간 소변 샘플은 각 동물을 개별 대사 우리에 24시간 동안 보관하여 얻었습니다. 소변 수집이 시작될 때 각 동물은 먹이를 주지 않고 8ml의 증류수를 경구로 받았습니다. 그런 다음 소변을 41C에서 15분 동안 3,{4}} rpm으로 원심분리하고 상청액을 단백질 측정에 사용했습니다. 실험 마지막 날, 마취된 쥐의 신정맥에서 2.{9}} ml의 혈액을 일회용 주사기로 채취하여 헤파린 0.125 ml가 들어 있는 튜브에 넣었습니다. 혈액을 5,{12}} rpm에서 원심분리하여 일부 매개변수를 결정하기 위한 혈장을 얻었습니다.

요단백 및 혈장 콜레스테롤 및 크레아티닌 함량 측정
요단백 배설은 Kingsbury et al. (13) mg/24hr 소변으로 표시됩니다. 콜레스테롤 함량은 상용 분석 키트(Determine TC-5; Kyouwa Medix Co., Ltd, Tokyo)(14)를 사용하여 측정하고 mg/dl 혈장으로 표시했습니다. 크레아티닌 함량은 크레아티닌 측정 키트(CRE-EN; Kainos, Inc., Tokyo)를 사용하여 측정하고 mg/dl 혈장/100g 체중으로 표시하였다.
-G에 대한 혈장 항체 역가 측정
rG에 대한 혈장 항체 역가는 감작된 양 적혈구를 사용한 간접 혈구응집에 의해 결정되었습니다(15).
혈장 보체 CH50 수준 측정
혈장 보체 CH50 수준은 Mayer(16)의 방법에 의해 결정되었습니다.
조직병리학적 매개변수의 평가
광학 현미경 연구를 위해 펜토바르비탈로 마취된 쥐에서 신장을 분리한 다음 탈수하고 고정하여 조직을 낮은 수준에서 높은 수준까지 에틸 알코올의 다양한 관심 전통에 단계적으로 담그었습니다. 그런 다음 조직을 파라핀에 포매하고 2-3 em 두께 조각으로 절단했습니다. 초승달형 항GBM 신염 연구에서 절편은 hematoxylin과 eosin과 Masson's trichrome으로 염색되었다. 핵의 수(과세포성), 초승달 형성, 모세혈관벽에 대한 보우만낭의 유착(유착), 사구체의 섬유소 괴사를 광학현미경으로 관찰하였다. 이러한 매개변수를 평가하기 위해 무작위 샘플링 방법으로 적도 단면을 선택했습니다. 50개의 사구체/단면이 관찰되었고, 초승달 형성, 유착 및 섬유소성 괴사의 출현율은 이전에 기술된 바와 같이 이러한 형태학적 변화를 갖는 사구체(발생률)의 백분율로 표현되었다(17). 평가는 각 샘플의 정체를 모르는 다른 사람이 수행했습니다. 세포과다를 평가하기 위해 적도 단면을 무작위 샘플링 방법으로 선택했습니다. 핵(사구체 세포의 핵 및 삼출성 백혈구 포함)의 수를 계산하고 10개의 사구체/단면에서 사구체 단면당 평균 수로 표현하였다.

면역조직화학
rat-IgG의 면역효소 염색을 위한 조직에서 파라핀 절편을 위에서 설명한 대로 절단하고 절편을 0에서 0.1% 프로테아제로 처리했습니다.05 M Tris- 7분 동안 HCl 완충액을 사용한 다음 냉각된 0.01M 인산염 완충 식염수(PBS), pH 7.4로 세척합니다. 그런 다음 섹션을 90분 동안 1:100의 희석으로 항-쥐 IgG 마우스 단일클론 항체(mAb)(Cappel, West Clester, PA, USA)와 함께 인큐베이션했습니다. 절편을 PBS로 다시 세척하고, 메탄올 중 0.3% 과산화수소로 20분 동안 처리하여 내인성 과산화효소를 차단하고, 비오틴화 친화성 정제된 항-마우스 IgG 및 아비딘화 양고추냉이 퍼옥시다제와 3,3'-디아미노벤지딘 사염산염(DAB)과 함께 인큐베이션했습니다. (Vecta stain ABC Kit; Vector 기관, Burlingame, CA, USA). 모든 단계는 실온에서 수행되었습니다.
세포 증식의 표지자인 PCNA(proliferating cell nuclear antigen)의 면역효소 염색을 위한 조직을 PBS에 녹인 10% 포르말린에 고정하고, 파라핀이 포매된 조직을 랫트-IgG와 동일한 방법으로 염색하였다. PCNA에 대한 mAb(19A2; Coulter Immunology, Hialeah, FL, USA)의 사용.
조직 섹션에서 쥐-IgG, C3 및 PCNA의 정량화
사구체 내 면역반응성 rat-IgG 및 C3의 총 면적은 이미지 분석기(Toyobo Image Analyzer V1; Toyobo Co., Ltd., Tokyo)를 사용하여 섹션당 30개의 사구체에서 측정되었고 mm2/사구체 단면(GCS)으로 표시되었습니다. ). 이미지 분석기로 사구체 내 PCNA 양성 세포를 계수하고 그 결과를 세포수/GCS로 표시하였다.
통계 분석
데이터는 평균 ± SD를 나타내며 결과는 ANOVA에 의해 통계적으로 평가되었습니다. 이러한 결과가 모수적일 때 Duncan's test에 의해 통계적으로 평가되었습니다. 결과가 비모수적일 경우 Kruskal-Wallis 테스트에 의해 통계적으로 평가되었습니다. 억제 백분율은 다음과 같이 계산되었습니다.
억제율(백분율)=(대조군 - 시험약) x 100 / (대조군 - 정상)
결과
초승달형 항GBM 신염에 대한 Acteoside의 효과
요단백 배설(Figs. 2, 3): 항GBM 혈청 주사 다음날(이종기)부터 ACT 치료를 시작한 경우 30mg 투여 5일차에 요단백의 유의한 억제가 처음 관찰되었다. /kg, 포; 20일째에 3 및 10 mg/kg, po; 40일째 Dip 100 mg/kg, po

항GBM 혈청 주사(자가기) 후 20일째부터 ACT를 투여한 경우 10 및 30mg/day의 ACT는 30일째까지 단백질 배설이 소변으로 증가하는 것을 억제했습니다. 반면에 50 mg/kg의 Aza는 30 mg/kg의 ACT보다 약했지만 유의하지는 않았으며 Dip은 효과가 없었습니다.

혈장 콜레스테롤 및 크레아티닌 함량(표 1): 혈장 콜레스테롤 및 크레아티닌 함량은 40일 또는 45일째에 측정되었습니다. 신염 대조군 쥐의 혈장 콜레스테롤 함량은 현저하게 상승했습니다. 대조적으로, 콜레스테롤 함량의 상승은 이종기로부터의 ACT(30 mg/kg)에서 대조군 수준의 60%만큼 감소하였고 자가기로부터 ACT(30 mg/kg)로 대조군의 62'o만큼 감소하였다. 수준. 신장염 쥐의 혈장 크레아티닌 함량도 증가했습니다. 반면, 두 상 처리 쥐의 ACT(30 mg/kg)에서는 혈장 크레아티닌 함량이 정상 쥐와 유사하였다.

rG에 대한 혈장 항체 역가: 신장염 쥐는 현저하게 가속화된 항체 생산을 보였습니다. 가속된 항체 생산은 이종기(표 2)에서 ACT(10 및 30 mg/kg), 자가기에서 ACT(30 mg/kg) 및 대조군의 70%와 51%(데이터는 표시되지 않음)이며 Dip의 영향을 받지 않았습니다.

조직학적 관찰(표 3, 그림 4 및 5): 신염 사구체의 광학 현미경 검사는 심각한 초승달 형성, 유착, 섬유소형 괴사 및 간질 세포의 증식을 특징으로 하는 병변을 나타냈다. 조직학적 관찰은 ACT(이종기 및 자가기 모두에서)가 40일 또는 45일까지 사구체에서 과세포성 및 초승달 형성, 유착 및 섬유소성 괴사의 발생을 억제하는 것으로 나타났습니다. Dip과 Aza를 처리한 신염 쥐의 병변도 신염 대조군 쥐보다 적었다. 그러나, 신염 래트가 자가기로부터 Dip으로 처리되었을 때, 조직학적 변화는 Dip에 의해 거의 영향을 받지 않았다(데이터는 표시되지 않음).



사구체 세포 증식, 즉 사구체에서 PCNA 양성 세포의 증가가 다음에서 관찰되었습니다.신염 쥐. 대조적으로, 30일에는 52% 감소했습니다.세포 증식이 관찰되었으며 이는 w사구체 세포의 현저한 감소대조군과 비교하여 luularity(표 3).
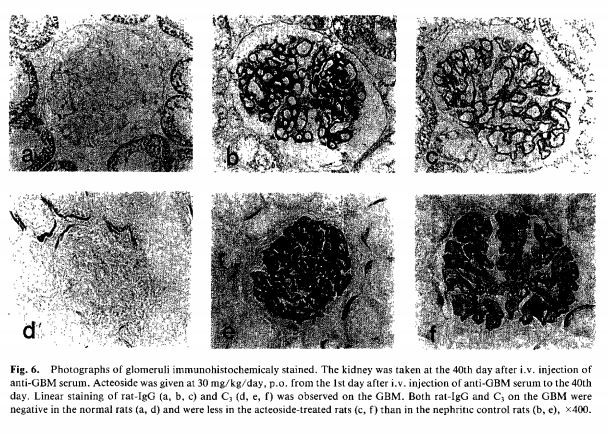
면역 반응물의 침착(표 2 및 도 6): 신염 대조군 쥐에서 GBM에 대한 쥐-IgG 및 C3 침착을 관찰할 수 있었다. 그러나 정상적인 쥐에서는 발견되지 않았습니다. 이종 단계의 ACT(30mg/kg)는 GBM에 대한 쥐-IgG 침착을 대조군 수준의 72%까지 감소시켰습니다. 또한, 이종 단계의 ACT(3, 10 및 30 mg/kg)는 40일째까지 GBM에 대한 rat-C3 침착을 60~69%까지 감소시켰습니다. 자가기로부터 ACT를 투여한 경우에도 rat-IgG 및 C3 침착 억제는 위의 결과와 유사하였다. 딥은 래트-IgG 및 C3 침착에 영향을 미치지 않았습니다. 그러나 Aza는 GBM에 대한 rat-IgG 및 C3 침착을 각각 67% 및 68% 감소시켰습니다(데이터는 표시되지 않음).
원래 유형의 항-GBM 신염에서 GBM에 대한 보체 활성 및 C3 침착물에 대한 ACT의 효과(그림 7)

원래 유형의 항-GBM 신염은 이전에 설명한 대로 0.6 ml의 항-GBM 혈청을 꼬리 정맥에 주사하여 쥐에서 유도되었습니다(18). 신염 쥐를 30 mg/kg의 ACT, po 및 코브라 독 인자(CVF)(Sigma)로 10 fig/rat, 복강내로 8시간마다 3회 전처리 및 후처리했습니다. ACT 및 CVF 치료는 약 50%의 억제 비율로 요단백 배설을 감소시켰습니다. 각각 35도 및 71%입니다. 신염 대조군 쥐의 CH50은 신염 유도 24시간 후 정상 쥐보다 현저히 낮았다. ACT는 신염 대조군 쥐에서 감소된 CH50과 GBM의 C3 침착 증가를 억제했습니다. CVF는 CH50 및 C3 증착을 폐지했습니다. 또한, 시험관 내 실험에서 ACT는 보체 활성화를 37% 억제했습니다. ACT가 정상 쥐에게 투여되었을 때, ACT는 생체 외 실험에서 보체 활성화를 감소시켰습니다(데이터는 표시되지 않음).
논의
Goodpasture 증후군에서 급속히 진행되는 사구체신염과 신장질환은 발병 후 2~3개월이 지나면 신부전으로 진행되는 악성질환이다(19). 이 신염의 특징은 세포과다, 호중구와 단핵구의 현저한 침윤, 사구체의 초승달 형성을 포함합니다. 면역억제제, 항혈소판제, 스테로이드를 이용한 칵테일 요법이 주로 이 질병에 적용되었습니다. 한편, CyA는 실험적 신염에 유익한 효과를 발휘하는 탁월한 면역억제제이지만(6, 8), CyA는 신장 기능 장애를 유발하고 사구체에서 비가역적인 조직학적 변화를 일으키는 것으로 보고되었습니다(11). Methylprednisolone은 많은 부작용을 가지고 있습니다. 또한, 이 약을 장기간 복용한 후 반동 현상과 금단 증후군이 두 가지 문제입니다. 따라서 부작용이 적은 새로운 신염 치료용 면역억제제의 개발이 필요하다.
Crescentic-type anti-GBM 신염은 Goodpasture 증후군의 급속 진행성 사구체 신염 및 신장 질환에서와 유사한 조직 및 병리학 적 변화를 나타내는 실험 모델입니다 (20). 이 신염의 발달과 진행은 면역 반응에 의해 매개되는 2단계로 구성됩니다. 소위 이종기(heterologous phase)라고 하는 초기 반응은 항-GBM 항체의 침착에 따른 다형핵 과립구의 보체 의존적 축적에 기인한다(21, 22). 후기 단계(자가기)는 GBM을 따라 침착된 자가 항체의 결합 및 이 반응 후 사구체에 대한 단핵구/대식세포의 유입에 의해 발생합니다(22, 23). 이 신염은 초승달 형성과 섬유소성 괴사를 수반하는 이상성 요단백 및 세포과다를 특징으로 합니다. 초승달 형성은 이동된 대식세포와 증식된 상피 세포에 의해 매개되는 것으로 생각됩니다(22, 24).
우리는 이전에 면역억제제인 mizoribine과 Aza(7)가 Poria cocos(18)의 주성분인 토끼 IgG와 Pachyman에 대한 혈장 항체의 상승을 억제하고 GBM의 C3 침착 정도를 감소시켰으며 둘 다 항GBM 신염에 현저하게 효과적입니다.
ACT 치료는 단백뇨 및 혈장 콜레스테롤 감소, 신장 기능 손상 예방 및 사구체 초승달 및 세포과다증의 발달을 포함한 진행성 조직학적 변화의 예방에 의해 평가된 바와 같이 항-GBM 사구체신염의 발병을 억제했습니다. 40일째에, 30 mg/kg의 ACT 단독은 이 신염 모델에서 항체 생성 억제에 의해 매개된 GBM에 대한 쥐-IgG 침착의 양을 유의하게 감소시켰다. 반면, GBM에 대한 C3 침전물의 양은 3, 10 또는 30 mg/kg에서 ACT에 의해 감소되었습니다. 또한, ACT는 시험관 내 및 생체 외 실험 모두에서 보체 활성화를 유의하게 억제했습니다. 신염 대조군 쥐에서 CH50의 감소는 ACT에 의해 억제되었습니다. 위의 데이터는 보체 활성화를 억제함으로써 ACT가 신장 손상을 억제한다는 것을 시사합니다. 왜냐하면 보체막 공격 복합체(complement membrane attack complex, MAC)가 사구체 손상의 발병기전에 관여하고(25), 승화성 MAC은 사구체 손상과 관련될 수 있는 잠재적인 염증 매개체를 가지고 있기 때문입니다. 활성 산소 종(26), 프로테아제(27), 프로스타글란딘(28) 및 인터루킨(29)과 같은 인터루킨(29) 및 콜라겐(30)과 같은 간질 세포 증식 및 세포외 기질 확산.
보체 활성화는 백혈구 침윤과 밀접한 관련이 있다고 믿어집니다. 최근 연구에서 C5a가 각각 단핵구 및 호중구 부착을 유발하는 것으로 보고되었습니다(31, 32). 따라서 추가 연구에서 우리는 사구체의 백혈구 축적에 대한 ACT의 영향을 조사할 것입니다.
참조
1 Yamahara J, Kitani T, Kobayashi H 및 Kawahara Y: Stachys sieboldii MIQ에 대한 연구. II 무산소 작용 및 활성 성분. Yakugaku Zasshi 110, 932-935 (1990) (Abstrin English)
2 Takeda Y, Fujita T, Satoh T 및 Kakegawa H: Stachys sieboldii MIQ의 글리코시드 성분에 대해. 및 히알루로니다제 활성에 대한 이들의 효과. Yakugaku Zasshi 105, 955-959 (1985) (영어로 Abstr)
3 Sasaki H, Nishimura H 및 Morita T: Rehmannia gluttons의 면역억제 원리 var. 휴이칭겐시스. Planta Med 55, 458-462 (1989)
4 Saito T 및 Atkins RC: 실험적 국소 사구체 경화증의 진행에 대한 단핵 백혈구의 기여. 신장 Int 37, 1076-1083 (1990)
5 Tipping PG, Neale TJ 및 Holdsworth SR: 항체 유도 실험적 사구체신염에 T 림프구 참여. 신장 Int 27, 530-537 (1985)
6 Neild GH, Ivory K 및 Williams DG: Cyclosporin A는 토끼의 sactus 혈청병을 억제합니다. Clin Exp Immunol 52, 586-594 (1983)
7 Okamoto K, Ito M 및 Suzuki Y: 새로운 면역억제제인 mizoribine(p-INN, Bredinin®) 및 azathioprine에 대한 항염 효과에 관한 연구(2): 쥐의 초승달형 항-GBM 신염에 미치는 영향. Jpn J Pharmacol 34, 33-41 (1984)
8 Nagamatsu T, Kojima N, Kondo N, Hattori T, Kojima R, Ito M 및 Suzuki Y: 쥐에서 항 GBM 신염의 사이클로스포린 A에 의한 억제. Jpn J Pharmacol 58, 27-36 (1992)
9 Taniguchi H, Nagamatsu T, Kojima R, Ito M 및 Suzuki Y: 쥐에게 간헐적 투여에 의한 methylprednisolone sultanate의 현저한 항신증 작용과 부작용 감소. Jpn J Pharmacol 64, 79-88 (1994)
10 Hattori T, Furuta K, Hayashi K, Nagamatsu T, Ito N 및 Suzuki Y: 식물 성분의 항염 효과에 관한 연구(6): 초승달에 대한 항신염 효과 및 펠로겐 drine(OB{2}}) 기작 쥐의 항-GBM 신염 유형(2). Jpn J Pharmacol 60, 187-195 (1992)
11 Mason J: Sandimmune이 신장에 미치는 영향. Clin Res Bull 6, 47-51 (1989)
12 Ito M, Yamada H, Okamoto Y 및 Suzuki Y: 쥐의 항사구체 기저막(GBM) 혈청에 의해 유도된 초승달형 신염. Jpn J Pharmacol 33, 1145-1154 (1983)
13 Kingsbury FB, Clark CP, Williams G 및 Post AL: 소변 내 알부민의 신속한 측정. J Lab Clin Med 11, 981-989 (1926)
14 Zurkowski P: 단일 시약으로 콜레스테롤 측정을 위한 신속한 방법. Clin Chem 10, 451-453 (1964)
15 Mcleish KR, Clark CP, Williams G 및 Post AL: 뮤린 면역 복합 사구체신염 예방을 위한 기전으로서 프로스타글란딘 E에 의한 항체 합성 억제. Lab Invest 47, 147-152 (1982)
16 Mayer MM: 보완 및 보완 고정. In Experimental Immunochemistry, pp 133-240, Charles C. Thomas, Springfield(1961)
17 Hattori T, Ito M, Nagamatsu T 및 Suzuki Y: 일본의 새로운 한약인 TJ{1}}의 항신염 효과에 관한 연구(3): 쥐의 초승달형 항GBM 신염에 대한 효과. Jpn J Pharmacol 52, 131-140 (1990)
18 Hattori T, Hayashi K, Nagao T, Furuta K, Ito M, 및 Suzuki Y: 식물 성분의 항염 효과에 관한 연구 (3): Poria cocos Wolf의 주성분인 pachyman이 원산지 nal-type anti-GBM에 미치는 영향 쥐의 신염과 그 기전. JpnJ Pharmacol 59, 89-96 (1992)
19 Shibata S, Miyakawa Y, Naruse T, Nagasawa T 및 Takuma T: 신독성 항체를 유도하는 당단백질: 쥐 사구체 기저막에서 분리 및 정제. J Immunol 102, 593 601 (1969)
20 포크 RJ: ANCA 관련 신장 질환. Kidney Int 38, 998-1010 (1990) 21 Mulligan MS, Johnson KJ, Todd RF III, Issekutz TB, Miyasaka M, Tamatani T, Smith CW, Anderson DC 및 Ward PA: 신독성 신염에서 백혈구 부착 분자에 대한 요구 사항. J Clin Invest 91, 577-587 (1993)
22 Nahas AME: 성장 인자 및 사구체 경화증. 신장 Int 41, Supp 36, S15-S20(1992)
23 Boyce NW, Holdsworth SR, Dijkstra CD 및 Atkins RC: 특정 단클론 항체를 사용한 쥐의 실험적 사구체신염에서 사구체 내 단핵 식세포의 정량화. 병리학 19, 290-293 (1987)
24 Becker GJ, Hancock WW, Stow JL, Glasgow EF, Atkins RC 및 Thomson NM: 실험적 만성 면역 복합 사구체 신염에서 대식세포의 관련. Nephron 32, 227-233 (1982) 25 Perkinson DT, Baker PT, Couuser WG, Johnson BJ 및 Adler S: 실험적 사구체 손상에서 막 공격 복합 침착. Am J Pathol 120, 121-128 (1985)
26 Alder S, Baker PJ, Johnson RJ, Ochi RF, Pritzl P 및 Couuser WG: 보체막 공격 복합체는 배양된 쥐의 혈관간 세포에 의한 반응성 산소 대사 산물의 생산을 자극합니다. J Clin Invest 77, 762-767 (1986)
27 Johnson RJ, Couuser WG 및 Alpers CE: 인간 호중구 필리스틴 프로테아제, 에스테라제 및 카텝신 G는 생체 내 사구체 손상을 중재할 수 있습니다. J 특급 Med 168, 1169-1174 (1988)
28 Cybusky AV, Lieberthal W, Quigg RJ, Rennke HG 및 Salant DJ: 보체 매개 사구체 손상에서 트롬복산의 역할. Am J Pathol 128, 45-51 (1987)
29 Lovett D, Hansch G, Resch K 및 Gemsa D: 말단 보체 성분에 의한 사구체 간질 세포의 활성화. 프로스타노이드 및 인터루킨-l 유사 인자 방출의 자극. 면역생물학 168, 34-35 (1986)
30 Torbohm I, Schonermark M, Wingen AM, Berger B, Rother K 및 Hansch GM: C5b_8 및 C5b_9는 인간 사구체 상피 세포의 콜라겐 방출을 조절합니다. 신장 Int 37, 1098-1104 (1990)
31 Lo SK, Detmers PA, Levin SM 및 Wrigh SD: 호중구가 내피에 일시적으로 부착됩니다. J Exp Med 169, 1779 -1793 (1989) 32 Brady HR, Denton MD, Jimenez W, Takata S, Palliser D 및 Brenner BM: 화학 유인 물질은 인간 메산지움 세포에 대한 단핵구 부착 및 메산지움 세포 손상을 유발합니다. 신장 Int 42, 480-487 (1992)






