장내 미생물총과 숙주 면역 사이의 혼선: 염증 및 면역요법에 미치는 영향(2)
Oct 24, 2023
7.2. 위장 감염
상황에 따라 장내 미생물군은 숙주를 보호하거나 외인성 병원체로부터 감염 위험을 증가시킬 수 있습니다. 보호력으로서의 미생물군집의 역할은 신생아의 미성숙 미생물군집이 병원균의 침입에 더 취약하다는 연구 결과에 의해 뒷받침됩니다[222]. 공생동물이 병원체에 의한 군집화를 방지하고 감염으로부터 보호할 수 있는 여러 가지 메커니즘이 있습니다. 여기에는 자원 경쟁, 박테리오파지 방출, 항균 대사산물 생산이 포함됩니다[237-241]. 대조적으로, 장출혈성 대장균에서 볼 수 있듯이 4-메틸 벤조산, 3,4-디메틸벤조산, 헥산산 및 헵타노산과 같은 미생물군집 대사산물은 결장 상피 손상을 증가시키는 것으로 나타났습니다. 오르간 온 칩(organ-on-a-chip) 모델에서 [223]. 더욱이, 공생 Escherichia albertii에서 채취한 상청액은 설사 유발성 대장균 종의 병독성을 증가시켜 TLR{10}}매개 IL의 증가-8를 일으키고 숙주 장 세포에 의한 염증 유발 반응을 전반적으로 증가시킬 수 있습니다. [242]. 특정 공생균의 존재와 미생물 구성의 변화는 Clostridium difficile, Salmonella typhimurium, Escherichia coli, 반코마이신 내성 Enterococcus spp. 및 Citrobacter Rodentium과 같은 유기체에 의한 감염 감수성과 관련이 있습니다. 가장 좋은 예 중 하나는 선천성 면역 세포가 염증복합체와 TLR4, TLR5 및 뉴클레오티드 결합 올리고머화 도메인 함유 단백질 1(NOD1) 신호 전달 경로를 통해 C. difficile 독소에 의해 자극되는 CDI를 포함합니다[246,247]. 수많은 전염증성 사이토카인(예: 인터류킨(IL)-12, IL-1, IL-18, 인터페론 감마(IFN- ) 및 종양 괴사 인자(TNF )) 및 케모카인 (MIP-1a, MIP-2 및 IL-8)이 이후에 생성되어 점막 투과성 증가, 비만 세포 탈과립, 상피 세포 사멸 및 호중구 침윤이 증가합니다[248] . 중요한 것은 CDI는 일반적으로 장내 미생물총의 항생제 매개 파괴의 결과입니다[249]. 특정 항생제, 특히 클린다마이신에 의해 장내 유익균이 박멸되면 C. difficile이 번성하여[250] 대장염과 그에 따른 설사가 발생합니다[251,252]. 장내 미생물총 불균형 외에도 Th{45}} 및 IL-17-발현 세포와 같은 면역 세포 집단은 재발성 CDI를 촉진할 수 있습니다[253]. 이에 비해 IL{48}}활성화된 ILC는 CDI를 예방할 수 있습니다[254]. 장내 미생물군 고갈은 CDI의 주요 원인이므로 미생물을 복원하는 개입은 치료 가치가 있을 수 있습니다. 식이섬유 및 그 발효 부산물, 즉 SCFA와 같은 프리바이오틱스는 CDI의 가능한 치료법입니다. 예를 들어, 펙틴과 같은 식이섬유는 장내 미생물군 유생(Lachnospiraceae 증가 및 Enterobacteriaceae 감소로 나타남)을 회복하고 C. difficile 유발 대장염 후 염증을 완화할 수 있었습니다[255]. 부티레이트 생성 박테리아인 Clostridium butyricum은 감염 초기 단계에서 호중구, Th1 및 Th17 세포를 증가시켜 CDI로부터 보호하는 것으로 유사하게 발견되었습니다. 이는 GPR43 및 GPR109a 신호전달과 무관했습니다[256]. 6.2절에서 언급한 바와 같이 CDI는 FMT로 효과적으로 치료될 수 있다[152]. FMT는 인간 대변에서 분리된 33개의 박테리아 균주로 구성된 미생물 생태계 치료제가 항생제 내성 C. difficile 대장염을 치료할 수 있음을 보여준 이전 연구에서 추가로 뒷받침됩니다[257]. 특히 Salmonella typhimurium 감염에 Microbial Ecosystem Therapeutic을 적용한 경우에도 유사한 관찰이 나타났습니다[258]. 이러한 발견은 장내 미생물총과 면역 반응의 적절한 조절이 감염을 예방하고 퇴치하는 데 필수적이라는 점을 강조합니다.

변비 치료 효과
7.3. 염증성 장 질환
염증성 장질환(IBD)은 환경, 장내 미생물, 면역체계, 유전적 요인 등 다양한 요인의 결함으로 인해 발생합니다. IBD는 GIT의 만성 염증과 관련이 있습니다. 크론병(CD)과 궤양성 대장염(UC)은 조직병리학적 특징, GIT의 질병 위치 및 증상에 따라 IBD의 두 가지 별개의 임상 조건입니다[259]. IBD에서는 점액 용해성 박테리아와 병원성 박테리아가 점막 장벽을 저하시키고 심부 장 조직으로 병원균의 침입을 증가시킵니다 [224,260-262]. 장내 미생물총 구성의 변화는 IBD의 발달 및 진행과 밀접한 관련이 있습니다. IBD 환자는 Firmicutes의 개체수가 감소하고 Proteobacteria, Bacteroidetes, Enterobacteriaceae 및 Bilophila의 확장을 보여줍니다 [263-265]. 또한, IBD 환자 및 대장염 마우스 모델에서 볼 수 있듯이 많은 전염증성 박테리아 종은 IgA로 코팅되어 있습니다[266,267]. 무균 마우스가 대장염으로부터 보호된다는 증거를 토대로 장내 미생물은 IBD 발달에 직접적인 역할을 하는 것으로 보입니다[268]. 이는 IBD 마우스의 장내 미생물을 무균 마우스에 이식하면 후자 그룹에서 IBD가 발생한다는 발견에 의해 강화됩니다[268]. 마찬가지로, IBD가 있는 어미는 본질적으로 'IBD 미생물군'을 자손에게 전달할 수 있으며, 이로 인해 새끼의 미생물 다양성이 감소하고 결장에서 클래스 전환 기억 B 세포 및 Treg 세포가 더 적습니다[269]. 미생물총과 IBD 사이의 강력한 연관성은 진단 및 치료 목표를 더 잘 식별하는 데 도움이 되는 메타게놈 접근법을 발전시켰습니다[270]. FMT는 잠재적인 치료법으로 제안되었으며, 여기서 치료받은 UC 환자는 더 적은 ROR t + Th17 세포 및 더 많은 Foxp3+ CD4+ Treg 세포와 일치하는 Faecalibatium의 풍부함이 증가한 것으로 나타났습니다[166]. SCFA의 투여는 또한 IBD 환자에 대한 잠재적인 치료법으로 생각됩니다[271]. 뒷받침하는 증거에는 전 염증성 호중구 반응, 즉 대장염 생쥐의 NET에 대한 부티레이트 매개 억제가 포함됩니다 [272]. SCFA의 전구체인 식이섬유가 IBD 환자에게 유익한 중재가 될 수 있는지 여부에 대해서는 상충되는 보고가 있습니다. 한편으로는 특정 다중 섬유 혼합물이 IL{26}} 및 Treg 세포를 증가시켜 장 염증을 중화시키는 것으로 밝혀졌습니다[273]. 반대로, 우리의 연구 결과는 대장염 생쥐에 대한 프리바이오틱 섬유 반응의 이분법을 나타냅니다. 여기서 펙틴은 이눌린과 비교하여 염증을 완화할 수 있으며, 이는 질병 병리를 악화시킵니다[274]. 더욱이, 우리의 연구는 부티레이트가 NLRP3 염증 신호를 증가시켜 해로운 미생물 대사산물이 될 수 있음을 시사했습니다[274]. 이에 비해 프로바이오틱 칵테일은 장내 미생물을 Akkermansia 및 Bifidobacterium을 포함하는 항염증 프로필로 전환하여 염증을 완화했습니다. 이러한 발견은 IBD의 프리바이오틱 섬유질과 SCFA를 임상에 적용하기 전에 이해하기 위해서는 더 많은 조사가 필요하다는 것을 종합적으로 나타냅니다. SCFA 외에도 2차 담즙산이 IBD와 관련되어 있습니다. DCA는 장 염증을 유발하는 것으로 잘 알려져 있습니다[276,277]. 이는 부분적으로 담즙산에 의한 Paneth 세포 기능의 억제 때문일 수 있습니다. 그러나 DCA를 포함한 담낭 절제술과 관련된 2차 담즙산은 단핵구/대식세포 동원을 억제하여 생쥐의 대장염을 개선했습니다[279]. 더욱이, UDCA는 Clostridium 클러스터 XIVa의 손실을 방지하고 A. muciniphila의 풍부함을 증가시켜 대장염 중증도를 낮출 수도 있습니다[280]. 담즙산의 다양한 효과는 화학 구조 및 잠재적인 결합 부분과 관련될 수 있습니다. 예를 들어, 황산화 2차 담즙산은 IBD 환자에서 볼 수 있듯이 비포합 담즙산에 비해 더 많은 염증 유발 효과를 나타낼 수 있습니다. 확실히, IBD 환자의 담즙산 프로필을 이해하고 각 유형의 담즙산의 염증 유발 효과 또는 항염증 효과를 결정하려면 더 많은 대사체 프로파일링이 필요합니다. 일반적으로 SCFA와 2차 담즙산은 모두 장에서 항염증 효과가 있는 것으로 보입니다(그림 1A, B). 최근 몇 년간 IBD 위험을 증가시키는 여러 감수성 유전자가 확인되었습니다. 현재 연구는 유전적 소인, 세균 불균형, 항생제와 같은 환경적 요인이 IBD에 함께 작용한다는 생각에 초점을 맞추고 있습니다. 뉴클레오티드 결합 올리고머화 도메인 함유 단백질 2(NOD2, 면역학적 세포내 인식 단백질)는 박테리아 세포벽의 필수 구성 요소인 세포내 무라밀 디펩티드(MDP)를 식별합니다[282]. NOD2 기능의 상실은 NF-κB의 TLR{54}} 매개 활성화 억제를 손상시켜 Th1 반응이 과도하게 활성화되고 미생물에 대한 면역학적 내성이 약화됩니다[282]. 더욱이, 자가포식 관련 16-1(ATG16L1), 카스파제 모집 도메인 함유 단백질 9(Card9) 및 C형 렉틴 도메인 패밀리 7 구성원 A(CLEC7A)를 포함하여 IBD에 대한 감수성을 증가시키는 여러 다른 유전자 , T 세포 반응 조절 장애 및 장내 미생물 불균형을 생성하여 IBD에도 기여합니다 [283-285]. 향후 연구에서는 IBD 환자의 미생물 대사산물 생산과 관련된 유전자에 단일 염기 다형성이 있는지 여부를 조사해야 합니다.

시스탄체 튜불로사의 장점-면역체계 강화
7.4. 대장암종(CRC)
점점 더 많은 문헌이 암의 발달과 진행에서 미생물군의 역할을 제시하고 있습니다. 면역 체계가 부적응적으로 발달하는 시나리오에서는 장내 미생물총 불균형이 위험이 높아지고 특정 미생물의 확장으로 인해 돌연변이 유발 독소가 생성될 수 있습니다[286]. 이러한 유전독소에는 Bacteroides fragilis 독소(Bft), 세포치사 팽창 독소(CDT) 및 colibactin이 포함됩니다. 그러나 이는 장내 미생물의 전체 범위에서 발암 가능성을 확인하고 이해하기 위해 더 많은 연구가 필요한 소수의 박테리아 관련 독소만을 강조합니다[225]. 선종성 폴립과 톱니 모양 폴립은 종종 대장암(CRC)으로 진행되는 두 가지 전암성 병변입니다. 선종 환자의 경우 Bilophila, Desulfovibrio, Mogibacterium 및 Bacteroidetes 문을 포함한 여러 종의 대변이 증가하는 반면, 톱니 모양 폴립 환자의 경우 Fusobacteria 및 Erysipelotrichia 분류군이 증가하는 것으로 나타났습니다 [226]. Fusobacterium nucleatum(F. nucleatum)은 CRC 진행에 중요한 미생물로 특징지어집니다[287,288]. F. nucleatum은 TLR4 신호 전달 및 E-cadherin/-catenin 신호 전달을 촉진하여 궁극적으로 NF-κB의 활성화 및 miR{11}} 발현 감소로 이어집니다[289]. miR-1322과 같은 조절 마이크로 RNA는 CRC 전이를 촉진하는 사이토카인인 CCL20의 발현을 직접 조절할 수 있습니다[287]. 다른 문헌에서는 F. nucleatum adhesin A(FadA)가 F. nucleatum이 결장 상피에 부착, 침입 및 침식되도록 하는 주요 병독성 인자라고 지적합니다[227]. 최근 한 연구에서는 F. nucleatum이 NK 세포와 T 세포를 하향 조절하는 억제 수용체 CEACAM1 및 TIGIT1의 활성화를 통해 항종양 면역을 억제함으로써 CRC를 촉진할 수 있음을 발견했습니다[290]. F. nucleatum 균주 Fn7-1은 또한 Th17 반응을 증가시켜 CRC 발달을 악화시키는 것으로 나타났습니다[74]. F. nucleatum에 대한 이러한 발견은 이것이 SCFA 생성 박테리아이고 [291] 일반적으로 SCFA가 많은 염증성 질환에 대한 잠재적인 치료 방법으로 강조되었기 때문에 놀랍습니다. F. nucleatum은 주로 아세테이트와 부티레이트를 생산하며, 최근 F. nucleatum이 SCFA 수용체인 유리 지방산 수용체 2(FFAR2)를 통해 Th17을 유도하는 것으로 제안되었습니다[74]. 그러나 생쥐에서 FFAR2의 손실은 종양 박테리아 부하를 악화시키고 DC를 과도하게 활성화시켜 결국 T 세포 고갈을 촉진했습니다. 더욱이, 식이섬유의 부티레이트는 Warburg 효과로 인해 CRC 세포에서 덜 대사되어 HDAC 억제제로 작용하고 세포사멸과 관련된 유전자의 아세틸화를 촉진하는 것으로 나타났습니다[293]. 이러한 발견은 F. nucleatum의 병리학적 효과가 SCFA와 무관할 수 있음을 강조하지만, 이 가능성을 확인하려면 추가 연구가 필요합니다. CRC 발생에서 제안된 또 다른 메커니즘은 설탕, 단백질 및 지질의 과도한 식이 섭취가 담즙 내성 미생물의 성장을 촉진하여 DCA 및 LCA와 같은 2차 담즙산 및 부산물의 생산을 증가시킬 수 있음을 시사합니다. 황화수소와 같은. 과도한 2차 담즙산은 유전독성이 있으며 CRC의 발달을 촉진할 수 있는 염증 유발 환경을 생성할 수 있습니다. 특히 DCA는 금속단백분해효소인 ADAM-17 [294]의 표피 성장 인자 수용체 의존성 방출을 활성화하여 장내 발암성을 자극할 수 있습니다.

변비 치료 효과
DCA는 또한 -카테닌 신호 전달을 활성화하고[295] CRC 성장 및 침습을 위해 Lgr{2}}발현(Lgr{3}}) 암 줄기 세포[296]에서 악성 변형을 유도합니다. 그러나 IBD 환자에서는 2차 담즙산 생성과 관련된 박테리아, 즉 Clostridium 클러스터 X1Va가 크게 감소했으며, 이는 1차 담즙산에서 2차 담즙산으로의 전환 감소를 동반했습니다[297]. 담즙산 외에도 장내 미생물 대사산물인 엽산은 AhR 신호 전달을 유발하고 Th17 수준을 확장하여 CRC 발병을 악화시킬 수 있습니다[298]. SCFA와 유사하게, 장내 미생물군 유래 담즙산의 잠재적인 종양 유발 효과를 식별하기 위해서는 더 많은 연구가 필요합니다. CRC에는 뚜렷한 미생물군 의존성 면역학적 반응이 있습니다. 선천적 면역 반응 측면에서 A. muciniphila 농축은 결장 종양 형성을 억제하는 NLRP{13}}의존 방식으로 M1 대식세포 분극을 촉진했습니다[299]. 마찬가지로 장내 부착성 대장균은 IL{15}}생성 대식세포를 증가시켜 장 염증을 제한하고 종양 형성을 제한할 수 있습니다[300]. 적응 면역 측면에서 미생물 불균형은 CD{17}} T 세포를 과도하게 자극하여 만성 염증과 조기 T 세포 고갈을 촉진하며, 이는 결장 종양 감수성에 기여합니다[301]. 장암 세포는 또한 항종양 CD8+ T 세포를 감소시키는 공동 억제 분자 B7H3/B7H4의 종양 발현을 촉진하는 칼시뉴린 의존성 IL-6 분비를 유도하여 미생물군에 반응할 수 있습니다[302]. 이에 비해 Helicobacter hepaticus의 도입은 마우스 CRC 모델에서 항종양 면역을 회복시키는 T 여포성 보조 세포를 유도했습니다[303]. 대식세포 및 Th17 세포와 비교하여, δ T 세포 및 상주 기억 T 세포는 CRC 환자의 결장 조직에서 더 낮은 빈도로 발견되었습니다[60]. CRC의 조기 진단을 위해 면역 세포 패널을 개발할 수 있는지 조사하는 것은 흥미로울 것입니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
7.5. 간세포암종(HCC)
가장 흔한 원발성 간암인 간세포암종(HCC)은 전 세계적으로 암 관련 사망의 네 번째 주요 원인입니다[304]. HCC 발병의 주요 병인은 비알코올성 지방간 질환(NAFLD) 및 지방간염과 같이 간경변을 유발하는 기존의 간 질환에서 비롯됩니다[305]. 이는 인슐린 저항성, 비만, IL{4}} 및 TNF-를 통해 간 염증 및 종양 형성을 더욱 촉진하는 대사 장애를 비롯한 NAFLD 환자의 다른 수반되는 요인으로 인해 더욱 복잡해집니다. 간은 장에서 나오는 정맥혈의 '첫 번째 정지'이므로 장-상피 장벽을 가로지르는 미생물 전이 또는 흡수된 미생물 대사산물과의 접촉을 통해 장내 미생물에 취약해집니다[307]. 장 장벽 파괴, 미생물의 혈류로의 이동, LPS와 같은 PAMP에 의한 PRR 유도를 통한 후속 염증성 면역 반응을 포함하여 앞서 언급한 장내 미생물총 불균형의 잘 알려진 효과는 NAFLD의 발병과 밀접한 상관관계가 있습니다. 간경변 및 HCC [228,307]. 장내 미생물총의 불균형이 HCC 발병에 앞서 발생한다고 오랫동안 생각되어 왔지만, 이 인과 관계는 최근까지 심도 있게 조사되지 않았습니다. Behary, Raposo 등. 최근 HCC가 진행되기 전에 장내 미생물총 불균형이 LPS 의존성 Th{12}} 및 Th{13}}매개 사이토카인 반응이 뒤따르는 조기 발병 간 손상과 병행된다는 사실이 발견되었습니다[308]. 장내 미생물총 불균형이 HCC 이전의 간 손상의 원인인지 결과인지 여부를 추가 조사에서 확인해야 합니다. CCL3, CCL4, CCL5, IL{18}} 및 IL-13과 같은 염증 매개체의 증가와 함께 Enterobacteriaceae 및 Streptococcus의 증가와 Akkermansia의 감소가 NAFLD 관련 간세포암 환자에서 나타났습니다. 309]. 보다 최근의 연구에 따르면 간경변증 유발 간세포암종 환자에서 SCFA 생성 박테리아의 양이 감소하고 LPS 생성 박테리아가 증가한 것으로 나타났습니다. 그러나 C형 간염, B형 간염 또는 알코올성 간과 같은 다른 간 질환에서는 장내 미생물총 불균형에 대한 유의미한 증거가 발견되지 않았습니다. 질병 [310]. 그러나 광범위하게 말하면 여러 연구에서 관찰된 변경된 미생물 개체군은 서로 일치하지 않는다는 점에 유의해야 합니다 [309,311-313]. 또한 일반적으로 장내 미생물에 의해 생성된 SCFA는 인간에게 여러 가지 이점이 있다고 생각되지만, 최근 SCFA 부티레이트의 전구체인 이눌린이 유전적으로 변형된 생체 장애 생쥐에서 간세포암종으로의 진행을 촉진할 수 있다는 것이 발견되었습니다[229]. 다른 연구에서는 미생물 대사산물이 HCC에 미치는 영향에 초점을 맞췄습니다. 예를 들어, 고지방 식단은 2차 담즙산, 즉 DCA를 생성하는 그람 양성 유기체의 장내 과성장을 초래했습니다. DCA는 리포테이코산과 협력하여 TLR2를 활성화하고 이후 항종양 면역을 하향조절하여 HCC 발병에 유리한 미세 환경을 조성할 수 있습니다[314,315]. 전반적으로, 장내 미생물군 대사산물은 잠재적으로 간에 대한 전종양 유발성인 것으로 보입니다.
7.6. 심혈관 질환
심혈관 질환(CVD)은 주로 죽상경화증, NAFLD, 고혈압 및 제2형 당뇨병(TIIDM)과 같은 일련의 상호 연관된 질병을 포함하는 대사 증후군과 밀접하게 연관되어 있으며 만성, 저등급 염증에서 발생합니다. . 간과 췌장의 실질 세포, 지방 세포, 골격근 세포 등 대사 활동이 높은 많은 세포는 면역 세포와 광범위한 누화에 참여합니다. 미생물군집의 모든 교란은 숙주의 면역 기능을 변화시킬 가능성이 있으며, 더 나아가 대사적으로 활동적인 조직에서 질병 과정을 유발하거나 변화시킬 수 있는 능력을 가질 수 있습니다. PRR에 의한 LPS 및 기타 미생물 PAMP의 인식은 이러한 저등급 염증 상태의 핵심 동인으로 생각됩니다[231]. 미생물 공동 대사산물인 트리메틸아민 N-산화물(TMAO)도 NF-κB 신호 전달, 염증복합체 활성화 및 자유 라디칼 생성 증가를 통해 낮은 등급의 염증을 유발하는 것으로 알려져 있습니다[317,318]. 또한 TMAO는 대식세포의 콜레스테롤 대사를 손상시키고 거품세포 형성에 기여하여 죽상동맥경화증을 유발하고 이에 따라 심장병을 유발합니다[319]. 실제로, 혈청 TMAO가 높을수록 죽상동맥경화증, 관상동맥질환, 뇌졸중, 혈관 염증의 위험 증가와 상관관계가 있으며[232,233], TMAO는 현재 심혈관계 부작용에 대한 바이오마커로 간주되고 있습니다[320]. 보다 최근의 연구에서는 아드레날린 수용체 활성화 및 혈전 촉진 효과를 통해 CVD와 관련된 미생물 대사산물로서 페닐아세틸글루타민(PAGln)이 발견되었습니다[321,322]. 진단 지표로 사용되거나 심지어 CVD 환자를 위한 α-차단제 치료에 대한 반응성을 예측하는 인자로 사용되는 등 심혈관 의학에서 PAGln에 대한 여러 잠재적인 새로운 역할이 있습니다[322].
7.7. 당뇨병
당뇨병은 두 가지로 구분되는 질병입니다. 1형 당뇨병(TIDM)은 췌장 섬세포의 자가면역 파괴와 관련이 있고, 2형 당뇨병(TIIDM)은 후천적 인슐린 무감각과 관련됩니다. 미생물군 및 당뇨병과 관련된 많은 연구가 TIIDM 및 비만을 중심으로 이루어지고 있지만, 식이 SCFA 섭취가 증가하면 TIDM 환자의 미생물군 및 뚜렷한 면역 프로필이 변경될 수 있는 것으로 나타났습니다[323]. 부티레이트 및 아세테이트와 같은 식이 SCFA의 증가는 또한 생쥐에서 자가반응성 T 세포 집단 및 TIDM에 대한 보호를 제공하기 위해 시너지 효과를 발휘하는 것으로 나타났습니다[100]. 이에 비해 Parabacteroides distasonis 투여는 마우스 모델에서 T1DM의 발달을 가속화시켰는데, 이는 CD{3}} T 세포 증가 및 Foxp{4}} CD{5}} Treg 감소를 포함한 비정상적인 면역 반응 때문이었습니다. 세포 [324]. 주목할 만한 점은 조절되지 않은 담즙산 대사가 섬 자가면역 및 제1형 당뇨병의 잠재적인 소인인 것으로 밝혀졌습니다[325]. 미생물군집과 면역체계는 모두 TIIDM의 발병에 크게 관여합니다. 분지쇄 아미노산은 Prevotella copri(P. copri)와 Bacteroides vulgatus spp.에 의해 생산되며, P. copri는 마우스 모델에서 직접적으로 인슐린 저항성을 유도합니다[326,327]. 공생 A. muciniphila의 고갈은 장 장벽을 손상시켜 내독소가 혈류로 이동하고 이후 CCR2+ 단핵구가 활성화됩니다. 이로 인해 췌장 B1a 세포가 4BL 세포로 전환되어 염증 매개체를 방출하고 가역적 또는 비가역적 인슐린 저항성을 유발합니다[328]. 반면, 리놀레산, 도코사헥사엔산 등 미생물 대사산물은 항염증 효과와 지방독성 예방을 통해 인슐린 저항성과 TIIDM에 대한 보호 효과가 있다[329]. FMT는 또한 TIIDM이 있는 생쥐에서 공복 혈당 수치를 낮추고 인슐린 저항성을 감소시키는 것으로 나타났습니다[330]. 더욱이, 여러 항당뇨병 약물의 치료 효과 중 일부는 부분적으로 미생물군을 변화시키는 능력에 기인할 수 있습니다[331-333].
7.8. 고혈압
몇몇 연구에서는 정상 혈압 마우스와 고혈압 마우스 사이에서 미생물군집 구성이 크게 변경된 것을 관찰했지만, 고혈압 마우스의 특정 미생물 프로필은 사용된 고혈압 모델에 따라 달라집니다[334-337]. 고혈압의 안지오텐신 II 모델에서 무균 쥐의 미생물군 부족은 부분적으로 혈액 내 염증 세포 집단을 감소시킴으로써 고혈압을 예방했습니다. 그러나 무균 쥐는 안지오텐신 II와 고염식 복합 요법에 따라 신장 손상이 더 쉽게 발생했습니다[339]. 더욱이, 저혈압 무균 마우스에 미생물군을 재도입하면 혈관 수축력이 다시 확립되었습니다[340]. 일반적으로 미생물군 구성은 고혈압 동물과 정상 혈압 동물 사이에 다르며, 흥미롭게도 정상 혈압 댐과 고혈압 새끼를 교차 육성하면 전자 그룹의 혈압을 낮출 수 있습니다[341]. CVD와 마찬가지로 장 대사산물인 TMAO도 고혈압과 관련이 있습니다. 최근 연구에 따르면 TMAO는 안지오텐신 II로 유발된 고혈압 쥐에서 ROS를 통해 혈관 수축을 악화시키는 것으로 나타났습니다. 마찬가지로, 고염에 의한 DC 활성화는 미생물 불균형으로 인한 고혈압과 관련이 있습니다 [343]. 이에 비해 케톤체-하이드록시부티레이트는 고염분을 섭취한 고혈압 쥐에서 감소합니다. α-히드록시부티레이트 전구체인 1,3 부탄디올을 사용하여 구출하면 NLRP{24}}매개 염증복합체를 예방하여 혈압과 신장 염증을 감소시켰습니다[344]. HSD는 다른 곳에서 Lactobacillus spp.를 감소시키는 것으로 나타났습니다. Th17 세포 집단을 유도하는데, 이는 명백히 다른 메커니즘을 통해 나타나는 것으로 보입니다[176].
7.9. 류머티스성 관절염
주로 관절 염증을 특징으로 하는 전신 자가면역 질환인 류마티스 관절염(RA)의 발병 기전이 점점 더 이해되고 있습니다. RA는 질병에 대한 감수성을 증가시키는 여러 개의 확인된 대립유전자 및 환경 요인을 갖는 다인성 질병입니다. RA 발병에 잠재적으로 중요한 미생물 속은 Prevotella입니다. 이는 2013년 Scher et al.에 의해 처음 확인되었으며, 새로 발병한 RA 환자는 건강한 대조군과 비교하여 Prevotella spp., 특히 Prevotella copri의 풍부함이 유의하게 증가했음을 발견했습니다[234]. 그러나 만성 RA 환자에서는 Prevotella 집단이 증가하지 않았다[234]. 그 이후로 여러 연구에서 다양한 Prevotella 종과 RA [345-347] 사이의 추가 상관 관계가 발견되었습니다. 그러나 Prevotella spp. 그 자체가 RA의 발병에 기여하거나 RA에 의해 생성된 면역학적 환경이 장내 프레보텔라의 풍부함을 증가시킵니다. RA 환자의 장내 미생물총에서 주목할만한 다른 박테리아 이동에는 Proteobacteria, Clostridium Cluster XlVa 및 Ruminococcus의 번성이 포함되며, 이는 더 적은 CD{6}} T 세포 및 Treg 세포와 상관관계가 있었습니다[348]. K/BxN 자가면역 관절염 모델을 사용하여 SFB 매개 세포독성 T 림프구 항원-4(CTLA-4) 감소가 자가반응성 T 여포 보조 세포를 유발한다는 사실이 밝혀졌습니다[349,350]. 관절염에서 T 여포 보조 세포와 Th17 세포의 축적은 연령에 따라 달라지는 것으로 보이며[351] 이는 RA가 주로 노년층에서 발견되는 이유를 설명하는 데 도움이 됩니다. 그러나 흥미롭게도 K/BxN 자가면역 관절염 모델의 항생제 치료로 확인된 바와 같이 장내 미생물군은 Th17 세포가 아닌 T 여포 보조 세포에 주로 영향을 미치는 것으로 보입니다[352]. 주목할 만한 점은 최근 생쥐의 콜라겐 유발 RA가 장내 미생물 군집의 일주기 리듬 패턴에 이상을 유발하여 트립토판 대사산물과 같은 순환 미생물 유래 인자의 변화로 인해 장벽 무결성이 감소한다는 것이 보고되었습니다[353]. SCFA, 특히 부티레이트는 RA의 치료 옵션으로 제안되었습니다. 부티레이트 보충은 HDAC 발현을 억제하여 Treg 세포를 촉진하는 것으로 밝혀졌으며 RA에서 전염증성 사이토카인 유전자를 하향 조절했습니다. 더욱이 부티레이트는 HDAC 억제를 통해 히스톤 아세틸화를 강화함으로써 시험관 내에서 기능성 난포 Treg 세포의 분화를 직접 유도함으로써 관절염을 완화했습니다. 또한, 부티레이트는 AhR 리간드, 즉 세로토닌 유래 대사산물 5-하이드록시인돌-3-아세트산의 수준을 증가시켜 관절염 중증도를 감소시켰는데, 여기서 AhR 활성화는 조절 B 세포 기능을 지원했습니다[356]. SCFA 외에도 장내 미생물 유래 대사산물인 LCA, DCA, isoLCA, 3-oxoLCA도 최근 항관절염 효과를 나타내는 것으로 밝혀졌습니다. 구체적으로 isoLCA와 3-oxoLCA는 Th17 분화를 억제하고 M2 대식세포 분극을 촉진했습니다. 2차 담즙산의 이러한 효과는 Parabacteroides distasonis probiotic 보충과 시너지 효과를 낼 수 있습니다. 2차 담즙산에 대한 새로운 발견은 기념비적이며 추가 조사가 필요합니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
7.10. 알레르기 질환
알레르기는 면역 체계가 비병원성 외부 항원에 과민해질 때 발생합니다. 일반적인 과민반응에는 알레르기성 비염, 음식 알레르기, 습진, 아토피성 피부염, 천식이 포함됩니다. 미생물 노출 감소, 제왕절개, 식이요법, 항생제 사용 등 알레르기 발생을 담당하는 여러 요인은 장내 미생물 구성의 변화와 밀접하게 연관되어 있습니다[358-361]. 장내 미생물총 불균형은 알레르기, 특히 음식 알레르기 위험을 증가시킵니다 [235,236]. 항생제 사용으로 유발된 세균불균형은 알레르기 증상을 증가시키고 장 염증을 증가시키며 감작된 쥐의 장 점막 밀착 접합을 방해하기에 충분합니다[362]. 고지 방식은 일반적으로 항생제와 유사한 효과를 가지며, 장내 미생물총 불균형을 유발하고 결과적으로 음식 알레르기 위험을 증가시킵니다 [363]. 출생 직후 장내 미생물총 구성의 변화(미생물군집이 여전히 확립되어 있음)는 나중에 알레르기 질환 발병에 특히 큰 영향을 미치는 것으로 보입니다[364]. 주목할 만한 점은 질 미생물군이 알레르기 위험을 반영할 수도 있다는 점입니다. 여기서 락토바실러스가 우세한 질 미생물군집은 1세의 유아 혈청 IgE 상태와 관련이 있습니다[365]. 여러 연구에서는 세균불균형이 알레르기 질환, 특히 천식과 밀접한 관련이 있다는 개념을 강화합니다. 아토피성 천식이 있는 사람은 건강한 사람에 비해 대변 내 Lactobacillus와 E. coli의 수치가 상당히 높습니다[366]. 미생물군 대사산물의 관점에서 볼 때, 12,13-diHOME(비교적 특징이 없는 리놀레산)은 천식 위험이 높은 신생아에서 흔히 발견됩니다[367]. 최근에는 12,13-diHOME을 생성하는 세균성 에폭사이드 가수분해효소도 폐 염증 동안 농도가 더 높고, 12,13-diHOME이 폐의 Treg 세포를 감소시키는 것으로 밝혀졌습니다[368,369]. 이에 비해 AhR 리간드인 테트라클로로디벤조-p-다이옥신은 Treg 세포를 유도하고 Th17 세포를 억제하며 장내 미생물총 불균형을 역전시킴으로써 지연형 과민증을 약화시킬 수 있었습니다[370]. 마찬가지로, 부티레이트 및 프로피오네이트와 같은 대변 SCFA가 높은 개인은 어릴 때 천식 및 아토피 발병 위험이 현저히 감소했습니다 [371]. 잠재적인 치료 가치 중 SCFA 보충은 T 세포와 DC를 조절하여 천식을 완화할 수 있습니다[372]. 마찬가지로, 산모에게 식이섬유나 아세테이트를 보충하면 Foxp3 유전자의 아세틸화를 촉진하여 신생아를 천식으로부터 보호하는 것으로 나타났습니다. 식이섬유 공급은 또한 CD{30}} DC의 망막 탈수소효소 활성을 통해 음식 알레르기 유발 물질로부터 보호해 줍니다[374]. 주목할 만한 점은 식이섬유 이눌린이 최근 알레르겐 및 기생충 유발 제2형 염증을 촉진하는 것으로 밝혀졌으며 이는 담즙산 의존성이었습니다[375]. 전반적으로, 장내 미생물총이 알레르기에 미치는 영향은 대사산물에 의해 고도로 조절되는 것으로 보이지만, 각 미생물 제품은 과민성을 촉진하거나 저하시킬 수 있는 독립적인 효과를 가지고 있습니다.
7.11. 정신 장애: 장-뇌 축
앞서 언급한 정보는 장내 및 장외 질환 모두에 영향을 미치는 장내 미생물군을 설명합니다. 장내 미생물군이 영향을 미칠 수 있는 또 다른 기관은 '스트레스받은 장'이 여러 신경 질환에서 병리학적 실체로 점점 더 인식되고 있는 뇌입니다. 미성숙 장내 미생물군이 있는 미숙아의 경우 Klebsiella 과증식은 뇌 손상을 예측할 수 있는 가능성이 높으며 전염증성 면역학적 기조와 관련이 있습니다[376]. 파킨슨병은 장에 알파-시누클레인이 축적되는 것이 특징이며, 환자들은 Prevotellaceae의 인구가 더 많아 미생물총 불균형으로 인해 장 누수로 고통받는 경우가 많습니다[13]. 이러한 증상은 프로바이오틱스를 투여하면 역전될 수 있습니다[377,378]. 최근에는 미생물이 정신 건강에 영향을 미친다는 생각이 주목을 받기 시작했습니다. 분류학적 및 대사적 특징은 주요 우울 장애를 경증, 중등도 및 중증 증상 범주로 분류하기 위한 바이오마커로 제안되었습니다[379]. 정신적으로 건강한 사람과 불안 및/또는 우울증과 같은 정신 건강 장애가 있는 사람 사이의 미생물군 차이를 연구한 여러 연구에서는 출생 전후의 미생물 군집화가 나중에 인생에서 중요한 역할을 한다는 것을 시사했습니다. 예를 들어, 산모의 스트레스는 자손의 비정상적인 신경 발달을 유발할 수 있으며, 이는 Bifidobacterium spp.의 상당한 감소로 표시됩니다. [380]. 더욱이 질식 분만과 달리 제왕절개를 통해 분만된 신생아는 나중에 정신병이 발생할 위험이 더 큽니다[377,381]. 놀랍게도, 조기 옥시토신 치료는 제왕절개 분만된 새끼에서 나타나는 행동 결함을 최소화할 수 있습니다[382]. 특히 출생 후 및 이유 단계에서 광범위한 장내 미생물군을 고갈시키는 항생제의 혼합은 청소년기와 성인기까지 불안 관련 행동 결과의 장기적인 영향을 미칠 수 있습니다[383]. Li 등의 최근 우아한 연구. 유아가 항생제에 노출되면 염증 환경의 증가와 동시에 불안 및 우울증과 유사한 행동 및 기억 장애가 발생한다고 설명했습니다. 생쥐의 청소년기 및 성인기 단계에서 장기간 항생제 치료를 한 후에도 유사한 결과가 나타났습니다 [384]. 장내 미생물총의 조기 붕괴는 성별에 따른 불안 유사 행동을 유발할 수도 있는데, Wistar 쥐의 LPS 치료는 사회적 행동이 증가한 암컷에 비해 수컷의 사회적 상호 작용이 적었습니다[385]. '나이 든 미생물군집'에서 무균 마우스까지의 FMT가 SCFA를 감소시켰으며 이는 인지 저하와 관련이 있다는 점은 주목할 만합니다[386]. 장내 미생물군-면역-뇌 축은 아직 초기 단계에 있으며 행동 이상 및 신경 장애를 담당하는 면역 조절과 관련된 메커니즘을 확립하기 위한 조사가 필요합니다. 그러나 점막 곰팡이는 보완적인 Th17 면역 메커니즘을 통해 사회적 행동을 촉진하는 것으로 밝혀졌기 때문에 박테리아 이외의 다른 미생물을 살펴보는 것이 강조되어야 합니다[387].
8. 면역치료에서 장내 미생물군과 대사산물의 관계
현재 최전선 면역요법 치료법에는 T 세포(관문 억제제, 보조자극 수용체 작용제), T 세포 변형, 입양 T 세포 전달, 자가 사이토카인 유발 살해 세포, 키메라 항원 수용체 치료법, 사이토카인, 종양 용해 바이러스 및 백신이 포함됩니다[388,389]. 최근 몇 년간 CTLA-4에 대한 항체, PD{5}}(프로그램된 세포사멸 단백질 1) 및 프로그램된 죽음 리간드 1(PD-L1)을 포함한 면역관문억제제(ICI) 적용을 기반으로 한 면역치료제가 개발되고 있습니다. )은 다양한 종양에서 1차 또는 2차 치료법으로 승인되었습니다[390]. 특히 PD{11}}와 그 리간드인 PD-L1을 표적으로 하는 ICI는 미국 식품의약국(FDA)의 10가지 암 유형 치료용으로 승인되었습니다[391]. 최근 연구에 따르면 장내 미생물군은 일부 전임상 및 임상 연구에서 암 면역요법에 대한 반응의 중요한 결정 요인이 될 수 있습니다[392-394]. Matsonet al. Bifidobacterium longum, Collinsella aerofaciens 및 Enterococcus faecium은 PD{18}} 억제제에 반응하는 환자에서 더 많이 존재한다는 것을 보여주었습니다[395]. 여러 연구에서 반응자에서 Faecalibacterium, Ruminococcus 및 Akkermansia의 증가와 비반응자에서 Bacteroides의 증가를 포함하여 PD-1 억제제에 대한 반응자 대 비응답자의 미생물 군집에 상당한 차이가 있음을 발견했습니다[392,396,397]. 또한, 간암 환자에 대한 항PD{27}} 치료는 Faecalibacterium의 풍부도를 높이고 무진행 생존율을 향상시켰습니다[398]. 추가 연구에서는 장내 세균의 구성이 특정 면역치료제의 대사에 영향을 미칠 수 있다는 사실도 밝혀졌습니다. PD{30}} 치료 반응 환자에서 무균 마우스로의 대변 전달은 T 세포 반응을 강화하고 PD{33}} 억제제 치료의 효과를 향상시켰습니다[395]. Bifidobacterium pseudolongum과 Akkermansia muciniphila가 생산하는 이노신은 또한 T 세포를 활성화하여 항CTLA{36}} 및 항PD-L1 치료를 촉진했습니다[213]. 이에 비해 Coutzac et al. 부티레이트와 프로피오네이트는 CTLA{41}} 억제제의 효능을 제한했으며 이는 더 높은 Treg 집단 및 더 낮은 생존율과 관련이 있음을 보여주었습니다[399]. 주목할 만한 점은 새로 분리된 프로바이오틱 락토바실러스 균주(L. paracasei sh2020)가 종양에서 CXCL10의 발현을 상향 조절하고 이어서 CD{48}} T를 강화함으로써 CRC 종양 보유 마우스에서 항PD{45}} 효과를 촉진했다는 것입니다. 세포 모집[400]. 놀랍게도, 이러한 항종양 효과는 장내 미생물총 불균형이 있는 경우에도 나타났습니다. 이러한 전임상 및 임상 증거는 면역요법의 최대 효능을 제공하기 위해 장내 미생물군에 대한 요구 사항을 결정하기 위한 지속적인 조사를 뒷받침합니다(그림 3). 여기에는 ICI 관련 심장 독성과 같은 면역 요법의 부정적인 부작용을 제한하기 위해 장내 미생물군을 활용하는 것이 포함될 수 있습니다. Chenet al. Prevotellaceae 및 Rikenellaceae 미생물 집단을 고갈시키고, 부티레이트 수준을 감소시키며, PPAR -CYP4 × 1 축의 하향 조절을 통해 전 염증성 대 식세포 M1 분극을 촉진하는 PD{53}}/PD-L1 억제제가 우아하게 설명되었습니다 [401]. 치료 관련성 측면에서 Prevotella loescheii 재집락화 및 부티레이트 보충은 PD{62}}/PD-L1 억제제 관련 심장 독성을 완화했습니다[401]. 면역 체크포인트는 종종 이질적이고 지속되지 않아 치료 반응률, 약물 내성 및 부작용이 낮아질 수 있으므로 [402-404], 장내 미생물군 표적 치료법이 필수적인 보조제가 될 수 있습니다(그림 3). 현재 승인되어 이용 가능한 IBD 치료법은 항TNF제, 항인테그린제, 항- 7 단클론 항체 및 야누스 키나제(JAK) 억제제입니다. JAK 억제제(예: baricitinib)는 고지방-고당 섭취 후 인슐린 신호 전달을 복원하고 근골증을 개선하는 데 성공했지만 쥐의 장내 미생물에 대한 식이 유발 변경을 역전시키지 못했습니다[405]. 항-TNF 억제제는 크론병과 궤양성 대장염 모두에서 개선된 임상 결과를 보였지만 여전히 더 많은 무작위 임상 시험이 필요합니다[402]. 그러나 최근 FMT가 이전에 항TNF 요법(즉, infliximab)에 대한 반응 상실 또는 불내성을 지닌 CD 환자에 대한 잠재적인 대체 요법인 것으로 밝혀졌다는 점은 주목할 만합니다[406]. 인상적으로, 프로바이오틱 Bifidobacterium longum(B. longum) CECT 7894는 기회감염 병원체, 즉 Enterococcus 및 Pseudomonas의 풍부함을 줄이고 2차 담즙산을 증가시킴으로써 마우스 대장염 모델에서 infliximab 효능을 촉진했습니다[407]. 또 다른 최근 연구에서도 마찬가지로 항-TNF와 항-IL-12/23 치료법 모두 장내 미생물군을 변경하여 2차 담즙산 생산이 가능한 미생물 종을 선호한다는 사실이 밝혀졌습니다[408]. 2차 담즙산의 증가는 Clostridia spp.의 증식을 촉진하는 항-TNF 치료로 인한 것일 수 있습니다. 장내 미생물 복원의 일환으로 [409]. 담즙산은 항-TNF 치료 반응에 대한 잠재적인 대사 바이오마커로 간주되지만[410] 담즙산이 면역치료 효능을 향상시키는지 여부를 결정하려면 더 많은 연구가 필요합니다(그림 3). NF-κB 신호 전달을 억제하여 CRC 재발을 예방하기 위한 UDCA 치료에 대한 증거를 고려할 때 2차 담즙산이 유익할 수 있다는 힌트가 있습니다[411,412]. 더욱이, UDCA는 항PD1 효과와 시너지 효과를 발휘하여 종양이 있는 쥐에서 암 진행을 억제하는 것으로 밝혀졌습니다[413]. 전반적으로, 장내 미생물군은 면역치료 반응을 개선하기 위한 바이오마커이자 치료 표적으로 활용될 수 있는 것으로 보입니다.
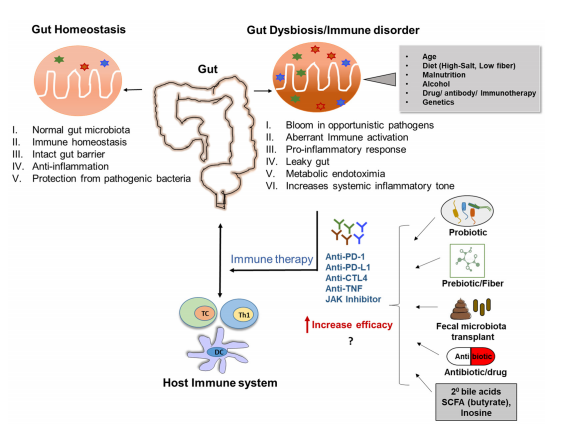
그림 3. 장내 미생물 집단의 풍부함을 수정하면 면역요법의 결과에 영향을 미칠 수 있습니다. 건강한 장내 미생물은 숙주에서 약물의 생체 이용률과 효능을 증가시킬 수 있습니다. 여러 가지 요인으로 인해 발생하는 세균불균형은 치료 약물의 효능을 감소시켜 치료 결과가 좋지 않을 수 있습니다. 장내 미생물총을 변형하면 항PD-1 항체, 항PD-L1 항체, 항CTL4 항체 치료와 같은 특정 면역치료제의 효과가 증가할 수 있습니다. 장내 미생물군은 항생제, 프로바이오틱스, 프리바이오틱스, 2차 담즙산, 단쇄 지방산(예: 부티레이트), 이노신 또는 대변 이식을 통해 바뀔 수 있습니다.
9. 면역-미생물 연구의 약속, 과제 및 위험
미생물군과 면역 체계 사이의 상호 작용과 이들이 IBD, 자가면역 관절염, 암 등의 질병에 미치는 영향은 놀라울 정도로 복잡합니다. 복잡성의 한 단계에는 질병의 발병이나 일반적인 숙주 생리학에서 특정 단일 또는 박테리아 그룹의 정확한 의미를 보여주는 과제가 포함됩니다. 무균 모델에 대한 미생물의 집락화는 숙주의 건강과 질병에 대한 장내 미생물의 잠재적 영향을 더 잘 이해하기 위한 관련 전략입니다[414]. 그러나 장내 미생물군은 선택된 소수의 종 그 이상입니다. 미생물군집 환경에는 종들이 자원을 놓고 상호 배타적이거나 경쟁적이며, 많은 미생물이 성장을 위해 서로 의존하는 강력한 역동성이 있습니다[415]. 또 다른 복잡성 계층에는 식이요법, 흡연, 약물 및 약물 치료와 같이 상호 작용하는 다른 유전적 및 환경적 요인이 포함됩니다(그림 2). 여기에는 개인의 도시 지역과 농촌 지역 간의 미생물총(및 잠재적인 면역 반응)의 차이가 포함됩니다[416]. 그럼에도 불구하고 설치류 모델에서 관찰된 내용이 항상 인간에게 전달되는 것은 아닙니다. 특정 병원균이 없는 환경에서 사는 연구용 설치류와 비교할 때 인간과 기타 포유류는 '더 더러운' 환경에서 살고 있다고 일반적으로 말할 수 있습니다. 따라서 위생 가설을 반영하는 환경의 청결도는 미생물군 구성과 질병 감수성에 영향을 미칠 수 있습니다. 이 개념은 수정된 생쥐(가축 농장 유형의 환경에 지속적으로 노출되는 동물)가 위생적으로 태어난 생쥐와 비교할 때 더 안정적인 장내 미생물군을 갖고 돌연변이 유발 및 대장염 유발 신생물에 대한 저항성을 유지한다는 최근 발견에 의해 뒷받침됩니다[417].
미생물군집-면역 연구에 중점을 둔 여러 연구에서는 미생물군집을 특성화하기 위해 16S rRNA 시퀀싱을 사용했지만 이 방법은 속을 성공적으로 식별할 수 있지만 종 수준에서 구별을 제공할 수 없다는 점에서 한계가 있습니다[418]. 따라서 미생물군집에 대한 보다 포괄적인 연구를 달성하려면 메타게놈학을 다른 오믹스 접근법과 결합하는 것이 바람직합니다[419]. 가장 최근에는 메타전사체학과 대사체학이 미생물군집 연구에 급속히 중요해지고 있습니다. Metagenomics는 샘플의 분류학적 프로필을 생성하고, Metatranscriptomics는 기능적 프로필을 얻고, Metabolomics는 환경에서 미생물군에 의해 방출되는 부산물을 결정하여 묘사를 마무리합니다[419]. 이러한 각각의 -omics 접근 방식은 그 자체로 귀중한 정보를 제공하지만, 결합된 -omics에서 보다 완전한 그림을 얻을 수 있다고 제안됩니다. 이러한 -omics 접근 방식의 중요한 이점 중 하나는 원시 파일을 데이터베이스에 보관한 다음 나중에 다른 연구 그룹에서 분석하기 위해 채굴할 수 있다는 것입니다. 여러 데이터베이스를 비교하기 위해 기계 학습을 적용할 때 발생할 수 있는 한 가지 제한 사항은 표본 크기의 불균일성입니다[420]. 더욱이, -omics 결과는 연구 및/또는 임상 연구 사이에서 장내 미생물 변화의 중복 패턴을 찾기 어려울 수 있으므로 연구별 결과로 간주될 수 있습니다. 이는 지리적 기원에 따라 인간의 장내 미생물군(및 대사산물)과 질병 감수성이 다를 수 있고[421] 심지어 일반 실험실 설치류의 박테리아 구성도 연구 시설과 공급업체에 따라 다를 수 있기 때문입니다[422]. 전반적으로 -omics는 잠재적인 진단 및 치료 목표를 식별하기 위해 생의학 분야를 확실히 발전시키고 있지만 여전히 극복해야 할 몇 가지 한계가 있습니다.
10. 결론
요약하면, 숙주 면역 체계와 장내 미생물은 숙주의 정상적인 기능과 웰빙을 위해 서로 크게 의존합니다(그래픽 요약에 요약됨). 이 리뷰에서는 태아의 면역 건강이 환경적으로 산모의 미생물총에 어떻게 의존하는지(건강한지, 장내 세균총 이상 또는 스트레스를 받는지)를 포함한 새로운 발견을 다루었습니다. Treg 세포 및 IL{1}} 분비를 유도하여 장 항상성을 조절하는 SCFA 및 2차 담즙산과 같은 새로운 기계적 경로가 논의되었습니다(그림 1A, B). 검토 전반에 걸쳐 부티레이트와 그 전구체 식이섬유는 면역 반응에 영향을 미치고 많은 질병에 대한 잠재적 치료제로 작용하기 위해 반복적으로 언급되었지만 일부 증거에 따르면 임상 실습은 질병 상황에 맞게 조정될 필요가 있을 수 있습니다. 이에 비해 프로바이오틱스와 FMT는 장내 미생물의 공생균을 복원하고 염증성 질환을 완화하는 데 더 유망한 것으로 보입니다. 더욱이, 장내 미생물군은 현재의 면역요법을 개선하고 부정적인 부작용을 줄이는 데 적절한 목표인 것으로 보입니다(그림 3). 우리는 또한 각 미생물군을 인간 사이에서 독특하게 만들고 종 모델을 비교할 때 본질적으로 유전적 및 환경적 요인(그림 2)에 뿌리를 둔 미생물군집 연구의 현재 과제에 대해 논의했습니다. 우리는 후성유전체학, 메타유전체학, 메타프로테오믹스, 대사체학, 배양체학, 단일 세포 전사체학을 포함한 다중 오믹스 방법의 최근 개발이 건강과 질병에서 장내 미생물군집과 면역체계 사이의 상호작용을 밝혀줄 것이라고 가정합니다[423] . 따라서 장내 미생물군유전체 프로파일을 기반으로 '특정' 숙주 면역 반응을 예측하는 것은 흥미로울 것이며, 이는 면역 질환에 대한 '맞춤형 미생물군집 표적' 치료법의 개발을 뒷받침할 것입니다.
참고자료
1. Donne, J. 사람은 섬이 아니다; 폴 피터 피에히(Paul Peter Piech) 그림; 황소 자리 출판사: Willow Dene, 영국, 1975.
2. 빔, A.; 클링거, E.; Hao, L. 장내 미생물 구성에 대한 식이 및 식이 성분의 영향. 영양소 2021, 13, 2795. [CrossRef] [PubMed]
3. 샤나한, F.; 고쉬, TS; O0 Toole, PW 건강한 미생물군집 - 건강한 장내 미생물군집의 정의는 무엇입니까? 위장병학 2021, 160, 483-494. [상호참조] [PubMed]
4. 오전 발데스; 월터, J.; 시걸, E.; Spector, TD 영양과 건강에서 장내 미생물의 역할. BMJ 2018, 361, k2179. [상호참조] [PubMed]
5. 불, MJ; Plummer, NT 1부: 건강과 질병의 인간 장내 미생물군집. 적분 메드. 2014, 13, 17–22.
6. 색스, D.; 백스터, B.; 캠벨, BC; 카펜터, JS; 코그나드, C.; 디펠, D.; 이사, M.; 피셔, U.; 하우세거, K.; Hirsch, JA 다사회 합의 품질 개선 급성 허혈성 뇌졸중의 혈관내 치료에 대한 합의 성명 개정. 국제 J. 뇌졸중 2018, 13, 612-632. [상호참조]
7. 마티자식, M.; 메스트로비치, T.; 팔제타크, HC; 페릭, M.; 바레식, A.; Verbanac, D. IBD의 박테리아-Mycobiome, Virome, Archaeome 및 진핵 기생충을 넘어서는 Gut Microbiota. Int J. Mol. 과학. 2020, 21, 2668. [상호참조]
8. 주프레, M.; 캄피고토, M.; 캄피시아노, G.; 코마르, M.; Croce, LS 간 및 장내 미생물 이야기: 장내 세균총은 간 질환에 어떤 영향을 미칩니까? 문헌 검토. 오전. J. Physiol. 위장관. 간 물리. 2020, 318, G889–G906. [상호참조]
9. Gomaa, EZ 건강 및 질병의 인간 장내 미생물군집/미생물군집: 검토. Antonie Van Leeuwenhoek 2020, 113, 2019-2040. [상호참조]
10. 밀스, S.; 스탠턴, C.; 레인, 재팬; 스미스, GJ; Ross, RP Precision Nutrition 및 Microbiome, 1부: 과학의 현재 상태. 영양소 2019, 11, 923. [CrossRef]
11. 아닥, A.; Khan, MR 장내 미생물군과 그 기능에 대한 통찰력. 셀. 몰. 생명 과학. 2019, 76, 473–493. [상호참조]
12. Gensollen, T.; 아이어, SS; 캐스퍼, DL; Blumberg, RS 초기 생명체의 미생물군집화가 면역체계를 형성하는 방법. 과학 2016, 352, 539-544. [상호참조] [PubMed]
13. 주프레, M.; 모레티, R.; 캄피시아노, G.; 다 실베이라, ABM; 몬다, VM; 코마르, M.; 디 벨라, S.; 안토넬로, RM; 루자티, R.; Croce, LS 나한테 말하는 거야? 미생물에 대한 장신경계(ENS)를 말합니다. 장내 미생물이 ENS와 상호 작용하는 방법. J. 클린. 메드. 2020, 9, 3705. [상호참조]
14. 조영수; 해안, SA 비만, 천식 및 미생물군집. 생리학 2016, 31, 108-116. [상호참조] [PubMed]
15. 맥콤, S.; 티리오트, A.; 아카체, B.; 크리슈난, L.; Stark, F. 면역 체계 소개. 방법 몰. Biol. 2019, 2024, 1–24. [상호참조] [PubMed]
16. 찬, 엘.; 카리미, N.; 모로바티, S.; 알리자데, K.; 카키시, JE; 밴더캠프, S.; 파젤, F.; 나폴레옹, C.; 알리자데, K.; 메라니, Y.; 외. 사이토카인 폭풍에서 호중구의 역할. 바이러스 2021, 13, 2318. [교차참조]
17. 도밍게즈-벨로, MG; 코스텔로, EK; 콘트레라스, M.; 마그리스, M.; 히달고, G.; 피어러, N.; Knight, R. 전달 모드는 신생아의 여러 신체 서식지에 걸쳐 초기 미생물군의 획득 및 구조를 형성합니다. 진행 Natl. Acad. 과학. 미국 2010, 107, 11971-11975. [상호참조]
18. 미첼, CM; 마조니, C.; 호그스트롬, L.; 브라이언트, A.; 베르제라트, A.; 쉐어, A.; 포찬, S.; 허먼, P.; 캐리건, M.; 샤프, K.; 외. 전달 방식은 초기 유아 장내 미생물의 안정성에 영향을 미칩니다. Cell Rep. Med. 2020, 1, 100156. [교차참조]
19. 셀마-로요, M.; Calatayud Arroyo, M.; 가르시아-만트라나, I.; 파라-요르카, A.; 에스큐리에, R.; 마르티네즈-코스타, C.; Collado, MC 주산기 환경은 미생물 군집화 및 유아 성장을 형성합니다. 숙주 반응 및 장 기능에 영향을 미칩니다. 마이크로바이옴 2020, 8, 167. [CrossRef]
20. 수브라마니안, S.; 겐, H.; 듀, C.; 주 PM; 부, HF; 왕, X.; 스와미나단, S.; 탄, 사우스캐롤라이나; 리들론, JM; 드 플렌, IG; 외. 급식 모드는 동적 장내 미생물군 특징에 영향을 미치고 신생아 생쥐에서 항-CD3 mAb 유발 장 손상에 대한 민감성에 영향을 미칩니다. 오전. J. Physiol. 위장관. 간 물리. 2022, 323, G205–G218. [상호참조]
21. 웜파치, L.; 하인츠-부샤르트, A.; 프리츠, JV; 라미로-가르시아, J.; 하비에르, J.; 헤롤드, M.; 나라야나사미, S.; 케이센, A.; 호건, 아하이오; 빈들, L.; 외. 출생 모드는 최초의 균주가 부여한 장내 미생물군집 기능 및 면역자극 잠재력과 관련이 있습니다. Nat. 커뮤니케이터 2018, 9, 5091. [CrossRef] 22. Negi, S.; 하시모토-힐, S.; Alenghat, T. 감염에 영향을 미치는 신생아 미생물군-상피 상호작용. 앞쪽. 미생물. 2022, 13, 955051. [CrossRef] [PubMed]
23. 센, V.; 배슬러, D.; 초우드리, R.; Scholkmann, F.; Righini-Grunder, F.; Vuille-Dit-Bile, RN; Restin, T. 태아부터 유아기까지의 미생물 집락화 - 종합적인 검토. 앞쪽. 셀. 감염. 미생물. 2020, 10, 573735. [CrossRef] [PubMed]
24. Rackaityte, E.; 할키아스, J.; 후쿠이, EM; 멘도사, VF; 헤이즐든, C.; 크로포드, ED; 후지무라, KE; 버트, TD; Lynch, SV 생존 가능한 박테리아의 집락화는 자궁 내 인간 장에서 매우 제한적입니다. Nat. 메드. 2020, 26, 599-607. [상호참조]
25. 리, Y.; 투테이커, JM; 벤-사이먼, S.; 오제리, L.; 슈바이처, R.; 맥코트, BT; 맥코트, CC; 베르너, L.; 스내퍼, SB; 슈발, DS; 외. 자궁 내 인간의 장에는 박테리아 대사산물을 포함한 독특한 대사체가 있습니다. JCI 인사이트 2020, 5, e138751. [상호참조] [PubMed]
26. Jain, N. 면역 체계의 조기 교육: 엄마, 미생물 및 (놓친) 기회. 장내 미생물 2020, 12, 1824564. [CrossRef]
27. Gierynska, M.; Szulc-Dabrowska, L.; 스트루지크, J.; 미엘카르스카, MB; Gregorczyk-Zboroch, 장 장벽의 KP 무결성: 상피 세포와 미생물총-A 상호 관계의 관련. 동물 2022, 12, 145. [CrossRef]
28. 웨스트롬, B.; Arevalo Sureda, E.; 피어지노프스카, K.; 피어지노프스키, SG; Perez-Cano, FJ 미성숙 장 장벽과 신생아 포유류의 면역력 확립에 있어서 그 중요성. 앞쪽. 면역. 2020, 11, 1153. [상호참조]
29. 라베, H.; 런델, AC; Sjoberg, F.; 융, A.; 스트롬벡, A.; 지오바타, M.; Maglio, C.; 노드스트롬, I.; 앤더슨, K.; 누카오, 나.; 외. 비피도박테리움(Bifidobacterium)에 의한 신생아 장내 군집화는 더 높은 유년기 사이토카인 반응과 관련이 있습니다. 장내 미생물 2020, 12, 1847628. [CrossRef]
30. 헨릭, BM; 로드리게스, L.; 락슈미칸트, T.; 포우, C.; 헨켈, E.; Arzoomand, A.; 올린, A.; 왕, J.; 마이크스, J.; 탄, Z.; 외. 비피도박테리아 매개 면역체계는 생애 초기에 각인됩니다. 셀 2021, 184, 3884–3898. [상호참조]
31. 친, 엔.; Mendez-Lagares, G.; 태프트, DH; Laleau, V.; 키우, H.; 나라얀, NR; 로버츠, SB; 밀스, DA; Hartigan-O0 코너, DJ; Flaherman, VJ 장내 미생물군에 대한 유아용 조제분유 보충의 일시적 효과. 영양소 2021, 13, 807. [CrossRef]
32. 알 나바니, Z.; 둘라우로이, S.; 마르케스, R.; 쿠수, C.; 알 바운니, S.; 데자르뎅, F.; 스파와서, T.; 베라드, M.; 서프-벤수산, N.; Eberl, G. 성인의 면역병리학에 대한 저항성을 위해서는 미생물총에 대한 이유 반응이 필요합니다. 면역 2019, 50, 1276-1288. [상호참조] [PubMed]
33. 루보-보드롱, C.; 루이즈, VE; 스완, AM, Jr.; 밸런스, BA; 오즈쿨, C.; 페이, Z.; 리, J.; 바타글리아, TW; 페레즈-페레즈, 조지아; Blaser, MJ 초기 항생제 노출이 후속 세균 감염에 대한 저항성에 미치는 장기적인 영향. mBio 2019, 10, e02820-19. [상호참조] [PubMed]
34. 카헨즐리, J.; 콜러, Y.; 와이스, M.; 괴킹, MB; McCoy, KD 초기 생애 동안의 장내 미생물 다양성은 장기적인 IgE 수준을 형성합니다. 세포 숙주 미생물 2013, 14, 559-570. [상호참조] [PubMed]
35. 엘 아이디, S.; 후이벨드, G.; 트레마롤리, V.; 백헤드, F.; Kleerebezem, M. 장내 미생물군과 점막 항상성: 출생 시 또는 성인기에 집락화되는 것이 중요합니까? 장내 미생물 2013, 4, 118-124. [상호참조]
36. 왕, 시.; 리, Q.; Ren, J. 장 유래 감염의 발병기전에서 미생물총-면역 상호작용. 앞쪽. 면역. 2019년 10월 1873일. [상호참조]
37. 매사추세츠주 맥거킨; 린든, SK; 서튼, P.; 플로린, TH 뮤신 역학 및 장내 병원균. Nat. 미생물 목사. 2011, 9, 265-278. [상호참조]
38. Mogensen, TH 선천적 면역 방어에서 병원체 인식 및 염증 신호 전달. 클린. 미생물. 2009, 22, 240-273. [상호참조]
9. 미나리에타, L.; 고르바니, P.; 스파와서, T.; Berod, L. Metabolites: DC와 환경 사이의 분자 언어 해독. 세민. 면역병리학. 2017, 39, 177-198. [상호참조]
40. 레비, M.; Kolodziejczyk, AA; 캘리포니아주 타이스; Elinav, E. Dysbiosis 및 면역 체계. Nat. Immunol 목사. 2017, 17, 219–232. [상호참조]
41. 모리카와, M.; 쓰지베, S.; 기요시마-시바타, J.; 와타나베, Y.; 카토-나가오카, N.; 시다, K.; Matsumoto, 소장의 S. 미생물군은 고유판과 Peyer{3}} 패치의 식세포에 의해 선택적으로 포식됩니다. PLoS ONE 2016, 11, e0163607. [상호참조]
42. 콜러, A.; 델보브, S.; 스마우트, J.; 토레스, D.; Flamand, V. 미생물군 유발 TNF에 대한 초기 노출은 신생아 pre-cDC1의 성숙을 촉진합니다. 구트 2021, 70, 511–521. [상호참조] [PubMed]
43. 메인 요한슨; Hansson, GC 장 점액과 뮤신의 면역학적 측면. Nat. Immunol 목사. 2016, 16, 639-649. [상호참조] [PubMed]
44. 후마윤, M.; 아유소, JM; 파크, 켄터키; 마르토렐리 디 제노바, B.; 스칼라, MC; 커, 사우스캐롤라이나; 놀, LJ; Beebe, DJ 인간 장 조직 미세 생리 시스템에서 숙주-기생충 상호 작용에 대한 선천적 면역 세포 반응. 과학. 고급 2022, 8, eabm8012. [상호참조] [PubMed]
45. 아티스, D.; Spits, H. 선천성 림프 세포의 생물학. 자연 2015, 517, 293-301. [상호참조] [PubMed]
46. 란켈마, JM; 루이지애나 반 뷰트; 벨저, C.; 슐츠, MJ; 반 데르 폴, T.; 드 보스, WM; Wiersinga, WJ 중병 환자는 장내 미생물 조절 장애에 큰 대인 관계 변화가 있음을 보여줍니다. 파일럿 연구. 집중 치료 Med. 2017, 43, 59–68. [상호참조]
47. BM 푸르니에; Parkos, CA 장 염증 중 호중구의 역할. 점막 면역. 2012, 5, 354-366. [상호참조]
48. 로, JT; 이경근; 이, AP; 테오, JKH; 임, HL; 김 SS; 탄, 아흐; Lam, KP DOK3는 호중구에서 JAK2/STAT3 신호 전달 및 S100a8/9 생산을 억제하여 장의 항상성을 유지합니다. 세포 사멸 Dis. 2021, 12, 1054. [상호참조]
49. 서DH; 체, X.; 김S.; 김동훈; 마, HW; 김진호; 김티; 김휘환; 김 SW; Cheon, JH 골수 세포에 발현된 트리거링 수용체-1 작용제는 Cd177(+) 호중구를 통해 장 염증을 조절합니다. 앞쪽. 면역. 2021, 12, 650864. [교차참조]
50. 봉, L.; 영, CW; 핀넬, LJ; Sherman, PM 부착성 침습성 대장균은 항생제 관련 장내 세균 불균형 및 호중구 세포외 트랩 활성화를 악화시킵니다. 염증. 창자 Dis. 2016, 22, 42–54. [상호참조]
51. 델라노, MJ; Ward, PA 패혈증 진행, 해결 및 장기 결과에서 면역 체계의 역할. 면역. 개정판 2016, 274, 330–353. [상호참조]
52. 아포스톨로프, 알래스카; 하마니, M.; 에르난데스-바르가스, H.; 이갈루젠, R.; Guyennon, A.; 페노, 오.; 마리, JC; Soudja, SM 장 상피내 감마델타 T 세포 및 기타 감마델타 T 세포 하위 집합의 공통적이고 독점적인 특징. Immunohorizons 2022, 6, 515–527. [상호참조] [PubMed]
53. 이스마일, AS; 세버슨, KM; 바이쉬나바, S.; 베렌트, CL; 유, X.; 벤저민, JL; 룬, KA; 허우, B.; 드프랑코, 앨라배마; 야로빈스키, F.; 외. 감마델타 상피내 림프구는 장 점막 표면에서 숙주-미생물 항상성의 필수 중재자입니다. 진행 Natl. Acad. 과학. 미국 2011, 108, 8743-8748. [상호참조]
54. 홀트마이어, W.; Kabelitz, D. Gammadelta T 세포는 선천성 면역 반응과 적응성 면역 반응을 연결합니다. 화학. 면역. 알레르기 2005, 86, 151–183. [상호참조]
55. 타일러, CJ; 매카시, 네브라스카; 린제이, 조; 스태그, AJ; 모저, B.; Eberl, M. 항원 제시 인간 감마델타 T 세포는 IL-22의 장 CD4(+) T 세포 발현 및 칼프로텍틴의 점막 방출을 촉진합니다. J. Immunol. 2017, 198, 3417-3425. [상호참조] [PubMed]
56. 리, Y.; 왕 Y.; 시, F.; 장, X.; 장 Y.; 비, K.; 첸, X.; 리, 엘.; Diao, H. 장내 미생물총의 인지질 대사산물은 CD1d 의존성 감마 델타 T 세포를 통해 저산소증으로 인한 장 손상을 촉진합니다. 장내 미생물 2022, 14, 2096994. [CrossRef] [PubMed]
57. 토마셀로, E.; Bedoui, S. 장 항상성 및 면역 감시의 장내 선천 면역 세포. 면역. 셀바이올. 2013, 91, 201-203. [상호참조] [PubMed]
58. 그리말디, D.; 르 부르히, L.; Sauneuf, B.; 디샤르트르, A.; 루소, C.; 우아즈, F.; 마일더, M.; 루이스, D.; 치체, JD; 미라, 일본; 외. 심각한 감염이 있는 중환자의 선천성 T 림프구 중 특정 MAIT 세포 거동. 집중 치료 Med. 2014, 40, 192-201. [상호참조]
59. JC 안드레우-발레스터; Tormo-Calandin, C.; 가르시아-발레스테로스, C.; 페레즈-그리에라, J.; 아미고, V.; 알멜라-퀼리스, A.; 루이즈 델 카스티요, J.; Penarroja-Otero, C.; Ballester, F. 패혈증 환자의 질병 중증도 및 사망률과 감마 델타 T 세포의 연관성. 클린. 백신 면역. 2013, 20, 738-746. [상호참조]
60. 노블, A.; 프링, 동부 표준시; 듀란트, L.; 남자, R.; 딜케, SM; 호일스, L.; 제임스, SA; 카딩, SR; 젠킨스, JT; Knight, SC 대장암에서 미생물군에 대한 면역력 변경, B 세포 활성화 및 감마-델타/상주 기억 T 세포 고갈. 암 면역. 면역. 2022, 71, 2619–2629. [상호참조]
61. 스즈키, H.; 정기; 이토, K.; Doi, K. 무균 및 특정 병원균이 없는 마우스에서 소장 상피내 림프구 분포의 지역적 변화. 특급. 몰. 파톨. 2002, 72, 230-235. [상호참조]
62. 베두이, S.; 히스, WR; Mueller, SN CD4(+) T 세포는 일차 CD8(+) T 세포 면역을 위한 선천적 신호를 증폭시킵니다. 면역. 개정판 2016, 272, 52–64. [상호참조] [PubMed]
63. 벨츠, GT; 쇼트먼, K.; 베번, MJ; Heath, WR CD8alpha+ 수지상 세포는 생체 내에서 MHC 클래스 I 제한 비세포용해성 바이러스 및 세포내 세균 항원을 선택적으로 제시합니다. J. Immunol. 2005, 175, 196-200. [상호참조] [PubMed]
64. 슈테인, MB; 배포드, AC; Salerno-Goncalves, R. Salmonella enterica serovar Typhi 노출은 인간 장 세포에서 생체 외 세포 유형별 후성 유전적 변화를 유도합니다. 과학. 2020, 10, 13581. [교차참조]
65. 베카티니, S.; 리트만, 응급실; 석, R.; 아모레티, L.; 폰타나, E.; 라이트, R.; 존발라지, M.; 라이너, IM; 플리타스, G.; 홀, TM; 외. 일시적인 미생물군 고갈을 통해 점막 면역을 강화합니다. Nat. 커뮤니케이터 2020, 11, 4475. [상호참조]
66. 드 위트, J.; 소우어, Y.; 요리츠마, T.; 클라세 보스, H.; 10 Brinke, A.; 네프제스, J.; van Ham, SM 항원 특이적 B 세포는 교차 제시를 통해 식세포 살모넬라에 대한 효과적인 세포 독성 T 세포 반응을 재활성화합니다. PLoS ONE 2010, 5, e13016. [상호참조] [PubMed]
67. 슈넬, A.; 황, L.; 가수, M.; 싱가라주, A.; 바릴라, RM; 리건, BML; 볼하겐, A.; PI 타코레; 디온, D.; 딜로리, TM; 외. 줄기형 장 Th17 세포는 자가면역 동안 병원성 이펙터 T 세포를 생성합니다. 셀 2021, 184, 6281–6298.e23. [상호참조]
68. 오메네티, S.; 부시, C.; 메티지, A.; 이세폰, A.; 이석수; 톨라이니, M.; 리, Y.; 켈리, G.; 차크라바티, P.; 쇼아이, S.; 외. 장은 기능적으로 별개의 항상성 조직 상주 세포와 염증성 Th17 세포를 보유하고 있습니다. 면역 2019, 51, 77–89. [상호참조] 69. Ivanov, II; 아타라시, K.; 마넬, N.; 브로디, EL; 시마, T.; Karaoz, U.; 웨이, D.; 골드파브, KC; 캘리포니아주 샌티; 린치, SV; 외. 분할된 사상균에 의한 장 Th17 세포의 유도. 셀 2009, 139, 485–498. [상호참조]
70. 탄, TG; 세피크, E.; 게바-자토르스키, N.; 쿠아, L.; 나스카, D.; 텡, F.; 파스만, L.; 오티즈-로페즈, A.; Jupp, R.; 우, HJ; 외. 단독으로 생쥐의 장내 Th17 세포를 유도할 수 있는 인간 장에서 공생 박테리아 종을 식별합니다. 진행 Natl. Acad. 과학. 미국 2016, 113, E8141–E8150. [상호참조]
71. 사노, T.; 카게야마, T.; 팡, V.; 케드미, R.; 마르티네즈, CS; 탤벗, J.; 첸, A.; 카브레라, I.; 고르쉬코, O.; 쿠라카케, R.; 외. 배수 림프절에서 장내 미생물에 의해 유발된 Th17 세포 분화에 대한 중복 사이토카인 요구 사항. Cell Rep. 2021, 36, 109608. [CrossRef]
72. 아이언스, EE; 코르테스 고메즈, E.; 안데르센, VL; Lau, JTY 박테리아 집락화 및 TH17 면역은 신생아 생쥐의 장내 시알릴화에 의해 형성됩니다. 당생물학 2022, 32, 414-428. [상호참조] [PubMed]
73. 알렉산더, M.; 앙, QY; 나약, RR; 버스션, AE; 샌디, M.; 장, B.; Upadhyay, V.; 폴라드, 캔자스; 린치, SV; Turnbaugh, PJ 인간 장내 세균 대사는 Th17 활성화 및 대장염을 유발합니다. 세포 숙주 미생물 2022, 30, 17–30. [상호참조] [PubMed]
74. 캘리포니아주 브레넌; 클레이, SL; 라부아, SL; 배, S.; 랭, JK; 폰세카-페레이라, D.; 로진스키, KG; 오, N.; 글릭먼, JN; Garrett, WS Fusobacterium nucleatum은 IL-17 발현의 대사산물 수용체 의존적 조절을 통해 전염증성 장 미세환경을 유도합니다. 장내 미생물 2021, 13, 1987780. [CrossRef] [PubMed]
75. Malchow, S.; 레벤탈, DS; 이V.; 니시, S.; Socci, ND; Savage, PA Aire는 자가반응성 T 세포를 조절 T 세포 계통으로 유도하여 면역 관용을 강화합니다. 면역 2016, 44, 1102-1113. [상호참조]
76. 양, S.; 후지카도, N.; 콜로딘, D.; 베노이스트, C.; Mathis, D. 면역 관용. 생애 초기에 생성된 조절 T 세포는 자기 관용을 유지하는 데 뚜렷한 역할을 합니다. 과학 2015, 348, 589-594. [상호참조]






