쌀 단백질 가수분해물의 항산화, 미백 및 노화 방지 특성 평가
Mar 19, 2022
연락하다:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Hui-Ju Chen 1,2, Fan-Jhen Dai 2, Cheng-You Chen 3, Siao-Ling Fan 2, Ji-Hong Zheng 4, Yu-Chun Huang 2, Chi-Fai Chau 1, Yung-Sheng Lin 3, 4,5,* 및 Chin-Shuh Chen 1,*
추상적인:식물 유래 단백질 가수분해물은 영양 분야에서 잠재적으로 응용할 수 있습니다. 우수한 단백질 공급원인 쌀 단백질 가수분해물(RPH)은 코스메슈티컬 개발로 주목받고 있습니다. 그러나 RPH 분석의 잠재적인 적용을 보고한 연구는 거의 없으며 이 연구에서는 RPH 분석의 가능성을 조사했습니다.항산화제활성 및 피부 노화 효소의 억제 활성. 결과는 총 페놀 및 플라보노이드 농도가 2.06 ± 0.13 mg 갈산 등가물/g RPH 및 25.96 ± 0.52μg 케르세틴 등가물/g RPH, 각기. RPH는 1,{10}}디페닐{11}피크릴히드라질[최대 억제 농도(IC50)=42.58 ± 2.1 mg/g RPH] 및 2에서 자유 라디칼 소거에 대한 용량 의존적 활성을 나타냈습니다. ,{19}}아지노비스({21}}에틸벤조티아졸린{22}}설폰산)(IC{23}}.11 ± 0.88 mg/g RPHs), 용량 의존적 감소 용량(6.95 ± 1.40 mg 비타민 C 등가물/g RPH) 및 산소 라디칼 흡광도(473 µmol Trolox 등가물/g RPH). 히알루로니다아제의 50% 억제를 달성하는 데 필요한 RPH 용액의 농도 및티로시나제활성은 각각 8.91 및 107.6 mg/mL로 측정되었습니다. 이 연구는 RPH가항산화제,항히알루로니다제 및 항티로시나제 활성은 미래의 화장품 응용 분야에 사용됩니다.
키워드:쌀 단백질 가수분해물;항산화제; 히알루로니다제;티로시나제; 화장품

1. 소개
자외선 노출은 광노화(또는 외부 노화)의 원인이 됩니다. 대조적으로, 세포 대사에서 생성되는 활성 산소종과 생물학적 기능의 저하가 내인성 노화의 원인이 됩니다[1,2]. 가공 식품에는 종종 천연항산화제카테킨, 아스코르브산, 토코페롤, 로즈마린산, 다양한 식물의 페놀 추출물 등. 천연 항산화제에 대한 연구는 이제 비전통적인 출처를 고려합니다. 자연산항산화제화학적으로 생산된 것보다 더 바람직하다항산화제일부 합성 항산화제가 발암성으로 보고되었기 때문입니다[3]. 쌀(Oryza sativa)은 전 세계 사람들, 특히 아시아에 사는 사람들의 주요 식단입니다. 전 세계의 연간 쌀 생산량은 약 7억 4,100만 톤입니다[4]. 아시아 국가에서 쌀은 20억 명이 넘는 사람들이 섭취하는 에너지의 75%를 차지하는 것으로 알려져 있습니다[5]. 광범위한 쌀 생산은 그에 상응하는 부산물 생산으로 이어집니다. 쌀 생산 과정에서 남은 제품은 곡물 단백질의 대부분(~60-85%)을 포함하지만 버려지거나 동물 먹이로 사용됩니다[6-8]. 다양한 단백질 가수분해물에서 얻은 펩티드가 잠재적으로 작용한다고 보고됨항산화제[9]. 따라서 천연 및 무독성 항산화제는 식품 단백질 가수분해물에서 잠재적으로 추출될 수 있습니다. 많은 학자들이 지질이 풍부한 모델을 사용하고 단백질 가수분해물과 우유, 제인, 대두 단백질 펩타이드가 자유 라디칼 소거, 음식 및 시험관 내 지질 과산화 억제, 전이 금속의 킬레이트화를 비롯한 중요한 항산화 특성을 가지고 있다고 보고했습니다. 12].
히알루론산(HA)은 점도를 높이고 수분을 함유하며 세포외액의 투과성을 낮추기 때문에 피부를 젊어지게 합니다. HA는 우수한 수분 보유력으로 피부의 젊음, 보습 및 부드러움을 증가시키고 주름의 정도를 감소시킵니다[13,14]. 불행히도 피부의 HA 수치는 나이가 들면서 자연적으로 감소합니다. Hyaluronidase는 HA를 파괴하는 효소로 피부의 힘, 유연성, 수분의 손실을 초래하여 피부 노화를 유발한다. 따라서 hyaluronidase를 억제하고 피부의 HA 함량을 유지하여 주름을 치료할 수 있다[15,16]. 멜라닌 생성 효소티로시나제멜라닌이 생성되는 과정의 속도 제한 단계에 결정적으로 기여합니다. 따라서 색소 침착 장애는 일반적으로 치료되며 피부 미백은 억제 또는 하향 조절하여 달성됩니다.티로시나제활동 [17,18].
여러 연구에서 곡물 단백질 가수분해물과 이들로부터 얻을 수 있는 펩타이드는 항산화, 항고혈압 및 항종양 활성을 갖는 것으로 밝혀졌습니다[19,20]. 식품 유래 펩타이드 및 단백질의 인간 건강에 대한 긍정적인 기여가 점차 인식되고 있습니다[21]. 소비자들은 점점 더 화장품 및 건강 관리 산업이 천연 생리 활성 화합물을 사용하도록 요구하고 있습니다. 쌀 단백질 가수분해물(RPH)은 우수한 단백질 공급원으로 주목받고 있습니다. 그러나 RPH의 특성화 및 기능 분석을 보고한 연구는 거의 없습니다. 따라서 본 연구에서는 항산화 활성과 hyaluronidase를 평가하고,티로시나제- RPHs의 억제 활동.
2. 결과 및 논의
2.1. 총 페놀 농도(TPC) 및 총 플라보노이드 함량(TFC)
TPC 분석의 표준은 여러 농도의 갈산이었습니다. 더 높은 흡광도는 더 높은 TPC를 나타냅니다. RPH 시료의 TPC는 RPH 시료의 흡광도 값을 갈산 검량선에 입력하여 구하였다. 페놀 농도에 대한 RPH 농도를 플롯팅하면(그림 1a), 2.{3}}6 ± 0.13 mg GAE/g RPH의 평균 TPC가 얻어졌습니다. 25.96 ± 0.52 µg QE/gRPHs의 TFC는 유사한 절차에 따라 얻어졌습니다(그림 1b). 그림 1c는 추가로 RPH 샘플의 TPC 및 TFC에 관한 것입니다. TPC와 TFC 사이의 관계는 y=0.0121x + 0.0659로 표현될 수 있음을 보여줍니다. 여기서 x와 y는 각각 TPC와 TFC입니다.
RPH의 TPC에는 페놀성 아미노산 및 펩티드의 페놀성 화합물의 농도가 포함되었습니다. 단백질-페놀 화합물 상호작용은 일반적으로 공유 및 비공유 결합을 포함합니다. 페놀 화합물은 효소 가수분해 중에 방출됩니다. 특정 효소는 단백질-폴리페놀 복합체를 가장 잘 파괴할 수 있으며, 이로 인해 티로신과 같은 페놀 그룹이 있는 더 많은 수의 페놀 화합물 및 펩티드가 방출됩니다[22]. 곡물의 총 폴리페놀 함량과 생물학적 활성 사이에는 강한 상관관계가 있는 것으로 보고되었습니다. 폴리페놀은 강력한 항산화 활성을 갖는 것으로 잘 알려져 있습니다[23]. 적은 양으로 발견되지만 쌀에 있는 테르펜[24] orsesquiterpenes[25]도 항산화 활성에 기여할 수 있습니다.
2.2. 항산화 활성
2.2.1. DPPH 자유 라디칼의 라디칼 소거 활성
그림 2는 RPH 용액에서 DPPH 자유 라디칼 소거 활성을 보여줍니다. 용액의 농도가 높을수록 활성이 더 높은 것으로 밝혀졌습니다. 모든 DPPH 자유 라디칼의 절반을 소거할 수 있는 추출물 농도인 최대 억제 농도의 절반(IC50)은 쌀 펩타이드 42.58 ± 2.1 mg/mL였습니다.
2.2.2. ABTS 자유 라디칼의 소거 활동
그림 3에 나와 있는 RPH의 ABTS 자유 라디칼 소거 활성은 추출물 농도가 높을수록 더 높았습니다. IC5{4}}는 쌀 펩타이드의 2.11 ± 0.88 mg/mL였습니다. 이 결과는 RPH가 강력한 ABTS 자유 라디칼 소거 활성을 가짐을 나타냅니다. Met 및 Cys를 포함한 황 함유 아미노산과 Ala, Val, Ile, Leu, Met, Cys, Tyr, Phe, Try 및 Pro를 포함한 소수성 아미노산은 ABTS 자유 라디칼과 관련하여 중요한 요소일 수 있습니다. 청소 활동.

본 연구에서 ABTS 자유 라디칼 소거 활성의 IC50 값은 DPPH 자유 라디칼 소거 활성보다 낮아 Jatropha curcas L. 종자 껍질 및 커널 [28] 및 대추 열매 종자 및 껍질 펄프 [29]의 결과와 일치합니다. 이 발견은 또한 DPPH 자유 라디칼 소거 활성 및 ABTS 자유 라디칼 소거 활성에 대해 각각 43.98-66.25 µmoL Trolox equivalent/g 샘플과 403.28-430.12 µmoL Trolox equivalent/g 샘플을 가진 쌀겨 단백질 가수분해물의 보고와 일치합니다[27].
한 가지 가능한 이유는 DPPH 자유 라디칼(유용성)과 ABTS 자유 라디칼(지용성/수용성) 간의 용해도 차이입니다[30,31]. 쌀겨 단백질 가수분해물의 항산화 잠재력은 분자량 프로파일, 아미노산 조성 및 소수성에 의해 영향을 받았다[32].
2.2.3. 감소 용량
RPH에 대한 감소 용량 분석 결과는 그림 4에 나와 있습니다. RPH 농도에 따라 감소 용량이 증가했습니다. 감소 용량은 6.95 ± 1.40 mg VCE/g RPH로, RPH가 효과적인 항산화제임을 나타냅니다.
2.2.4. 산소 라디칼 흡광도(ORAC)
ORAC 분석은 생리학적 산화제에 대한 유사한 반응 메커니즘 및 산화환원 잠재력을 갖는 과산화 라디칼인 반응물을 포함하여 항산화 활성 측정에 대한 다른 접근 방식에 비해 장점이 있습니다. 전체 전하와 양성자 상태항산화제인체의 반응과 유사합니다[33]. ORAC 방법은 또한 인체에서 항산화제의 효능과 생물학적 관련성이 있습니다. 그림 5는 다양한 농도의 RPH 및 Trolox 표준에 대한 ORAC 분석 결과를 보여줍니다. ORAC는 순 AUC와 Trolox 농도를 관련시키는 보정 곡선의 회귀 방정식에서 파생되었습니다. 결과는 RPH가 473 µmol TE/g RPH의 ORAC를 나타냄을 나타냅니다.
항산화 펩타이드 또는 아미노산은 효소적 단백질 가수분해에 의해 얻어질 수 있으며, 그 결과 산화제에 대한 활성이 높다[34]. 생물학적 활성 펩타이드의 금속 이온 킬레이트화, 지질 과산화 억제 및 자유 라디칼 소거는 항산화 활성의 원인입니다. 자유 라디칼은 억제될 수 있고 산화 스트레스 감소 단백질과 효소의 발현은 항산화 펩타이드에 의해 상향 조절될 수 있습니다. 단백질 가수분해물 및 펩타이드의 항산화 효능은 가수분해 조건, 단백질 공급원 및 프로테아제 유형에 영향을 받는 아미노산의 서열 및 펩타이드의 크기에 의존하는 것으로 보고되고 있다[35]. Adebiyi et al. 소화 가능한 가장 큰 쌀겨 단백질은 subtilisin에 의해 더 작은 조각으로 쪼개질 수 있으며, 그 결과 단백질 수율과 함량이 높아집니다. 가수분해물의 TPC와 항산화 활성은 효소의 특이성에 의해 영향을 받을 수 있습니다. 따라서 펩타이드의 항산화 활성은 단백질 공급원의 특성, 효소의 특이성, 가수분해 정도에 의해 영향을 받을 수 있다[37].

식물 유래 단백질을 가수분해하여 항산화 펩티드를 얻기 위해 프로테아제(예: 알칼라제, 바실러스 종의 서브틸리신 A의 상품명)를 사용하는 보고가 많이 있습니다. 이와 관련하여 대두 단백질은 가장 많이 보고된 단백질 중 하나이다[38]. 또한, 쌀겨 단백질의 알칼라아제 가수분해도 발견됩니다. 최적의 조건에서 찹쌀의 알칼라아제 가수분해는 DPPH 자유 라디칼 소거에서 IC50 값이 0.87 ± 0.02 mg/mL인 단백질 가수분해물을 생성했습니다[39]. 우리 연구에서 RPH의 IC50 값은 42.58 ± 2.1 mg/mL였습니다. 이 연구에서 DPPH 자유 라디칼 소거의 IC50 값은 쌀겨 단백질만큼 효과적이지 않았지만 ABTS 자유 라디칼 소거(IC{14}}.11 mg/mL)는 Alcalase가수분해로 얻은 대두 단백질 가수분해물보다 더 효과적이었습니다( IC{16}}.93 mg/mL) [40].
2.3. 히알루로니다제 저해 활성
단백질 분해 효소인 hyaluronidase는 진피에서 발견되며 세포외 기질에서 HA의 분해를 촉매합니다[41]. 이 연구는 비교 목적을 위해 양성 대조군으로 탄닌산을 사용했습니다. 도 6은 탄닌산이 더 높은 히알루로니다제 활성 억제를 갖는다는 것을 나타내고; IC50는 0.14 mg/mL로 Nishida 등이 얻은 값과 유사합니다. (0.121 mg/mL; 71.1 mM) [42]. 대조적으로, 8.91 mg/mL의 IC50이 RPH 용액에 대해 계산되었습니다. RPH 용액의 이 결과는 우리의 이전 IC50 값인 7.61 mg/mL에 해당합니다[43]. 단백질, 다당류, 식물 유래 및 합성 화합물은 히알루로니다제 억제제가 존재하는 화합물 범위에 속합니다. 이러한 억제제는 HA 합성-분해 균형을 유지하는 데 도움이 됩니다[44]. 피부의 낮은 HA 농도는 건조함과 주름을 유발합니다. 따라서 히알루로니다제 활성의 억제는 피부의 형태를 개선하고 노화를 지연시키는 경로이다.
2.4. 티로시나제 억제 활성
천연 공급원의 단백질 가수분해물은티로시나제 활성. 체외 tyrosinase 억제 시험은 일반적으로 피부 미백제가 tyrosinase 활성에 직접적인 영향을 미치는지를 평가하는 데 사용됩니다[45]. 멜라닌 합성 속도 제한 단계에 참여함으로써 티로시나아제는 L-티로신 하이드록실화를 L-DOPA로 촉매한 다음 후자를 o-도파퀴논으로 산화시킵니다. 멜라닌의 생합성을 방지하는 것이 바람직할 때 L-티로시나제 활성의 억제가 중요할 수 있습니다. 여기,티로시나제RPH 항티로시나제 활성을 측정하는 데 사용되었습니다. 그림 7에서 볼 수 있듯이1{7}}7.6mg/mL 농도는 티로시나제 활성을 50% 억제했습니다. Ascorbic acid는 Seo et al.의 0.102 mg/mL와 유사한 높은 티로시나제 억제 활성(IC{5}}.098 mg/mL)을 나타냈습니다. 보고되었다[46].
쌀겨 단백질 가수분해물은티로시나제-억제 활동 [47,48]. RPH 용액의 티로시나제 억제 활성은 펩타이드의 아미노산 프로파일에서 기인할 수 있습니다. Schurink et al. 효과적이라고 설명티로시나제-억제 펩티드는 아르기닌 잔기와 페닐알라닌으로 구성됩니다[49]. Tyrosinase 억제 활성은 소수성 아미노산 잔기(예: 알라닌)에 의해 향상될 수 있으며, 멜라닌 생성은 알라닌에 의해 중단될 수 있습니다[50]. 게다가 Zhang et al. 또한 쌀 단백질 가수분해물이 UVB 유도 세포 모델에서 멜라닌 함량과 티로시나아제 활성을 감소시킬 수 있다고 보고했습니다[51].

시스탄체 보디빌딩
2.5. RPH의 아미노산 프로필 및 MW
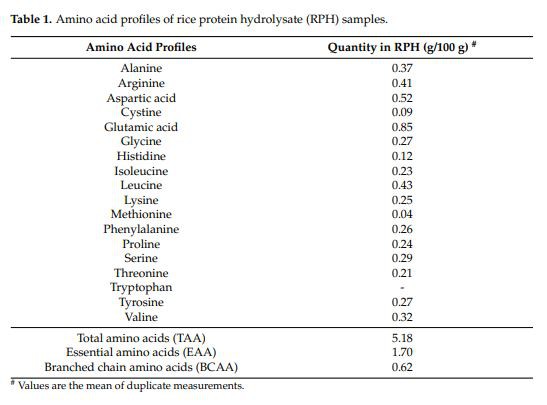
본 연구에서 전분 제거 후 쌀의 단백질 함량은 23.56중량%였고, 단백질 분해효소에 의해 가수분해된 시료의 가수분해도는 9.36%였다. RPH의 아미노산 조성은 Table 1과 같다. 샘플에서 각 100g에는 5.18g의 아미노산이 포함되어 있습니다. 아미노산 성분과 관련하여 RPH는 알라닌, 류신, 아르기닌, 글루탐산 및 아스파라긴산이 풍부하였다. 시료 100g에는 소수성 아미노산(알라닌, 발린, 류신, 이소류신, 프롤린, 페닐알라닌, 시스테인)이 총 1.73g 포함되어 있습니다. 이 결과는 전분 제거를 위한 아밀라아제 용액 및 처리 온도에서 우리의 이전 보고서[43]와 완전히 달랐다. 소수성 아미노산의 함량은 이전 보고서보다 1.90배 높았습니다. 본 연구에서 낮은 처리 온도(60℃)는 단백질의 변성을 다량으로 방지하여 아미노산의 활성을 더 잘 보존할 수 있다. 또한 백미의 전분을 당화하는 다른 곰팡이 아밀라아제와 글루코아밀라아제에서도 유사한 결론을 얻을 수 있다[52].
연구에 따르면 소수성 아미노산이항산화제다양한 단백질 공급원의 단백질 가수분해물 및 펩타이드에서 지질 기반 용해도를 높여 자유 라디칼과의 상호 작용을 촉진합니다[38,53]. 일부 아미노산은 Chen et al. [54] 일반적으로항산화제; 언급된 산에는 트립토판, 시스테인, 메티오닌, 티로신 및 히스티딘이 포함됩니다. 본 연구에서 방향족 아미노산(페닐알라닌, 티로신 및 트립토판)은 0.53g/100g RPH를 구성했습니다. 따라서 이러한 펩타이드 유래 아미노산은 아마도 RPH의 항산화 활성에 대한 책임이 있을 것입니다.
또한, 더 짧은 펩타이드로 가수분해된 단백질은 MW분포가 다르며 완전한 천연단백질 분자의 내부에 접힌 소수성 그룹은 일반적으로 수상에 노출됩니다. 이것은 단백질 분자가 구조적으로 재배열되고 따라서 단백질의 기능적 특성과 관련이 있습니다[55,56]. tricine-SDS-PAGE 데이터는 RPH의 MW가 5-35kDa 범위에 있음을 나타냅니다(그림 8a).
그림 8b는 RPH에서 다양한 MW의 상대적 함량을 보여줍니다. 전체적으로, 전체 단백질의 45.24%가 메인 밴드에 있었습니다(MW ≈ 2.4 kDa). 쌀겨 단백질 가수분해물의 펩타이드에 대해서도 유사한 결과가 얻어졌다. Thamnarathip et al.에 의해 얻은 가장 높은 항산화 활성. [37] MW=6-50 kDa의 펩타이드에 대한 것이었습니다. 또한, 단백질 가수분해물의 기능과 MW 분포 및 아미노산 조성 사이에는 관계가 존재한다[57]. 이것은 본 연구에서 관찰된 RPH의 항산화 활성을 설명합니다.
2.6. 세포독성시험
향후 적용을 위해서는 낮은 세포 독성이 필요합니다. RPH의 세포독성 및 생체적합성을 평가하기 위해 RPH 용액에서 raw 264.7 세포의 세포 생존력을 MTT 방법을 통해 측정했습니다. 그림 9에서 볼 수 있듯이 24시간과 48시간 동안 25-2000μg/mL RPH로 처리했을 때 세포 생존율은 100% 이상이었습니다. 결과는 RPH의 현저하게 낮은 세포독성을 나타냅니다. 따라서 RPH는 세포 독성이 매우 낮은 화장품 용도로 잠재적으로 사용될 수 있습니다.
3. 재료 및 방법
3.1. 시약
염화철(III), 2,20-아지노비스(3-에틸벤조티아졸린-6-술폰산)(ABTS), Trolox(6-히드록시-2,5 ,7,8-테트라메틸크로만{10}}카르복실산), l{11}},{12}}디히드록시페닐알라닌(L-DOPA), 1,{15}}디페닐{16}} picrylhydrazyl (DPPH) 및 trichloroacetic acid는 Alfa Aesar (Tewksbury, MA, USA)에서 구입했습니다. 2,{18}}아조비스({19}}메틸프로피온아미딘) 이염산염(AAPH), Folin–Ciocalteu의 페놀 시약, 갈산, 아스코르브산, 버섯티로시나제및 플루오레세인 나트륨은 Sigma-Aldrich(St. Louis, MO, USA)에서 구입했습니다. 탄산나트륨은 Riedel-de Haën(Seelze, Germany)에서 구입했습니다. 마지막으로, 칼륨 페리시안화물, 인산수소나트륨 및 인산이수소나트륨은 Showa Chemical(Tokyo, Japan)로부터 입수하였다.
3.2. RPH의 준비
RPH는 고온에서 세균성 아밀라아제 가수분해로 인한 아미노산 손상을 방지하기 위해 쌀가루의 전분을 당화하기 위해 곰팡이 아밀라아제를 채택한 것을 제외하고는 이전에 설명한 대로 준비했습니다[43,58]. 100g의 쌀가루를 0.5%의 곰팡이 아밀라아제(Genencor, NY, USA)를 함유한 1{3}}00mL의 증류수에 담그고 혼합물을 60℃까지 24시간 동안 가열했습니다( pH 4.2), 그 후 실온으로 냉각되도록 하였다. 나머지 상층액을 제거하기 위해 1968×g에서 10분 동안 원심분리를 수행하였다. 20-배수와 2mL의 0.1% 가수분해 프로테아제(Healthmate, Changhua, Taiwan)를 불용성 부분에 첨가한 후 용액을 흔들고 55℃에서 4시간 동안 배양했습니다. 용액의 pH를 최적의 수준으로 유지하기 위해 pH-stat 방법을 사용하고 효소 불활성화를 위해 85℃에서 10분간 가열하였다. 나머지 불용성 분획을 3075×g에서 15분 동안 원심분리를 통해 제거하였다. 상층액에 대해 동결건조를 수행한 후 사용하기 전에 -20℃에서 보관하였다.
3.3. RPH의 항산화 활성
3.3.1. 총 페놀 농도(TPC)
RPH의 TPC를 알아내기 위한 Folin-Ciocalteu 방법이 사용되었습니다[59]. 먼저 Folin-Ciocalteu의 페놀 시약(0.3M) 2{{2}0μL를 200과{4}}분 동안 흔들어 균일하게 혼합했습니다. RPH 용액의 μL 및 이 혼합물에 400 μL의 탈이온수 및 200 μL의 10%(w/v) 탄산나트륨 용액을 첨가했습니다. 혼합 용액은 실온의 어둠 속에서 60분 동안 배양되었습니다. 그런 다음 3000 rpm에서 15분 동안 원심분리했습니다. 측정에는 100μL의 상청액이 사용되었습니다. 건조 RPH 샘플(단위: mg GAE/g RPHs)당 갈산 당량(GAE)의 TPC(단위: mg)를 결정하기 위해 광 흡광도 데이터를 갈산을 나타내는 표준 곡선에 입력했습니다. EpochMicroplate Spectrophotometer(BioTek, VT, USA)를 사용하여 700 nm에서 흡광도를 얻었다.
3.3.2. 총 플라보노이드 함량(TFC)
TFC는 Wathoni et al.의 접근에 따라 얻어졌습니다. 약간의 수정 [60]. 먼저, 각 샘플 500μL와 2%(w/v) 염화알루미늄 용액을 혼합했습니다. 반응액을 충분히 혼합하여 10분간 방치한 후 흡광도 415 nm를 평가하였다. 결과는 건조 RPH 샘플의 그램당 케르세틴 등가물(QE)의 마이크로그램으로 보고됩니다(µg QE/g RPH).

시스탄체 보디빌딩
3.3.3. DPPH 자유 라디칼 소거 활성
먼저 198 μM DPPH 에탄올 용액(50 μL)과 RPH 용액 또는 탈이온수(각각 0.5 μL; 시료와 대조군)를 혼합한 다음 실온에서 암실에서 30분간 방치하였다. 517 nm에서 용액의 흡광도를 연속적으로 얻었다. 샘플과 대조군 사이의 흡광도 차이를 결정하여 상대적 소거 활성을 계산했습니다. 높은 DPPH 자유 라디칼 소거 활성은 낮은 광 흡광도에 의해 반영되었습니다. RPH 용액의 DPPH 자유 라디칼 소거 활성 평가에서 사용된 표준은 비타민 C[61-63]였습니다.
3.3.4. ABTS 자유 라디칼의 소거 활동
Wu et al.이 보고한 접근 방식. RPH 용액의 항산화 활성을 평가하기 위해 사용되었다[64]. 먼저, 7mM ABTS 스톡 용액(250μL)을 2.45mM 과황산칼륨(25{13}} μL)과 반응시켜 ABTS 자유 라디칼 양이온(ABTS• plus)을 생성하고 혼합물을 유지했습니다. 사용하기 전에 어둠 속에서 4 oC에서 16시간 동안. 실온의 어둠 속에서 평형화한 후, 0.1 M 인산염 완충 식염수(PBS, pH 7.4)를 사용하여 용액을 734 nm에서 0.70 ± 0.02 흡광도로 희석했습니다. 그 다음, 희석된 ABTS 용액 180μL에 Trolox(양성대조군) 또는 RPH 용액(샘플) 20μL를 첨가하였다. 그런 다음 혼합물을 실온에서 10분 동안 인큐베이션했습니다. 이 연구는 734 nm에서 흡광도를 측정했습니다. 더 낮은 흡광도는 더 높은 ABTS 자유 라디칼 소거 활성에 해당합니다. RPHsolution의 ABTS 자유 라디칼 소거 활성을 평가하는 데 사용된 표준은 항산화제 Trolox였습니다.
3.3.5. 감소 용량
제2철 환원 항산화력 분석은 RPHsolution의 총 항산화 활성을 결정하기 위해 사용되었습니다. Lin et al. [29], RPH 용액(200 μL)을 1%(w/v) K3Fe(CN)6 및 0.2M PBS 버퍼(pH 6.6, 각각 100μL)와 균일하게 혼합했습니다. .20분 동안 50℃ 수조를 사용하여 혼합물을 가열했습니다. 욕에서 혼합물을 제거한 후, 3분 동안 빠르게 냉각시켰다. 이어서, 10%(w/v) 트리클로로아세트산(100μL)을 첨가하고 3000rpm에서 10-분 원심분리를 수행했습니다. 이어서 상등액(400μL)을 추출하고 0과 균일하게 혼합했습니다. 1%(w/v) FeCl3(100µL) 및 탈이온수(400µL). Fe4[Fe(CN)6]3는 이 혼합물을 어둠 속에서{27}}최소 반응을 통해 얻었다. 그 후, 광 흡광도(700 nm에서 측정)가 높을수록 환원능이 높음을 나타냅니다. 표준 비타민 C를 사용하여 RPH 그램당 비타민 C 등가물(VCE) 함량을 결정했습니다.
3.3.6. 산소 라디칼 흡광도(ORAC)
본 연구는 이전에 보고된 방법을 수정하여 ORAC를 얻었다[65]. RPH 샘플을 증류수에 용해한 후 RPH 용액(50μL)을 96-웰 마이크로타이터 플레이트에서 플루오레세인(10μM)과 혼합했습니다. 용액은 37℃에서 15-분 인큐베이션한 후 50μL의 AAPH(500mM)를 첨가했습니다. 5분마다 그리고 총 120분에 걸쳐 형광이 기록되었습니다(각각 λex 및 λem{10}} 및 528 nm). RPH의 항산화 능력은 곡선 아래 면적(AUC)을 계산하여 형광 붕괴 동역학에서 발견되었습니다. ). RPH ORAC를 계산할 때 표준은 15–250 µM Trolox였습니다. ORAC는 건조 RPH 샘플의 1g당 Trolox 등가물(TE)의 마이크로몰(μmol TE/g RPH)로 보고됩니다.
3.4. 히알루로니다제 저해 활성
히알루로니다제 억제 테스트는 {{0}well microplate와 이전에 보고된 방법을 약간 수정하여 수행했습니다[4{15}}]. N-아세틸글루코사민은 히알루로니다제를 HA 기질과 반응시켜 방출되었다. 억제제의 존재하에서 N-아세틸글루코사민 방출은 감소되었으며, 이 방출은 600-nm 흡광도를 획득함으로써 검출되었습니다. HA는 0.1M 아세테이트 완충액(pH 3.9) 및 소 혈청 알부민(1mg/mL)으로 구성된 산성 알부민 용액으로 침전되었습니다. 샘플 용액과 5 mg/mL hyaluronidase는 37 ºC에서 20-분 배양되었습니다. 인큐베이션 혼합물에 HA(1{{20}}0 μL; 0.1 M 아세테이트 완충액 중 5.0 mg/mL)를 후속적으로 첨가했습니다. 37℃에서 40분 동안 추가 배양을 수행했습니다. 0.1mL 0.4M 알칼리성 붕산염 용액을 첨가하여 효소 반응을 중단시켰다.
3.5. 티로시나제 억제 활성
본 연구는 이전에 보고된 수정된 프로토콜을 사용하여 RPH의 항티로시나제 활성을 평가했습니다[66]. 효소 용액(135 U/mL)은 티로시나제를 20mM 인산 완충액(pH 6.8)에 용해시켜 제조하였다. 또한, 1.25mM L-DOPA 용액 준비를 위해 DIwater를 사용했습니다. 그런 다음 40μL의 다양한 농도의 RPH 시료 용액을 40μL의 티로시나아제 용액과 120μL의 L-DOPA 용액과 혼합했습니다. 30분 동안 이 혼합물을 37℃에서 유지하여 RPHs의티로시나제활동. 분광광도계(FLUOstar Omega MicroplateReader, BMG Labtech GmbH, Germany)를 사용하여 475-nm 흡광도를 얻었습니다. 모든 측정은 3회 수행되었습니다. 해당 그룹의 흡광도는티로시나제존재하지 않음을 뺀 것입니다. 효소 억제율은 다음과 같이 결정되었다.
3.6. RPH의 특성화
3.6.1. 아미노산 프로필
이 연구는 RPH의 아미노산 구성을 발견했습니다. 먼저, 115℃에서 24시간 동안 4M 메탄설폰산을 사용하여 진공 밀봉된 튜브의 샘플을 가수분해했습니다. 2개의 Waters 510 용매 전달 시스템과 아미노산 분석기(L 8900; Hitachi, Tokyo, Japan)는 25m 측정 aSpherisorb ODS2 컬럼에서 유도체화된 아미노산 분리를 위해 사용되었습니다. × 64.6mm. 이 연구에서는 (a) 아세트산나트륨(0.14M) 및 트리에틸아민(850μL/L, pH 5.6) 및 (b) 60% 아세토니트릴(2분 동안 기울기가 0%인 용매)을 사용했습니다. 15.5분 동안 0-42%(볼록 곡선), 4분 동안 100%. 254 nm에서 아미노산 프로파일을 측정하기 위해 중복 샘플을 채취했습니다[67,68].
3.6.2. 단백질의 분자량(MW)
Schägger의 방법[69]에 따라 환원 조건에서 이 연구는 약간의 수정을 가하여 트리신-나트륨 도데실 설페이트(SDS)-폴리아크릴아미드겔 전기영동(PAGE)을 통해 MW 분포를 얻었습니다. 샘플 버퍼(30 g/L SDS, 0.375 MTris-HCl, 0.125 g/L Coomassie Brilliant Blue G-250 및 75 g/ L 글리세롤, pH 7)을 사용하여 동결 건조된 샘플을 분산시키고 원심분리를 수행한 다음 로딩 전에 수행했습니다. 총 20μL의 2-머캅토에탄올을 1mL의 트리신-SDS-PAGE 샘플에 첨가했습니다. 샘플을 90초 동안 100℃에서 가열하였다. microsyringe를 이용하여 각 시료와 Unstained Protein Standard Broad Range(Bio-Rad Laboratories, Germany)를 시료 웰에 로딩하였다. 그런 다음, 전체 샘플이 스태킹 겔 내에 포함될 때까지 일정한 30mV에서 전기영동을 수행한 다음 일정한 100mV에서 완료될 때까지 전기영동을 수행했습니다. 이어서 0.02% Coomassie Brilliant Blue R{23}} 용액을 젤 염색에 적용했습니다. 겔의 절대 배경 탈염은 겔을 10% 아세트산에서 밤새 흔들어서 수행했습니다. 마지막으로, 레인의 단백질 밴드를 식별하기 위해 젤 이미지를 분석했습니다. 이 분석은 ImageJ(USNational Institutes of Health, Bethesda, MD, USA)에서 수행되었습니다. 표준 마커를 사용하여 MW를 추정한 보정 곡선을 얻었다. 간단히 말해서, 첫 번째 단계는 분리 젤의 상단에서 각 밴드의 이동 길이(Rf)를 결정하는 것이었습니다. 두 번째 단계는 주어진 MW가 있는 표준 마커에 대해 Rf 및 log(MW)를 사용하여 보정 곡선을 계산하는 것입니다. MW 결정은 RPH에서 단백질 밴드의 Rf를 사용하여 수행되었습니다.
3.7. 세포독성 분석
Raw 264.7 세포는 10% FBS(fetal bovine serum), 4.5g/L Glucose, 1% 항생제 용액(1{33}}0units/ mL 페니실린 및 100μg/mL 스트렙토마이신), 4mM L-글루타민 및 1.5g/중탄산나트륨(37ºC 및 5% CO2에서). RPH에 대한 원시 264.7 세포의 세포 독성은 3-(4,{19}}디메틸티아졸{20}}일)-2,5 디페닐-테트라졸륨 브로마이드(MTT) 증식 분석법으로 측정되었습니다. . 웰당 약 1 × 104세포를 96-웰 플레이트에 플레이팅했습니다. 24시간 후 다양한 농도의 RPH(0–2000 µg/mL)를 세포에 추가했습니다. 24시간 및 48시간 배양 후, 100μL의 MTT 용액(0.5mg/mL)을 첨가했습니다. 현미경으로 관찰했을 때 청색 포마잔결정이 관찰되었다. DMEM을 제거하고 100 μL의 디메틸 설폭사이드(DMSO)를 웰당 첨가했습니다. 흡광도는 마이크로타이터 플레이트 리더를 사용하여 측정하였다. 그런 다음 세포 생존율(%)은 [A570(처리된 세포) - A570(배경)] / [A570(미처리된 세포) - A570(배경)] × 100%[70]로 계산되었습니다.
3.8. 통계 분석
각 가수분해물 샘플에 대한 보고서는 3개의 독립적으로 반복된 실험 및 결정의 평균값이었습니다. 평균 ± 표준 편차(SD)로 표현된 결과는 StatisticalAnalysis System(버전 20.0; SPSS, Armonk, NY, USA)을 사용하여 일원 ANOVA 및 Duncan의 사후 검정으로 분석되었습니다. p < 0.05의="" 값은="" 통계적="" 유의성으로="">
4. 결론
이 연구는 RPH의 기능을 조사했습니다. 실험 결과 RPH는 페놀성 화합물과 플라보노이드를 함유하고 있으며 DPPH, ABTS 소거능, 환원능, ORAC 등 다양한 항산화 활성을 나타냈다. 또한, RPHs는 효과적으로 억제티로시나제및 히알루로니다제 활성. 프로테아제는 RPH의 MW 패턴에 영향을 미치는 중요한 요소였습니다. RPH의 분석은 화장품의 성분으로 사용할 수 있는 가능성을 나타냅니다.

시스탄체 보디빌딩
참고문헌
1. Ichihashi, M.; 안도, H.; 요시다, M.; 니키, Y.; Matsui, M. 피부의 광노화. 안티에이징메드. 2009, 6, 46–59. [교차 참조]
2. 김재성; 김디.; 김혜지; 장 A. 당나귀 가죽 젤라틴 가수분해물의 UVB 유발 인간 피부 섬유아세포 광노화에 대한 보호 효과. 프로세스. 바이오켐. 2018, 67, 118–126. [교차 참조]
3. Carocho, M.; Ferreira, IC 항산화제, 산화촉진제 및 관련 논쟁에 대한 검토: 천연 및 합성 화합물, 스크리닝 및 분석 방법론 및 미래 전망. 식품화학 톡시콜. 2013, 51, 15–25. [교차 참조]
4. 구오, X.; Zhang, J.; 5월.; Tian, S. 쌀 잔류물에서 단백질의 제한된 가수분해 최적화 및 제품의 기능적 특성 특성화. J. Food Proc. 보존 2013, 37, 245–253. [교차 참조]
5. 박혜영; Lee, K.-W.; 최 H.-D. 쌀겨 성분: 면역 조절 및 치료 활동. 식품 기능. 2017, 8,935–943. [교차 참조] [PubMed]
6. Zhou, K.; 캐닝, C.; Sun, S. 미생물 프로테아제 및 한외 여과에 의해 제조된 쌀 단백질 가수분해물이 자유 라디칼 및 육류 지질 산화에 미치는 영향. LWT 2013, 50, 331–335. [교차 참조]
7. 피우', LD; 타소니, A.; 세라자네티, DI; 페리, 엠.; 바비니, 이.; Tagliazucchi, D.; Gianotti, A. 쌀 가수분해 단백질로부터 생리활성 펩티드를 생산하기 위한 전분 산업 액체 부산물의 이용. 식품화학 2014, 155, 199–206. [교차 참조]
8. 페리, 엠.; Graen-Heedfeld, J.; Bretz, K.; Guillon, F.; Michelini, E.; 칼라브레타, MM; 람보르기니, M.; Gruarin, N.; Roda, A.; Kraft, A.; et al. 환경 친화적인 공정을 통해 쌀 부산물에서 얻은 펩티드 분획은 In VitroHealth 관련 생체 활성을 보여줍니다. 플로스 원 2017, 12, e0170954. [교차 참조]
9. 웬, C.; Zhang, J.; Zhang, H.; 두안, Y.; Ma, H. 식물성 단백질 유래 항산화 펩타이드: 식품 시스템에서의 분리, 식별, 작용 기전 및 적용: 검토. 트렌드 식품 과학. 기술. 2020, 105, 308–322. [교차 참조]
10. Phelan, M.; Aherne, A.; 피츠제럴드, RJ; O'Brien, NM 카제인 유래 생리 활성 펩티드: 생물학적 효과, 산업적 용도, 안전 측면 및 규제 상태. 국제 Dairy J. 2009, 19, 643–654. [교차 참조]
11. Udenigwe, CC; Aluko, RE 식품 단백질 유래 생리활성 펩타이드: 생산, 가공 및 잠재적인 건강상의 이점. J. 식품 과학. 2012, 77, 11–24. [교차 참조] [PubMed]
12. Fardet, A.; Rock, E. 우유, 요구르트, 발효유 및 치즈의 시험관 내 및 생체 내 항산화 가능성: 증거의 서술적 검토. 뉴트르. 해상도 개정판 2018, 31, 52–70. [교차 참조]
13. 리치, JB; 캐서린, AB; 찰스, WPJ; Christine, ES 광가교 히알루론산 하이드로겔: 천연 생분해성 조직 공학 스캐폴드. 생명공학. 바이오엔. 2003, 82, 578–589. [교차 참조]
14. Jegasothy, SM; Zabolotniaia, V.; Bielfeldt, S. 인간의 새로운 국소 나노 히알루론산 효능. J. 클린. 에스테틱.더마톨. 2014, 7, 27–29.
15. Ndlovu, G.; Fouch, G.; Tselanyan, M.; 코디어, 더블유.; Steenkamp, V. 4남부 아프리카 약용 식물의 노화 방지 잠재력에 대한 시험관 내 결정. BMC 보완. 대체. 메드. 2013, 13, 304. [교차참조]
16. Jiratchayamaethasakul, C.; 딩, Y.; 황오.; 임, S.-T.; 장영; 명승우; 이재엠; 김혜수; 고에스씨.; Lee, S.-H.신규 코스메슈티컬에 대한 22가지 염생식물 추출물의 엘라스타제, 콜라게나제, 히알루로니다제 및 티로시나제 억제 및 항산화 활성의 시험관내 스크리닝. 생선. 아쿠아. 과학. 2020, 23, 1–9. [교차 참조]
17. 강엠.; 박성희; 오, SW; 이세; 유재아; 노, YH; 이에스; 한학사; 조재영; Lee, J. 레조르시놀의 멜라닌 생성 억제 효과는 cAMP 신호 전달의 억제와 p38 MAPK 신호 전달의 활성화에 의해 매개됩니다. 생명과학. 생명공학. Biochem.2018, 82, 1188-1196. [교차 참조]
18. Chatatikun, M.; Yamauchi, T.; Yamasaki, K.; 아이바, 에스.; Chiabchalard, A. -MSH 자극 B16F10 세포에서 Croton roxburghii 및 Crotonsublyratus 잎의 항멜라닌 생성 효과. J. 전통. 보어. 메드. 2019, 9, 66–72. [교차 참조] [PubMed]
19. 리젤로, CG; Nionelli, L.; Coda, R.; Gobbetti, M. Sourdough 발효 중 젖산 박테리아에 의한 암 예방 펩티드 Lunasin의 합성. 뉴트르. 암 2012, 64, 111–120. [교차 참조] [PubMed]
20. 리젤로, CG Tagliazucchi, D.; 바비니, 이.; 루텔라, GS; 사, DLT; Gianotti, A. 식물성 식품 매트릭스의 생리 활성 펩티드: 합성 및 회수를 위한 연구 동향 및 새로운 생명 공학. J. 기능. 식품 2016, 27, 549–569. [교차 참조]
21. 코스쿠에타, ER; 캄포스, DA; 오소리오, H.; 네를리, BB; Pintado, M. 효소적 콩 단백질 가수분해: 생체 기능 식품 성분 생산을 위한 도구. 식품화학 X 2019, 1, 100006. [교차 참조]
22. Aydemir, LY; Yemenicioglu, A. 펄스의 단백질 결합 페놀 항산화제는 빙산의 보이지 않는 부분입니까? 제이 플랜트. Biochem.Physiol. 2013, 1, 1–3. [교차 참조]
23. 황, SH; Ng, LT 대만의 일부 상업용 쌀 품종의 폴리페놀 함량 및 생리 활성 성분의 정량화. J. Food Compos. 항문. 2012, 26, 122–127. [교차 참조]
24. Yoshitomi, K.; 다니구치, S.; 다나카, K.; 우지, Y.; 아키미츠, K.; Gomi, K. Rice terpene synthase 24(OsTPS24)는 쌀 병원체에 대해 항균성 테르피넨을 생성하는 자스모네이트 반응성 모노테르펜 합성효소를 암호화합니다. 제이 플랜트. 생리. 2016, 191,120–126. [교차 참조]
25. Kamolsukyeunyong, W.; 수카켓, W.; Pitija, K.; Thongkham, P.; Mahatheeranont, S.; 투진다, T.; Vanavichit, A. RiceSesquiterpene은 벼의 갈색 매실균에 대한 항염에 중요한 역할을 합니다. 식물 2021, 10, 1049. [CrossRef][PubMed]
26. Liu, Y.; Wang, Z.; 리, H.; Liang, M.; Yang, L. 알칼리도 및 위장 프로테아제 소화에 의해 영향을 받는 쌀 단백질의 시험관내 항산화 활성. J. Sci. 식품 농업. 2016, 96, 4940–4950. [교차 참조] [PubMed]
27. S. 퐁타이; D'Amico, S.; Schoenlechner, R.; Homthawornchoo, W.; Rawdkuen, S. 체외 위장 소화에 의해 자극된 쌀겨 단백질 가수분해물의 분획화 및 항산화 특성. 식품화학 2018, 240, 156–164. [교차 참조][PubMed]
28. 황, S.-L.; 왕 W.-H.; Zhong, X.-Y.; Lin, C.-T.; Lin, W.-S.; Chang, M.-Y.; 린, Y.-S. Jatropha curcas L.Seed Shell 및 Kernel 추출물의 항산화 특성. 적용 과학. 2020, 10, 3279. [교차참조]
29. Lin, Y.-S.; Lin, W.-S.; Tung, J.-W.; Cheng, Y.-C.; Chang, M.-Y.; Chen, C.-Y.; 황, S.-L. 대추 종자 및 껍질 과육의 항산화 능력. 적용 과학. 2020, 10, 6007. [교차참조]
30. Shahi, Z.; SZ 사이드 알랑이; Najafian, L. 가수분해 정도, 전기영동 밴드 및 탈지 Bunium persicum Bioss에서 파생된 가수분해 단백질의 항산화 특성에 대한 효소 유형 및 공정 시간의 영향. 프레스 케이크. Heliyon 2020, 6,e03365. [교차 참조] [PubMed]
31. Xie, H.; 황, J.; 우 MW; Hu, J.; Xiong, H.; Zhao, Q. 쌀 찌꺼기 단백질 가수분해물의 구조적 및 기능적 특성에 대한 저온 및 고온 효소 비활성화의 영향. 식품화학 2021, 345, 128784. [교차참조]
32. 라니, 에스. 푸자, 케이.; Pal, GK 항산화 잠재력에 대한 특별한 참조와 함께 쌀 단백질 가수분해물 및 펩티드 탐색: 생물 활성 측정을 위한 전산 유도 접근법. 트렌드 식품 과학. 기술. 2018, 80, 61–70. [교차 참조]
33. 비스비, RH; 브룩, R.; Navaratnam, S. 산소 라디칼 흡수 능력(ORAC) 분석에서 항산화 산화 전위의 효과. 식품화학 2008, 108, 1002–1007. [교차 참조]
34. 엘리아스, RJ; 켈러비, SS; Decker, E. 단백질 및 펩티드의 항산화 활성. 크리. 식품 과학 목사. 뉴트르. 2008, 48, 430–441.[교차 참조] [PubMed]
35. 광산, Y.; 이찬, 이.; Jiang, B. (Eds.) 기능성 식품 및 기능식품으로서의 생리활성 단백질 및 펩티드; Wiley-Blackwell: Hoboken, NJ, USA, 2010년; 29~42쪽.
36. Adebiyi, AP; 아데비이, AO; 야마시타, J.; 오가와, T.; Muramoto, K. 쌀겨 단백질 가수분해물에서 유래한 항산화 펩티드의 정제 및 특성화. 유로 식품 해상도 기술. 2008, 228, 553–563. [교차 참조]
37. Thamnarathip, P.; 장추, K.; Nitisinprasert, S.; Vardhanabhuti, B. 높은 항산화 활성을 가진 쌀겨단백질 가수분해물의 펩타이드 분자량 확인. J. 시리얼 Sci. 2016, 69, 329–335. [교차 참조]
38. Tacias-Pascacio, VG; Morellon-Sterling, R.; 시어, E.-H.; 타바노, 오.; 베렝게르-무르시아, Á.; Fernandez-Lafuente, R. Alcalasein의 생리 활성 펩티드 생산 사용: 검토. 국제 J. Biol. 마크로몰. 2020, 165, 2143–2196. [교차 참조] [PubMed]
39. Sarringkarin, W.; Laokuldilok, T. 항산화 특성이 있는 찹쌀강 단백질 가수분해물의 생산 조건 최적화. CMU J. Nat. 과학. 2017, 16, 1–18. [교차 참조]
40. Zhang, Q.; 통, X.; 기, 비.; Wang, Z.; 리, Y.; 수이, X.; Jiang, L. 모의 위장 소화 및 경상피 수송 하에서 Alcalase 가수분해 대두 가수분해물의 항산화 활성 변화. J. 기능. 식품 2018, 42, 298–305. [교차 참조]
41. 투, PTB; Tawata, S. Alpinia zerumbet의 두 가지 품종에서 추출한 에센셜 오일의 항산화, 노화 방지 및 멜라닌 생성 방지 특성. 분자 2015, 20, 16723–16740. [교차 참조]
42. Nishida, Y.; Sugahara, S.; 와다, 케이.; 토요히사, D.; 다나카, T.; 오노, M.; Yasuda, S. Scilla scilloides의 구근에서 추출한 에틸 아세테이트 추출물이 lipoxygenase 및 hyaluronidase 활성에 미치는 억제 효과. 제약 바이올. 2014, 52, 1351–1357. [교차 참조]
43. Chen, H.-J.; 다이, F.-J.; 팬, S.-L.; 황, Y.-C.; Chau, C.-F.; Lin, Y.-S.; 첸, C.-S. 쌀(Oryza sativa L.) 단백질 가수분해물에 의한 Hyaluronidase 억제의 동역학. 적용 과학. 2020, 10, 9087. [교차참조]
44. Girish, K.; Kemparaju, K. 마법의 접착제 hyaluronan 및 지우개 hyaluronidase: 생물학적 개요. 생활과학. 2007, 80,1921–1943. [교차 참조] [PubMed]
45. 졸가드리, S.; A. 바라미; 칸, MTH; Munoz-Munoz, J.; 가르시아-몰리나, F.; Garcia-Canovas, F.; Saboury, AA 티로시나제 억제제에 대한 포괄적인 검토. J. 효소. 억제 메드. 화학 2019, 34, 279–309. [교차 참조] [PubMed]
46. 서이제; 홍에스; 최민호; 김, KS; Lee, SJ 쑥 추출물의 항산화 및 피부 미백 효과. 한국어J. 식품 과학. 기술. 2010, 42, 750–754.
47. 오치아이, A.; 다나카, S.; 다나카, T.; Taniguchi, M. 미강 단백질은 Tyrosinase억제 활성이 있는 항멜라닌 생성 펩티드의 강력한 공급원입니다. J. Nat. 찌르다. 2016, 79, 2545–2551. [교차 참조] [PubMed]
48. Kubglomsong, S.; Theerakulkait, C.; 리드, RL; 양엘.; 마이어, CS; Stevens, 가수분해된 쌀겨 유래 알부민에서 티로시나제 억제 및 구리 킬레이트화 펩티드의 JF 분리 및 식별. J. Agric. 식품화학 2018, 66, 8346–8354.[교차 참조]
49. Schurink, M.; 반 버클, WJ; Wichers, H.; Boeriu, CG 티로시나제 억제 활성을 갖는 신규 펩타이드. 펩티드 2007, 28,485–495. [교차 참조]
50. 이시카와, M.; Kawase, I.; Ishii, F. 아미노산 조합은 B16F0 흑색종 세포에서 색소 침착을 감소시킵니다. 바이올. 약.불. 2007, 30, 677–681. [교차 참조] [PubMed]
51. Zhang, R.; 웨이, Y.; 리, 엠.; 카이, 엠.; 구, 알.; 5월.; 첸, 엘.; Wang, J. UVB 유도 인간 표피 멜라닌 세포에 대한 쌀 단백질 가수분해물 및 그 특성 펩타이드 Leu-Leu-Lys, Leu-Pro-Lys 및 pyroGlu-Lys의 멜라닌 생성 효과. 푸드펑크. 2020, 11, 8757–8767. [교차 참조]
52. Wang, Y.; 카이, 디.; 그, 엠.; Wang, Z.; 진, 피.; Tan, T. 당화와 발효를 동시에 하여 백미겨를 이용한 l-락트산의 개방형 발효 생산. 생물자원. 기술. 2015, 198, 664–672. [교차 참조] [PubMed]
53. Pan, M.; 장, TS; Pan, JL 유채 단백질 가수분해물의 항산화 활성. 식품 바이오 프로세스. 기술. 2009, 4, 1144–1152.[교차 참조]
54. 첸, HM; 무라모토, K.; Yamauchi, F.; Nokihara, K. 대두 단백질의 소화물로부터 분리된 항산화 펩티드에 기초한 설계된 펩티드의 항산화 활성. J. Agric. 식품화학 1996, 44, 2619–2623. [교차 참조]
55. Liu, Q.; 공, B.; Xiong, YL; Xia, X. 가수분해 정도에 따른 돼지 혈장 단백질 가수분해물의 항산화 활성 및 기능적 특성. 식품화학 2010, 118, 403–410. [교차 참조]
56. Lemes, A.; 살라, 엘.; 광석, JDC; 브라가, ARC; 에게아, MB; Fernandes, KF 단백질이 풍부한 폐기물에서 암호화된 생체 활성 펩티드의 최신 발전에 대한 검토. 국제 J. 몰. 과학. 2016, 17, 950. [교차참조] [PubMed]
57. Wang, J.-S.; Zhao, M.-M.; Zhao, Q.-Z.; 장, Y.-M. 차별화된 산화 시스템에서 밀 글루텐의 파파인 가수분해물의 항산화 특성. 식품화학 2007, 101, 1658-1663. [교차 참조]
58. Gao, M.-T.; 카네코, M.; 히라타, M.; Toorisaka, E.; Hano, T. 발효 젖산 생산을 위한 영양원으로 쌀겨의 활용. 생물자원. 기술. 2008, 99, 3659–3664. [교차 참조] [PubMed]
59. 황, 와이오밍; 린, YR; 호, RF; 리우, HY; Lin, YS 녹차 잎 추출에 대한 수용액의 효과. 과학. World J. 2013,2013, 368350. [교차참조]
60. Wathoni, N.; 샨, CY; Shan, 와이오밍; 로스티나와티, T.; 인라디, RB; Pratiwi, R.; Muchtaridi, M. 인도네시아 망고스틴(Garcinia mangostana L.) 껍질에서 펙틴의 특성화 및 항산화 활성. Heliyon 2019, 5, e02299. [교차 참조]
61. Tsai, C.-C.; 찬, C.-F.; Huang, W.-Y.; Lin, J.-S.; 찬 피.; Liu, H.-Y.; 린, Y.-S. 화장품 항산화, 미백 및 수분 유지 응용 분야에서 Lactobacillus rhamnosus SpentCulture 상청액의 응용. 분자 2013, 18, 14161–14171.[교차 참조]
62. Huang, W.-Y.; Lee, P.-C.; Hsu, J.-C.; Lin, Y.-R.; Chen, H.-J.; 린, Y.-S. Yerba Mate 추출물 분말의 용출에 대한 수질의 영향. 과학. 세계 J. 2014, 2014, 1–6. [교차 참조] [PubMed]
63. 찬, C.-F.; Wu, C.-T.; Huang, W.-Y.; Lin, W.-S.; Wu, H.-W.; 황, T.-K.; Chang, M.-Y.; 린, Y.-S. 각종 덴드로비움 토사엔스 추출물의 항산화 및 멜라닌 생성 억제 분자 2018, 23, 1810. [CrossRef] [PubMed]64. Wu, C.-T.; 아그라왈, DC; Huang, W.-Y.; Hsu, H.-C.; Yang, S.-J.; 황, S.-L.; 린, Y.-S. 열수법으로 얻은 폐커피가루 추출물의 기능성 분석. J. Chem. 2019년, 2019년, 1–8. [교차 참조]
65. Dorta, E.; Rodríguez-Rodríguez, EM; Jiménez-Quezada, A.; Fuentes-Lemus, E.; 스페이스키, H.; Lissi, E.; López-Alarcón, C. 육류 단백질 산화를 억제하기 위한 망고(Mangifera indica L.) 부산물의 용량을 예측하기 위한 산소 라디칼 흡광도(ORAC) 분석의 사용. 음식 항문. 방법 2016, 10, 330–338. [교차 참조]
66. Lin, Y.-S.; Chen, H.-J.; 황, J.-P.; Lee, P.-C.; Tsai, C.-R.; Hsu, T.-F.; 황, W.-Y. Vitis vinifera 잎 추출물을 이용한 Tyrosinase 억제 활성의 동역학. 바이오메드 해상도 국제 2017, 2017, 5232680. [교차참조] [PubMed]
67. Bidlingmeyer, BA; 코헨, SA; Tarvin, TL 사전 컬럼 유도체화를 사용한 아미노산의 신속한 분석. J. Chromatogr. 비바이오메드. 과학. 적용 1984, 336, 93–104. [교차 참조]
68. 아사이, TT; 오이카와, F.; Yoshikawa, K.; 이노우에, N.; Sato, K. 식품 유래 콜라겐 펩티드, 프롤릴-히드록시프롤린(Pro-Hyp) 및 히드록시프롤릴-글리신(Hyp-Gly)은 히드록시프롤릴 펩티드에서 유래하지 않은 소 태아 혈청을 사용하여 1차 배양된 마우스 피부 섬유아세포의 성장을 향상시킵니다. 국제 J. 몰. 과학. 2019, 21, 229. [교차참조]
69. Schägger, H. Tricine-SDS-PAGE. Nat. 프로토콜 2006, 1, 16–22. [교차 참조]
70. Diao, J.; 치, 지.; Guo, Z.; Zhang, L. 녹두 단백질 가수분해물은 NF-kB 경로 인리포다당류로 자극된 RAW 264.7 대식세포를 통해 면역 반응을 조절합니다. J. 식품 과학. 2019, 84, 2652–2657.[교차 참조]
