외래 진료소에서 신장 기능을 평가하는 방법
Mar 03, 2022
PE 코호넨1,2,3
요약
배경
2002년에 만성질환의 새로운 정의와 분류신장병3개월 이상 동안 사구체 여과율 < 60 ml/min/1.73 m2를 수정하여 다음을 정의했습니다.만성 신장 질환다른 징후와 상관없이신장 손상. 목표: 다양한 평가 방법에 대해 논의신장 기능외래 환자 진료소, 특히 1차 진료에서. 방법: Pub-Med 데이터베이스에서 관련 기사를 검색했습니다. 결과: 혈장 크레아티닌, 연령, 성별, 인종 및 신체 크기를 고려한 추정 사구체 여과율 방정식이 만성 질환 환자를 식별하기 위해 개발되었습니다.신장병이전에는 신장 기능이 혈장 크레아티닌만으로 평가되었다면 간과되었습니다. Cystatin C 기반 방정식은 크레아티닌 기반 추정치가 있는 개인의 정확도를 향상시키기 위해 개발되었습니다.신장 기능덜 정확하다고 인정됩니다. 고찰: 진단검사가 적용되는 환자의 특성은 검사의 민감도에 영향을 미칠 수 있다. 따라서 오늘날 가장 좋은 평가 방법에 대한 논쟁이 있습니다.신장 기능일반 인구에서. 결론: 현재 일차 진료를 받고 있는 대다수의 환자에서 CKD-EPI 크레아티닌 방정식은 신장 기능을 추정하는 데 적합합니다. CKD-EPIcr-cys 방정식은 CKD-EPI 크레아티닌 eGFR이 45–59 ml/min/1.73 m2인 개인에게 더 높은 신뢰성을 제공하지만 혈청 시스타틴 C 분석 비용으로 인해 일상적인 일반 진료에서의 사용이 제한됩니다.

소개
2002년에 의 정의 및 분류만성 신장 질환미국이 도입한신장재단 (K/DOQI) (표 1) (1). 이 틀은 오랫동안 덜 심각한 만성 질환으로 무시되었던 의료계에 새로운 '질서'를 제공신장병말기 신장 질환보다, 신부전이나 전요독증과 같이 잘 정의되지 않은 용어를 사용했습니다. 사구체여과율(GFR) < 60="" ml/min/1.73="" m2는="" 최소="" 3개월="" 간격으로="" 반복적으로="" 측정하여="" 만성을="" 정의하기="" 위해="">신장병다른 징후와 상관없이신장 손상,이는 젊은 성인에서 정상 수치인 125ml/min/1.73m2의 절반 이상 감소를 나타내고 이 GFR 수준은신부전, 여러 심혈관 위험 요인의 증가된 유병률을 포함합니다(2). GFR은 기능하는 모든 네프론의 여과율의 합과 같으며 그 수를 대략적으로 측정한 것으로 간주할 수 있습니다. 만성 신장 질환에 대한 새롭고 일관된 정의는 중재가 다음의 합병증을 예방할 수 있는 초기의 무증상 단계를 식별하는 것을 목표로 합니다.만성 신장 질환그리고 최종 단계로의 진행신장병.

그러나 의료 행위에서 항상 그렇듯이 치료의 성패는 진단의 정확성에 달려 있습니다. GFR은 이눌린이나 방사성의약품(125I-iothlamate, 51Cr-EDTA, 99mTc-DTPA)과 같이 주입된 외인성 물질의 제거로 매우 정확하게 측정(GFR, mGFR 측정)할 수 있지만 사용상의 어려움과 비용으로 인해 이러한 방법을 적용할 수 없습니다. 대규모 임상 실습. 이 문서는 평가에 사용 가능한 정보를 검토합니다.신장 기능안정적인 단계에서. PubMed 데이터베이스는 '라는 용어를 사용하여 관련 기사를 검색했습니다.크레아티닌', '크레아티닌 청소율', '시스타틴 C', 'Cockcroft-Gault', '사구체 여과율', 'MDRD' 'CKD-EPI'. 검색에 날짜 제한이 없었습니다. 20개의 기사가 확인되었습니다.
이 문서는 평가에 사용 가능한 정보를 검토합니다.신장 기능안정적인 단계에서. PubMed 데이터베이스에서 '크레아티닌, '크레아티닌 청소율', '시스타틴 C', 'Cockcroft-Gaul', '사구체 여과율', 'MDRD' 'CKD-EPI'라는 용어를 사용하여 관련 기사를 검색했습니다. 검색에 날짜 제한이 없었습니다. 20개의 기사가 확인되었습니다.
임상적으로 관련된 주제에 초점을 맞춘 선택된 논문의 참조 및 관련 인용을 통해 추가 논문을 식별했습니다.
혈청 크레아티닌
평가신장 기능수십 년 동안 임상 실습에서 저렴하고 일반적인 테스트인 혈청 크레아티닌 농도를 기반으로 했습니다. 그러나 혈청 또는 혈장 크레아티닌을 추정하기에는 상당히 부정확한 검사입니다.신장 기능: GFR이 1/2로 감소했을 때만 상승하기 시작하고 그 이후에는 상승이 GRF 악화에 선형적이지 않고 지수적입니다(3). 혈청 크레아티닌은 또한 연령, 성별, 근육량 또는 파괴, 식이, 인종, 세뇨관 분비, 약물(예: amiloride, triamterene, spironolactone, trimethoprim) 및 실험실 분석 방법의 영향을 받습니다(3,4). 다행히도, 혈청 크레아티닌 분석에 대한 보정 표준화의 구현, 동위원소 희석 질량 분석법(IDMS) 추적 가능한(금 표준) 크레아티닌 분석은 혈청 크레아티닌 결과의 실험실 간 차이를 크게 해결했습니다(5).
크레아티닌 청소율
GFR은 24-시간 소변 수집으로 혈청에서 크레아티닌 제거를 측정하여 간접적으로 평가할 수 있습니다.
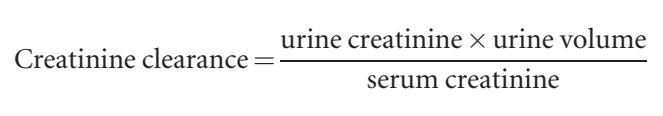
그러나 크레아티닌 청소율을 계산하는 것은 크레아티닌 측정의 모든 한계를 공유하고 일상적인 임상 실습에서 신뢰성에 도전하는 정확한 소변 수집을 요구합니다.
혈청 시스타틴 C
Cystatin C는 모든 유핵 세포에서 합성 및 분비되는 비당화 단백질이며 사구체에서 자유롭게 여과된 다음 근위 세뇨관에서 재흡수 및 이화됩니다(6-8). 따라서 GFR은 시스타틴 C 혈청 농도의 주요 결정 요인입니다. 크레아티닌과 대조적으로 시스타틴 C 농도는 연령, 성별, 근육량 또는 식이의 영향을 덜 받지만 비만(9), 갑상선 기능(10), 흡연(11,12), 염증(11,13)의 영향을 받을 수 있습니다. ), 스테로이드 요법(14) 및 HIV의 바이러스 부하(15). 오늘날 시스타틴 C에 대한 국제 실험실 참조 표준이 있지만 분석 비용은 혈청 크레아티닌 농도를 측정하는 것보다 약 2배 더 높습니다.
사구체 여과율 추정 방정식
평가에서 크레아티닌 측정의 함정을 극복하기 위해 몇 가지 접근 방식이 만들어졌습니다.신장 기능.추정 사구체 여과율(eGFR) 방정식은 내인성 크레아티닌 생성 및 배설을 위한 대리인으로 연령, 성별, 인종 및 신체 크기를 사용합니다. 그러나 이러한 공식은 여전히 혈청 크레아티닌을 기반으로 하며 개인 간의 크레아티닌 생산, 세뇨관 분비 또는 신외 배설의 차이를 인식할 수 없습니다. 이러한 오류 구성 요소를 고려하여 mGFR의 30% 이내의 eGFR은 다음을 가진 개인을 식별하기 위한 임상 해석을 위해 K/DOQI에서 허용 가능한 것으로 간주됩니다.만성 신장 질환 (1)
콕크로프트-골트 방정식
Cockcroft와 Gault는 1976년에 소수의 입원 환자 집단에서 GFR을 추정하는 방정식을 개발했습니다(16). 방정식은 수학적으로 간단합니다.

이 방정식에는 중요한 한계가 있습니다. 개발 데이터 세트에는 백인 피험자(4% 여성)만 포함되었고, 사용된 참조 방법은 크레아티닌 청소율(GFR 아님)이었고, 공변량 체중은 비만 피험자 또는 저체중 환자에서 잠재적인 오류 소스입니다. 질량 지수.
신장 질환 방정식에서 식단의 수정
1999년 Levey et al. Iothalamate 제거에 의해 측정된 GFR 값을 기반으로 하는 새로운 eGFR 방정식을 도입했습니다(17). 이 공식은 1.73m2의 표준 체표면적에 대해 GFR을 정규화하기 때문에 가중치 변수가 필요하지 않습니다. 방정식은 다양한 비당뇨병 환자를 포함하는 MDRD(Modification of Diet in Renal Disease) 연구 데이터베이스에서 개발되었습니다.신장 질환(평균 GFR 40ml/min/1.73m2) (17). IDMS 추적 가능(금 표준) 혈청 크레아티닌 분석(18)과 함께 사용하기 위한 단순화된 4변수 MDRD 연구 방정식은 오늘날 eGFR에 대해 가장 일반적으로 사용되는 방정식입니다.
eGFR(ML/MIN/1.73m2
=175 x(혈청 크레아티닌/88.4) -1.154
x(나이){{0}}.203 x(여성의 경우 0.742)
x(뒤로 있는 경우 1.212)
최근 일반 인구 코호트에 대한 메타 분석에서 총 사망 위험은 eGFR 60ml/min/1.73m2 부근에서 유의미해졌으며 eGFR 30–45ml/min/1.73m2 부근에서 최적 eGFR 수준에 비해 2배 더 높았습니다. MDRD 공식(19)으로 계산한 104ml/min/1.73m2.
영국에서 MDRD 연구 방정식을 사용한 eGFR 보고가 처음 도입되었을 때 1차 진료에서 신장 전문의에게 진료를 의뢰한 사람의 수가 2.{1}}배(20) 증가했습니다. 이는 이전에 만성 질환이 의심되지 않은 환자의 식별이 증가했음을 반영합니다.신장병단순한 크레아티닌 측정을 기반으로 하지만,만성 신장 질환일반 인구에서 (21). 사실, MDRD 연구 방정식은 측정된 GFR이 60ml/min/1.73m2(22-25) 이상인 피험자의 실제 GFR을 체계적으로 과소평가하는 것으로 나타났습니다.
만성 신장 질환 크레아티닌 방정식
그만큼만성 신장 질환Epidemiology Collaboration(CKD-EPI)은 GFR이 정상이거나 약간 감소한 개인 간의 GFR을 보다 정확하게 추정하기 위해 새로운 eGFR 방정식을 개발했습니다(26).
CKD-EPI 방정식은만성 신장 질환, 요오탈라메이트 청소율로 측정한 광범위한 GFR(평균 GFR 67ml/min/1.73m2)을 가졌습니다(27). CKD-EPI 방정식에서 크레아티닌 수치와 성별에 따라 혈청 크레아티닌에 다른 지수가 적용됩니다.
eGFR(ml/분/1.73m2)
=141 x 분(혈청 크레아티닌/k,1)
x 최대 (혈청 크레아티닌 /k,1)-1.209
x 0.993 나이x 1.018(여성의 경우) x 1.159(뒤쪽의 경우)
min은 혈청 크레아티닌/k 또는 1의 최소값을 나타내고, 최대값은 혈청 크레아티닌/k 또는 1의 최대값을 나타냅니다.
k {{0}}.7 여성, 0.9 남성
여성의 경우 -0.329, 남성의 경우 -0.411
CKD-EPI 방정식은 특히 GFR이 60ml/min/1.73m를 초과하는 개인의 경우 MDRD 연구 방정식을 능가하는 것으로 나타났습니다.2; 추정된 GFR(편향 측정)과 측정된 GFR 간의 중앙값 차이는{0}}.6ml/min/1.73m입니다.2 MDRD 연구 방정식 및{0}}.5ml/min/1.73m2CKD-EPI 방정식(26)에 대해.
3개의 대규모 인구 기반 코호트가 최근 CKD-EPI 및 MDRD 방정식을 비교했습니다. 20세 이상의 미국 성인 인구에서 유병률은만성 신장 질환CKD-EPI 방정식을 사용하면 11.6%이고 MDRD 방정식을 사용하면 13.1%입니다(26). 일반 호주 성인 인구의 해당 수치는 11.5%와 13.4%(28명)였습니다. 유병률만성 신장 질환3단계(eGFR 30–59 ml/min/1.73 m2)는 45–64세의 미국 인구 집단에 CKD-EPI 공식을 적용한 경우 MDRD 공식의 경우 2.5%에서 1.4%로 감소했습니다(29). 중요하게도, MDRD 공식을 기반으로 eGFR 30–59 ml/l/1.73 m2에서 CKD-EPI 공식을 사용하여 eGFR 60–89 ml/min/1.73 m2로 상향 재분류된 마지막 두 연구의 참가자는 재분류되지 않은 사람들에 비해 모든 원인으로 인한 사망, 주요 심혈관 사건 및 말기 신장 질환의 위험이 더 낮습니다(28,29).
CKD-EPI 시스타틴 C 및 CKD-EPI 크레아티닌-시스타틴 C 방정식
최근 CKD-EPI 컨소시엄은 GFR 추정을 위한 두 가지 새로운 방정식을 제안했습니다. 하나는 혈청 시스타틴 C(CKD-EPIcys)를 사용하고 다른 하나는 혈청 크레아티닌과 혈청 시스타틴 C(CKD-EPIcrcys)를 모두 사용합니다(30). CKD-EPI 시스타틴 C 방정식:
133 x min(혈청 시스타틴 C/0.8,1)-0.499
x 최대(혈청 시스타틴 C/0.8,1)-1.328 x 0.996나이
x 0.932(여성인 경우)
min은 혈청 시스타틴 C/k의 최소값 또는 1을 나타내고, max는 혈청 시스타틴 C/k의 최대값 또는 1을 나타냅니다. CKD-EPI 크레아티닌-시스타틴 C 방정식:
135 x min(혈청 크레아티닌/k,1)
x 최대 (혈청 크레아티닌 /k,1)-0.601
x분(혈청 시스타틴 C/0.8,1)-0.375
x 최대(혈청 시스타틴 C/0.8,1)-0.711 x 0.995나이
x 0.969(famle인 경우) x 1.08(뒤로 있는 경우)
k는 여성의 경우 {{0}}.7이고 남성의 경우 0.9입니다.
여성의 경우 -0.248이고 남성의 경우 -0.207입니다. min은 최소 혈청 크레아티닌/k 또는 1을 나타내고, 최대는 최대 혈청 크레아티닌/k 또는 1을 나타냅니다.
다양한 모집단의 13개 코호트 데이터가 이러한 방정식의 개발에 사용되었으며 GFR 측정은 외인성 여과 마커의 요 또는 혈장 청소율을 기반으로 했습니다. CKD-EPIcys 방정식은 체질량 지수가 낮은 환자를 포함하여 환자의 다른 하위 그룹에서 CKD-EPI 크레아티닌 방정식과 유사하게 수행되었습니다. 흥미롭게도 결합된 CKD-EPcr-cys 방정식은 크레아티닌 또는 시스타틴 C만 사용한 방정식보다 더 나은 성능을 보였습니다. CKD-EPI 크레아티닌에 기반한 eGFR이 45–59 ml/min/1.73 m2인 참가자에서 CKD-EPIcr-cys 방정식은 GFR이 60 ml/min/1.73 m2 이상인 17%를 올바르게 재분류했습니다( 30).
11개 일반 인구 연구에 대한 메타 분석에서 eGFR < 6{13}}="" ml/min/1.73="" m2의="" 유병률은="" ckd-epi="" 크레아티닌="" 방정식에서="" 9.7%,="" ckd-epicys="" 방정식에서="" 13.7%,="" 결합된="" ckd-cys="" 방정식(31)과="" 함께="" 10.0%.="" 메타="" 분석에는="" 5가지="" 항목도="">만성 신장 질환2960명의 참가자가 있는 코호트. 시스타틴 C 기반 eGFR 계산에서는 크레아티닌 기반 eGFR이 45–59 ml/min/1.73 m2인 연구 참가자의 42%를 > 60 ml/min/1.73 m2로 재분류했습니다. 더욱이, 재분류된 피험자는 eGFR이 재분류되지 않은 사람에 비해 모든 원인으로 인한 사망 위험이 34% 상대적으로 감소했습니다(31). CKD-EPIcys 및 CKD-EPIcr-cys 값이 임계값 85ml/min/1.73m2 미만인 경우 모든 eGFR 수준에서 모든 원인 및 심혈관 질환으로 인한 사망 위험이 증가했습니다(31). 따라서 시스타틴 C 측정에 기반한 eGFR 방정식은 eGFR의 유일한 크레아티닌 기반 계산으로 감지되지 않는 불리한 결과의 증가된 위험을 감지하는 데 사용할 수 있습니다.
그만큼신장병Improving Global Outcome (KDIGO) 2012 Clinical Practice Guideline은 혈청 크레아티닌에 기초한 eGFR이 45-59 ml/min 범위 내에 있는 성인에서 CKD-EPIcr-cys 결합 질문에 의한 혈청 시스타틴 C 측정 및 GFR 추정을 권장합니다. /1.73 m2, 그러나 다음의 마커가 없는 사람신장 손상 (32).
74세 이상의 유럽 가계 인구에 대한 연구에서 3개의 CKD-EPI 방정식이 MDRD 연구 방정식보다 더 정확한 것으로 나타났지만 그 차이는 eGFR이 60ml/ 최소/1.73m2(33). 따라서 MDRD 연구 방정식은 근육량, 식이 단백질 섭취 및 GFR이 MDRD 연구의 질병 발병 코호트와 더 유사한 노인들 사이에서 임상 실습에서 꽤 잘 수행됩니다(33). 더욱이 시스타틴 C 수치에 대한 노화의 영향은 특히 남성에서 강력합니다(34).
요약
진단검사가 적용되는 환자의 특성과 질병의 병기 또는 중증도(Table 2)는 검사의 민감도에 영향을 미칠 수 있다(35). 현재 1차 진료를 받고 있는 대다수의 환자에서 CKD-EPI 크레아티닌 방정식은 신장 기능을 추정하는 데 적합합니다. CKD-EPIcr-cys 방정식은 CKD-EPI 크레아티닌 eGFR이 45–59 ml/min/1.73 m2인 개인에게 더 많은 신뢰성을 제공하지만(31), 혈청 시스타틴 C 분석 비용과 노인 대상자의 정확도는 여전히 제한적입니다. 일상적인 일반 관행에서의 사용.

삽화에 설명된 환자의 eGFR은 MDRD 연구 및 CKD-EPI크레아티닌 방정식에 따라 각각 58 및 62ml/min/1.73m2입니다. 그녀의 비만 때문에 Cockcroft-Gault 공식은 편향된 것으로 간주되었습니다. 혈청 시스타틴 C가 측정되지 않아 CKD-EPIcys 및 CKD-EPIcr-cys 방정식을 사용할 수 없었습니다.
환자는 알부민뇨나 다른 증상이 없더라도신장 손상, 그녀는 진단만성 신장 질환MDRD 연구 방정식에 따라. 이것은 그녀의 의사가 실제로 배설되는 약물인 ACE 억제제와 메트포르민의 복용량을 줄이도록 촉발할 수 있습니다. 그러나 만성 신장 질환의 진단은 최소 3개월 간격으로 두 번의 eGFR 측정이 필요합니다(32). 의 후속조치가 강조되어야 한다.신장 기능임상 의사 결정에 매우 중요합니다. 만약 우리 환자가 추적 관찰 동안 안정적인 신장 기능을 보인다면, 그녀는 허혈 및 신장 기능 장애와 함께 수년에 걸쳐 고혈압, 당뇨병 및 이상지질혈증의 누적 효과로 고통받았을 가능성이 높습니다. 이 경우 그녀는 ACE 억제제 및 메트포르민과 같은 심장 및 신장 보호 약물의 처방으로 계속 혜택을 받을 것입니다. KDIGO 가이드라인은 eGFR이 기준선보다 25% 이상 감소하거나 eGFR > 5ml/min/1.73m2의 지속적인 감소를 동반한 eGFR 범주(표 1)의 감소를 기반으로 만성 신장 질환 진행을 정의합니다. 연간 (33).
그러나 우리 환자는 최소한 경미하게 감소했습니다.신장 기능급성 또는만성 신장 손상생리적 스트레스를 받을 때. 따라서 잠재적으로 신독성이 있고 실제로 배설되는 약물(ACE 억제제, 안지오텐신 수용체 차단제, 알도스테론 억제제, 레닌 억제제, 이뇨제, NSAID, 메트포르민, 리튬, 디곡신)은 급성 질환 동안 적어도 일시적으로 중단해야 합니다. 심각한 감염, 구토, 설사 또는 수술 절차(33).
혈압 관리는 예방에 매우 중요합니다.만성 신장 질환진행. KDIGO 2012 임상 진료 가이드라인(33), 유럽 고혈압 학회 및 유럽 심장 학회 2013 동맥 고혈압 관리 가이드라인(36), 제8차 공동 국가 위원회(JNC 8) 가이드라인 2014(37)에서 다음을 권장합니다. 환자만성 신장 질환알부민뇨가 없는 경우 목표 혈압은 140/90mmHg 미만이어야 하며 초기 약물 치료 옵션은 ACE 억제제 또는 안지오텐신 수용체 차단제입니다. 따라서 삽화에 설명된 환자는 이 수준에 지속적으로 도달하기 위해 혈압을 낮추어야 합니다.
![]() 2014 John Wiley & Sons Ltd
2014 John Wiley & Sons Ltd
Int J Clin Pract, 2015년 2월, 69, 2, 156–161. DOI: 10.1111/ijcp.12516
참고문헌
1 국립신장재단. K/DOQI 임상진료지침서만성 신장 질환: 평가, 분류 및 계층화. 실행 요약.Am J 신장 장애2002; 39: S17–31.
2 Sarnak MJ, Levey AS, Schoolwerth AC 외.신장병심혈관 질환 발병의 위험 요소로. 심혈관 질환, 고혈압 연구, 임상 심장학, 역학 및 예방에서 신장에 대한 미국 심장 협회 협의회의 성명.고혈압2003; 42: 1050–65.
3 Shemesh O, Golbety H, Kriss JP, Myers BD. 사구체 병증 환자에서 여과 마커로서의 크레아티닌의 한계.신장 INT1985; 28: 830–8.
4 Perrone RD, Madias NE, Levey AS. 신장 기능의 지표로서의 혈청 크레아티닌: 오래된 개념에 대한 새로운 통찰력.클린켐1992; 38: 1933–53.
5 Pieroni L, Delanaye P, Boutten A, et al. IDMS 추적 가능한 크레아티닌 효소 분석 및 다중심 평가.클린켐 액타2011; 412: 2070–5.
6 Abrahamson M. 인간 시스타틴 C 유전자의 구조와 발현.바이오켐1990; 268: 287–94.
7 Jacobsson B, Lignelid H, Bergerheim 미국. 트랜스티레틴과 시스타틴 C는 근위부에서 이화됩니다.관상 상피 세포 및 단백질은 신세포 암종의 표지자로 유용하지 않습니다. 조직병리학 1995; 26: 559–64.
8 Tenstad O, Roald AB, Grubb A, Aukland K. 쥐에서 방사성 표지된 인간 시스타틴 C의 신장 처리. Scand J Clin Lab Invest 1996; 56: 409–14.
9 Naour N, Fellahi S, Renucci JF et al. 인간 비만에서 증가된 혈청 시스타틴 C에 대한 지방 조직의 잠재적 기여. 비만 2009; 17: 2121~6.
10 Fricker M, Wiesli P, Brandle M, Schwegler B, Schmid C. 갑상선 기능 장애가 혈청 시스타틴에 미치는 영향 C. Kidney Int 2003; 63: 1944–7.
11 Knight EL et al. 신장 기능 이외의 혈청 시스틴 C 수치에 영향을 미치는 요인 및 신장 기능 측정에 미치는 영향. 신장 Int 2004; 65:1416~21.
12 Galteau MM, Guyon M, Guueguen R, Siest G. 시스타틴 C의 측정; 생물학적 변이 및 참조 값. Clin Chem Lab Med 2001; 39: 850–7.
13 Stevens LA, Schmid CH, Greene T et al. 사구체 여과율 이외의 요인이 혈청 시스타틴 C 수치에 영향을 미칩니다. 신장 Int 2009; 75: 652–60.
14 Risch L, Huber AR. 글루코코르티코이드 및 증가된 혈청 시스타틴 C 농도. Clin Chim Acta 2002; 320: 133–4
15 Gagneux-Brunon A, Mariat C, Delaney P. Cystatin C HIV 감염 환자: 유망하지만 아직 황금기를 맞이할 준비가 되지 않았습니다. Nephrol 다이얼 이식 2012; 27: 1305~13.
16 Cockcroft DW, Gault MH. 혈청 크레아티닌에서 크레아티닌 청소율 예측. 네프론 1976; 16: 31~41.
17 Levey AS, Bosch JP, Lewis JB, Greene T, Rogers N, Roth D. 혈청 크레아티닌에서 사구체 여과율을 추정하는 보다 정확한 방법: 새로운 예측 방정식. 신장 질환 연구 그룹의 식단 수정. Ann 인턴 메드 1999; 130: 461–70.
18 Levey AS, Coresh J, Greene T et al. IDMS 추적 가능한(금 표준) 혈청 크레아티닌 값으로 GFR을 추정하기 위한 MDRD 연구 방정식 표현. J Am Soc Nephrol 2005; 16: 69A.
19 만성 신장 질환예후 컨소시엄. 일반 인구 집단의 모든 원인 및 심혈관 사망률과 사구체 여과율 및 알부민뇨의 연관성: 공동 메타 분석. 란셋 2010; 375: 2073–81.
20 Richards N, Harris K, Whitfield M, et al. 인구 기반 식별의 영향만성 신장 질환추정 사구체 여과율(eGFR) 보고 사용. Nephrol 다이얼 이식 2008;
21 Moynihan R, Glassock R, Doust J.만성 신장 질환논쟁: 정의의 확장이 어떻게 많은 사람들을 질병에 걸린 것으로 불필요하게 표시하는지.비엠제이2013; 347: f4298.
22 Stevens LA, Coresh J, Feldman HI et al. 다양한 인구 집단에서 신장 질환 연구 방정식의 식이 수정 평가.J Am Soc 네프롤2007; 18: 2749–57.
23 Rule AD, Larson TS, Bergstralh EJ, Slezak JM, Jacobsen SJ, Cosio FG. 혈청 크레아티닌을 사용하여 사구체 여과율 추정: 건강 상태 및만성 신장 질환. 앤 인턴 메드2004; 141: 929–37.
24 Rule AD, Gussak HM, Pond GR et al. 건강한 잠재적인 신장 기증자의 측정 및 추정된 GFR.Am J 신장 장애2004; 43: 112–9.
25 Stevens LA, Coresh J, Greene T, Levey AS. 평가신장 기능– 측정 및 추정된 사구체 여과율.N 영어 J Med2006; 354: 2473–83.
26 Levey AS, Stevens LA, Schmid CH 외. 사구체 여과율을 추정하는 새로운 방정식.앤 인턴 메드2009; 150: 604–12.
27 Levey AS, Coresh J, Balk E et al. 만성 신장 질환에 대한 국립 신장 재단 진료 지침: 평가, 분류 및 계층화.앤 인턴 메드2003; 139: 137–47.
28 White SL, Polkinghorne KR, Atkins RC, Chadban SJ. 호주의 만성신장질환 유병률 및 사망률 비교만성 신장 질환역학 협력(CKD-EPI) 및 신장 질환의 식이 요법 수정(MDRD) 연구 GFR 추정 방정식: AusDiab(호주 당뇨병, 비만 및 생활 습관) 연구. Am J 신장 질환 2010; 55: 660–70.
29 Matsushita K, Selvin E, Bash LD, Astor BC, Coresh J. 새로운 위험 영향만성 신장 질환추정된 GFR에 대한 MDRD 연구 방정식과 비교한 역학 협력(CKD-EPI) 방정식: 지역사회의 동맥경화 위험(ARIC) 연구. Am J 신장 질환 2010; 55: 648–59.
30 Inker LA, Schmid CH, Tighiouart MS et al. 혈청 크레아티닌 및 시스타틴으로부터 사구체 여과율 추정 C. N Engl J Med 2012; 367: 20–9.
31 Shlipak MG, Matsushita K, J 등의 Arnel €. 신장 기능을 기반으로 위험을 결정하는 데 있어 시스타틴 C 대 크레아티닌. N Engl J Med 2013; 369: 932–43.
32 신장 질환e: 글로벌 성과 개선(KDIGO) c만성 신장 질환작업 그룹. KDIGO 2012 만성신장질환 평가 및 관리를 위한 임상진료지침서. 신장 Int 2012; 2013(보충 3): 1–150.
33 Kilbride HS, Stevens PE, Eaglestone G et al. MDRD(신장질환에서의 식이요법 수정) 연구 및 CKD-EPI(만성 신장 질환역학 협력) 노인의 GFR 추정을 위한 방정식. Am J 신장 질환 2013; 61: 57-66.
34 Werner KB, Elmstahl S, Christensson A, Pihlsgard M. 남성의 성 및 혈관 위험 요인은 당뇨병이나 명백한 혈관 질환이 없는 노인에서 혈청 시스타틴 C 유래 신장 기능에 영향을 미칩니다. 연령 및 노화 2013; 43: 411–7.
35 Machin D, Campbell MJ, Walters SJ. 의료 통계. 건강 과학 교과서. 4판. 치체스터: John Wiley & Sons Ltd, 2007.
36 유럽고혈압학회(ESH)와 유럽심장학회(ESC)의 동맥성 고혈압 관리 태스크포스. 동맥성 고혈압 관리를 위한 ESH/ESC 가이드라인. J Hypertens 2013; 2013(31): 1281–357.
37 제8차 전국공동위원회(JNC 8)에 임명된 패널 위원들의 보고서. 성인의 고혈압 관리를 위한 증거 기반 가이드라인. JAMA 2014; 311(5): 507–20.




