신장 발달과 질병의 마이크로RNA Ⅰ
Apr 30, 2024
소개
MicroRNA(miRNA)는 일반적으로 길이가 19~22개 뉴클레오티드인 내인성 소형 비암호화 RNA입니다. 인간 게놈에는 주석이 달린 1917개의 헤어핀 전구체와 2654개의 성숙한 miRNA가 포함되어 있으며(1), 이는 인간 단백질 코딩 유전자의 60% 이상을 조절합니다(2). MiRNA는 번역 억제와 mRNA 불안정화를 통해 전사 후 수준에서 유전자 발현을 조절합니다(3-5). 1993년에 선충류 Caenorhabditis elegans에서 세포 계통 결정을 조절하는 것으로 밝혀진 최초의 확인된 miRNA 기능이 발견된 이후(6, 7), miRNA는 다음을 포함한 다양한 생물학적 과정을 조절하는 것으로 입증되었습니다.신장 형태 형성. miRNA 발현 조절 장애초기 신장 발달을 방해합니다그리고 발달의 병인에 연루되어 있다.신장 질환. 이 리뷰에서는 miRNA 생합성, 기능 및 표적화에 대한 현재 지식을 요약합니다. 그런 다음 신장 형태 형성에서 miRNA의 역할에 중점을 두고발달성 신장 질환, 포함선천적 기형~의신장과 요로(CAKUT) 및윌름스 종양. 급성 신장 손상(8-10), 다낭성 신장 질환(11) 및 신장 이식(10)과 같은 다양한 다른 신장 질환에서 miR NA의 역할을 포함한 추가적인 흥미로운 연구 영역이 다음에서 광범위하게 다루어졌습니다. 다른 최근 리뷰. 마지막으로, 잠재적으로 새로운 바이오마커 및 치료제로서 miRNA의 유용성에 대해 논의함으로써 결론을 내립니다.

CISTANCHE가 신장 질환 환자를 치료하는 데 얼마나 걸리나요?
miRNA 생합성 및 기능
miRNA의 생합성은 핵에서 시작되며, 여기서 RNA 중합효소 II는 miRNA 코딩 유전자를 캡이 있는 폴리아데닐화된 헤어핀 전사체로 전사하는데, 이를 일차 miRNA 또는 pri-miRNA라고 합니다(그림 1)(12, 13). 게놈 위치에 따라 miRNA 코딩 유전자는 유전자 내(숙주 유전자의 인트론 내에 위치, 참조 14) 또는 유전자 간(숙주 유전자와 독립적으로 전사되고 전사 조절 요소를 가짐, 참조 15)으로 분류될 수 있습니다. 또한 일부 miRNA는 클러스터로 존재하며 폴리시스트론 전사체로 전사됩니다(16).
전사 후, pri-miRNA는 마이크로프로세서 복합 서브유닛 DGRC8과 함께 리보뉴클레아제 III 유사 효소 DROSHA에 의해 pre-miRNA라고 불리는 70-뉴클레오티드 헤어핀 구조로 절단됩니다(17-20). 엑스포틴 5/GTP 결합 핵 단백질 RAN은 pre-miRNA를 세포질로 내보내는데(21, 22), 여기서 pre-miRNA는 RNase III DICER 및 TRBP(또는 TARBP2)에 의해 말단 루프를 절단하여 { {14}} 가이드 가닥과 패신저 가닥으로 구성된 뉴클레오티드 miRNA 이중 가닥(각각 miRNA:miRNA*). 다음 단계에서는 miRNA 이중가닥이 AGO(Argonaute) 단백질에 로딩되어 RISC를 형성합니다(23). 가닥 선택 및 풀림 후 패신저 가닥은 풀려 분해되는 반면(24), 가이드 가닥은 RISC에 남아 있으며 Watson-Crick 염기쌍을 통해 표적 mRNA 인식을 유도합니다.
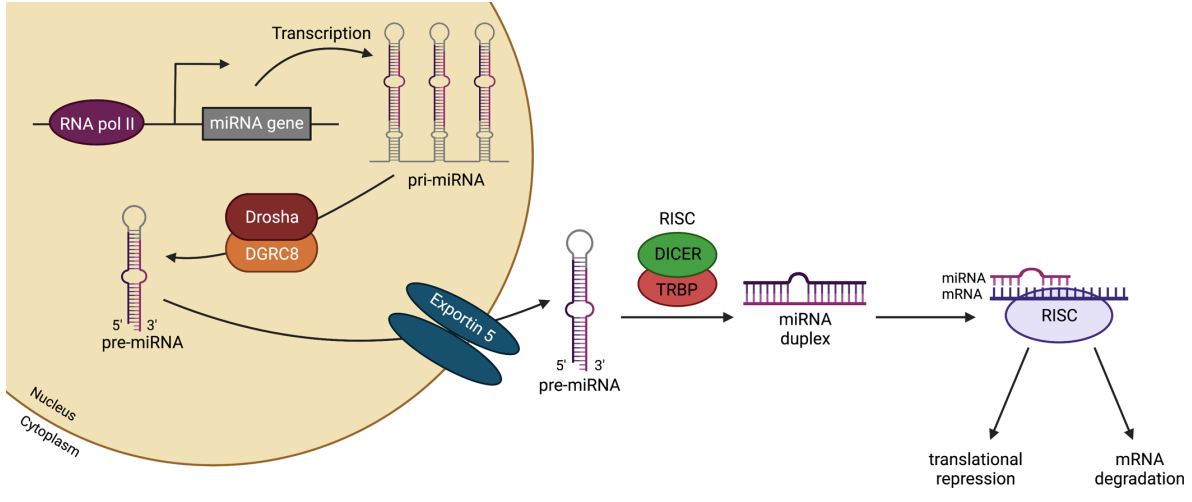
그림 1. miRNA의 생물 발생. MiRNA를 코딩하는 유전자는 RNA 중합효소 II에 의해 1차 miRNA(pri-miRNA)로 전사됩니다. 다음으로, RNA 결합 단백질 DGRC8과 RNase III 효소 Drosha가 형성한 복합체가 pri-miRNA를 절단하여 전구체 miRNA(pre-miRNA)를 생성하고, 이는 엑스포틴 5를 통해 세포질로 내보내집니다. 세포질에 들어가면 Dicer가 /TRBP 복합체는 pre-miRNA를 절단하여 성숙한 miRNA를 방출합니다. 마지막으로, 성숙한 miRNA가 RISC에 로드되어 Watson-Crick 염기쌍을 통해 표적 mRNA 인식을 유도하고 번역 억제 또는 mRNA 분해를 통해 유전자 침묵을 초래합니다. DGRC8, 디조지 증후군 중요 영역 8; RISC, RNA 유도 침묵 복합체; TRBP, TAR RNA 결합 단백질. BioRender.com으로 제작되었습니다.

대부분의 연구에서는 miRNA의 5' 말단에 있는 도메인(뉴클레오티드 위치 2에서 7까지 확장되는 시드 서열이라고 함)이 표적 mRNA의 3' 비번역 영역(3'UTR)에 있는 특정 영역과 상호작용하여 유도하는 것으로 나타났습니다. 번역 억제 및/또는 mRNA 탈아데닐화 및 붕괴(3-5). 그러나 miRNA 결합 부위는 5'UTR(25, 26), 코딩 서열(27) 및 유전자 프로모터(28-30)를 포함한 다른 영역에서도 확인되었습니다. miRNA는 주로 유전자 억제와 연관되어 있지만 miRNA에 의한 전사 후 상향 조절은 특정 상황에서 발생할 수도 있습니다(28, 31-33).

miRNA 매개 유전자 조절과 관련된 몇 가지 독특한 특징이 있습니다(34, 35). 첫째, 단일 miRNA는 수백 개의 mRNA를 표적으로 삼고 억제할 수 있지만 일반적으로 각 표적에 대해 상대적으로 약한 정도입니다. 따라서 miRNA는 유전자 발현을 미세 조정하는 기능을 하는 것으로 생각됩니다. 그러나 각 mRNA는 동일하거나 다른 miRNA에 대한 여러 결합 부위를 포함할 수 있으므로 결과적인 결합 효과는 더욱 강력합니다(36-38). 더욱이, 주어진 신호 전달 경로 내의 여러 구성요소는 개별 miRNA 또는 miRNA 클러스터에 의해 조절될 수 있습니다(39, 40). 둘째, miRNA가 리보솜 수준에서 단백질 합성을 차단하기 때문에 miRNA 매개 억제는 비교적 빠르게 발생합니다(41). 셋째, miRNA는 특정 세포하 구획에 집중되어 부위별 단백질 번역을 조절할 수 있습니다(42, 43). 마지막으로, miRNA의 작은 하위 집합이 다양한 세포 유형의 전체 miRNA 풀을 지배하며, 이는 이들이 마스터 miRNA로 기능할 수 있음을 시사합니다(44). 이 아이디어에 따르면, 가장 풍부한 miRNA 중 일부는 많은 세포 유형에서 AGO 단백질에 의해 매개되는 전사 후 조절의 대부분을 구성하는 것으로 보입니다(44, 45). 예를 들어, 불멸화 인간 배아 신장 세포주(HEK293T)에서 백만 개당 100~1000개 읽기 미만으로 발현된 miRNA는 높은 처리량 miRNA 센서 라이브러리를 사용하여 억제 활성을 나타내지 않았습니다(45).
miRNA의 생물 발생은 다양한 세포 신호에 반응하여 적절한 miRNA 발현을 보장하기 위해 엄격한 공간적 및 시간적 제어를 받습니다. miRNA 생합성 조절은 miRNA 유전자의 인핸서 및/또는 프로모터에 결합하는 전사 인자, pri-miRNA의 DROSHA 처리, pre-miRNA의 DICER 처리, RNA 메틸화, miRNA 전구체 편집, 아데닐화, 유리딜화, RNA 붕괴 및 기타 여러 메커니즘. 이에 대한 심층적인 검토는 하씨와 김(46)의 글을 참고하기 바란다. 최근 슈퍼인핸서는 전사와 DROSHA/DGCR8-매개 pri-miRNA 처리를 모두 향상시켜 miRNA 생합성을 제어하는 새로운 종류의 규제 요소로 등장했습니다. 광범위한 H3K4me3 시그니처와 결합하여 슈퍼인핸서 활성은 조직 특이적 miRNA 발현 패턴 및 기능을 형성합니다(47).

