1부 신장 질환에서 면역 조절제로서의 Heme Oxygenase-1의 역할
Jun 05, 2023
추상적인
단백질 헴 옥시게나제(HO)-1는 여러 면역학적 과정의 조절과 관련되어 있습니다. 신장 손상이 면역 메커니즘에 의해 영향을 받고 다양한 신장 질환 형태가 자가면역 질환의 결과일 수 있다는 것은 잘 알려져 있습니다. 현재 연구는 신장 질환에서 HO-1의 역할을 자세히 설명하고 면역 매개 질병 형태의 동물 모델과 입원 연구.
키워드
헴 옥시게나아제; 신장; 면역 손상.

소개 Heme oxygenase(HO)-1는 염증, 세포 사멸, 세포 보호와 같은 면역학적 및 병리생리학적 과정의 조절과 관련이 있으며, 이는 주로 다운스트림 이펙터 분자, 일산화탄소, 빌리루빈 및 빌리베르딘을 통해 이루어집니다. 염증과 자가면역질환은 신장질환의 핵심요인이다. 신장에서 사구체 모세혈관은 염증의 표적이 되어 궁극적으로 심각하고 돌이킬 수 없는 조직 손상을 일으킬 수 있습니다. 면역 매개 형태의 신장 손상에 HO-1가 관여하는 것이 광범위하게 연구되었습니다. 현재 연구는 다양한 형태의 신장 손상에서 질병 발현 및 진행을 유도하는 면역학적 메커니즘의 중재자로서 HO-1의 잠재적인 역할을 자세히 설명합니다.
다양한 형태의 신장 손상은 일반적으로 신장 사구체의 손상으로 인해 발생합니다. 고도로 특화된 구조와 기능으로 인해 신장 사구체는 특히 손상에 취약한 것으로 알려져 있습니다. 간단히 말해서, 사구체(그림 1)는 사구체(Bowman's) 캡슐로 둘러싸인 삼중 세포 구조입니다. 내피 세포는 사구체 기저막(GBM)의 내강측에 늘어서 있습니다. podocytes라고도 알려진 상피 세포는 GBM의 외부 표면에 고정되어 있습니다. 메산지움 세포는 모세혈관 고리를 지지합니다. 사구체는 복잡한 미세혈관층인 사구체 다발을 형성하며, 이는 고분자량 분자와 순환 세포를 유지하면서 매우 선택적인 플라즈마 필터 역할을 합니다(그림 1).

HO-1 및 IgA 신병증
IgA 신병증은 사구체에 IgA 면역 복합체의 침착을 특징으로 하는 만성 사구체신염의 한 형태입니다. 전 세계적으로 사구체신염의 가장 흔한 형태이다(1).대부분의 경우가 특발성이나 최근에는 다양한 감염(Haemophilus para in. influenza, HIV cytomegalovirus) 후에 이차적인 형태의 질병이 나타났다[2].
증상으로는 일반적으로 열성 감염 에피소드 1~2일 후에 육안적 혈뇨가 시작되어 감염성 사구체신염과 유사한 증상이 나타납니다. lgA 환자의 소변 분석에서 변형된 적혈구의 존재와 때때로 적혈구 주형이 발견되었습니다. 가벼운 단백뇨(<1 g/day) is also typical and may occur without hematuria, while serum creatinine levels are usually normal at diagnosis [3].
IgA 신병증을 일으키는 병원성 기전은 아직 알려지지 않았지만 축적된 증거는 IgA(갈락토스 결핍 IgA1)의 비정상적인 글리코실화 패턴으로 시작하여 불량한 O-갈락토실화된 lgA1(gd -IgA1) 혈액 순환에서 순환하는 자가 항체 생성을 유발하고 결과적으로 메산지움에서 면역 복합체의 형성 및 침착을 유발합니다[4,5].
IgA 신병증 진단은 증식성 또는 괴사성 분절 병변의 병소가 있는 메산지움에 위치한 과립형 IgA 및 보체 인자 3(C3) 침착물을 나타내는 신장 생검 및 면역형광법으로 확인됩니다. 그러나 mesangiallgA 침착물은 비특이적인 것으로 간주되며 면역글로불린 A 관련 혈관염, HIV 감염, 건선, 폐암 및 결합 조직의 기타 여러 장애와 같은 많은 다른 장애에서 발견될 수 있습니다. IgA 환자에게서 채취한 신장 조직 절편을 전자현미경으로 검사한 결과 세포충실도가 증가했고 메산지움의 기질이 증가했으며 호중구의 모세혈관 내 증식, 내피하 침착물이 관찰되었습니다. 마지막으로, 정상 수준의 보체 인자는 면역분석으로 검출되는 반면, 상승된 lgA 혈장 농도는 때때로 혈청 전기영동으로 검출될 수 있습니다(6).

Cistanche 보충제 및 Cistanche 알약
산화질소(NO) 및 고급 산화 단백질 제품(AOPP)은 산화 스트레스의 강력한 마커이며, 심각한 IgA 사구체병증 환자의 혈청 샘플에서 높은 농도가 결정되었습니다[7]. Nakamuraet al. IgA 신염을 앓고 있는 환자를 건강한 대조군과 비교하여 IgA의 산화 스트레스에 대한 노출이 신장 손상의 진행에 해로운 중요성을 드러냈습니다[8]. 이는 SOD(superoxide dismutase)의 과소발현과 ROS(reactive oxygen species) 소거 능력의 억제로 인한 조직 손상의 악화 때문일 수 있습니다(10). 또한, 연구에서는 GT 길이가 더 짧을 때(S-대립유전자) HO-1 발현을 증가시키는 HO-1 유전자 프로모터의 디뉴클레오타이드 구아노신 티민(GT) 반복 다형성을 확인했습니다. 더 길다(L-대립유전자). 이 두 가지 다른 대립유전자는 많은 다른 신장 질환의 발병과 진행에 영향을 미칠 수 있으며[9], 여러 연구에서 짧은 (GT)n 반복과 더 높은 HO-1 유도율 사이의 직접적인 연관성을 보여주었습니다. IgA 신병증의 진행[10].
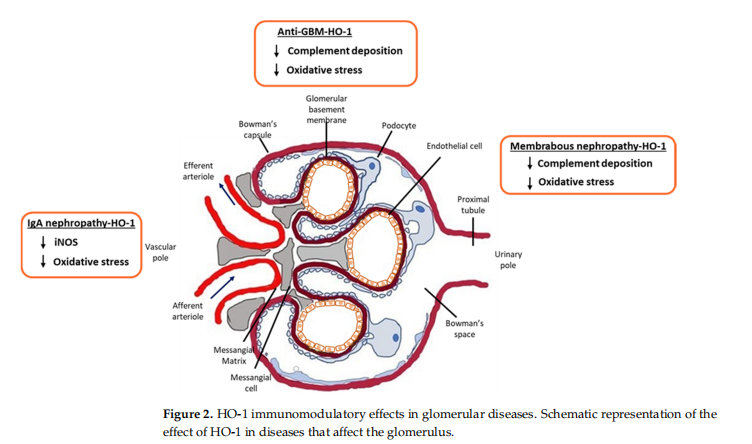
혈관 내 용혈 후, HO-1의 천연 기질이자 보체 캐스케이드의 강력한 활성제인 자유 헴이 방출됩니다. Heme은 대체 보체 경로를 활성화하는 것으로 보고되었으며[11] 따라서 보체 매개 신장 손상과 관련이 있을 수 있습니다[12]. 자유 헴은 Toll-like receptor 4 및 ROS 의존적 경로의 활성화를 통해 선천적 면역 반응에 영향을 미치며, 이는 복잡한 신호 전달 경로를 통해 전염증성 사이토카인의 발현을 촉진합니다. 또한 heme 분해 부산물(CO, biliverdin, bilirubin) 및 HO-1는 IL-10와 같은 항염증성 사이토카인의 분비를 상향 조절하는 핵심 분자를 구성합니다[13](그림 2). 반면에 cyclooxygenase-2(COX-2) 및 inducible nitric oxide synthase(iNOS)와 같은 많은 전 염증 효소는 자유 헴이 충분하지 않아 기능이 손상될 수 있는 혈액 단백질입니다. heme은 HO-1 [14]에 의해 촉매되었습니다. 미세 및/또는 거시적 혈뇨는 사구체에서 HO-1의 잠재적 유도를 암시하는 IgA 신병증의 전형적인 증상입니다[15]. 이전 연구에서는 시험관 내에서 사구체 HO-1 발현을 유도하기 위해 다양한 농도의 hemin을 사용했으며 hemin 농도가 200 μM의 임계 수준에 도달했을 때 HO{-1 발현이 감소하기 시작했다고 보고했습니다. 이것은 부분적으로 다양한 형태의 사구체 질환이 자유 라디칼(OH-), 과산화수소(H2O2) 및 활성 Fe의 수치를 증가시킨다는 사실에 의해 설명될 수 있습니다.2 플러스. 이들은 H2O의 헴 분해에 의해 더욱 강화될 수 있습니다. 따라서 HO-1 표현 제한 메커니즘이 필요할 수 있습니다[16].
IgAN의 임상 경과는 매우 다양합니다. 많은 경우에 질병은 눈에 띄지 않고 치료가 필요하지 않습니다. 질병의 진행에 영향을 미치는 가장 중요한 매개변수는 단백뇨의 정도, 조절되지 않는 고혈압, 생검에서 조직병리학적 병변을 포함합니다[17].
환자 평가는 일반적으로 조직학적 소견, eGFR, 단백뇨 정도, 혈압 값, 생검 전 약물, 인구통계(성별, 연령, 민족성)와 같은 매개변수를 사용하는 "IgA 신병증 예측 도구"(IIgAN-PT)로 수행됩니다. ) 말기 신장 질환(ESRD)으로의 신장 진행의 개별 5년 위험도를 추정합니다. IIgAN-PT 결과와 독립적으로 모든 환자는 지지 고혈압 및 단백뇨 치료를 받아야 합니다. 지지 요법은 안지오텐신 수용체 차단제(ARB) 또는 안지오텐신 전환 효소 억제제(ACEi)와 같은 레닌-안지오텐신 축삭을 억제하는 약물로 구성됩니다[18]. 이들은 전신 및 사구체내 혈압을 모두 감소시켜 고혈압으로 인한 사구체 손상을 감소시키고 단백뇨의 정도를 낮춥니다. 환자의 eGFR이 30mL/min/1.73m보다 큰 경우2, 그들의 치료에 나트륨-포도당 공동 수송체 2(SGLT2)를 추가하면 단백뇨를 더 줄일 수 있습니다[19]. 마지막으로, 독성 효과로 인해 스테로이드 사용은 신기능이 급격히 감소하고 조절되지 않는 단백뇨가 증가하는 경우에만 지원됩니다[20].
HO-1 및 막성 신병증(MN)
MN은 자가면역 사구체 질환이며 성인 인구에서 신증후군의 주요 원인입니다. 증상으로는 잠행성 부종, 경미한 요침전을 동반한 현저한 단백뇨, 정상 또는 악화된 신장 기능, 정상 또는 상승된 혈압 등이 있습니다 21]. 자연 관해는 환자의 약 30%에서 볼 수 있습니다. 대부분의 경우(약 70%) MN은 특발성으로 보고됩니다. 이 경우 족세포에서 발견되는 M형 포스포리파제 A2 수용체(PLA2R)에 대한 항체는 특정 위치에 연결되어 보체 막 공격 복합체(MAC, C5b-9)를 활성화하는 면역 복합체를 제자리에서 형성합니다. 그러나 MN은 특정 병인학적 요인으로 인해 이차 MN으로 발전할 수도 있습니다. 주요 원인은 고형 종양(폐, 결장, 직장, 신장, 유방 위), 자가 면역 질환 및 미생물 감염입니다. 사실, 말라리아나 주혈흡충증과 같은 감염이 만연한 지역에서는 후자가 MN의 주요 원인으로 구성될 것입니다[21].
MN의 진단은 또한 신장 생검을 기반으로 합니다. 광학 현미경 검사는 면역 복합체의 상피하 형성에 대한 반응으로 GBM의 확산 비후를 보여줍니다. 세포 증식이나 염증 세포는 검출되지 않습니다. 사구체 기저막은 균질하게 두꺼워지지만 점차적으로 상피하 공간으로 돌출부를 생성하여 결국 면역 복합체를 포용하고 통합합니다. Immunofluorescence는 기저막을 따라 lgG 및 C3의 세분화된 침전물을 감지합니다. 반면에 전자현미경은 상피하 영역의 조밀한 침전물뿐만 아니라 족세포 발 과정의 확산 소멸을 발견합니다(21). Heymann 등은 면역 복합체의 병원성 역할이 (22) Heymann 신염(HN)은 근위세뇨관 brush border 항원(active HN) 또는 그에 상응하는 항체(passive HN)를 쥐에 주입하여 유도되었습니다. 쥐의 근위 세뇨관 및 족세포 발 과정에서(23) 능동 및 수동 HN에 대한 연구는 상피하 침착물이 순환하는 면역 복합체를 통해서가 아니라 체질 내인성 항원에 대해 제자리에서 형성됨을 입증했습니다.24) HN 모델을 통해 연구자들은 이 모델에서 족세포 손상 및 단백뇨에서 보체 매개 세포독성의 중요한 역할을 식별하기 위해 HN에 대한 초기 연구는 C3 및 C5b-9가 면역 침착물에 공동 국소화됨을 보여주었습니다. 또한 수동 HN 쥐의 소변에 존재하는 족세포가 C5b-9로 코팅되어 있음이 밝혀졌습니다[25]. HN 진행은 C5b-9의 지속적인 소변 배설과 상관관계가 있었으며, 이는 GBM에서 지속적인 보체 활성화를 나타냅니다.

허바 씨스탄체
보체 조절 단백질(CRP)로 알려진 막 결합 단백질은 보체 활성화를 제거하여 MAC 형성 및 용해를 제거하는 역할을 합니다. 잘 알려진 CRP는 부패 촉진 인자(DAF, CD55)입니다. DAF는 C3 및 C5 전환 효소의 붕괴를 가속화하여 MAC 형성을 제한합니다[26]. 쥐에서 다른 CRP는 Crry와 CD59입니다[26]. 쥐에서 DAF 발현에 대한 연구는 족세포에서만 구성적 DAF 발현을 나타냈다[27]. 보체 유발 발세포 손상에서 DAF의 보호 역할을 연구하기 위해 이전 연구에서 DAF 고갈(Daf -/-)의 형질전환 쥐 모델을 생성했습니다[28]. Daf plus/plus 및 Daf -/- 래트에서 조직학적, 임상적 및 생화학적 검사(크레아티닌 수치, 알부민뇨, 소변 알부민 대 소변 크레아티닌 비율)는 보체 고정 항체 항-Fx1A 투여 전에 유의미한 차이를 나타내지 않았습니다. 항-Fx1A 투여 후, Daf -/- 래트에서 단백뇨 수준이 상당히 상승하였다. 항-Fx1A를 받은 래트의 면역형광 염색은 Daf 플러스/플러스 래트보다 Daf -/- 래트에서 더 큰 C3 침착을 입증했으며, 이는 족세포 보체-유도 손상에서 DAF의 보호 역할을 시사합니다[28]. 여러 연구에서 HO-1가 DAF를 상향 조절하여 보체 활성화 및 보체 매개 손상을 감소시키는 것으로 나타났습니다[16]. 그런 맥락에서 HO-1 유도는 DAF 유도를 포함한 면역 조절 효과를 통해 보체 매개 사구체신염에 대한 잠재적인 치료 전략으로 유용한 도구가 될 수 있습니다.
앞서 언급한 HO-1의 속성을 탐색하기 위해 Wu et al. 은 BALB/c 마우스에 양이온성 소 혈청 알부민을 정맥 내로 도입하고 동물을 세 그룹으로 나누어 유도된 MN의 실험 동물 모델을 사용했습니다. 첫 번째 그룹은 HO-1 유도제인 코발트 프로토포르피린(CoPP)을 매주 복강내 투여했습니다. 두 번째는 H2O-1 억제제인 주석 프로토포르피린(SnPP); 세 번째는 식염수입니다. MN-CoPP 그룹은 HO-1 상향조절을 보였고 명확한 증상 개선(단백뇨 감소 및 혈청 알부민 및 콜레스테롤 수치의 정상화)을 나타냈습니다. CoPP 치료는 또한 혈청 항-cBSA 항체 생산을 상당히 감소시켰습니다. 면역 형광 염색이 세 그룹 모두에서 양성으로 유지되었지만 MN-CoPP 그룹은 사구체 막에서 더 낮은 강도를 보였고 다른 두 그룹, 특히 MN-SnPP 그룹과 관련된 C3 침착이 감소했습니다. TBARS(thiobarbituric acid reactive substance)와 같은 산화 스트레스 마커의 농도는 혈청과 신장 모두에서 평가되었으며 비 MN 마우스에 대해 현저하게 더 높은 것으로 나타났지만 MN-CoPP 그룹 간에는 상당한 차이가 평가되었습니다. 및 MN-SnPP 그룹. CoPP 치료는 혈청과 신장 모두에서 산화 스트레스 마커를 감소시켰으며, 이는 HO-1가 국소 및 전신 수준에서 항산화 효과를 가질 수 있음을 시사합니다[29].
보체 활성화는 MN에서 미토콘드리아 조절 장애를 겪는 족세포에서 ROS를 유도하는 것으로 보입니다[24]. Pyroptosis는 박테리아 또는 바이러스 감염에 뒤따르는 최근에 확인된 조절된 세포 사멸 유형입니다(40). inflammasomes 및 pro-inflammatory cytokine의 활성화를 포함한 복잡한 신호 경로는 caspase-1의 활성화로 이어지고 결과적으로 막에 기공을 형성하여 세포 사멸 및 과도한 pro-inflammatory cytokine 및 ROS를 초래합니다[30]. Wang et al. 동시 미토콘드리아 탈분극 및 ROS 생산과 함께 podocytes에서 보완 매개 pyroptosis를 설명했습니다. ROS 생산을 차단하면 보체 매개 파이롭토시스가 역전되었습니다. MN 사구체의 면역조직화학은 카스파제-1 및 가스트린 D(GSDMD)와 같은 파이롭토시스 관련 단백질과 족세포에서 발견되는 액틴 관련 단백질인 시냅토포딘의 공동 국소화를 확인했습니다. 또한, C3a 및 C5a는 in vitro에서 족세포에서 caspase-1 및 GSDMD의 과발현을 촉진하고 세포막의 완전성과 족세포 미토콘드리아 막의 탈분극에 영향을 미쳤습니다. MN 환자의 족세포를 주요 파이롭토시스 분자의 억제제와 함께 배양했을 때 C3a와 C5a는 족세포 막 완전성에 영향을 미치지 않았습니다[31].

계피 추출물
최근 연구에서는 열병을 차단하는 데 있어서 HO-1의 역할을 평가했습니다. hemin의 H2O-1 촉매 작용의 부산물인 일산화탄소(CO)는 유도 분자인 NLRP3-ASC의 직접적인 억제를 통해 caspase-1의 활성화를 차단하는 것으로 보입니다[32,33] . NFE2- 관련 인자(Nrf2)는 항산화 및 세포 보호 분자의 발현을 유도하여 산화 스트레스에 대한 세포 항산화 반응을 조절하는 전사 인자이며, 그 중 하나는 H2O-1입니다[34]. 시르투인은 족세포의 세포골격의 완전성에 필수적인 탈아세틸라제 단백질입니다[35]. 스트레스 조건에서 시르투인은 족세포에서 HO-1 발현의 상향 조절을 유도하는 Nrf2의 과발현을 유도하는 것으로 보입니다[36]. 쥐 신장 허혈/재관류(I/R) 손상 모델에서 Diao et al. NF-E2-관련 인자/헴 옥시게나제-1(Nrf2/HO-1)의 역할을 파이롭토시스에 대한 보호 인자로 조사했습니다[37]. 단백질 아르기닌 메틸화 전이 효소 5(PRMT5)는 배아 발달, 조직 항상성 및 악성 종양을 비롯한 수많은 생리학적 및 병리학적 상태에 관여합니다[38]. PRMT5는 I/R 유발 ROS 생성과 관련이 있습니다. 그것의 억제는 Nrf2/HO-1의 상향 조절, 산화 스트레스 마커의 감소 및 조직 손상의 감소를 가져왔습니다[37].
MN의 매우 다양한 과정은 신장 손상 진행의 위험에 따라 개인화된 치료를 필수적으로 만듭니다. 자발적 완화는 환자의 약 30%에서 발생할 수 있습니다. 그러나 단백뇨가 있는 모든 환자는 3~6개월 동안 안지오텐신 수용체 차단제(ARB) 또는 ACEi로 치료해야 합니다. 최신 MN 치료 가이드라인에 따르면, 모든 환자는 치료 전과 치료 중 혈중 항-M형 포스포리파제 A2 수용체(PLA2R) 항체 수치를 평가해야 합니다. 테스트는 완화를 나타냅니다. 코르티코스테로이드와 시클로포스파마이드 투여는 보조 요법과 함께 중증 신증후군 및 질병 발병 시 급격한 신기능 저하가 있는 환자에게 권장됩니다[39]. 중등도에서 고위험 환자의 경우 지지 요법만으로 6개월 이내에 관해에 도달하지 못한 경우 리툭시맙, 칼시뉴린 억제제(CNI) 및 코르티코스테로이드와 시클로포스파미드를 병용하는 면역억제 치료를 사용할 수 있습니다. 또는 재발성 감염[18].
참조
1. Barratt, J.; Feehally, J. IgA 신장병증. J.Am. Soc. 네프롤. JASN 2005, 16, 2088–2097. [교차 참조]
2. 사하, MK; 줄리안, 학사; 노박, J.; Rizk, DV 이차 IgA 신병증. 신장내과 2018, 94, 674–681. [교차 참조]
3. 펜폴드, RS; 프렌데키, M.; McAdoo, S.; Tam, FW 원발성 IgA 신병증: 현재의 과제 및 전망. 국제 J. 네프롤. 리노프 디스. 2018, 11, 137–148. [CrossRef] [펍메드]
4. Suzuki, H. 멀티 히트 병인에 기초한 IgA 신증에 대한 바이오마커. 클린. 특급 네프롤. 2019, 23, 26–31. [CrossRef] [펍메드]
5. 도츠, V.; 비스콘티, A.; 로맥스-브라운, HJ; 클레르크, F.; 힙그레이브 에더빈, AL; Medjeral-Thomas, NR; 쿡, HT; 피커링, MC; 우러, M.; Falchi, M. 혈청 면역글로불린 A의 O- 및 N-당화는 IgA 신병증 및 사구체 기능과 관련이 있습니다. J.Am. Soc. 네프롤. JASN 2021, 32, 2455–2465. [교차 참조]
6. 야우, T.; 코베트, 에스엠; 슈워츠, MM; Cimbaluk, DJ IgA 신병증의 옥스퍼드 분류: 후향적 분석. 오전. J. 네프롤. 2011, 34, 435–444. [교차 참조]
7. Descamps-Latscha, B.; Witko-Sarsat, V.; Nguyen-Khoa, T.; 응우옌, AT; 가우송, V.; Mothu, N.; 카르도소, C.; 노엘, LH; 게린, AP; 런던, GM; 외. IgA 신병증 진행의 조기 예측: 단백뇨와 AOPP는 강력한 예후 지표입니다. 신장내과 2004, 66, 1606–1612. [CrossRef] [펍메드]
8. 나카무라, T.; 이노우에, T.; 스가야, T.; Kawagoe, Y.; 스즈키, T.; Ueda, Y.; 코이데, H.; Node, K. 면역글로빈 A 신병증이 있는 정상혈압 환자에서 요로 간형 지방산 결합 단백질 수치에 대한 olmesartan과 temocapril의 유익한 효과. 오전. J. Hypertens. 2007, 20, 1195–1201. [CrossRef] [펍메드]
9. Courtney, AE; 맥나미, 태평양 표준시; 헤가티, S.; 미들턴, D.; Maxwell, AP Association of functional haem oxygenase-1 유전자 프로모터 다형성과 다낭성 신장 질환 및 IgA 신장병증. 네프롤. 다이얼. 이식. 끄다. 출판 유로. 다이얼. 번역 Assoc.-Eur. 렌. 협회 2008, 23, 608–611. [교차 참조]
10. 진현주; 조현정 ; 이태우; 나, 켄터키; 윤효진; 채동원; Kim, S.; 전, 미국; 도, JY; 박정우; 외. heme oxygenase-1 유전자형은 진단 시 IgA 신병증의 신장애에 대한 위험 인자이며, 이는 사망률의 강력한 예측인자입니다. J. Korean Med. 과학. 2009, 24, S30–S37. [교차 참조]
11. 멀, NS; 그루넨발트, A.; 라자라트남, H.; Gnemmi, V.; Frimat, M.; Figueres, ML; Knockaert, S.; 부제크리, S.; Charue, D.; 노에, R.; 외. 혈관내 용혈은 무세포 헴 및 헴 적재 미세소포를 통해 보체를 활성화합니다. JCI 인사이트 2018, 3. [CrossRef]
12. Frimat, M.; 타바린, F.; 디미트로프, JD; Poitou, C.; Halbwachs-Mecarelli, L.; Fremeaux-Bacchi, V.; Roumenina, LT 비정형 용혈성 요독 증후군에 대한 2차 히트로서 헴에 의한 보체 활성화. 혈액 2013, 122, 282–292. [교차 참조]
13. Li, Y.; Ma, K.; Han, Z.; 치, 엠.; 사이, X.; 주, P.; 딩, Z.; 송엘; Liu, C. 신장 질환에서 Heme Oxygenase-1의 면역 조절 효과. 앞쪽. 중간 2021, 8, 708453. [교차 참조]
14. 고셀린, R.; 제니, V.; Soares, MP heme oxygenase에 의한 세포 보호 메커니즘-1. 안누. Pharmacol 목사. 독성. 2010, 50, 323–354. [교차 참조]
15. 셰퍼드, M.; Dhulipala, P.; 카바리아, S.; 아브라함, NG; Lianos, EA Heme oxygenase-1는 쥐의 네프론에 위치합니다. 네프론 2002, 92, 660–664. [교차 참조]
16. 데치카, MG; Lianos, 신장 손상에서 Heme Oxygenase-1(HO-1)에 의한 보체 활성화의 EA 규정. 항산화제 2021, 10, 60. [CrossRef] [PubMed]
17. 트리마르키, H.; 배럿, J.; Cattran, DC; 쿡, HT; 코포, R.; 하스, M.; 리우, ZH; 로버츠, IS; 유자와, Y.; 장허; 외. 2016년 IgA 신병증의 옥스퍼드 분류: IgA 신병증 분류 작업 그룹의 업데이트. 신장내과 2017, 91, 1014–1021. [교차 참조]
18. 로빈, BH; 애들러, SG; 배럿, J.; Bridoux, F.; 버지, KA; 찬, TM; 쿡, HT; 페르벤자, FC; 깁슨, KL; 글래삭, RJ; 외. 사구체 질환 관리를 위한 KDIGO 2021 지침 요약. 신장내과 2021, 100, 753–779. [CrossRef] 19. Barratt, J.; Floege, J. SGLT-2 IgA 신병증 억제: 치료의 새로운 표준? 신장내과 2021, 100, 24–26. [CrossRef] [펍메드]
20. 신장 질환: 글로벌 결과 향상 사구체 질환 작업 그룹. KDIGO 2021 사구체질환 관리 임상진료지침. 신장내과 2021, 100, S1–S276. [CrossRef] [펍메드]
21. KC 케리; Blumenthal, S.; 쿨카르니, V.; 벡, L.; Chongkrairatanakul, T. 원발성 막성 신장병: 포괄적인 검토 및 역사적 관점. 대학원 중간 J. 2019, 95, 23–31. [교차 참조]
22. 헤이만, W.; 해켈, DB; Harwood, S.; 윌슨, SG; Hunter, JL 프로인트 보조제 및 쥐 신장 현탁액에 의한 쥐의 신증후군 생산. 절차 Soc. 특급 비올. 약. Soc. 특급 비올. 중간 1959, 100, 660–664. [교차 참조]
23. Farquhar, MG; 사이토, A.; Kerjaschki, D.; Orlando, RA Heymann 신염 항원 복합체: Megalin(gp330) 및 RAP. J.Am. Soc. 네프롤. JASN 1995, 6, 35–47. [교차 참조]
24. Cybulsky, AV; 퀴그, RJ; Salant, DJ 실험적 막성 신증 redux. 오전. J. Physiol. 렌. 피시올. 2005, 289, F660–F671. [교차 참조]
25. 마, H.; 산도르, DG; Beck, LH, Jr. 막성 신증에서 보체의 역할. 세민. 네프롤. 2013, 33, 531–542. [CrossRef] [펍메드]
26. 미와, T.; 송, WC 막 보완 조절 단백질: 동물 연구 및 인간 질병과의 관련성에 대한 통찰력. 국제 면역약물. 2001, 1, 445–459. [CrossRef] [펍메드]
27. 바오, L.; 스필러, OB; 세인트 존, PL; 하스, M.; 핵, BK; 렌 지.; 커닝햄, PN; Doshi, M.; 에이브러햄슨, DR; 모건, BP; 외. 쥐의 신장에서 부패 촉진 인자 발현은 족세포의 정단 표면으로 제한됩니다. 신장내과 2002, 62, 2010–2021. [교차 참조]
28. 데치카, MG; Goudevenou, K.; Geurts, AM; Gakiopoulou, H.; 그라프사, E.; Lianos, EA 클러스터링된 규칙적으로 간격을 둔 짧은 회문 반복(CRISPR)/관련 단백질 9(Cas9), 게놈 편집을 사용하여 새로운 붕괴 가속 인자(DAF) 녹아웃 쥐 모델의 생성. 트랜스제닉 해상도 2021, 30, 11–21. [CrossRef] [펍메드]
29. 우, CC; 루, KC; 린지제이; Hsieh, HY; Chu, P.; 린, SH; Sytwu, HK 멜라토닌은 내인성 헴 옥시게나아제-1를 강화하고 면역 반응을 억제하여 실험용 쥐의 막성 신장병을 개선합니다. J. Pineal Res. 2012, 52, 460–469. [교차 참조]
30. Yu, P.; 장 X.; 리우, N.; Tang, L.; Peng, C.; Chen, X. Pyroptosis: 메커니즘 및 질병. 신호 전달. 표적. 그. 2021, 6, 128. [교차 참조]
31. 왕, H.; Lv, D.; Jiang, S.; 허우, Q.; 장, L.; 리, S.; 주, X.; Xu, X.; 웬, J.; Zeng, C.; 외. 보체는 미토콘드리아 기능 장애를 매개하여 막성 신증에서 족세포 열분해증을 유도합니다. 세포 사멸 Dis. 2022, 13, 281. [교차 참조]
32. Shi, J.; Zhao, Y.; 왕케이; 시, X.; Wang, Y.; 황, H.; Zhuang, Y.; 카이, T.; 왕, F.; Shao, F. 염증성 caspases에 의한 GSDMD의 절단은 pyroptotic cell death를 결정합니다. 자연 2015, 526, 660–665. [교차 참조]
33. 푸, L.; 장 DX; 장, LM; Song, YC; 리우, FH; 리, 와이.; 왕 XP; 정, WC; 왕 XD; 구이, CX; 외. 외인성 일산화탄소는 출혈성 쇼크 및 소생술 모델에서 미토콘드리아 DNA 유도 해마 발열증으로부터 보호합니다. 국제 J.Mol. 중간 2020, 45, 1176–1186. [교차 참조]
34. Ryter, SW Heme Oxgenase-1, 조절된 세포 사멸 및 염증의 주요 조절자. 세포 2021, 10, 515. [CrossRef]
35. 나카타니, Y.; Inagi, R. Podocytes에서 SIRT1을 통한 후생적 조절. 현재 고혈압. 2016, 12, 89–94 개정. [CrossRef] [펍메드]
36. 첸, XJ; 우, WJ; Zhou, Q.; 지에, JP; 첸, X.; 왕, F.; Gong, XH Advanced glycation end-products는 당뇨병 상태에서 AGE 수용체와 상호 작용하여 Sirt1/Nrf2 축을 통해 산화 스트레스를 유도합니다. 제이셀. 생화학. 2018. [크로스리프] [펍메드]
37. 디아오, C.; 첸, Z.; Qiu, T.; 리우, H.; 양유; 리우, X.; 우제이; Wang, L. PRMT5의 억제는 신장 허혈-재관류 손상의 마우스 모델에서 Nrf2/HO-1 신호 경로의 활성화를 통해 산화 스트레스 유발 파이로프토시스를 약화시킵니다. 산화제 셀. 장수. 2019, 2019, 2345658. [CrossRef] [PubMed]
38. 김효리; Ronai, ZA PRMT5 기능 및 암에서의 표적화. 세포 스트레스 2020, 4, 199–215. [교차 참조]
39. Fernandez-Juarez, G.; 로하스-리베라, J.; Logt, AV; Justino, J.; 세비야노, A.; Caravaca-Fontan, F.; 아빌라, A.; 라바스코, C.; Cabello, V.; 바렐라, A.; 외. STARMEN 시험은 원발성 막성 신장병증에서 코르티코스테로이드와 시클로포스파미드의 교대 치료가 타크로리무스와 리툭시맙의 순차적 치료보다 우수함을 나타냅니다. 신장내과 2021, 99, 986–998. [교차 참조]
버지니아 Athanassiadou 1 , Stella Plavoukou 1 , Eirini Grapsa 1 및 Maria G. Detsika 2 ,
1. 아테네 국립 및 카포디스트리아 대학교 의과대학 신장내과, Aretaieion 대학 병원, 11528 아테네, 그리스
2. 10675 아테네, 그리스 아테네 국립 및 카포디스트리아 대학교 Evangelismos 병원, GP Livanos 및 M Simou Laboratories, 중환자 의학 및 폐 서비스의 1과






