Cistanche Tubulosa의 물 추출물의 안전성은 규제에 따른 새로운 식품으로
Mar 23, 2022
연락처: Audrey Hu Whatsapp/hp: 0086 13880143964 이메일:audrey.hu@wecistanche.com
EFSA NDA 패널(영양에 관한 EFSA 패널, 새로운 식품 및 식품 알레르기 유발 물질), Dominique Turck, Jacqueline Castenmiller, Stefaan De Henauw, Karen Ildico Hirsch-Ernst, John Kearney, Alexandre Maciuk, Inge Mangelsdorf, Harry J McArdle, Androniki Naska, Carmen Pelaez , 크리스티나 펜티에바, 알폰소 시아니, 프랭크 티스, 소피아 차부리, 마르코 빈세티, 프란체스코 쿠바다, 토마스 프렌젤, 마리나 하이노넨, 로잔젤라 마르첼리, 모니카 노이하우저-베르톨트, 모르텐 폴센, 미구엘 프리에토 마라도나, 요제프 루돌프 헨크 반 러베렌, € 겔브만과 헬레 카트린 크누센
추상적인
유럽연합 집행위원회의 요청에 따라 EFSA 영양, 신규 식품 및 식품 알레르겐 패널(NDA)에 물 추출물에 대한 의견을 제출하라는 요청을 받았습니다.시스탄체세뇨관식품 보조제(FS) 및 특수 의료용 식품(FSMP)에 사용하기 위한 신규 식품(NF)으로 유래합니다. 대상 인구는 임산부와 수유부를 제외한 일반 성인 인구입니다. 신청자는 FS의 경우 1일 최대 섭취량을 2g, FSMP의 경우 최대 사용 수준을 10%로 제안합니다. 추출물의 특징적인 성분은페닐에타노이드배당체(NF의 최소 70%), 특히,에키나코사이드(NF의 25-45%). NF는 2005년 중국에서 혈관성 치매 치료제로 처방의약품으로 승인됐다. 패널은 제안된 NF로 1일 용량 1,800mg으로 치료받은 1,076명의 혈관성 치매 환자를 대상으로 한 3건의 연구에 대한 통합 분석에서 12건의 부작용(AE)이 '확실히', '아마도' 또는 ' NF에 대한 노출과 관련이 있을 수 있습니다. 이들 AE 중 2개는 중증으로 분류되었다(뇌출혈 및 간질). 패널은 보고된 AE가 안전 문제를 제기한다고 생각합니다. 패널은 또한 제공된 독성 연구의 한계, 특히 유전독성 시험 전략에 대한 EFSA 접근 방식의 비준수 및 GLP(우수 실험실 관리 기준) 및 반복 투여 독성에 대한 해당 OECD 지침 문서의 비준수에 주목합니다. 연구. 인체 연구에서 AE의 관점에서 패널은 테스트 지침에 따른 추가 독성 연구는 인체 연구에서 제기된 우려를 극복할 수 없을 것이라고 생각합니다. 패널은 NF의 안전성이 확립되지 않았다고 결론지었습니다.
키워드:새로운 음식,시스탄체 튜불로사, 페닐에타노이드 배당체,에키나코사이드, 식품 보조제, 특수 의료용 식품

1. 소개
1.1. 유럽 위원회에서 제공한 배경 및 참조 조건
2019년 10월 1일, Sinphar Tian-Li Pharmaceutical Co., Ltd.는 유럽연합 집행위원회에 유럽연합(EU) 2015/22831 규정 10조에 따라시스탄체(C.) 세뇨관새로운 식품(NF)으로 추출합니다. 응용 프로그램은 특수 의료 목적을 위한 식품 보조제 및 식품에 C. tubulosa 추출물의 사용을 승인하도록 요청합니다. 신청자는 또한 규정(EU) 2015/2283의 26조에 따라 데이터 보호를 요청했습니다. 규정(EU) 2015/2283의 10(3)조에 따라 유럽 위원회는 유럽 식품 안전청에 C. tubulosa 추출물에 대한 과학적 의견을 NF로 제공할 것을 요청합니다. 또한, 유럽 식품 안전청(European Food Safety Authority)은 신청자가 데이터 보호를 요청하는 독점 데이터가 규정에 따라 의견을 구체화하는 데 사용되었는지, 그렇다면 어느 정도 사용되었는지에 대한 진술을 과학적 의견에 포함하도록 요청받았습니다. 규정(EU) 2015/2283의 26(2)(c)조의 요구 사항.
2. 데이터 및 방법론
2.1. 데이터
이 NF의 안전성 평가는 애플리케이션에 제공된 데이터를 기반으로 합니다.
규정(EU) 2015/2283의 10조에 언급된 NF 신청에 대한 행정 및 과학 요구 사항은 위원회 시행 규정(EU) 2017/24691에 나열되어 있습니다.
NF 응용 프로그램의 프레젠테이션을 위한 일반적이고 구조화된 형식은 NF 응용 프로그램의 준비 및 프레젠테이션에 대한 EFSA 지침(EFSA NDA 패널, 2016)에 설명되어 있습니다. 이 지침에 명시된 바와 같이, NF의 안전과 관련된 모든 이용 가능한(독점, 기밀 및 출판된) 과학 데이터(찬성 및 비선호 데이터 포함)를 제공하는 것은 신청자의 의무입니다.
이 NF 애플리케이션에는 규정(EU) 2015/2283의 26조에 따른 독점 데이터 보호 요청이 포함됩니다. 보호를 위해 신청자가 요청한 데이터는 이 신청에 대한 모든 독성 및 인체 연구를 포함합니다.

2.2. 방법론
평가는 NF 신청에 대한 EFSA 지침(EFSA NDA 패널, 2016)에 명시된 방법론과 EFSA 과학 위원회의 관련 기존 지침 문서에 설명된 원칙을 따릅니다. 평가에 대한 법적 조항은 규정(EU) 2015/2283의 11조와 집행위원회 시행 규정(EU) 2017/2469의 7조에 명시되어 있습니다.
이 평가는 제안된 사용 조건에서 NF의 소비와 관련될 수 있는 위험에만 관련되며 청구된 혜택과 관련하여 NF의 효능에 대한 평가가 아닙니다.
3. 평가
3.1. 소개
적용 대상인 NF는 중국에서 재배되는 C. tubulosa 줄기의 물 추출물이다. 70% 이상 함유페닐에타노이드배당체. NF는 식품 보조제 및 특수 의료용 식품의 성분으로 사용하기 위한 것입니다. 대상 인구는 임산부와 수유부를 제외한 일반 성인 인구입니다.
3.2. NF의 아이덴티티
NF는 건조 줄기에서 추출한 물 추출물입니다.시스탄체세뇨관(쉥크) 와이트.
3.3. 생산 과정
C. tubulosa의 재배는 먼저 기생 식물 C. tubulosa로 접종되는 숙주 식물 Tamarix Chinensis의 재배를 필요로 합니다. C. tubulosa를 수확한 후 줄기를 씻고 조각으로 자르고 말립니다. NF의 생산 공정은 물 추출, 농축, 에탄올 침전 및 분무 건조 단계로 구성됩니다.
3.4. 구성 데이터
두 배치에 대한 근접 분석에 따르면, NF는 100g당 약 93g의 탄수화물, 약 1.3g이 섬유질, 1.5g 단백질, 1.3g 지질, 3.2g 수분 및 0.2g 회분을 포함합니다. 추출물의 주요 성분은페닐에타노이드배당체(NF의 70% 이상) 특히에키나코사이드(NF의 25-45%). 뿐만 아니라에키나코사이드, 다른페닐에타노이드 배당체NF에서 확인된 것은 20 -아세틸락테오사이드, 악테오사이드, 캄프네오사이드 I, 캄프네오사이드 II, 시스탄투불로사이드 A, 시스탄투불로사이드 B1, B2, 시스탄투불로사이드 C1, C2, 크레나토사이드, 디카페오일락테오사이드,에키나코사이드, isoacteoside, Rhodiola side, syringalide A 30 -aL-rhamnopyranoside 및 tubuloside A.
신청자는 다음의 내용을 보여주는 7개 배치의 결과를 제공했습니다.페닐에타노이드배당체그리고에키나코사이드각각 73.5%와 79.8%, 31.9%와 38.9% 사이입니다.
이 7개 배치는 잔류 용매, 중금속 및 미생물학적 매개변수에 대해서도 분석되었습니다. 살충제와 아플라톡신에 대해 NF뿐만 아니라 일부 원료 배치에 대한 추가 테스트를 수행했습니다.

3.4.1. 안정
신청자는 6개의 배치에 대해 48-월(25도 /RH 60%) 및 가속 6-월(40도 /RH 75%) 안정성 테스트를 수행했습니다. 48개월이 끝나갈 무렵,페닐에타노이드배당체그리고에키나코사이드각각 7{14}}.1%와 79.1%, 30.1%와 37.1% 사이였습니다. 가속 저장 조건에서 6개월 말의 범위는 각각 71.3~75.3% 및 28.0~35.1%였습니다.
3.5. 명세서
신청자가 제안한 NF의 사양은 Table 1과 같다.

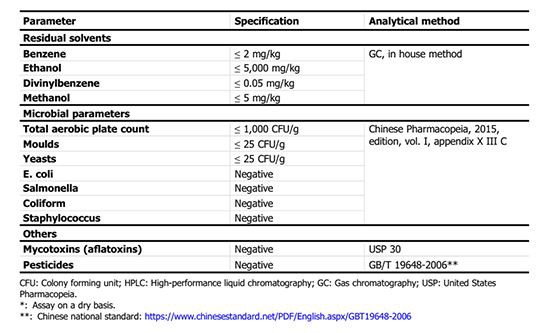
패널은 유전독성 및 발암성인 사양 매개변수 '벤젠'에 주목합니다.
3.6. NF 및/또는 해당 소스의 사용 이력
3.6.1. 소스 사용 이력
신청자에 따르면, 이 식물은 아시아, 특히 중국 전통 의학에서 오랜 사용 역사를 가지고 있습니다. 신청인은 또한 C. tubulosa의 뿌리가 캐나다에서 '의약품 및 건강 제품' 중 하나로 사용된다는 정보를 제공했습니다(Health Canada, 2019).
3.6.2. NF 사용 이력
신청자에 따르면 추출물은 대만에서 일일 최대 450mg의 식품 사용이 승인되었습니다(Taiwan Food and Drug Administration, 2017). 혈관성 치매 치료제로 2005년 중국에서 처방의약품으로 시판 허가를 받았다.
3.7. 제안된 용도 및 사용 수준 및 예상 섭취량
3.7.1. 표적 집단
신청인이 제시하는 대상 인구는 임산부와 수유부를 제외한 일반 성인 인구이다. 이 하위 집단 그룹에 대한 '불충분한 데이터'가 제외된 이유가 되었습니다.
3.7.2. 제안된 용도 및 사용 수준
신청자는 2g/day 사용 수준의 식품 보조제 및 100g/kg 식품의 특수 의료용 식품(FSMP)에 대한 NF의 사용을 제안합니다. FSMP에 대해 NF의 최대 일일 섭취량은 제안되지 않았습니다.
3.8. 흡수, 분포, 대사 및 배설(ADME)
신청자의 문헌 검색을 통해 ADME 및 C. tubulosa 줄기 추출물과 관련된 7개의 논문에 발표된 7개의 연구가 확인되었습니다. 이러한 연구에는 다음의 대사 산물을 연구하기 위한 시험관 내 모델(Li et al., 2016a, 2017)에 대한 정보가 포함되었습니다.에키나코사이드, 시스타노사이드, 악테오사이드 및 이소악테오사이드에키나코사이드및 쥐 모델(Jia et al., 2006; Wang et al., 2009; Cui et al., 2016; Li et al., 2016a,b; Qi et al., 2013)을 사용하여 생체이용률, 분포, 대사를 연구합니다. , 일부 제거페닐에타노이드배당체~와 같은에키나코사이드, 악테오사이드, 및 이소악테오사이드.
3.9. 영양정보
섹션 3.4(구성 데이터)에 제공된 근접 분석을 고려하여 패널은 하루에 NF 2g을 섭취하는 것이 영양학적으로 불리하지 않다고 생각합니다.
3.10. 독성에 관한 정보
신청자는 몇 가지 독성 연구를 제공했으며 신청자에 따르면 모든 연구는 NF로 수행되었지만 연구 보고서에 포함된 정보에 의해 입증되지 않았습니다.
유전독성은 4개의 박테리아 역돌연변이 테스트(후난성 질병통제예방센터, 2005; 생명공학 개발센터, 2008a; 후베이성 질병통제예방센터, 2010a; Liao et al., 2018)에서 연구되었습니다. 체외 염색체 이상 테스트(Liao et al., 2018) 및 2개의 생체 내 마우스 소핵 테스트(생명 공학 개발 센터, 2008b; 후베이성 질병 통제 및 예방 센터, 2010b).
동물 실험과 관련하여, 출원인은 쥐를 대상으로 한 급성 연구(후베이성 질병통제예방센터, 2010b)와 쥐를 대상으로 한 두 가지 아급성 독성 연구(후난성 질병통제예방센터, 2005; Liao et al., 2018)를 제공했습니다. , 쥐에 대한 1건의 아만성 독성 연구(후베이성 질병 통제 및 예방 센터, 2010b) 및 6-만성 독성 및 발암성 연구를 목적으로 하는 쥐와 개에 대한 월간 연구(Peking University School of Pharmaceutical Sciences, 1998a,b. )
패널은 유전독성 시험 전략이 세균 역돌연변이 시험과 시험관내 소핵 시험(EFSA Scientific Committee, 2011)으로 첫 번째 단계에서 유전독성을 다루기 위한 단계적 접근을 요구하는 EFSA 지침을 준수하지 않았다고 지적합니다. 패널은 또한 급성 독성 연구가 NF의 안전성 평가와 관련이 없다고 생각합니다. 또한, 반복 투여 독성 연구는 GLP(우수 실험실 관리 기준) 및 해당 OECD 지침 문서를 준수하지 않습니다. 이는 후베이성 질병통제예방센터(2010b)의 미공개 보고서에서 8페이지로 불충분하게 기술된 아만성 독성 연구에도 적용됩니다.
3.10.1. 인적 데이터
신청자는 표 2에 요약된 NF로 수행된 4개의 인간 연구를 제시했습니다.

중등도 알츠하이머병을 앓고 있는 18명의 환자를 대상으로 한 비통제 공개 시험에서 한 기사가 48주 동안 NF 3{12}0mg 2캡슐을 하루 3회(1일 총 복용량 1,800mg) 치료했습니다. (Guo et al., 2013). 안전 관련 종점은 활력 징후(혈압, 심박수 및 체중)였습니다. 혈액학적 매개변수(백혈구 총 수 및 감별 수, 헤모글로빈, 적혈구 수 및 혈소판 수), 혈액 화학, 심전도(ECG); 및 유해 사례(AE). 24주, 36주, 48주에 이완기 혈압은 0주에 비해 6-7 mmHg만큼 통계적으로 유의하게 낮은 것으로 보고되었습니다. 1명의 환자는 8주 후에 메스꺼움을 보고했으며 1명의 환자는 연구 시작 시 환각을 겪었으며, 12주차에 재발. 1명과 3명의 환자는 24주차와 48주차에 각각 알라닌 아미노트랜스퍼라제(ALT)의 증가(그림은 제공되지 않음)를 보였습니다. 모든 AE는 저자에 의해 경미한 것으로 보고되었습니다. 패널은 통제되지 않은 연구 설계에 주목하고 보고된 AE가 치료와 인과적으로 관련되었는지 여부에 대해 결론을 내릴 수 없다고 생각합니다.
또한 신청자는 혈관성 치매 환자를 대상으로 한 3건의 임상 시험(2상, 3상, 4상)의 안전성 데이터에 대한 통합 분석도 제공했습니다(Sinphar, 2011). 이 보고서는 3-개월 기간 동안 이 세 가지 시험에서 보고된 AE를 분석했습니다. 이 3건의 시험에서 NF를 1일 1,800mg 투여한 환자 1,076명의 안전성 데이터를 에르고로이드 메실레이트 1일 6mg으로 치료한 환자 229명(대조군)의 안전성 데이터(3가지 혼합물의 혼합물)와 비교했습니다. 맥각 알칼로이드) 2개의 대조 시험(즉, II상 및 III상 시험)에서.
이 3개의 연구를 통해 46명의 피험자가 49개의 AE를 경험했습니다. AE의 발생률은 NF 그룹의 경우 3.72%(n=40), 비교 그룹의 경우 3.93%(n=9)였습니다. '중증'으로 분류된 총 8건의 AE 중 6건이 NF 그룹에서 발생했으며, 이는 두 그룹에서 유사한 발생률을 나타냅니다. NF 그룹에 대해 보고된 40개의 AE 중 연구 책임 연구자는 1개가 NF(중등도의 위염)와 '확실히 관련이 있는' 것으로 간주되었으며, 3개의 AE는 NF(중등도의 변비)와 '아마도 관련이 있는' 것으로 간주되었습니다. 정도, 간질 또는 중증도 및 경미한 졸음) 및 8개의 AE는 NF(심각한 정도의 뇌출혈, 위출혈성 궤양 및 중등도의 혼수, 2회 변비, 각각 1회 현기증, 피로 및 졸음)와 '관련될 수 있는' 것으로 분류되었습니다. 가벼운 정도). NF 치료와 확실히, 아마도 또는 관련이 있는 것으로 간주되는 AE의 발생률은 약 1.1%였습니다. 이 통합 분석의 저자에 따르면 C. tubulosa 줄기 추출물은 연구 집단, 즉 혈관성 치매로 고통받는 환자에게 '합리적으로 안전한' 것으로 나타났습니다. 이 보고서는 또한 5-중국에서 혈관성 치매 치료를 위해 처방약으로 승인된 항목에 대한 정기 안전성 업데이트 보고서를 참조했으며, 이는 2005년 시판 승인 이후 치료를 받은 844명의 환자에 대해 AE가 발생하지 않았음을 나타냅니다. 보고되었다.

4. 토론
패널은 3건의 인간 연구에 대한 통합 분석이 1,800mg의 일일 용량으로 제안된 NF로 치료받은 1,076명의 혈관성 치매 환자를 대상으로 했다고 언급합니다. 패널은 또한 인체에 대한 안전성을 평가하는 접근 방식과 인체 연구의 설계(특히 II상 및 III상 연구에서 대조약으로 승인된 약물의 사용)의 임상 개발을 위해 취한 일반적인 접근 방식을 따랐다고 언급합니다. 새로운 음식이 아닌 마약. 위약 대조군 대신에 대조약으로 약물을 사용하는 것은 NF의 안전성 평가를 위한 그러한 연구에서 도출할 수 있는 결론을 제한합니다. 약물의 안전성을 평가하는 목적은 특정 환자 그룹에 대한 위험-유익성 평가를 지원하는 것이지만, NF의 안전성을 다루는 무작위 대조 인간 시험은 오히려 위약 대조군과 이상적으로는 일반 인구를 사용해야 합니다.
신청자가 혈관성 치매로 고통받는 환자와 해당 환자에게 안전하다고 생각한 3건의 시험에 대한 통합 분석에서 고려한 것과 달리, 패널은 잠재적인 이점을 고려합니다. 패널은 주 연구 조사자가 NF 치료와 '확실히', '아마도' 또는 '관련 가능성이 있는' 것으로 판단한 1,076명의 피험자를 대상으로 한 3건의 연구에서 12건(1.1%)의 AE 발생에 주목했습니다. 이들 AE 중 2개는 중증으로 분류되었다(뇌출혈 및 간질).
패널은 보고된 AE가 안전 문제를 제기한다고 생각합니다. 패널은 또한 제공된 독성 연구의 한계, 특히 유전독성 시험 전략에 대한 EFSA 지침 미준수 및 GLP 및 반복 투여 독성 연구의 해당 OECD 지침 문서 미준수에 주목합니다. 인체 연구에서 AE의 관점에서 패널은 테스트 지침에 따른 추가 독성 연구는 인체 연구에서 제기된 우려를 극복할 수 없을 것이라고 생각합니다.
5. 결론
패널은 NF의 안전성이 확립되지 않았다고 결론지었습니다.
6. EFSA가 취한 조치
1) 2020년 5월 29일 EFSA는 유럽연합 집행위원회로부터 물 추출물의 안전성에 대한 과학적 의견을 요청하는 서한을 받았습니다.시스탄체세뇨관줄기, 참조. 아레스 (2020) 2872765 – 2020년 3월 6일.
2) 2020년 5월 29일에 물 추출물에 대한 유효한 신청시스탄체세뇨관회사 이름으로 제출된 줄기는 위원회 전자 제출 포털(NF2019/1318)을 통해 유럽 위원회에 의해 EFSA에 제공되었으며 과학적 평가 절차가 시작되었습니다.
3) 2020년 11월 24일 회의에서 NDA 패널은 데이터를 평가한 후 다음과 같은 물 추출물의 안전성에 대한 과학적 의견을 채택했습니다.시스탄체 세뇨관규정(EU) 2015/2283에 따라 NF로 파생됩니다.
From: ' 물추출물의 안전성시스탄체 세뇨관줄기', Dominique Turck 외
---EFSA 저널 2021;19(1):6346
참고문헌
Cui Q, Pan Y, Bai X, Zhang W, Chen L 및 Liu X, 2016. 대사 산물의 체계적인 특성화에키나코사이드그리고악티오사이드~에서시스탄체 세뇨관UPLC-ESI-Q-TOF-MS를 기반으로 한 쥐의 혈장, 담즙, 소변 및 대변에서. 생의학 크로마토그래피, 30, 1406–1415.
생명 공학 개발 센터, 2008a. AMES TEST STA-1 원료의약품(C. tubulosa 추출물). 생명공학 개발센터, 2008b. 마우스 소핵 분석 - STA-1 약물 물질(C. tubulosa 추출물).
EFSA NDA 패널(식이 제품, 영양 및 알레르기에 관한 EFSA 패널), 2016. 규정(EU) 2015/2283의 맥락에서 신규 식품 승인 신청서의 준비 및 제출에 관한 지침. EFSA 저널 2016;14(11):4594, 24페이지 https://doi.org/10.2903/j.efsa.2016.4594
EFSA 과학 위원회, 2011. 식품 및 사료 안전성 평가에 적용 가능한 유전독성 시험 전략에 대한 과학적 의견. EFSA 저널 2011;9(9):2379, 69페이지 https://doi.org/10.2903/j.efsa.2011.2379
Guo Q, Zhou Y, Wang CJ, Huang YM, Lee YT, Su MH 및 Lu J, 2013. 중등도 알츠하이머 치료를 위한 C. tubulosa 배당체 캡슐(Memoregain(®))에 대한 공개 라벨, 비 위약 대조 연구 질병 Am J Alzheimers Dis Other Demen, 28, 363–370.
캐나다 보건부, 2019. 천연 건강 제품 성분 데이터베이스: C. tubulosa 2019. 온라인에서 사용 가능: http://webprod.hc-sc.gc.ca/nhpid-bdipsn/orgReq.do?id{4}}&lang{{ 5}}영어
후베이성 질병통제예방센터, 2010a. C. tubulosa (추출물) Ames 테스트 보고서.
후베이성 질병통제예방센터, 2010b. C. tubulosa의 안전성 독성에 관한 실험 보고서.
후난성 질병통제예방센터, 2005. C. 추출물의 독성학 안전성 평가에 대한 시험 보고서.
Jia C, Shi H, Wu X, Li Y, Chen J, Tu P, 2006. 결정에키나코사이드역상 고성능 액체 크로마토그래피에 의한 쥐 혈청 내 자외선 검출 및 약동학 및 생체 이용률에 대한 적용. 크로마토그래피 저널. B, 생물 의학 및 생명 과학의 분석 기술, 844, 308–313.
Li Y, Zhou G, Peng Y, Tu P 및 Li X, 2016a. 대표적인 3가지의 선별 및 식별페닐에타노이드배당체UPLC/Q-TOF-MS를 사용하여 인간 장내 세균에 의한 Cs Herba의 대사 산물. 제약 및 생물 의학 분석 저널, 118, 167–176.
Li Y, Peng Y, Wang M, Zhou G, Zhang Y 및 Li X, 2016b. UPLC-Q-TOF-MS 결합 패턴 인식 분석을 통해 쥐에서 C. Deserticola와 C. tubulosa 물 추출물의 대사 산물 간의 차이점을 신속하게 스크리닝하고 식별합니다. 제약 및 생물 의학 분석 저널, 131, 364–372.
Li Y, Peng Y, Wang M, Tu P 및 Li X, 2017. 시험관 내 Cs Herba 물 추출물의 인간 위장 대사: 위액, 장액, 인간 장내 세균, 및 장 마이크로솜. 농업 및 식품 화학 저널, 65, 7447–7456.
Liao PL, Li CH, Tsa LS, Kang JJ 및 Chang YW, 2018. C. tubulosa 건강 식품 Memoregain®의 안전성 평가: 유전 독성 및 {{1}일 반복 투여 독성 시험. 식품 및 화학 독성학, 118, 581–588.
북경대학교 약학대학, 1998a. 쥐에서 STA-1의 경구 만성 독성. 북경대학교 약학대학, 1998b. 개의 STA-1에 대한 경구 만성 독성 연구.
Qi M, Xiong A, Li P, Yang Q, Yang L 및 Wang Z, 2013년. 전자분무 이온화 사중극자 비행 시간 탠덤 질량 분석과 결합된 초고성능 액체 크로마토그래피에 의한 쥐 소변의 악테오사이드 및 주요 대사 산물 식별. 크로마토그래피 저널. B, 생물 의학 및 생명 과학의 분석 기술, 940, 77–85.
Sinphar, 2011. 3건의 임상 시험에서 얻은 안전성 데이터의 통합 분석. 대만 식품의약국, 2017. 식품에 사용할 수 있는 원료 목록: C. tubulosa 2017.
Wang Y, Hao H, Wang G, Tu P, Jiang Y, Liang Y, Dai L, Yang H, Lai L, Zheng C, Wang Q, Cui N 및 Liu Y, 2009. 전형적인 페닐에타노이드 배당체,에키나코사이드, 액체 크로마토그래피-이온 트랩-비행 시간 질량 분석 분석을 기반으로 합니다. 탈란타, 80, 572–580.
약어
ADME 흡수, 분포, 대사 및 배설
AE 부작용
ALT 알라닌 아미노전이효소
CFU 식민지 형성 단위
ECG 심전도
FS 식품 보조제
특수 의료용 FSMP 식품
GC 가스 크로마토그래피
GLP 우수 실험실 관행
HPLC 고성능 액체 크로마토그래피
영양, 새로운 식품 및 식품 알레르겐에 관한 NDA 패널
NF 참신한 식품
OECD 경제협력개발기구
상대습도
SC 과학 위원회
TID 하루 세 번
TLC 박막 크로마토그래피
USP 미국 약전

