STEAP1 키메라 항원 수용체 T 세포 및 종양 국소화 IL-12 면역요법을 이용한 진행성 전립선암 표적화
Sep 18, 2023
STEAP1(6대 전립선 상피 항원)은 전립선암의 치료 표적화를 위한 세포 표면 항원입니다. 여기에서 우리는 치명적인 전이성 전립선암에서 전립선 특이 막 항원(PSMA)에 비해 STEAP1의 광범위한 발현과 STEAP{4}}지정 키메라 항원 수용체(CAR) T 세포 치료법의 개발을 보고합니다. STEAP1 CAR T 세포는 낮은 항원 밀도에서의 반응성, 전이성 전립선암 모델 전반에 걸친 항종양 활성, 인간 STEAP1 녹인 마우스 모델에서의 안전성을 입증했습니다. STEAP1 항원 탈출은 치료 저항성의 재발 메커니즘이며 종양 항원 처리 및 제시 감소와 관련이 있습니다. STEAP1 CAR T 세포 치료법과 결합된 콜라겐 결합 도메인(CBD)-IL{15}} 융합 단백질 형태의 종양 국소 인터루킨-12(IL{12}}) 치료법을 적용하면 전립선암의 면역학적으로 차가운 종양 미세환경을 리모델링하고 숙주 면역과 에피토프 확산을 통해 STEAP1 항원 탈출을 막아 항종양 효능을 나타냅니다.

한약재 시스탄체 식물-항종양
Metastatic prostate cancer represents an incurable disease responsible for over 33,000 deaths per year in the United States1. Prostate cancer is critically reliant on androgen receptor (AR) signaling and thus the suppression of gonadal androgen production through surgical or chemical castration (androgen deprivation therapy) has been a mainstay of treatment for advanced disease. However, metastatic prostate cancer inevitably develops resistance to androgen deprivation therapy and enters a stage called metastatic castration-resistant prostate cancer (mCRPC). mCRPC is currently incurable and is considered the end stage of the disease and is associated with a median overall survival of three years2. In the past decade, multiple therapies including an inhibitor of extragonadal androgen synthesis (abiraterone acetate)3, second-generation AR antagonists (enzalutamide)4, radioactive isotope (radium-223)5, and a prostate-specific membrane antigen (PSMA)-specific radioligand therapy (lutetium Lu 177 via votide tetraxetan)6 have been approved for mCRPC. Each of these agents extends survival on average by several months but long-term remissions are rare. Strategies to reprogram the immune system to combat prostate cancer first gained traction with the clinical approval of the dendritic cell vaccine sipuleucel-T for asymptomatic mCRPC7. More recently, several types of immunotherapies including immune checkpoint inhibitors, a DNA cancer vaccine, antibody-drug conjugates (ADC), T cell engaging bispecific antibodies (T-BsAb), and chimeric antigen receptor (CAR) T cell therapies have been under active clinical investigation8,9. CARs are synthetic receptors that leverage the potency, expansion, and memory of T cells and can be engineered against virtually any tumor-associated cell surface antigen. The adoptive transfer of CAR T cells has rapidly become an established treatment for hematologic malignancies with exceptional response rates leading to six clinical approvals in the last five years10. In contrast, CAR T cell therapies targeting solid tumors have lagged due to additional challenges related to the lack of bona fide tumor-specific antigens, inhospitable tumor microenvironments, and poor trafficking, persistence, and expansion of CAR T cells11. Despite the challenges observed in driving effective immune responses toward solid tumors, recent early-phase clinical trials investigating CAR T cell therapies targeting PSMA in mCRPC have reported safety and evidence of significant biochemical and radiographic responses12,13. These preliminary results serve to embolden efforts to develop and optimize new CAR T cell therapies for prostate cancer. While PSMA is the preeminent target for therapeutic and diagnostic development in prostate cancer, recent work indicates that PSMA expression may be quite heterogeneous in mCRPC14. Tumor antigen heterogeneity, especially in the context of single antigen-targeted CAR T cell therapies for solid tumors like prostate cancer, is an important barrier to therapeutic efficacy15. Thus, identifying cell surface antigens with broad and relatively homogeneous expression in prostate cancer is imperative. In addition, very few if any tumor-associated antigens demonstrate tumor-restricted expression—most also exhibit low-level expression in normal tissues that could represent liabilities for CAR T cell therapies due to on-target off-tumor toxicities which can lead to devastating consequences including death16. We previously performed integrated transcriptomic and cell surface proteomic profiling of human prostate adenocarcinoma cell lines and identified six transmembrane epithelial antigens of the prostate 1 (STEAP1) as one of the most highly enriched cell surface antigens17. STEAP1 was first described over two decades ago18 and was recognized as being highly expressed in prostate cancer. STEAP1 is strongly expressed in >뼈 또는 림프절 침범이 있는 mCRPC의 80%19, 유잉 육종의 62%20 및 기타 여러 유형의 암21. STEAP1은 다른 STEAP 단백질과 동종삼량체 또는 이종삼량체를 형성할 수 있는 STEAP Metallo 환원효소 계열에 속합니다. STEAP1은 암세포 증식, 침입 및 상피에서 중간엽으로의 전이를 촉진하는 데 확립된 기능적 역할을 가지고 있습니다.

cistanche tubeulosa-항종양의 장점
또한, STEAP1은 정상 조직에서 제한된 발현을 보여 암 치료를 위한 매우 강력한 표적이 됩니다. STEAP1을 표적으로 하는 다양한 면역치료제가 개발되었지만 임상적으로 승인된 약물은 없습니다. 모노메틸 아우리스타틴 E에 연결된 인간화 항-STEAP1 IgG1 항체로 구성된 ADC 반도르 투주맙 베오틴(DSTP3086S)은 mCRPC에 대한 제1상 임상 시험에서 허용 가능한 안전성 프로파일을 갖는 것으로 밝혀졌지만 객관적인 종양 반응은 거의 관찰되지 않았습니다28. 2개의 항-STEAP1 단편-항원 결합(Fab) 도메인, 항-CD3 단일 사슬 가변 단편(scFv) 및 AMG 509라는 효과기 기능이 부족하도록 조작된 단편 결정성(Fc) 도메인을 통합한 T-BsAb가 현재 평가 중입니다. mCRPC29에 대한 1상 임상 시험(NCT04221542)에서. BC261이라고 불리는 비대칭 이중 2가 T-BsAb도 최근 전립선암과 유잉 육종의 여러 전임상 모델에서 강력한 항종양 활성을 입증한 것으로 보고되었습니다30. 또한, STEAP1 펩타이드에 특이적인 인간 백혈구 항원(HLA) 클래스 I 제한 T 세포 수용체(TCR)는 형질전환 T 세포의 입양 전달 후 전임상 이종 이식 모델에서 국소 및 전이성 유잉 육종 성장을 억제하는 것으로 나타났습니다. 본 연구에서는 PSMA 치료치료의 현재 시대에 STEAP1을 표적으로 삼는 유용성을 조사하기 위해 치명적인 mCRPC에서 STEAP1과 PSMA의 상대적 발현에 대한 비교 분석을 수행합니다. 우리는 항원 특이적 T 세포 활성화 및 표적 세포 세포 용해를 위한 2세대 STEAP1 CAR을 엔지니어링하고 스크리닝하여 추가 특성화를 위한 선두 후보를 산출합니다. 우리는 STEAP1 CAR T 세포의 기능적 에피토프 특이성을 결정하고 여러 기증자의 STEAP1 CAR T 세포 제품의 확장 및 면역 표현형을 프로파일링합니다. 그런 다음 우리는 전립선암의 관련 전임상 모델에서 STEAP1 CAR T 세포 치료의 효능과 예비 안전성을 확립했지만 치료 저항의 메커니즘으로 STEAP1 항원 발현의 반복적인 손실을 관찰했습니다. 이 문제를 극복하기 위해 우리는 전립선암의 면역억제 종양 미세환경을 리모델링하고 내인성 면역을 활성화하여 항종양 반응을 확대하는 CBD-IL-12의 병용 투여를 평가합니다. 종합적으로, 이러한 연구는 mCRPC가 있는 남성에 대한 STEAP1 CAR T 세포 치료법의 임상적 전환에 대한 강력한 근거를 제공하고 치료 저항의 잠재적 메커니즘을 극복하기 위한 전략을 안내합니다.

cistanche tubeulosa-항종양의 장점
결과
STEAP1은 치료 불응성 mCRPC 조직에서 광범위하게 발현됩니다
We first set out to determine the pattern and extent of STEAP1 expression relative to PSMA in advanced metastatic prostate cancer. We performed immunohistochemical (IHC) staining on a duplicate set of tissue microarrays consisting of 121 metastatic tumors (each with up to three cores represented) collected from 44 men with lethal mCRPC patients collected by rapid autopsy between the years 2010 and 2017 through the University of Washington Tumor Acquisition Necropsy Program32 (Fig. 1a). Plasma membrane staining for STEAP1 and PSMA in each tissue was scored by a research pathologist and semiquantitative H-scores were determined based on the staining intensity (Supple mentary Fig. 1a) multiplied by the percentage of cancer cells staining at each intensity (Supplementary Fig. 1b). By implementing a minimal staining threshold with an H-score cut-off of 30, we found that 87.7% of evaluable matched mCRPC tissues (100 of 114) demonstrated staining for STEAP1 compared to only 60.5% (69 of 114) for PSMA (Fig. 1b). In addition, 28.1% of mCRPC tissues (32 of 114) showed STEAP1 but not PSMA staining (Fig. 1b, c) whereas only 0.9% (one of 114) exhibited PSMA but not STEAP1 staining. Based on these results, we used a linear mixed statistical model to determine that the odds of non-zero (H-score >{{0}}) 염색은 PSMA보다 STEAP1에서 22-배(95% CI 6-173) 더 높았으며 H-점수가 3 이상일 확률{{ 27}}은 STEAP1이 PSMA보다 84-배(95% CI 30-317) 더 높습니다. 뼈의 평균 STEAP1 H-점수(193; 95% CI 171 ~ 215)는 림프절 전이보다 유의하게 높았습니다(차이 -48; 95% CI −21 ~ -76; p < 0.001) 내장 전이보다 유의하게 높았다(차이 −59; 95% CI −42 ~ −77; p < 0.001). 내장 전이와 비교하여 림프절 전이의 평균 STEAP1 H 점수 사이에는 유의 한 차이가 없었습니다 (차이 11; 95 % CI -16 ~ 39; p=0.4) (보충 그림 1c). 우리는 또한 mCRPC 생검에서 종양 내 PSMA 이질성에 대한 최근 보고서와 일치하는 코어 내에서 PSMA의 이질적인 발현이 있는 여러 사례를 관찰했습니다(그림 1d). 30보다 크거나 같은 평균 H-점수 역치와 McNemar의 테스트를 사용한 환자 수준 분석에서 평가 가능한 환자의 95%(44명 중 42명)가 STEAP1 발현 종양을 갖고 있었고 68%(44명 중 30명)가 PSMA에 양성인 것으로 나타났습니다. (보조 그림 1d). STEAP1 및 PSMA 발현과 관련된 환자 간 및 환자 내 이질성 패턴을 연구하기 위해 STEAP1 및 PSMA H 점수를 사용하여 초기하학, Simpson 및 Shannon 다양성 점수를 평가했습니다. 우리는 모든 전이성 부위 (높은 STEAP1)에서 STEAP1 발현을 보이는 환자의 68 % (30/44)와 STEAP1 발현 유무에 관계없이 전이성 부위를 나타내는 32 % (14/44)의 환자에서 STEAP1 발현의 두 가지 패턴 (그림 1e)을 관찰했습니다. (이기종 STEAP1). 모든 전이성 조직에서 STEAP1 발현이 부족한 환자는 확인되지 않았습니다. 동일한 코호트에서 PSMA 발현에 대한 유사한 분석에서는 PSMA 발현이 높은 환자 45%(20/44), 이종 PSMA 발현이 있는 환자 32%(14/44), PSMA 발현이 없는 환자 23%(10/44)가 나타났습니다. AR을 사용한 mCRPC 조직의 분자 하위 분류와 IHC에서 평가한 신경내분비 표지자 시냅토파이신(SYP) 발현을 기반으로, STEAP1 및 PSMA 발현이 높거나 이질적인 대부분의 환자는 AR 양성 전립선암(AR+/SYP- 또는 AR+/SYP+)을 가지고 있는 반면, PSMA 발현이 없는 경우에는 AR-무효 전립선암(AR-/SYP+ 또는 AR-/SYP-)이 있었습니다. 우리는 STEAP1이 안드로겐이라는 점을 감안할 때 예상되는 조직 마이크로 어레이 (보조 그림 2a, b)에 표시된 경우 무작위 효과가있는 적합 선형 혼합 모델에 의해 STEAP1과 AR (p <0.001)의 발현 사이의 양의 상관 관계를 확인했습니다. -조절 유전자33,34. 대조적으로, STEAP1과 SYP의 발현 사이에는 부정적인 경향이 나타났습니다 (보충 그림 2c). 이러한 발견은 PSMA35와 마찬가지로 STEAP1 발현이 전립선암의 신경내분비 전환분화로 손실될 수 있음을 시사합니다.

Fig. 1 | Comparative analysis of STEAP1 and PSMA in lethal, metastatic castration-resistant prostate cancer (mCRPC). a Characteristics of the mCRPC tissues represented on University of Washington Tissue Acquisition Necropsy Tissue Microarray 92 (UW TAN TMA92). b Contingency table showing the frequency of mCRPC tissues with STEAP1 or PSMA IHC staining above or below an H-score threshold of 30. Micrographs of select mCRPC tissues after STEAP1 and PSMA IHC staining to highlight the (c) absence of PSMA but the presence of STEAP1 expression and (d) intratumoral heterogeneity of PSMA expression but not STEAP1. Scale bars = 50 µm. For panels (c, d) n = 332 mCRPC cores were immunostained for STEAP1 and PSMA. e Dot and box plot showing the distribution of STEAP1 (top) and PSMA (bottom) H-scores in 44 patients from the UW TAN TMA92 cohort. Each dot represents a tumor specimen/core (n = 319 cores for PSMA and 333 cores for STEAP1) and the color indicates the molecular subtype: AR+/SYP+ (red), AR+/SYP− (green), AR−/SYP+ (yellow) and AR−/SYP− (purple). Gray rectangles show interquartile ranges spanning the 25th to the 75th percentiles of PSMA H-scores from each patient. Bar plots (on the right) summarize the frequencies of patients classified based on STEAP1 and PSMA expression as no expression (all cores with H-score ≤30, light grey), heterogeneous expression (at least one core with H-score ≤30 and H-score >30, mid grey) and high expression (all cores with H-scores >30, 짙은 회색). 소스 데이터는 소스 데이터 파일에 제공됩니다.
데벨강력한 항원 특이적 STEAP1 CAR의 가능성
말기 mCRPC에서 STEAP1의 광범위한 발현과 암 진행에서 보고된 기능적 역할27,36,37을 고려하여 우리는 다음으로 렌티바이러스 STEAP{5}}특이적 2세대 CAR을 설계하기 시작했습니다. 우리는 조혈줄기세포 유전자 치료에 널리 사용되어 온 pCCL-c-MNDU3-X 렌티바이러스 백본38을 사용했으며 내부 MNDU3 프로모터에 의해 구동되는 T 세포에서의 CAR 발현은 EFS 프로모터40. 4-1BB 공동자극 도메인은 T 세포 기억 형성 및 지속성 연장과 관련되어 선호되었으며41 CD28 막횡단 도메인은 2세대 4-1BB에 대한 항원 역치를 감소시키는 것으로 나타났기 때문에 도입되었습니다. CAR T 세포 활성화42. 우리는 1상 임상 시험 이후 개발이 중단된 STEAP1을 표적으로 하는 ADC인 vandor tuzumab vedotin에서 파생된 완전 인간화 scFv를 통합했습니다. 이 scFv는 원래 Agensys, Inc.에서 개발한 쥐 단클론 항체(mAb 120.545)의 인간화 변종으로, 세포 기반 결합 분석에서 1nM 친화력을 보여줍니다43. CAR 활동을 잠재적으로 조정하기 위해 짧은(IgG4 힌지), 중간(IgG4 힌지-CH3) 및 긴(IgG4 힌지-CH2- CH3)을 포함한 세 가지 힌지/스페이서 길이를 구현했습니다. 긴 스페이서는 CH2 도메인에서 이전에 설명한 4/2- NQ 돌연변이44로 조작되어 Fc-감마 수용체 결합 및 긴 스페이서 CAR T 세포를 면역결핍 마우스로 입양 전달하면서 발생하는 활성화 유발 세포 사멸을 방지합니다. 세 가지 후보 CAR은 형질도입 마커로서 잘린 표피 성장 인자 수용체(EGFRt)를 공동 발현하는 렌티바이러스 벡터(그림 2a)에 클로닝되었습니다. 렌티바이러스를 생성하여 성분채집에서 수집한 인간 기증자 말초 혈액 단핵 세포(PBMC)로부터 농축된 인간 CD4 및 CD8 T 세포를 형질도입하는 데 사용했습니다. 확장된 CD4 및 CD8 CAR T 세포를 면역 표현형 분석하고(보충 그림 3a) 정상적인 CD4/CD8 비율로 정의된 구성의 세포 산물로 재구성하여 기능적 활성을 평가했습니다. 동질유전자 방식으로 STEAP1 발현을 제어하기 위해 우리는 천연 STEAP1 발현을 입증하고 CRISPR/Cas9 게놈 편집을 통해 STEAP1 녹아웃(ko)을 수행한 22Rv1 인간 전립선암 세포주에 중점을 두었습니다. 그런 다음 STEAP1 발현 렌티바이러스를 형질도입하여 22Rv1 STEAP1 ko에서 STEAP1 구조 라인을 생성했습니다(그림 2b). 그런 다음 이 라인을 사용하여 T 세포 활성화의 지표로 인터페론-감마(IFN-γ) 방출을 판독하여 공동 배양 분석에서 3개의 짧은, 중간 및 긴 스페이서 STEAP1 CAR T 세포를 스크리닝했습니다. 긴 스페이서 STEAP1 CAR T 세포(이하 STEAP1-BBζ CAR T 세포라고 함)만이 예상되는 IFN-방출의 항원 특이적 패턴을 입증한 반면, 짧은 및 중간 스페이서 STEAP1 CAR T 세포는 그렇지 않았습니다(그림 2c). , 보충 그림 3b, c). 또한, STEAP1-BBζ CAR T 세포는 형질도입되지 않은 T 세포에 비해 22Rv1 세포의 상당한 용량 의존적 세포용해를 나타냈고(그림 2d), 22Rv1 STEAP1 ko 세포의 상대적 보존을 입증했습니다(그림 2e). 그런 다음 천연 STEAP1 발현이 부족하지만 렌티바이러스 형질도입을 통해 STEAP1(DU145 STEAP1)을 발현하도록 조작된 DU145 인간 전립선암 세포주에서도 유사한 연구가 수행되었습니다(보충 그림 4a). 이 설정에서 STEAP1-BBζ CAR T 세포 활성화는 DU145 STEAP1 세포와의 공동 배양에서만 관찰되었으며 부모 DU145 세포에서는 관찰되지 않았습니다 (보충 그림 4b). 세포 용해 활성은 STEAP1-BBζ CAR T 세포에서만 평가되었으며 DU145 STEAP1 세포와의 공동 배양에서 형질도입되지 않은 T 세포에서는 평가되지 않았습니다(보충 그림 4c). 우리는 이후에 면역블롯 분석을 통해 기본 STEAP1 발현을 특성화하기 위해 더 큰 규모의 인간 전립선암 세포주 패널을 분석했습니다. AR 발현/활성이 알려진 세포주(LNCaP, 22Rv1, VCaP 및 LNCaP95)는 다양한 수준의 STEAP1 발현을 보인 반면, AR이 없는 세포주(PC3, DU145, MSKCC EF1 및 NCI-H660)는 발현하지 않는 것으로 나타났습니다. STEAP1의 검출 가능한 수준(그림 2f). 우리는 IFN-방출에 기초한 항원 특이적 활성화를 추가로 검증하기 위해 STEAP1-BBζ CAR T를 이 세포주와 함께 공동 배양하는 작업을 진행했습니다(그림 2g). 그러나 우리는 STEAP1 단백질 발현이 뚜렷하지 않은 PC3 계통(그림 2f)이 STEAP1-BBζ CAR T 세포의 실질적인 활성화를 유도한다는 점에서 일치하지 않는 결과를 관찰했습니다. 이전 문헌에서는 STEAP1이 PC3 세포주에서 낮은 수준으로 발현된다고 제안했습니다. 실제로, 장기간의 면역블롯 노출은 STEAP1의 발현이 매우 낮다는 것을 암시하는 밴드를 나타냈습니다(그림 2h). STEAP1-BBζ CAR T 세포 활성화가 PC3 세포에서 이러한 작은 STEAP1 발현으로 인한 것인지 확인하기 위해 3개의 PC3 STEAP1 ko 하위 계열을 생성하고(그림 2h) 다시 STEAP와 공동 배양을 수행했습니다. }BBζ CAR T 세포. PC3 계열의 STEAP1 ko는 STEAP1-BBζ CAR T 세포 활성화를 폐지하고(그림 2i) 특이성을 더욱 검증하고 STEAP1-BBζ CAR T 세포의 낮은 민감도에 대한 증거를 제공합니다. 항원 밀도 조건.
마우스 Steap1 및 인간 STEAP1B와 STEAP1-BBζ CAR의 교차 반응성 부족

cistanche 보충 혜택 - 면역력 증가
vandor tuzumab vedotin의 항인간 특이성과 일치하여 STEAP1-BBζ CAR T 세포는 마우스 Steap1과 교차 반응성을 나타내지 않았습니다(보충 그림 4a, d, e). 그러나 우리는 이를 마우스 Steap1(보조 그림 4f)에 3개의 인간 STEAP1 세포외 도메인(ECD)을 개별적으로 재구성하여 STEAP1-BBζ CAR T 세포의 에피토프 인식에 중요한 ECD를 결정하는 기회로 사용했습니다. 마우스 ECD를 인간 ECD로 개별적으로 대체하여 마우스 Steap1을 발현하도록 조작된 STEAP1-BBζ CAR T 세포 및 DU145 세포를 사용하여 공동 배양 실험을 수행했습니다. 우리는 ECD1이나 ECD3가 아닌 인간 STEAP1 ECD2가 STEAP1-BBζ CAR T 세포 활성화와 연관되어 있음을 발견했습니다(보충 그림 4g). 흥미롭게도 인간 STEAP1과 마우스 Steap1 ECD2는 93.9%(31/33 아미노산) 상동성을 나타냈으며(보충 그림 4h), 이는 인간 STEAP1의 Q198 및/또는 I209가 STEAP{30}}BBζ의 생산적 인식에 중요하다는 것을 나타냅니다. CAR T 세포. Q198은 극저온 전자 현미경으로 해결된 최근 구조를 기반으로 하는 상호 작용 핫스팟의 일부로 Fab 120.545와 상호 작용하는 것으로 나타났습니다. 인간 STEAP 단백질 계열 중에서 STEAP1B는 STEAP145와 가장 큰 상동성을 가지고 있습니다. 3개의 STEAP1B 전사체가 확인되었으며, 그 중 모두 인간 STEAP1 ECD2의 아미노산 서열이 완전히 보존되어 있음을 보여줍니다(보충 그림 5a). 합의 막 토폴로지 예측 알고리즘 TOPCONS46은 5개의 토폴로지 예측 모델 간의 합의가 부족하여 hSTEAP1에 비해 STEAP1B에 대한 신뢰성 점수가 낮음에도 불구하고 3개의 STEAP1B 단백질 이소형(보조 그림 5b)에서 ECD2 도메인 서열을 세포 외인 것으로 예측했습니다. TOPCONS에서 사용하는 (OCTOPUS, Philius, PolyPhobius, SCAMPI 및 SPOCTOPUS) (보충 그림 5c). 또 다른 in silico 숨겨진 Markov 모델 기반 토폴로지 예측 도구 TMHMM47을 사용한 이전 분석에서는 이 서열이 STEAP1B 단백질 이소형 1 및 245에서 세포외가 아닌 세포내일 수 있음을 시사했습니다. 그러나 STEAP1B의 결정 구조는 아직 직접적으로 입증되지 않았습니다. 이러한 예측. STEAP1- BBζ CAR T 세포가 STEAP1B에도 반응할 수 있는지 여부를 기능적으로 평가하기 위해 STEAP1B의 세 가지 isoform을 각각 발현하도록 조작된 DU145 라인을 사용하여 공동 배양을 수행했습니다. 우리는 STEAP1-BBζ CAR T 세포 활성화의 증거를 확인하지 못했습니다(보조 그림 5d). 이는 STEAP1-BBζ CAR T 세포가 인식하는 STEAP1 에피토프가 엑토도메인의 일부로 제시되지 않을 수 있음을 시사합니다. 명백한 서열 상동성에도 불구하고 STEAP1B에 의해.

그림 2|STEAP1 CAR T 세포 치료에 대한 리드를 식별하기 위해 2세대 4-1BB 키메라 항원 수용체(CAR)를 스크리닝합니다. 짧은, 중간 및 긴 스페이서를 기반으로 한 렌티바이러스 STEAP1 CAR 구성 및 변형의 도식입니다. LTR 긴 말단 반복, MNDU3 몰로니 쥐 백혈병 바이러스 U3 영역, scFv 단일 사슬 가변 단편, VL 가변 경쇄, VH 가변 중쇄, tm 막횡단, EGFRt 잘린 표피 성장 인자 수용체, 4/2 NQ {{1{{28 }}}} Fc-감마 수용체에 대한 결합을 방지하기 위한 CH2 도메인 돌연변이. b 22Rv1 모 세포, STEAP1 녹아웃(ko) 세포 및 STEAP1을 구조한 STEAP1 ko 세포의 STEAP1 면역블롯. c IFN-효소 결합 면역흡착 분석(ELISA)은 형질도입되지 않은 T 세포 또는 STEAP1-BBζ CAR T 세포와 각 22Rv1 하위 계열을 24시간에 1:1 비율로 공동 배양한 결과입니다(p < 0.001). (d) 22Rv1 및 (e) 22Rv1 STEAP1 ko 표적 세포의 시간 경과에 따른 상대적 세포 생존율은 (왼쪽) STEAP1-BBζ CAR T 세포(p < 0.001) 또는 (왼쪽)과의 공동 배양 시 형광 라이브 세포 이미징으로 측정됩니다. 오른쪽) 다양한 효과기 대 표적(E:T) 세포 비율의 형질도입되지 않은 T 세포. f 안드로겐 수용체(AR) 양성 인간 전립선암 세포주에서는 STEAP1의 발현을 입증하지만 AR 음성 전립선암 세포주에서는 발현되지 않는 면역블롯. g 비형질도입 T 세포 또는 STEAP1- BBζ CAR T 세포와 (f)의 각 인간 전립선암 세포주를 24시간에 1:1 비율로 공동 배양하여 ELISA를 통해 정량화합니다. h 22Rv1, PC3 및 PC3 STEAP1 ko 하위 계열의 STEAP1에 대한 면역블롯. I IFN-형질도입되지 않은 T 세포 또는 STEAP1- BBζ CAR T 세포와 (h)의 각 세포주를 24시간에 1:1 비율로 공동 배양하여 ELISA로 정량화(p < 0.001). 패널(c–e, g 및 i)의 경우 조건당 n=4 생물학적 복제가 사용되었으며 오류 막대는 SEM의 평균을 나타냅니다. 패널 (b, f, h)는 n=3 생물학적 복제물을 나타내는 결과를 표시합니다. GAPDH는 단백질 로딩 컨트롤로 사용되었습니다. 패널 (c) 및 (i)의 경우 Sidak의 다중 비교 테스트를 사용한 양방향 ANOVA가 사용되었습니다. 패널 (d) 및 (e)의 경우 Tukey의 다중 비교 테스트를 사용한 양방향 ANOVA가 사용되었습니다. 소스 데이터는 소스 데이터 파일에 제공됩니다.
일련의 기증자에 대한 STEAP1-BBζ CAR T 세포 제품의 특성 분석
다음으로 우리는 건강한 기증자로부터 수집한 세 가지 독립적인 말초 혈액 단핵 세포(PBMC) 세트를 사용하여 STEAP1-BBζ CAR T 세포 제품의 확장, 형질도입 효율성 및 면역 표현형을 프로파일링했습니다. 우리는 일반적으로 배양 11일 이내에 STEAP1-BBζ CAR T 세포의 20- ~ 40-배 확장을 관찰했습니다(보충 그림 6a). EGFRt+ CD8 T 세포의 비율은 24.3~54.2% 범위인 반면, STEAP1-BBζ CAR T 세포 제품에서는 EGFRt+ CD4 T 세포의 비율이 더 높고 60.1~74.9% 범위였습니다(보충 그림 6b). 우리는 형질도입되지 않은 STEAP1- BBζ CAR T 세포 하위 집합에서 T 세포 고갈 마커 PD-1 및 LAG-3의 발현을 조사한 결과 발현이 크게 증가하지 않음을 관찰했습니다(보충 그림 6c) ). 이 발견은 구성적 CAR 신호 전달이 CAR T 세포 효과기 기능에 부정적인 영향을 미칠 수 있기 때문에 고무적인 STEAP{24}}BBζ CAR에 의한 강장제 신호 전달이 낮거나 없음을 시사합니다48. 줄기세포 기억 T 세포(Tscm)와 중심 기억 T 세포(TCM) 표현형은 모두 생체 내에서 지속적인 증식과 지속성을 촉진하므로 CAR T 세포 치료의 치료 효능과 관련이 있습니다49-51. 형질도입되지 않은 STEAP1-BBζ CAR T 세포 하위 집합의 면역 표현형 분석은 세포 산물이 파생된 기증자 PBMC의 T 세포 하위 집합에 비해 Tscm 세포의 빈도가 더 높은 것으로 나타났습니다(보충 그림 6d). 이 효과는 IL{30}} 및/또는 IL-15을 T 세포 확장 배지에 추가한 것에 기인할 가능성이 높습니다. 이러한 사이토카인은 Tscm 분화를 보존하고 향상시키는 것으로 나타났습니다51,52. 우리의 분석은 또한 특히 CD8 STEAP1-BBζ CAR T 세포에서 Tcm 집단의 농축을 보여주었습니다(보충 그림 6e).
STEAP1-BBζ CAR T 세포는 면역결핍 마우스에서 확립된 천연 STEAP1 발현을 통해 파종성 전립선암 모델에서 상당한 항종양 효과를 나타냅니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
생체 내 항종양 활성에 대한 초기 화면으로 수컷 NOD scid 감마(NSG) 마우스에서 22Rv1 피하 이종 이식 종양을 확립했습니다. 종양이 약 100 mm3까지 성장했을 때, 마우스에 5 x 106 비형질도입 T 세포 또는 STEAP1-BBζ CAR T 세포를 단일 종양내 주사로 치료했습니다. STEAP1- BBζ CAR T 세포를 이용한 종양 내 치료는 치료 18일차까지 통계적으로 유의미한 종양 성장 억제와 관련이 있었습니다(그림 3a). 25일째에 마우스를 희생시켰고 STEAP1-BBζ CAR T 세포로 처리한 마우스의 잔여 종양에서 큰 면적의 괴사 잔해가 나타났으며 생존 가능한 종양 부위에 CD3+ STEAP1-BBζ가 침윤되었습니다. CAR T 세포(보조 그림 7a). STEAP1 발현은 치료 그룹 전체에서 종양에서 보존되었습니다 (보충 그림 7b). 우리는 반딧불이 루시퍼라제(Luc) 발현을 강화하기 위해 렌티바이러스로 22Rv1 세포를 형질도입했고 106 22Rv1-fLuc 세포를 수컷 NSG 마우스의 꼬리 정맥에 주입했습니다. 전이성 집락화는 2주 후에 실시간 생물발광 영상화(BLI)로 시각화되었으며, 이 시점에서 마우스는 5 x 106 비형질도입 T 세포 또는 STEAP{23}}BBζ CAR T 세포의 단일 정맥 주사로 치료되었습니다(그림 3b). . 일련의 BLI는 형질도입되지 않은 T 세포로 치료한 쥐에서 급속한 질병 진행을 나타냈고, STEAP{25}}BBζ CAR T 세포를 투여받은 쥐는 종양 진행(그림 3c, d)과 생존 기간 연장(97일 대 31일)의 상당한 지연을 보여주었습니다. , 로그 순위 테스트에 의한 p=0.0018, 그림 3e). 치료군 간 마우스 체중에는 유의 한 차이가 없었습니다 (보충 그림 7c). 연구가 끝날 때 종양의 IHC 염색은 STEAP1 발현의 상당한 감소를 보여 주었으며 (보충 그림 7d), 이는 항원 탈출이 저항 메커니즘임을 나타냅니다. 그러나 이는 형태학적 변화, AR 및 PSMA 발현의 상실 또는 SYP 발현의 증가(보충 그림 7d)를 인식하지 못했기 때문에 변이형 전립선암 상태로의 전환분화의 결과일 가능성은 없습니다. 전립선암에서 STEAP1 손실의 전체적인 영향을 조사하기 위해 우리는 이전에 준비한 동질성 22Rv1 야생형(wt), 22Rv1 STEAP1 ko 및 22Rv1 STEAP1 ko + 구조 세포주의 전사체 프로파일링을 수행했습니다(그림 2b). 22Rv1 STEAP1 ko 세포와 22Rv1 wt 세포를 비교하는 차별적 유전자 발현 분석을 통해 ~1700개의 유전자가 상당히 하향조절된 것으로 확인되었습니다(FDR 0.05 이하, 배수 변화).<2) with STEAP1 knockout. Rescue of STEAP1 expression in the 22Rv1 STEAP1 ko cells revealed that ~600 genes were significantly upregulated (FDR ≤ 0.05, fold-change>2) STEAP1 애드백(보충 그림 8a). GSEA(Gene Set Enrichment Analysis)는 STEAP1 발현 조절에 의해 조절 장애가 발생할 수 있는 여러 생물학적 경로를 지정했습니다. 이들 중 눈에 띄는 것은 세포주기 진행과 STEAP1 녹아웃에 의해 부정적으로 강화되고 STEAP1의 추가로 구조되는 Kreb주기 및 해당 분해를 포함한 다중 대사 과정이었습니다 (보충 그림 8b). 우리는 검증된 31-유전자 세포 주기 진행(CCP) 시그니처54를 데이터에 적용했는데, 이는 STEAP1 녹아웃과 관련된 CCP 시그니처의 상당한 하향 조절을 보여 주며 점수는 -0.8로 상당히 증가하여 {{ 14}}.5 STEAP1 발현을 구출함(보조 그림 8c). 이러한 데이터는 LNCaP 전립선암 세포주에서 STEAP1의 녹다운이 세포사멸을 유도하면서 세포 생존력과 증식을 손상시킨다는 것을 나타내는 이전 간행물과 일치합니다. 우리는 또한 항원 처리 및 제시가 STEAP1 녹아웃을 통해 가장 현저하게 농축되지 않은 KEGG 경로 중 하나라는 점에 주목했습니다(보충 그림 8b). 우리는 면역프로테아좀 복합체의 구성원인 PSME1(프로테아좀 활성자 하위 단위 1), 주요 조직 적합성 복합체(MHC) 클래스 I 펩타이드에 중요한 TAP1(수송체 1, ATP 결합 카세트 서브패밀리 구성원)을 포함한 유전자의 상당한 하향 조절을 관찰했습니다. 로딩 복합체 및 MR1 (주요 조직 적합성 복합체, 클래스 I 관련), HLA-DQ-B1 및 HLA-DQB2 (보충 그림 8d)와 같은 여러 MHC 클래스 I 및 II 유전자. 우리는 전사체 분석을 통해 항원 손실을 입증한 STEAP1- BBζ CAR T 세포 치료법으로 치료된 22Rv1 파종 모델에서 수집된 종양을 추가로 조사했습니다(그림 3c, 보충 그림 7d). STEAP{43}}BBζ CAR T 세포 치료로 치료한 쥐의 22Rv1 전이성 종양과 비형질도입 T 세포로 치료한 쥐의 22Rv1 전이성 종양을 비교하는 차별적 유전자 발현 분석 및 후속 GSEA는 MHC, 세포독성 림프구 및 T 세포 활성화와 관련된 경로의 음성 농축을 보여주었습니다. 보충 그림 9a, b). 우리는 또한 MHC 클래스 I 및 II 유전자의 발현을 구체적으로 평가하고 STEAP{47}}BBζ CAR T 세포 치료로 치료한 22Rv1 종양에서 이들의 현저한 하향 조절을 관찰했습니다(보충 그림 9c). 이 결과는 이들 종양에서 IHC에 의한 HLA-A, B, C 염색의 유의한 감소에 의해 더욱 입증되었습니다(보충 그림 9d). 이러한 데이터의 잠재적인 의미는 STEAP1-BBζ CAR T 세포 치료법을 사용한 치료와 그에 따른 전립선암의 STEAP1 종양 항원 발현 상실로 인해 항원 처리 및 제시 장애를 통해 추가적인 면역요법 내성이 발생할 수 있다는 것입니다. 우리는 또한 꼬리 정맥 주사를 통해 수컷 NSG 마우스에 C4-2B-fLuc 세포를 접종했습니다. C4-2B는 LNCaP55의 거세 저항성 하위계통으로 성장 동역학이 일반적인 전립선암과 더 유사합니다. 주입 4주 후, BLI를 통해 전이성 집락화가 확인되었고, 마우스에 5 x 106 비형질도입 T 세포 또는 STEAP1-BBζ CAR T 세포를 단일 정맥 주사하여 치료했습니다(그림 3b). 연속 BLI는 치료 5주 이내에 STEAP1-BBζ CAR T 세포를 받은 모든 마우스에서 완전한 반응을 보여주었습니다(그림 3f, g). 우리는 형질 도입되지 않은 T 세포 치료 그룹에서 체중 감소가 증가하는 경향을 확인했지만 (보조 그림 10a) 이는 통계적으로 유의하지 않았습니다. STEAP1-BBζ CAR T 세포로 처리된 생쥐의 부검에서는 육안적 질병이 나타나지 않았으며 장기의 생체 외 BLI에서는 어떠한 신호도 나타나지 않았으며(보충 그림 10b), 이는 이들 생쥐가 치료되었을 가능성이 있음을 시사합니다. 우리는 검출 가능한 CD3+ EGFRt+ 비장 세포의 존재를 기반으로 실험 종료 시 STEAP1-BBζ CAR T 세포의 말초 지속성을 확인했습니다(그림 3h).

그림 3|천연 STEAP1 발현이 있는 전립선암 모델에서 STEAP1-BBζ CAR T 세포 치료의 생체 내 항종양 활성. a 5의 단일 종양 내 주사 후 시간 경과에 따른 NSG 마우스의 22Rv1 피하 종양의 부피(형질도입되지 않은 T 세포 그룹의 경우 n{5}}, STEAP1-BBζ CAR T 세포 그룹의 경우 n{6}}) × 106개의 비형질도입 T 세포 또는 STEAP{{1{27}}}}정상 CD4/CD8 비율의 BBζ CAR T 세포. 20일과 25일에 p < 0.0001. 막대는 SEM의 평균을 나타냅니다. b 22Rv1(상단) 및 C4-2B(하단) 파종 모델에 대한 종양 유발 실험의 도식. Luc 반딧불이 루시퍼라제, BLI 생물발광 이미징. c 22Rv1-fLuc 전이가 이식되고 정상 CD4/에서 5 × 106 비형질도입 T 세포 또는 STEAP{24}}BBζ CAR T 세포의 단일 정맥 주사로 치료된 NSG 마우스의 연속 생체 발광 영상(BLI) 0일째의 CD8 비율. 빨간색 X는 죽은 마우스를 나타냅니다. 래디언스 스케일이 표시됩니다. d (c)에서 각 마우스의 실시간 BLI로부터 시간에 따른 총 플럭스의 정량화를 보여주는 플롯. e 로그 순위 (Mantel-Cox) 테스트에 의해 결정된 통계적 유의성을 갖는 ( c ) 마우스의 Kaplan-Meier 생존 곡선. 패널 (c-e)의 경우 조건당 n=5 마리의 마우스가 사용되었습니다. f C4-2B 전이가 이식되고 정상적인 CD4/CD8 비율로 5 × 106 비형질도입 T 세포 또는 STEAP{34}}BBζ CAR T 세포를 단일 정맥 주사로 치료한 NSG 마우스의 연속 라이브 BLI 0. 빨간색 X는 죽은 마우스를 나타냅니다. 래디언스 스케일이 표시됩니다. g (f)에서 각 마우스의 실시간 BLI로부터 시간에 따른 총 플럭스의 정량화를 보여주는 플롯. 패널(f, g)의 경우 n= 4 마우스를 비형질도입 T 세포 그룹에 사용하고 n=5 마우스를 STEAP1-BBζ CAR T 세포 그룹에 사용했습니다. h 마지막에 STEAP1-BBζ CAR T 세포(n= 4)로 처리한 마우스의 비장 세포에서 유세포 분석을 통해 CD3+ EGFRt+ STEAP1-BBζ CAR T 세포의 정량화 49일째 실험. 막대는 평균을 나타냅니다. 패널 (a)의 경우 Sidak의 다중 비교 테스트를 사용한 양방향 ANOVA가 사용되었습니다. 소스 데이터는 소스 데이터 파일에 제공됩니다.
마우스 내 STEAP1 CAR T 세포 연구에서 항종양 치료 효능 입증
PC3 세포주의 매우 낮은 STEAP1 항원 밀도(~1500 분자/세포) 환경에서 관찰된 STEAP1-BBζ CAR T 세포의 활성화 및 세포용해 활성(그림 2g-i, 보충 그림 11a, b) ) 및 파종된 PC3-fLuc 종양 모델(보조 그림 11c-e)에서의 생체 내 항종양 활성 증거는 표적 외 종양 독성 가능성에 대한 우려를 제시했습니다. 다루기 쉬운 모델 유기체의 잠재적 독성을 평가하기 위해 우리는 인간 STEAP1 유전자가 C57Bl/6 배경의 마우스 Steap1 유전자 유전자좌에 두드려지는 인간 STEAP1 녹인(hSTEAP{12}}KI) 마우스를 생성했습니다( 그림 4a). 꼬리 DNA의 중합효소연쇄반응(PCR)을 통해 유전자형 분석을 수행하여 마우스 콜로니를 확립했습니다(그림 4b). 동형접합성 및 이형접합성 hSTEAP1-KI 마우스 모두 야생형 동배에 비해 뚜렷한 표현형 또는 생식 이상을 나타내지 않았습니다. 정량적 역전사 PCR(qRT-PCR)을 기반으로 한 인간 STEAP1 발현에 대한 조직 조사를 수컷 및 암컷 이형접합성 hSTEAP1-KI(hSTEAP{23}}KI/ + ) 마우스에서 수행하여 가장 큰 상대적 발현을 밝혀냈습니다. 전립선에 이어 자궁과 부신이 뒤따릅니다(그림 4c). 남성 hSTEAP1-KI/+ 전립선 및 부신에 대한 STEAP1 IHC에 의한 추가 현장 분석에서는 인간 STEAP1 발현이 전립선의 내강 상피 세포에 국한되어 있고(그림 4d) 부신 피질에서 발현되는 것으로 나타났습니다(그림 4e). . STEAP1-mBBζ CAR이라고 불리는 STEAP1 CAR의 쥐화 버전. 여기서 scFv 및 IgG4 힌지-CH2-CH3 스페이서는 유지되었지만 CD28 막횡단 도메인, 4-1BB 보조자극 도메인 , CD3ζ 활성화 도메인은 마우스 오솔로그로 대체되어 감마레트로바이러스 구조물에 클로닝되었습니다(그림 4f). 또한, 잠재적인 면역원성을 최소화하기 위해 인간 EGFRt 형질도입 마커를 잘린 마우스 CD19(mCD19t)로 대체했습니다. 우리는 마우스 비장세포로부터 농축된 T 세포의 효율적인 레트로바이러스 형질도입을 확인했고(그림 4g), 마우스 STEAP1-mBBζ CAR T 세포가 인간 STEAP1을 발현하도록 조작된 RM9 마우스 전립선암 세포주56의 세포용해를 유도하는 능력을 입증했습니다. (RM9- hSTEAP1) 렌티바이러스 형질도입에 의한 것입니다(그림 4h). 마우스 STEAP1-mBBζ CAR T 세포의 생체내 효능은 NSG 마우스의 파종성 RM9-STEAP1-fLuc 종양 모델에서 검증되었습니다(보충 그림 12a). RM9-STEAP1-fLuc 세포의 꼬리 정맥 주사 1주일 후, 마우스에 꼬리 정맥 주사를 통해 5 x 106 비형질도입 마우스 T 세포 또는 마우스 STEAP1-mBBζ CAR T 세포를 처리했습니다. . 형질도입되지 않은 마우스 T 세포를 투여받은 마우스는 확인되지 않은 질병 진행을 보인 반면, STEAP1-mBBζ CAR T 세포로 치료한 마우스는 균일하게 빠른 질병 퇴행을 보였으며 이후 10일 후에 재발이 발생했습니다(보충 그림 12b, c). STEAP1-mBBζ CAR T 세포 치료법은 통계적으로 유의미한 생존 이점과 관련이 있었습니다(22일 대 12일, 로그 순위 검정에 의한 p= 0.0039, 보충 그림 12d). 사망 전 종양 부담이 증가함에 따라 두 치료군 모두에서 체중 감소가 분명했습니다 (보충 그림 12e, f). 부검에서 수집된 마우스 비장세포 분석에서는 입양 전달 후 최대 24일까지 mCD3+ mCD19t+ 세포가 검출되면서 STEAP1-mBBζ CAR T 세포의 말초 지속성이 나타났습니다(보충 그림 12g). 폐는 두 치료 그룹 모두에서 마우스로부터 수확되었으며 STEAP1 IHC는 STEAP1-mBBζ CAR T 세포로 치료된 마우스의 폐 전이에서 STEAP1 발현의 손실을 보여주었습니다(보충 그림 12h). 우리는 관찰된 종양 항원 탈출이 STEAP1 발현의 기존 이질성 결과일 수 있는지 여부를 확인하기 위해 클론성 RM9-STEAP1-fLuc 계통을 확장했습니다. NSG 마우스에서 클론성 파종성 RM9-STEAP1- fLuc 종양 모델을 사용하여 실험을 반복했습니다(보충 그림 13a). 이러한 맥락에서 STEAP1-mBBζ CAR T 세포로 치료된 마우스는 신속하고 지속적인 완전 반응을 보여주었습니다(보충 그림 13b-d). 이러한 발견은 STEAP1+ 전립선암 근절에 있어 STEAP1-mBBζ CAR T 세포의 효능을 강조하고, 나아가 STEAP1의 이질성이 있는 진행성 전립선암 환자의 하위 그룹에서 저항성을 극복하기 위해 보조 치료 전략이 필요할 수 있음을 시사합니다. 표현이 존재합니다 (그림 1e).

남성의 면역체계 강화를 위한 시스탄체의 효능
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
STEAP1 CAR T 세포 치료법은 인간화 STEAP1 마우스 모델에서 안전합니다.
STEAP1-mBBζ CAR T 세포 치료법의 전임상 안전성과 효능을 모두 조사하기 위해 수컷 이형접합 hSTEAP1-KI 마우스에 동계 비클론성 RM9-STEAP{{4}을 접종했습니다. }꼬리 정맥 주입에 의한 fLuc 세포(그림 5a). 약 일주일 후 BLI를 통해 전이성 집락화를 확인한 후, 생쥐는 복강내 주사를 통해 전처리된 시클로포스파미드 100mg/kg을 투여받았습니다57. 하루 후, 마우스를 꼬리 정맥 주사를 통해 5 x 106 비형질도입 마우스 T 세포 또는 마우스 STEAP1-mBBζ CAR T 세포로 처리하도록 무작위화했습니다. 마우스 STEAP1-mBBζ CAR T 세포를 투여받은 모든 마우스는 BLI를 기반으로 한 치료 시작 첫 주 이내에 종양 부담이 감소한 것으로 나타났습니다(그림 5b, c). 관찰된 반응은 수명이 짧았지만 약간의 생존 연장을 가져왔습니다(21일 대 12일, 로그 순위 테스트에 의한 p= 0.0138, 그림 5d). 이는 비클론 RM의 결과와 유사합니다. NSG 마우스의 9-STEAP1-fLuc 실험(보충 그림 12d). 항종양 효능에 대한 명확한 증거가 관찰된 이 용량 수준에서 마우스 STEAP1-mBBζ CAR T 세포 치료와 특별히 관련된 총 독성이나 조기 사망은 없었습니다. 체중 감소는 종양 부담 증가와 관련이 있었지만 두 치료군 모두에 공통적이었습니다 (그림 5e, f). STEAP1-mBBζ CAR T 세포 요법의 잠재적 독성을 추가로 평가하기 위해, 종양은 없고 RM{29}}hSTEAP1 종양을 보유하는 이형접합 hSTEAP1-KI 마우스에서 유사한 실험을 병행하여 수행했습니다. 형질도입되지 않은 T 세포 또는 STEAP1- mBBζ CAR T 세포로 처리된 비종양 보유 마우스는 생존율(보충 그림 14a) 또는 체중 감소를 포함한 총 독성(보충 그림 14b)에 차이를 나타내지 않았습니다. STEAP{36}}BBζ CAR은 잠재적으로 면역원성이 있을 수 있는 변형된 IgG4 스페이서로 구성되어 있기 때문에 이 실험에서 마우스의 안와후 출혈을 수집하여 마우스 항인간 항체(MAHA) 반응을 평가했습니다. STEAP1-BBζ CAR T 세포로 처리한 후 8일째에 마우스의 혈청에서 항인간 IgG 및 IgM 항체가 검출되지 않았습니다(보충 그림 14c).
중요한 것은, STEAP1-mBBζ CAR T 세포로 처리된 이형접합성 hSTEAP1-KI 마우스는 전립선에서 뚜렷한 조직 파괴나 CD{2}} T 세포의 침윤 증가를 나타내지 않았습니다(보조 그림 15a, b). ) 또는 부신 (보충 그림 15c, d)은 형질 도입되지 않은 T 세포로 처리 된 대응 물에 비해 표적 외 종양 독성이 없음을 나타냅니다. 실험이 끝날 때 수집된 폐는 형질도입되지 않은 마우스 T 세포로 처리된 마우스에서 지역적 이질성을 갖는 RM9-hSTEAP1 폐 전이에서 인간 STEAP1 발현을 보여주었습니다(그림 5g). 반면, 마우스 STEAP1-mBBζ CAR T 세포로 처리한 마우스의 종양에서는 다시 인간 STEAP1 발현이 없는 것으로 나타났습니다(그림 5h). 마우스 STEAP1- mBBζ CAR T 세포 치료와 인간 STEAP1 항원 손실이 RM9-hSTEAP1 종양의 항원 제시에 영향을 줄 수 있는지 평가하기 위해 쥐 베타-2-마이크로글로불린(B2m)에 대해 IHC를 수행했습니다. ) 이는 MHC 클래스 I 분자의 핵심 구성 요소입니다. 우리는 22Rv1 모델에서의 발견과 일치하는 비형질도입 T 세포(보충 그림 15e, f)와 비교하여 마우스 STEAP1-mBBζ CAR T 세포로 치료한 후 진행성 종양에서 B2m 발현의 유의미한 하향조절을 관찰했습니다.

그림 4|인간 STEAP1 녹인(hSTEAP1-KI) 마우스 모델과 쥐화된 STEAP1 CAR을 사용하여 마우스 내 시스템 구축. 인간 STEAP1 엑손 2-5를 C57Bl/6 배경의 마우스 Steap1 유전자좌에 녹인하는 표적 벡터를 사용하는 상동 재조합 전략을 보여주는 도식. FRT Flippase 인식 대상. b 야생형 또는 hSTEAP1-KI 대립유전자의 일부를 증폭시키기 위한 프라이머 쌍을 사용하여 야생형(+/+), 이형접합성(KI/+) 또는 동형접합성(KI/KI) 마우스의 꼬리 끝 유전형 분석에서 얻은 PCR 산물 시각화 . NTC 널 템플릿 제어. n개의=3 생물학적으로 독립적인 실험의 대표적인 젤 이미지입니다. c hSTEAP1-KI/+ 마우스의 조직 조사에서 18 S 발현으로 정규화된 인간 STEAP1 발현에 대한 qPCR. 성별에 따른 장기의 경우 n=3이고 일반 장기의 경우 n=6입니다. 막대는 SEM의 평균을 나타냅니다. (d) (왼쪽) +/+ 및 (오른쪽) KI/+ 마우스의 전립선 조직과 (e) KI/+ 마우스의 부신의 STEAP1 IHC 염색 사진 현미경 사진. 스케일 바=50 µm. 패널 (d, e)의 경우 STEAP1 면역염색은 n= 3 생물학적으로 독립적인 표본에서 수행되었습니다. f 레트로바이러스 쥐화 STEAP1 CAR 구조의 도식. MuLV 쥐 백혈병 바이러스, mCD19t 마우스 잘린 CD19. g 유세포 분석법을 통해 마우스 CD3+ CD19t+ 세포의 빈도를 기반으로 한 세 가지 독립적인 실험에서 활성화된 마우스 T 세포의 레트로바이러스 형질도입 효율을 정량화했습니다(p{{40}}.0003). h 마우스 STEAP1-mBBζ CAR T 세포 또는 형질도입되지 않은 T 세포와 1:1 비율로 공동 배양 시 형광 라이브 세포 이미징으로 측정한 시간 경과에 따른 RM9 또는 RM9-hSTEAP1 표적 세포의 상대적 세포 생존율 (p < 0.0001). n 조건당=4 생물학적 복제. 오차 막대는 SEM의 평균을 나타냅니다. 패널(g)의 경우 Welch 보정을 사용한 짝이 없는 양측 스튜던트 t-검정을 사용했습니다. 패널(h)에서는 Sidak의 다중 비교 테스트를 사용한 양방향 ANOVA가 사용되었습니다. 소스 데이터는 소스 데이터 파일에 제공됩니다.
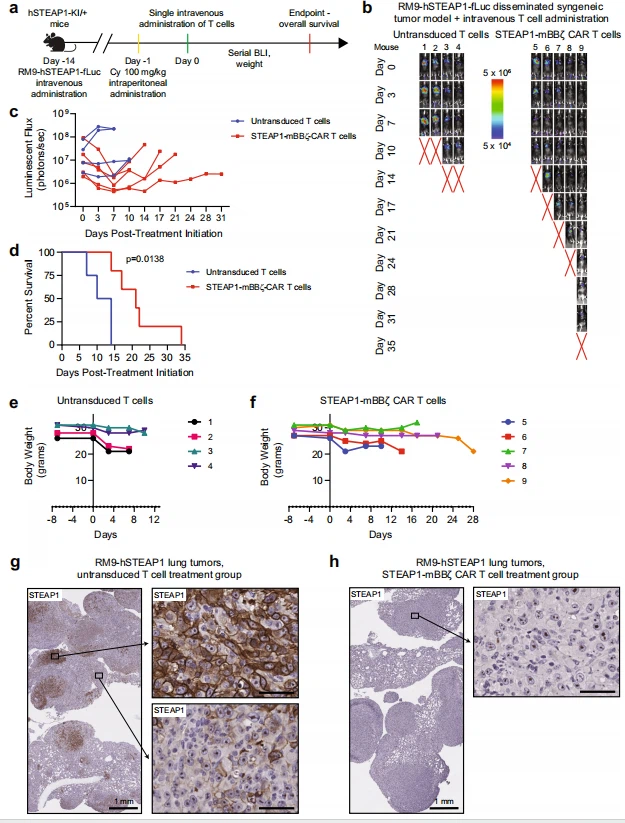
그림 5|동계 파종성 전립선암이 있는 hSTEAP1-KI 마우스에서 마우스 STEAP1-mBBζ CAR T 세포의 효능 및 안전성 확인.
콜라겐 결합 도메인-IL-12 융합 사이토카인은 향상된 T 세포 수용체 신호 전달 및 항원 제시를 통해 항종양 반응을 유도합니다.
IL{0}}는 T 세포 반응을 조절하고 IFN- 생성을 유도하는 p40 및 p35 하위 단위로 구성된 이종이합체 사이토카인입니다. 전신 IL{4}} 투여와 관련된 놀라운 항종양 반응은 여러 전임상 모델에서 입증되었지만58,59 이러한 치료 접근법의 임상 적용은 용량 제한 독성 및 비효율성60-63으로 인해 중단되었습니다. 이러한 문제를 회피하기 위한 대체 전략은 종양 내 전달 또는 IL{11}} 융합 단백질을 조작하여 종양 미세 환경의 고유한 특성을 활용하여 IL{{1{81}}}}을 종양에 국한시키는 것을 목표로 했습니다. 최근에 기술된 접근법 중 하나는 콜라겐 결합 도메인(CBD, 그림 6a) 역할을 하고 무질서한 종양 혈관계에서 노출된 콜라겐에 융합 단백질의 결합을 가능하게 하는 von Willebrand 인자 A3 도메인에 대한 융합입니다. 전신 CBD-IL-12 치료법은 향상된 IFN- 신호 전달을 통해 면역학적으로 "감기" 쥐과 유방암 및 흑색종 모델의 종양 미세환경을 재구성하고 항PD와 협력하는 것으로 나타났습니다{{20}} 종양 근절을 유도하는 면역 체크포인트 억제. 우리는 CBD-IL-12이 전립선암을 "차가운" 암에서 "뜨거운" 암으로 전환하고 항종양 반응을 유도하는 데 효과적인지 질문했습니다. 피하 동계 RM9 및 Myc-CaP 종양은 각각 수컷 C57Bl/6 및 FVB 마우스에서 확립되었으며, 마우스는 비히클, 항PD-1 또는 CBD-IL-12로 치료하도록 무작위 배정되었습니다. . 전신 CBD-IL-12 투여는 동계 RM9 및 Myc-CaP 종양 모델 모두에서 유의미한 종양 성장 억제를 유도했는데, 그렇지 않은 경우 항-PD-1 치료에 제대로 반응하지 않았습니다(그림 6b, 보충 그림 16a). . CBD-IL-12의 작용 메커니즘에 대한 추가 통찰력을 얻기 위해 우리는 비히클 또는 CBDIL-12로 처리한 마우스의 RM9 종양에 대한 단일 세포 RNA-seq(scRNA-seq) 분석을 수행했습니다. 균일한 다양체 근사화 및 투영 플롯은 항종양 활성과 일치하는 종양 상피, 섬유모세포 및 내피 세포 구획의 실질적인 감소를 나타냈습니다(보조 그림 16b). scRNA-seq 데이터에서 선천성 및 적응성 면역 세포 하위 집합(그림 6c,d)에 대한 마커 기반 프로파일링을 통해 CD{51}} T 세포의 상당한 증가가 확인되었습니다(7.55 대 0.76%). , XCR1+ IRF8+ 기존 1형 수지상 세포(cDC1, 1.33 대 0%), CD86+ INOS2+ M1 극성 대식세포( 비히클 대조군과 비교하여 CBDIL-12 처리군의 종양에서 CD64+ F4/80+ 단핵구/대식세포(29.2 대 4.43%) 및 2.26 대 0%). 면역억제성 CD163+ CD206+ M2 극성 대식세포(0 대 0.25%) 및 Ly6G+ 호중구(0.52 대 1.08%)의 감소도 CBD-IL-12 치료와 관련이 있었습니다. IHC 분석에 따르면 비히클로 치료한 RM9 종양에는 일반적으로 CD8+ T 세포가 부족한 반면 CBD-IL-12로 치료한 종양에는 CD8+ T 세포가 눈에 띄게 유의하게 침윤된 것으로 나타났습니다(보충 그림 16c). . 종양 세포에서는 프로테아좀 및 면역프로테아좀 하위 단위인 Psmb8 및 Psmb9와 주요 조직 적합성 복합체 클래스 I(MHC I) 유전자 H2-K1, H2-D1 및 B2m의 풍부한 발현이 나타났으며 이는 항원 처리의 상향 조절과 일치합니다. 및 프리젠 테이션 기계 (그림 6e, 보충 그림 16d). 동시에, T 세포는 T 세포 수용체 신호 전달 및 림프구 세포와 비림프 세포 사이의 면역 조절 상호 작용과 관련된 향상된 유전자 발현을 나타냈습니다(그림 6f, 보충 그림 16e). 단핵 식세포 시스템(MPS)의 세포는 항원 처리 및 교차 제시뿐만 아니라 사이토카인 신호 전달과 관련된 풍부한 유전자 발현을 보여주었습니다(보충 그림 16f, g). 이러한 연구는 종양 미세환경의 재프로그래밍과 선천적 및 적응성 면역체계의 참여를 통해 전립선암 모델에서 CBD-IL- 12의 항종양 활성을 확립했습니다.
STEAP1-mBBζ CAR T 세포 및 CBD-IL-12 요법을 병용하여 종양 제어 강화
다음으로 우리는 CBD-IL-12 치료법으로 항종양 면역 반응을 확대하면 종양 항원 이질성과 항원 처리 구조를 억제함으로써 전립선암에서 STEAP{2}}mBBζ CAR T 세포 치료법의 치료 효능을 향상시킬 수 있다는 가설을 세웠습니다. 프레젠테이션. 따라서 우리는 수컷 이형접합성 hSTEAP1-KI 마우스에서 동계 비클론성 RM9-STEAP1-fLuc 전이를 확립하고 5 × 106 안와후동 주사에 의한 매주 CBD-IL-12 치료 유무에 관계없이 꼬리 정맥 주사에 의한 비형질도입 마우스 T 세포 또는 마우스 STEAP1-mBBζ CAR T 세포. CBD-IL-12 요법을 단독으로 또는 STEAP1-mBBζ CAR T 요법과 병용하여 투여받은 그룹은 림프 고갈 시클로포스파미드를 투여받지 않았습니다(그림 7a). 일련의 BLI는 형질도입되지 않은 T 세포와 CBD-IL-12로 치료한 쥐에서 급속한 질병 진행을 보여주었고, CBD-IL-12 치료와 함께 STEAP1-BBζ CAR T 세포를 투여받은 쥐에서는 유의미한 질병 진행을 보여주었습니다. 종양 진행 지연 (그림 7b, c). 중요한 것은 마우스 STEAP1- mBBζ CAR T 세포와 매주 CBD-IL-12을 병용한 치료가 다른 모든 치료 그룹과 비교할 때 전체 생존율의 통계적으로 유의미한 연장과 관련이 있다는 것입니다(그림 7d). 치료 0일차와 8일차에 수집된 안와후 출혈에 대한 혈장 사이토카인 분석에서는 전염증성 사이토카인 IFN-, TNF-, IL{30}} 및 IL{31}} 수준이 유의하게 증가한 것으로 나타났습니다(그림 7e, 보충 그림 . 17) STEAP1-mBBζ CAR T 세포 및 CBD-IL-12으로 처리된 마우스에서. 부검 시 잔여 종양을 수집했으며 STEAP1 IHC는 STEAP1- mBBζ CAR T 세포 단독 및 CBD-IL-12과 함께 처리한 마우스의 종양에서 항원 손실을 보여주었습니다(그림 8a). 또한 CBD-IL{45}} 치료와 관련된 종양 B2m 발현의 증가(그림 8a)가 관찰되었습니다. CD3+ T 세포도 IL-12 치료를 받은 종양 상태에서 증가했지만(그림 8b) 경향이 평가되었지만 우리는 IL-12 치료를 받은 종양 상태에서 종양 내 T 세포의 통계적으로 유의미한 증가를 발견하지 못했습니다. STEAP1-mBBζ CAR T 세포 및 STEAP1-mBBζ CAR T 세포와 CBD-IL-12 결합 치료군. 10일째 최대 치료 반응(최저) 및 종양 진행(재발)에 대한 동정적인 종료점에서 수집된 STEAP1-mBBζ CAR T 세포와 CBD-IL-12을 병용하여 치료한 마우스의 종양을 포함한 잔류 종양은 단일 세포로 해리되고 면역 세포 하위 집합은 다중 매개 변수 유동 세포 계측법으로 특성화되었습니다 (보충 그림 18). scRNA-seq 결과에 따르면, CBD-IL-12 처리는 단독으로 또는 STEAP1-mBBζ CAR T 세포와 결합하여 CD11b+ Ly6C-/+F4/{{68 }} MHC-II+ 대식세포(그림 8c, d, 보충 그림 19a). CD11b+ Ly6CF4/80+ MHC-II+ 세포는 성숙한 항원 제시 대식세포를 나타내며66 이 집단은 우선적으로 풍부했고 CBD-IL에 의한 전염증성 M1 극성화의 지표로서 유도된 산화질소 신타제(iNOS) 발현의 증가를 입증했습니다.{{84} } 치료. 우리는 또한 cDC1 집단의 확장과 기존의 2형 수지상 세포(cDC2) 집단의 감소를 관찰했습니다(그림 8e, 보충 그림 19b). cDC1은 항종양 세포독성 CD{91}} T 세포의 활성화 및 치료 저항성의 잠재적 메커니즘과 관련이 있습니다. cDC2는 Tregs를 포함한 CD4+ T 세포의 KLRG1+ 및 KLRG1- 자연 살해 비율의 중요한 차이를 활성화하는 데 중요하지만 종양으로의 세포 이동 징후는 발견되지 않았습니다67 . cDC2 결과와 일치하여 치료 그룹 전체의 세포 (보충 그림 19d). CD4+ FOXP3+ Tregs의 주파수 프로파일링에서는 F40/80+ SiglecF+ 호산구의 Tregs 계열이 감소한 반면 Ly6G+는 CBD-IL-12 치료로 중화되었습니다(보충) 그림 19c). 흥미롭게도 STEAP1-에 CBD-IL-12을 추가하면 영양제가 감소했으며, STEAP1-mBBζ mBBζ CAR T 세포 치료를 결합한 후 재발된 종양에서 관찰되었습니다(그림 8f, g). 특히, 이러한 CAR T 세포 및 CBD-IL{116}} 요법의 빈도는 Treg의 증가로 치료를 통해 cDC1이 감소하고 종양 관련 호중구가 높아졌는데, 이는 세포독성 CD8 STEAP의 프라이밍 감소를 의미합니다. }}형질도입되지 않은 T 세포와 비교한 mBBζ CAR T 세포(T 세포 54 대 T 세포 및 면역억제성 Treg 신호 강화 34%)는 CBD-IL-12 치료 조건에서 감소했지만 STEAP 병용 후 종양 재발 시 증가했습니다. 1-mBBζ CAR T 세포 및 CBD-IL-12 치료법(19~42%). 이러한 발견은 종양 관련 호중구의 면역억제 특성이 치료 저항성과 종양 진행을 중재하는 데 중요한 역할을 할 수 있음을 시사합니다. 전반적으로, 이러한 분석은 CBD-IL-12 치료가 적대적인 면역억제 종양 환경을 전염증 상태로 되돌리고 입양 전달된 STEAP1-mBBζ CAR T 세포 치료와 함께 항종양 활동을 확장한다는 것을 나타냅니다. 우리는 부검 시 각 치료 그룹에서 수집한 폐 보유 종양에 대해 다중 PCR 기반 TCR 베타 사슬 서열 분석68을 사용하여 TCR 레퍼토리 분석을 추가로 수행했습니다. 우리는 CBD-IL-12 단독 및 STEAP1-mBBζ CAR T 세포 치료와 함께 치료한 생쥐의 샘플에서 Simpson 클론성이 유의하게 감소하는 것을 관찰했는데, 이는 종양 내 T 세포 다양성의 증가를 나타냅니다(그림 1). 8시간). 이러한 연구 결과는 STEAP1 CAR T 세포 치료의 보조물로 CBD-IL{143}}을 추가하는 것이 전립선암 종양 미세환경의 리모델링, 항원 처리 및 제시 강화, 숙주 면역 참여를 통해 에피토프 확산을 촉진함으로써 유익할 수 있음을 입증합니다.
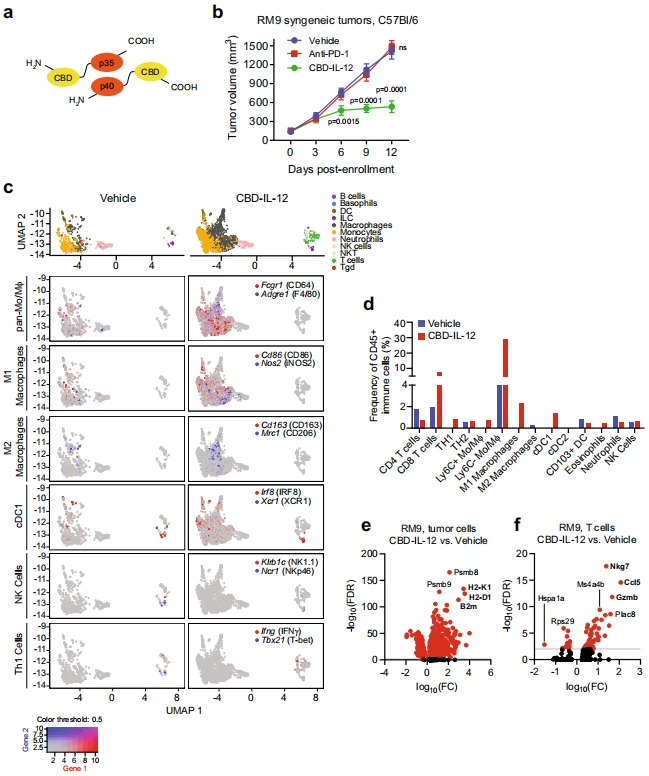
그림 6|전신 콜라겐 결합 도메인 IL-12(CBD-IL-12) 사이토카인 융합 요법은 전립선암 종양 성장을 억제하고 종양 면역 미세환경을 재프로그램합니다. von Willebrand 인자 도메인 A3의 CBD에 융합된 p35 및 p4{23}} 하위 단위로 구성된 CBD-IL-12의 도식. b 매 5일마다 복강내 주사에 의한 비히클, 항-PD-1(클론 29 F.1A12) 200μg으로 치료한 시간 경과에 따른 동계 C57Bl/6 마우스의 RM9 피하 종양의 부피, 또는 CBD-IL-12 25 Μg 0일부터 5일마다 정맥 주사. 비히클 및 CBD-IL-12 처리 그룹에서는 n=7 마우스, 항 항에서는 n=8 마우스 -PD1 처리군. 9일과 12일에 p < 0.0001. 막대는 SEM의 평균을 나타냅니다. P-값은 Dunnett의 다중 비교 테스트를 통해 양방향 ANOVA에서 파생되었으며 ns는 중요하지 않습니다. c 비히클 또는 CBD-IL로 처리된 마우스에서 각각 응집된 5개의 RM9 종양에 대한 단일 세포 RNA-seq(scRNA-seq) 분석에서 얻은 다양한 면역 세포 하위 집합(상단)의 균일 다양체 근사 및 투영(UMAP) 플롯{{41} }. 범단핵구/대식세포, M1 및 M2 극성 대식세포, 기존 1형 수지상 세포(cDC1), 자연 살해(NK) 세포 및 T 도우미 1형(Th1)에 대한 면역 세포 하위 집합 특이적 마커의 유전자 발현으로 색칠된 UMAP 플롯 세포. d CD4+ 및 CD8+ T 세포, Th1(Infg+ Tbx{ {56}} ) 및 Th2(cMAF+ Gata3+ ) 세포, Ly6C+/− 단핵구/대식세포(Ly6C+/− Adgre1+ ), M1 대식세포(CD80+ CD{{67} } INOS2+ ), M2 대식세포(CD163+ Mrc1+ cMAF+ ), cDC1(XCR1+ IRF8+ ), 기존 2형 수지상 세포(cDC2 , CD1+ IRF4+ ), 이동성 CD103+ 수지상 세포(Itgae+ ), 호산구(SiglecF+ ), 호중구(Ly6G+) 및 NK 세포(Klrb1c+ Ncr1+ ) 비히클 또는 CBDIL로 치료된 종양에서-12. (e) 종양 세포 및 (f) 비히클로 처리된 쥐와 비교하여 CBD-IL{91}}을 처리한 쥐의 RM9 종양의 T 세포에서 차별적인 유전자 발현을 보여주는 화산 도표. FC 폴드 변경, FDR 잘못된 발견 비율. 소스 데이터는 소스 데이터 파일에 제공됩니다.
논의
CAR T 세포 치료법과 기타 면역 기반 표적 치료법의 효과는 개별 환자 내 종양 집단을 구성하는 모든 세포 또는 대부분의 세포에서 일관된 항원 발현에 크게 좌우됩니다. 그러나 항원 이질성은 전립선암을 포함한 고형 종양에서 두드러지며, mCRPC로의 진행과 치료 저항성은 별개의 전사 프로그램 및 세포 표면 항원 발현으로 표시되는 다양한 질병 하위 유형의 출현과 관련됩니다. PSMA는 질병 진행의 스펙트럼 전반에 걸쳐 상당한 과발현이 발견되는 전립선암의 가장 중요한 바이오마커 중 하나로 간주되지만, 우리 연구는 PSMA 발현이 치명적인 mCRPC에서 이질적임을 나타내는 최근 간행물14의 결과를 확증합니다. 우리는 이 설정에서 STEAP1이 PSMA보다 더 광범위하게 발현되지만 모든 mCRPC 조직에서 높은 수준으로 균일하게 발현되지는 않는다는 것을 보여줍니다. CAR T 세포 치료법을 포함한 단일 항원 표적 치료법은 mCRPC의 기존 종양 항원 이질성을 극복할 수 없습니다. 따라서 극복할 수 없는 치료 압력을 가하는 조합 치료법을 가능하게 할 수 있는 mCRPC의 STEAP1과 같은 추가 치료 표적을 철저하게 인증하는 것이 매우 중요합니다. 여기에는 이중 항원 표적화(예: PSMA 및 STEAP1) CAR T 세포 치료법 또는 CAR T 세포 치료법과 ADC, T-BsAbs 또는 항원 독립적 및 의존적 종양 살해를 잠재적으로 촉진하는 기타 치료법을 결합한 다중 모드 전략이 포함됩니다. 우리는 항원 특이성이 높고 CAR이 인식하는 에피토프를 STEAP1의 두 번째 ECD에 기능적으로 국한시키는 STEAP{12}}표적 CAR T 세포 치료법을 설계했습니다. 당사의 STEAP1-BBζ CAR T 세포는 인간-마우스 연구 및 마우스-마우스 연구 모두에서 여러 파종성 전립선암 모델에 대해 상당한 항종양 활성을 나타냈습니다. 중요한 것은 당사의 STEAP{20}}BBζ CAR이 PC3 전립선암 모델에 대한 반응성에서 입증된 바와 같이 낮은 항원 밀도 조건에서도 T 세포 활성화 및 표적 세포 세포용해를 유도할 수 있다는 것입니다. 그러나 낮은 수준의 STEAP1 발현에 대한 STEAP1-BBζ CAR T 세포의 이러한 민감성은 항종양 효능을 강화한다는 관점에서 유리할 수 있지만 표적 외 종양 독성으로 인한 책임을 강조할 수도 있습니다. STEAP1의 전신 발현은 이전에 전립선 상피 세포의 막 발현이 기술된 전립선을 제외하고 정상적인 인간 조직에서는 사실상 없는 것으로 보고되었습니다. 전임상 환경에서 STEAP{30}}BBζCAR T 세포 치료의 안전성을 조사하기 위해 인간화 STEAP1 마우스 모델을 생성했습니다. hSTEAP1-KI 마우스 모델은 전립선에서 인간 STEAP1 발현을 요약하고 부신 피질에서 발현을 보여주었습니다. 안심할 수 있는 것은, 항종양 활성을 유도하기에 충분한 용량의 STEAP{34}BBζ CAR T 세포 치료는 인간 STEAP1 부위의 표적 외 종양 독성을 포함하여 hSTEAP{35}}KI 마우스에서 뚜렷한 전신 독성을 나타내지 않았습니다. 표현. 우리 연구에서 STEAP{39}}BBζ CAR T 세포 치료 후 전립선암 재발 및 진행의 재발 메커니즘은 종양 항원 탈출이었습니다. 한편으로, 이 발견은 STEAP{40}}BBζ CAR T 세포 치료법의 전반적인 효능을 강조합니다. 그러나 종양 STEAP1 발현의 상실이 단지 내재된 종양 항원 이질성으로 인한 것인지 아니면 STEAP1 발현의 적응성 하향 조절도 있는지는 확실하지 않습니다. 최근 간행물에 따르면 STEAP1의 프로모터 메틸화가 STEAP1 발현을 조절하고 DNA 메틸트랜스퍼라제에 의한 후생적 조절 완화와 히스톤 데아세틸라제 억제가 STEAP1 발현을 유의하게 상향 조절하는 데 충분하다는 사실이 밝혀졌습니다. STEAP1 CAR T 세포 치료법과 병용한 후성유전학적 억제제를 사용한 치료는 동시에 종양 STEAP1 발현을 향상시키고 CAR T 세포를 유리한 탈진 저항성 분화 상태로 재프로그램화하여 전립선암에서 종양 항원 손실을 완화하고 항종양 효능을 향상시킬 수 있습니다. 우리 연구는 또한 STEAP1이 전립선암에서 세포 주기 진행과 세포 대사를 조절하는 기능적 역할을 한다는 것을 암시합니다. STEAP1은 메탈로 환원효소 활성에 필요한 세포내 산화환원효소 도메인이 부족하다는 점에서 다른 STEAP 계열 구성원(STEAP2, 3, 4)과 다릅니다. 결과적으로, STEAP1 동종삼량체(다른 STEAP 단백질과의 이종삼량체는 아님)에는 Fe3+를 Fe2+로, Cu2+를 Cu1+로 감소시키는 효소 기능이 부족합니다. 금속 이온 및 세포 대사에 STEAP1이 관여하는지 여부와 방법이 암 진행을 촉진하는지 여부와 방법은 아직 결정되지 않았으며 추가 조사가 가치가 있습니다. 전립선암의 면역학적으로 '차가운' 종양 미세환경은 암 면역요법의 효능에 대한 주요 장벽입니다. 예를 들어, mCRPC에서 우성-음성 형질전환 성장 인자-수용체(TGF R-DN)를 발현하도록 강화된 PSMA CAR T 세포 치료법의 I상 임상 시험과 관련된 탐구 연구에서는 종양 미세 환경에서 면역억제 신호 분자의 발현이 증가하는 것으로 나타났습니다. CAR T 주입 후13. 우리 연구에서 중요한 발견은 STEAP1-BBζ CAR T 세포 치료 후 STEAP1 녹아웃 세포와 STEAP1 항원 손실 종양 모두에서 STEAP1 발현 손실과 항원 처리 및 제시의 하향 조절 사이의 연관성이었습니다. 따라서 전립선암에서 STEAP1 항원 손실은 STEAP1-BBζ CAR T 세포 치료에 대한 직접적인 내성을 촉진할 뿐만 아니라 숙주 적응성 항종양 면역을 제한할 수도 있습니다. 재발성 교모세포종 환자를 대상으로 한 EGFR-vIII CAR T 세포에 대한 1상 연구에서는 Treg의 침윤 증가와 면역억제 분자의 발현 증가로 인해 종양 표적 항원 발현의 상실과 보다 면역억제적인 상태로의 전환이 관찰되었습니다76. STEAP1 항원 손실의 기본 기능적 메커니즘과 보다 일반적으로 입양 CAR T 세포 치료의 동적 효과가 고형 종양에서 종양-면역-기질 상호 작용을 조절하여 항원 손실 및 면역 편집에 기여할 수 있는 방법을 이해하려면 추가 작업이 필요할 것입니다.

그림 7|CBD-IL-12과 STEAP1-mBBζ CAR T 세포 치료법을 결합하면 전반적인 생존율과 염증성 사이토카인 수준이 향상됩니다. CBD-IL-12과 STEAP{{1{18}의 조합을 조사하는 hSTEAP1-KI/+ 마우스의 RM9-hSTEAP1 파종 모델에 대한 종양 유발 실험의 도식 }}}mBBζ CAR T 세포 치료법. Cy 사이클로포스파미드(전처리용). BioRender.com으로 제작되었습니다. b RM9-hSTEAP1- fLuc 전이가 이식되고 형질도입되지 않은 마우스 5 × 106마리를 단일 정맥 주사로 처리한 hSTEAP1-KI/ + 마우스의 연속 라이브 BLI 매주 CBD-IL- 12 처리 여부에 관계없이 0일의 T 세포 또는 STEAP1-mBBζ CAR T 세포. 빨간색 X는 죽은 쥐를 나타냅니다. 광도 규모가 표시됩니다. (c) (b)에서 각 마우스의 실시간 BLI로부터 시간에 따른 총 플럭스의 정량화를 보여주는 플롯. d 로그 순위(Mantel-Cox) 테스트(p= 0.002)에 의해 결정된 통계적 유의성을 갖는 (b)의 생쥐의 Kaplan-Meier 생존 곡선. e hSTEAP1-KI/+ 마우스의 안와후 출혈에서 얻은 ProcartaPlex 면역검정을 기반으로 한 IFN-(왼쪽, p= 0.002) 및 TNF-(오른쪽, p < 0.0001)의 혈청 사이토카인 수준을 보여주는 플롯( n 형질도입되지 않은 마우스 T 세포 또는 마우스 STEAP로 처리하기 전(0일) 및 처리 후(8일)에 RM9-hSTEAP1-fLuc 전이가 있는 그룹당=4마리의 마우스){{38} }CBζ-IL{40}} 치료 유무에 관계없이 mBBζ CAR T 세포. 오류 막대는 SEM의 평균을 나타냅니다. 패널 (e)의 경우 p-값은 Sidak의 다중 비교 테스트를 통해 양방향 ANOVA에서 파생되었습니다. 소스 데이터는 소스 데이터 파일에 제공됩니다.

그림 8|CBD-IL-12과 STEAP1-mBBζ CAR T 세포 치료법을 결합하면 종양 면역 미세환경을 재프로그램하고 항원 제시 및 에피토프 확산을 촉진합니다. a 마우스 비형질도입 T 세포 또는 STEAP{9}}mBBζ CAR T 세포로 처리한 후 RM9-hSTEAP1 폐 종양의 STEAP1(상단), B2m(중간) 및 CD3(하단) IHC 염색의 현미경 사진 또는 CBD-IL-12 처리 없이. 스케일 바=50 µm. b 전이성 폐 종양에 침윤하는 CD3 양성 세포의 IHC 정량을 보여주는 막대 그래프(그룹당 n= 4 종양). 일원 분산 분석 p=0.{{80}}021. 오류 막대는 SD의 평균을 나타냅니다. (c) Ly6C− F4/{{20}} MHC-II+의 빈도를 보여주는 플롯(왼쪽, 일원 분산 분석 p=0.00{ {98}}5) 및 Ly6C − F4/80+ iNOS2+ (오른쪽, 일원 분산 분석 p=0.0017) 대식세포, (d) Ly6C+ F4/ {{36} } MHC-II+(왼쪽, 일원 분산 분석 p=0.0038) 및 Ly6C+ F4/80+ iNOS2+(오른쪽, 일원 분산 분석 p=ns) 대식세포, (e) CD11b+ XCR1+ cDC1(단방향 ANOVA p=0.0003), (f) F4/80+ SiglecF+ 호산구(단방향 ANOVA p=0). 0008) 및 (g) 비형질도입 T 세포, STEAP{67로 처리한 후 다중 매개변수 유세포 분석법으로 측정한 총 CD45+ 세포로 정규화된 Ly6G+ 호중구(일원 ANOVA p= 0.0035) }}최대 치료 반응(최저) 및 종양 재발 시 mBBζ CAR T 세포, 비형질도입 T 세포 및 CBD-IL-12 및 STEAP1- mBBζ CAR T 세포 및 CBD-IL-12 (재발). h (a)에서 마우스로부터 수집한 종양 침윤 세포에 대한 TCRB 시퀀싱에 의해 분석된 TCR 레퍼토리의 '균등성'의 척도로서 Simpson 클론성을 나타내는 막대 그래프. n 그룹당=4개의 종양. 형질도입되지 않은 T 세포 및 STEAP1-mBBζ CAR T 세포와 비교하여 형질도입되지 않은 T 세포 + CBD-IL-12에 대한 P-값은 각각 0.008 및 0.02입니다. 및 STEAP1-mBBζ CAR T 세포 + CBD-IL-12은 형질도입되지 않은 세포 및 STEAP1-mBBζ CAR T 세포와 비교하여 각각 0.004 및 0.01입니다. 오류 막대는 SD의 평균을 나타냅니다. 그룹당 패널 (c–g) n=3 종양의 경우 *p < 0.05; **p < 0.01, ***p < 0.001, 패널(b-h)의 p-값은 Dunn의 다중 비교 테스트를 사용한 일원 분산 분석에서 나온 것입니다. 소스 데이터는 소스 데이터 파일에 제공됩니다.
항종양 반응을 확대하기 위해 우리는 hSTEAP의 파종성 동계 RM9-hSTEAP1 종양 모델에서 STEAP1-BBζ CAR T 세포 치료와 함께 CBD-IL-12의 전신 투여를 조사했습니다. 1-KI 마우스는 RM9의 이전 특성을 면역원성이 낮은 모델로 기반으로 하여 mCRPC의 면역억제 특성을 근사화합니다57,77. CBD-IL12와의 공동 치료는 전체 생존율, 사이토카인 생산, 종양 항원 제시 및 에피토프 확산과 일치하는 종양 내 T 세포 다양성의 개선을 가져왔습니다. 종양 면역 미세환경에 대한 면밀한 조사 결과, STEAP1-BBζ CAR T 세포 치료에 CBD-IL-12을 추가하면 종양 간질 복귀가 유도되고 활성화된 대식세포와 cDC1이 강화되는 동시에 종양 관련 호중구가 감소하는 것으로 나타났습니다. 그러나 우리 연구에서는 치료법이 달성되지 않았으며 Treg 유도를 촉진할 수 있는 면역억제성 호중구 및 cDC2의 빈도 증가를 포함하여 저항 및 종양 진행의 잠재적인 보상적, 적응적 메커니즘을 강조합니다. 항종양 반응을 최대화하려면 CBD-IL-12의 용량과 투여 일정을 더욱 최적화해야 할 수도 있다는 점에 유의하는 것이 중요합니다. 그러나 이러한 결과는 CAR T 세포가 재조합 사이토카인78(예: IL-2, IL-12, IL-15 또는 IL{24)을 발현하도록 강화하는 것과 같은 조합 면역치료 접근법의 조사를 뒷받침합니다. }}), 전립선암 종양 미세환경을 재형성하고 CAR T 세포 효과기 기능을 강화하기 위한 면역조절제(예: 항PD-1/PD-L1 또는 항CTLA4)를 사용한 동시 치료 또는 종양 지향 방사선요법. 이 원고가 준비되는 동안 노르웨이의 한 그룹 연구에서는 면역 저하 마우스의 피하 22Rv1 모델에서 항종양 활성을 갖는 STEAP1 CAR T 세포 치료법의 전임상 개발을 보고했습니다79. 보고된 STEAP1 CAR은 Oslo1이라는 합성 scFv와 CD8 힌지 및 막횡단 도메인을 통합한다는 점에서 STEAP{37}}BBζ CAR과 다릅니다. 또 다른 차별화 특징은 STEAP{40}}BBζ CAR T 세포가 CD4/CD8 T 세포의 정상적인 비율을 갖는 정의된 제품으로 준비되는 반면 Oslo1 STEAP1 CAR T 세포는 그렇지 않다는 것입니다. Oslo1 STEAP1 CAR T세포치료제에 대한 내성 기전 및 안전성 연구는 보고되지 않았다. 그러나 CAR 엔지니어링 및 세포 제품 구성의 이러한 차이가 Oslo1 STEAP1 CAR T 세포 치료법과 당사의 STEAP{49}}BBζ CAR T 세포 치료법 모두에서 항종양 효능, 지속성 및 안전성에 어떤 영향을 미칠 수 있는지 알아보는 것은 흥미로울 것입니다. 프로그램이 클리닉으로 번역됩니다. 우리의 연구 결과는 STEAP1-BBζ CAR T 세포 치료법을 mCRPC 남성을 위한 최초의 인간 실험으로 전환하기 위해 국립 암 연구소(NCI) 실험 치료법(NExT) 프로그램과의 파트너십으로 이어졌습니다. 이 초기 단계 임상 시험의 안전성 및 효능 신호는 STEAP1을 고도로 발현하는 다른 유형의 암에 대한 이 치료 접근법을 조사하는 데 가치가 있는지 여부를 결정하는 데 도움이 될 것입니다.
참고자료
1. Siegel, RL, Miller, KD, Fuchs, HE & Jemal, A. 암 통계, 2022. CA: Cancer J. Clinicians 72, 7–33 (2022).
2. 암스트롱, AJ 외. PREVAIL 시험에서 화학 요법을 받은 적이 없는 전이성 거세 저항성 전립선암 남성에서 엔잘루타마이드를 사용한 5년 생존 예측 및 안전성 결과. 유로. 우롤. 78, 347–357(2020).
3. Fizazi, K. et al. 전이성, 거세민감성 전립선암에 대한 아비라테론과 프레드니손의 병용요법. N.Engl. J. Med. 377, 352–360 (2017).
4. Scher, HI et al. 화학요법 후 전립선암에서 엔잘루타마이드를 사용하면 생존율이 높아졌습니다. N.Engl. J. Med. 367, 1187-1197(2012).
5. Parker, C. 외. 알파 방출체 라듐-223 및 전이성 전립선암에서의 생존. N.Engl. J. Med. 369, 213–223 (2013).
6. Sartor, O. 외. 전이성 거세 저항성 전립선암에 대한 Lutetium-177–PSMA-617. N.Engl. J. Med. 385, 1091–1103(2021).
7. 칸토프(Kantoff), PW 외. 거세 저항성 전립선암을 위한 Sipuleucel-T 면역치료제. N.Engl. J. Med. 363, 411-422(2010).
8. Jackson, HJ, Rafiq, S. & Brentjens, RJ 추진 CAR T 세포 앞으로. Nat. 클린 목사. 온콜. 13, 370–383(2016).
9. Weiner, GJ 더 나은 단클론 항체 기반 치료법을 구축합니다. Nat. Cancer 15, 361–370 (2015).
10. Chavez, JC, Bachmeier, C. & Kharfan-Dabaja, MA B 세포 림프종에 대한 CAR T 세포 치료: 이용 가능한 제품의 임상 시험 결과. 치료 보조. 헤마톨. 10, 2040620719841581(2019).
11. Sterner, RC & Sterner, RM CAR-T 세포 치료: 현재의 한계와 잠재적인 전략. 혈액암 J. 11, 69(2021).
12. Slovin, SF 외. 전이성 거세저항성 전립선암(mCRPC) 환자를 대상으로 한 P-PSMA-101 CAR-T 세포에 대한 1상 연구. J. 클린. 온콜. 40, 98–98(2022).
13. Narayan, V. et al. 전이성 거세 저항성 전립선암의 PSMA 표적화 TGF 비감수성 장갑 CAR T 세포: 1상 시험. Nat. 메드. 28, 724–734(2022).
14. Paschalis, A. et al. 전립선암의 전립선 특이적 막항원 이질성과 DNA 복구 결함. 유로. 우롤. 76, 469–478(2019).
15. Chen, N., Li, X., Chintala, NK, Tano, ZE & Adusumilli, PS 고형 종양에서 항원 이질성의 고르지 않은 길에서 CAR을 운전합니다. 현재 의견. 면역. 51, 103–110 (2018).
16. Morgan, RA 등. ERBB2를 인식하는 키메라 항원 수용체로 형질도입된 T 세포 투여 후 심각한 이상반응에 대한 사례 보고입니다. 몰. 거기. J.Am. Soc. 진 터. 18, 843–851 (2010).
17. Lee, JK et al. 전신 표면체 프로파일링은 진행성 전립선암의 하위 유형에서 면역 기반 치료를 위한 표적 항원을 식별합니다. 진행 Natl. Acad. 과학. 미국 115, E4473–e4482(2018).
18. Hubert, RS 등. STEAP: 인간 전립선 종양에서 고도로 발현되는 전립선 특이적 세포 표면 항원. 진행 Natl Acad. 과학. USA 96, 14523-14528(1999).
19. Nolan-Stevaux, O. Abstract DDT02-03: AMG 509: XmAb® 2+1 항체를 모집하는 새로운 인간화 반감기 연장 이중특이적 STEAP1 × CD3 T 세포. 암 입술. 80, DDT02-03-DDT02-03(2020).
20. Grunewald, TG et al. 높은 STEAP1 발현은 유잉 육종 환자의 결과 개선과 관련이 있습니다. 앤. 온콜. 끄다. J. Eur. Soc. 메드. 온콜. 23, 2185-2190(2012).
21. Moreaux, J., Kassambara, A., Hose, D. & Klein, B. STEAP1은 암에서 과발현됩니다: 유망한 치료 목표입니다. 생화학. 생물 물리학. 결의안. 커뮤니케이터 429, 148–155 (2012).
22. Oosterheert, W. & Gros, P. Cryo-전자 현미경 구조 및 전립선의 인간 6-막횡단 상피 항원 1(STEAP1)의 잠재적인 효소 기능. J. Biol. 화학. 295, 9502-9512(2020).
23. Jiao, Z. et al. 전립선 1 발현의 6개 막횡단 상피 항원은 상피-중간엽 전이의 진행을 보조함으로써 난소암 전이를 촉진합니다. 히스토켐. 셀바이올. 154, 215–230(2020).
24. Gomes, IM, Arinto, P., Lopes, C., Santos, CR & Maia, CJ STEAP1은 전립선암 및 전립선 상피내 종양 병변에서 과발현되며 Gleason 점수와 긍정적인 연관이 있습니다. 비뇨기과 종양학: 세미나 및 독창적인 조사. 권. 32, 53.e23–53.e29(엘스비어, 2014).
25. Huo, S.-f. 외. STEAP1은 JAK2/STAT3 신호 전달 경로를 통해 폐 선암종의 전이 및 상피-중간엽 전이를 촉진합니다. Biosci. 국회의원 40, BSR20193169(2020).
26. Gomes, IM 외. STEAP1의 녹다운은 세포 성장을 억제하고 안드로겐의 효과를 방해하는 LNCaP 전립선암 세포의 세포사멸을 유도합니다. 메드. 온콜. 35, 1–10(2018).
27. Gomes, IM, Maia, CJ & Santos, CR STEAP 단백질: 구조부터 암 치료의 적용까지. 몰. 암 입술. MCR 10, 573–587(2012).
28. Danila, DC 외. 전이성 거세 저항성 전립선암에서 전립선 1의 6개 막관통 상피 항원을 표적으로 하는 항체-약물 접합체인 DSTP3086S에 대한 1상 연구입니다. J. 클린. 온콜. 끄다. J.Am. Soc. 클린. 온콜. 37, 3518–3527(2019).
29. Kelly, WK 외. 전이성 거세 저항성 전립선암(mCRPC) 환자를 대상으로 XmAb 2+1 면역 요법을 모집하는 STEAP1 x CD3 T 세포인 AMG 509에 대한 1상 연구입니다. J. 클린. 온콜. 38, TPS5589-TPS5589(2020).
30. Lin, T.-Y., Park, JA, Long, A., Guo, H.-F. & Cheung, N.-KV 암 면역요법을 위해 T 세포의 방향을 바꾸는 새로운 강력한 항-STEAP1 이중특이적 항체. J. 면역 다른. 암 9, e003114(2021).
31. Schober, SJ 외. STEAP1에 대한 MHC 클래스 I 제한 TCR 형질전환 CD4(+) T 세포는 생체 내 유잉 육종의 국소 종양 제어를 중재합니다. 셀 9, 1581(2020).
32. Roudier, MP 외. 뼈로 전이되는 말기 전립선암의 표현형 이질성. 흠. 파톨. 34, 646-653(2003).
33. Gomes, IM, Santos, CR, Socorro, S. & Maia, CJ 전립선 1의 식스 경막 상피 항원은 전립선 세포의 성호르몬에 의해 하향 조절됩니다. 전립선 73, 605–613 (2013).
34. Sharp, A. et al. 안드로겐 수용체 스플라이스 변형-7 발현은 전립선암에서 거세 저항과 함께 나타납니다. J. 클린. 투자하다. 129, 192-208(2019).
35. Bakht, MK et al. 전립선암의 신경내분비 분화는 PSMA 억제로 이어진다. Endocr.-Relat. 암 26, 131–146 (2018).
36. Ihlaseh-Catalano, SM 외. STEAP1 단백질 과발현은 전립선 암종의 생화학적 재발에 대한 독립적인 지표입니다. 조직병리학 63, 678-685 (2013).
37. Gomes, IM 외. STEAP1의 녹다운은 세포 성장을 억제하고 안드로겐의 효과를 방해하는 LNCaP 전립선암 세포의 세포사멸을 유도합니다. 메드. 온콜. 35, 40(2018).
38. Logan, AC 외. 렌티바이러스 벡터의 역가 및 감염성에 영향을 미치는 요인. 흠. 진 터. 15, 976-988(2004).
39. Morgan, RA, Gray, D., Lomova, A. & Kohn, DB 조혈 줄기 세포 유전자 치료: 진행 상황 및 교훈. 세포줄기세포 21, 574–590 (2017).
40. 라슨(Larson), SM 외. 암 면역치료를 위한 키메라 항원 수용체를 이용한 조혈줄기세포 유전자 변형의 전임상 개발. 흠. 백신 면역 다른. 13, 1094-1104(2017).
41. Salter, AI et al. 키메라 항원 수용체 신호전달의 인단백질체 분석은 세포 기능에 영향을 미치는 동역학 및 정량적 차이를 보여줍니다. 과학. 신호. 11, eaat6753(2018).
42. Majzner, RG 외. CAR T 세포 활동에 대한 항원 밀도 요구 사항을 조정합니다. 암 발견. 10, 702-723(2020).
43. Challita-Eid, PM 외. 전립선의 6개 막관통 상피 항원에 대한 단일클론 항체-1는 시험관 내 세포 간 통신과 생체 내 인간 종양 이종이식편의 성장을 억제합니다. 암 입술. 67, 5798-5805(2007).
44. Hudecek, M. 외. 키메라 항원 수용체의 비신호전달 세포외 스페이서 도메인은 생체내 항종양 활성에 결정적이다. 암 면역. 결의안. 3, 125–135(2015).
45. Gomes, IM, Santos, CR & Maia, CJ 전립선 세포주에서 STEAP1 및 STEAP1B의 발현 및 전사 후 및 번역 후 메커니즘에 의한 STEAP1의 추정 조절. 유전자 암 5, 142–151 (2014).
46. Bernsel, A., Viklund, H., Hennerdal, A. & Elofsson, A. TOPCONS: 막 단백질 토폴로지의 합의 예측. 핵산 해상도. 37, W465-W468(2009).
47. Krogh, A., Larsson, B., Von Heijne, G. & Sonnhammer, EL 숨겨진 Markov 모델을 사용한 막횡단 단백질 토폴로지 예측: 완전한 게놈에 적용. J.Mol. Biol. 305, 567-580(2001).
48. Long, AH 등. 4-1BB 공동 자극은 키메라 항원 수용체의 강장제 신호 전달에 의해 유발된 T 세포 피로를 개선합니다. Nat. 메드. 21, 581-590(2015).
49. Berger, C. 외. 중앙 기억 세포에서 유래된 이펙터 CD8+ T 세포의 입양 전달은 영장류에서 지속적인 T 세포 기억을 확립합니다. J. 클린. 조사하다. 118, 294-305(2008).
50. Gattinoni, L. 외. 줄기세포와 유사한 특성을 지닌 인간 기억 T 세포 하위 집합입니다. Nat. 메드. 17, 1290-1297(2011).
51. Xu, Y. et al. 밀접하게 관련된 T-기억 줄기 세포는 CAR의 생체내 확장과 상관관계가 있습니다. CD19-T 세포는 IL-7 및 IL-15에 의해 보존됩니다. 블러드 123, 3750–3759(2014).
52. Cieri, N. et al. IL-7 및 IL-15은 순수 전구체로부터 인간 기억 줄기 T 세포의 생성을 지시합니다. 블러드 121, 573–584 (2013).
53. Hansel, DEet al. 형태학적 및 표현형적으로 구별되는 동시 원발성 소세포 신경내분비 암종 및 전립선 선암종에서 공유된 TP53 유전자 돌연변이. 전립선 69, 603–609(2009).
54. Cuzick, J. 외. 전립선암 환자의 세포주기 증식 유전자에서 유래된 RNA 발현 시그니처의 예후 가치: 후향적 연구. 란셋온콜. 12, 245–255 (2011).
55. Chen, ME, Lin, SH, Chung, LW & Sikes, RA PAGE-1 및 GAGE-7의 분리 및 특성화. 흑색종 관련 항원과 상동성을 공유하는 LNCaP 전립선암 진행 모델에서 발현되는 새로운 유전자. J. Biol. 화학. 273, 17618-17625(1998).
56. Baley, PA, Yoshida, K., Qian, W., Sehgal, I. & Thompson, TC 전립선암에 대한 새로운 시험관 내 마우스 모델에서 안드로겐 무감각으로의 진행. J. 스테로이드 생화학. 몰. Biol. 52, 403-413(1995).
57. Murad, JP 외. 사전 컨디셔닝은 TME를 수정하여 고형 종양 CAR T 세포 효능 및 내인성 보호 면역을 강화합니다. 몰. 거기. J.Am. Soc. 진 터. 29, 2335–2349(2021).
58. Brunda, MJ 외. 쥐 종양에 대한 인터루킨 12의 항종양 및 항전이 활성. J. 특급. 메드. 178, 1223-1230(1993).
