식물 이차 대사산물에 의한 미토콘드리아 표적화: 파킨슨병 퇴치를 위한 유망한 전략
Mar 20, 2022
연락하다:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
추상적인
파킨슨병질병(PD)는 가장 널리 퍼져 있고 쇠약하게 만드는 것 중 하나입니다.신경퇴행성조건이며 현재 상승하고 있습니다. 여러 조절 장애 경로가 PD의 발병 기전 뒤에 있습니다. 그러나 중요한 목표는 불분명합니다. 따라서, PD의 주요 조절 장애 경로를 밝히는 것이 시급합니다. 널리 퍼진 보고서는 PD의 신경 장애, 유전적 변화 및 관련 합병증에서 미토콘드리아 및 누화 매개체의 중요성을 강조했습니다. PD의 다양한 병태생리학적 기전과 기존의 신경보호 요법의 낮은 효능 및 부작용으로 인해 새로운 대체 약제를 찾아야 할 필요성이 대두되고 있습니다. 최근에는 미토콘드리아를 표적으로 하여 PD 관련 증상을 조절하기 위해 식물 2차 대사 산물(예: 플라보노이드/페놀 화합물, 알칼로이드 및 테르페노이드)을 사용하는 데 많은 관심을 기울이고 있습니다. 이 계통에서 식물 2차 대사산물은 미토콘드리아 세포자멸사와 활성산소종의 동시 조절에 대한 유망한 잠재력을 보여주었다. 이 검토는 식물 유래 이차 대사 산물에 의한 PD의 미토콘드리아 및 여러 조절 장애 경로를 해결하는 것을 목표로 했습니다.
키워드:신경퇴행성질병;파킨슨병질병; 이차 대사 산물; 파이토케미컬; 미토콘드리아; 신호 경로

시탕슈 비엔페이
1. 소개
인간은 항상 다양한 신경학적 합병증의 영향을 받아 왔습니다[1,2].신경퇴행성질병은 중추 및 말초 신경계에 큰 영향을 미치며 신체적, 정신적 기능의 손실을 초래합니다[3,4]. 신경 변성 뒤에는 신경 염증, 산화 스트레스, 세포 사멸, 세포 사멸을 유발하는 자가포식 등 여러 기전이 있습니다[1,3,5].
신경퇴행성 질환의 병인에서 조절되지 않는 여러 경로의 관여를 고려할 때, 이러한 장애에서 중요한 신호 전달 경로를 밝히는 것은 대체 요법을 개발할 수 있는 길을 열어주는 것으로 보입니다. 따라서 미토콘드리아 관련 장애, 상호 연결된 산화 스트레스 및 활성산소종(ROS)이 신경퇴화에 관여하는 일반적인 매개체로 보입니다[1,5]. 이 라인에서 미토콘드리아 관련 신호 전달 경로를 표적으로 하는 것은 전쟁에서 새로운 길을 열 수 있습니다파킨슨병질병(PD), 허혈성 뇌 손상(IBI), 척수 손상(SCI), 알츠하이머병(AD), 헌팅턴병(HD), 다발성 경화증(MS) 및 근위축성 측삭 질환(ALS) [6-8].
Sajad Fakhri 1,†, Sadaf Abdian 2,†, Seyede Nazanin Zarneshan 2, Esra Küpeli Akkol 3, Mohammad Hosein Farzaei 1,* 및 Eduardo Sobarzo-Sánchez 4,5,*
1 약학 연구 센터, 건강 연구소, Kermanshah University of Medical Sciences, Kermanshah 6734667149, 이란;
2 학생 연구 위원회, Kermanshah University of Medical Sciences, Kermanshah 6734667149, Iran; abdian.ph@gmail.com (SA);
3 Gazi University, 약학부, 약학부, 06330 Ankara, Turkey;
4 산티아고데콤포스텔라대학교 약학부 유기화학과, 15782 Santiago de Compostela, Spain
5 Instituto de Investigación y Postgrado, Facultad de Ciencias de la Salud, Universidad Central de Chile, Santiago 8330507, 칠레
미토콘드리아는 진핵 세포의 중요한 구성 요소이며 세포 에너지 [7,8], 특히 신체의 더 활동적인 세포 [9] 생성을 담당합니다. 미토콘드리아는 관련 복합체에 의한 산화적 인산화 메커니즘을 통해 이 에너지를 공급합니다[10]. 에너지 생산 작업 외에도 미토콘드리아는 이온과 세포 금속의 균형을 유지하는 것뿐만 아니라 세포 생존/사망과 관련된 절차에도 관여합니다[5]. 미토콘드리아에서 이러한 다양한 기능은 세포 평형의 정상적인 조건에서 구성 요소에 의해 수행됩니다[8]. 신경 기능 장애에서는 앞서 언급한 세포 균형이 상실되고 신경 세포의 미토콘드리아 기능이 손상됩니다[8,11]. 이러한 신경 손상 상황에서 미토콘드리아는 ROS 생성의 조절 장애와 산화 스트레스에 대한 민감성을 만나 세포 손상을 유발합니다[12,13]. 미토콘드리아의 기능적, 형태적 변화와 효소의 이상은 신경 손상과 그에 따른 신경 퇴행성 질환을 유발합니다[8]. 따라서 미토콘드리아 기능장애는 퇴행성 신경질환의 원인 중 하나이다[5,8,12].

신경 퇴행성 질환에서 미토콘드리아는 PD에서 도파민성 뉴런의 파괴를 방지하기 위해 신경 세포의 에너지와 안정성을 공급하는 데 중요한 역할을 합니다. 또한 미토콘드리아 독소의 역할도 부인할 수 없습니다. 예를 들어, 1- 메틸-4-페닐{2}},2,3,{5}}테트라하이드로피리딘(MPTP)은 미토콘드리아에서 복합체 I의 활성을 차단하고 ROS 생산량을 증가시키며 궁극적으로 세포 사멸을 일으키는 세포 사멸 단백질의 방출 [14,15]. 또한 미토콘드리아는 PD의 여러 조절 장애 경로와 긴밀한 상호 연결을 가지고 있습니다.
따라서 미토콘드리아와 긴밀한 누화 매개체의 동시 표적화는 PD 퇴치를 위한 길을 닦을 수 있습니다. PD 및 기타 NDD에 대한 확실한 치료법은 없지만 조절 장애 기전에 영향을 주어 관련 증상을 제어하기 위해 다양한 전략이 사용되었습니다[16]. 신경 합병증 퇴치에서 합성 요법의 더 높은 수준의 부작용과 낮은 효능을 고려하여 천연물은 새로운 대체 요법에 대한 관심을 불러일으켰습니다[17-19]. 결과적으로, 식물 유래 2차 대사산물은 미토콘드리아 장애 및 신경 장애에서 상호 연결된 염증/산화 경로를 조절하는 데 매우 중요합니다[8,19]. 이러한 2차 대사산물은 미토콘드리아 복합체 및 ROS 관련 경로의 억제, 세포자멸사 경로의 억제, -synuclein 잘못 접힌 응집체의 생성 방지를 포함한 여러 메커니즘을 통해 미토콘드리아 기능을 동시에 약화시킵니다[20,21].
이전 연구에서는 세포 보호를 위해 미토콘드리아를 표적으로 하는 플라보노이드의 역할을 검토했습니다[22]. 포스포이노시티드 3-키나제(PI3K)/단백질 키나제 B(Akt) 및 핵인자 적혈구계-2-관련 인자 2(Nrf2)의 관여도 PD 동안 미토콘드리아 활성을 조절하는 데 강조 표시됩니다[23,24]. 그러나 미토콘드리아 활성의 조절에 잠재적인 대체 요법이 거의 도입되지 않았습니다. 이것은 식물 2차 대사산물에 의한 미토콘드리아 경로의 표적화와 PD의 병리학적 상태의 조절에 대한 첫 번째 검토입니다.
2. PD의 미토콘드리아
파킨슨병은 안정떨림(rest tremor), 강직(rigidity), 운동완화(bradykinesia) 등의 특정 증상을 보이는 가장 흔한 신경계 질환 중 하나이다[8,25]. 사람들의 평균 연령이 증가함에 따라 영향을받는 환자의 수가 증가 할 것으로 예상됩니다 [11,26]. 파킨슨병 발병 환자의 평균 연령은 50세 이상이나 다양한 환경적, 유전적 요인의 영향을 고려할 때 더 어린 나이에도 다양한 증상으로 나타날 수 있다[26]. 증상으로는 운동장애, 비자발적 움직임, 강직, 정신 장애와 관련된 문제 등이 있습니다[3,26]. 신경퇴행의 발병기전에는 수많은 분자 기전이 관여하고 있지만, 도파민의 시냅스 파괴와 미토콘드리아 기능장애가 주요 역할을 한다[8]. 파킨슨병의 기본적인 신경병리학은 흑색질의 치밀부(SNc)에서 도파민성 뉴런의 점진적인 고갈과 루이소체(LB) 및 루이 신경돌기(LN)의 존재를 특징으로 합니다[26]. 이 단백질은 신경 세포의 시냅스 전 단백질인 -synuclein과 가족성 및 간헐성 PD에 관여하는 도파민성 신경 세포의 파괴에서 유래합니다[25]. 기능을 수행하기 위해 뉴런은 미토콘드리아에서 제공하는 에너지를 공급해야 합니다[8,27]. 또한 미토콘드리아는 신경 세포의 안정성을 유지하는 데 중요한 역할을 합니다. 따라서 미토콘드리아와 관련된 기전을 교란하여 신경 세포가 손상되고 신경 퇴행성 질환, 특히 PD가 발생합니다[8,12].
구체적으로, PD 동안 미토콘드리아 전자 수송 사슬(ETC) 및 복합체 I, II, III, IV, V의 조절 장애는 세포 에너지의 변화를 초래하고, 산화 스트레스를 증가시키고, 미토콘드리아 게놈의 돌연변이를 유발하고, DNA 기형을 유발하고, PD와 관련된 유전자를 변경합니다[28]. 미토콘드리아 복합체의 역할과 관련하여 전자 이동을 통해 미토콘드리아에서 산화적 인산화 시스템의 에너지 생산에 5가지 효소 하위 집합이 관여합니다. 복합체는 복합체 I(유비퀴논 산화환원효소 또는 NADH 탈수소효소), 복합체 II(숙시네이트 탈수소효소), 복합체 III(사이토크롬 c-산화환원효소 또는 시토크롬 bc1), 복합체 IV(사이토크롬 c 산화효소) 및 복합체 V(ATP 합성효소)로 명명됩니다[25 ]. 미토콘드리아에는 서로 다른 양의 ROS를 생성하는 3개의 효소 복합체가 있습니다[12]. Complex I 또는 NADH CoQ reductase는 미토콘드리아에서 ROS의 가장 중요한 1차 생산자 중 하나입니다. 이 복합적이고 산화적인 매개체의 구조 변화는 PD 발달에 관여합니다[29]. 복잡한 I 미토콘드리아 ETC의 차단제는 사람과 동물에서 PD를 유발하고, 유전성 PD와 관련된 파킨 또는 DJ{6}}의 녹아웃은 손상된 미토콘드리아 활성을 나타냅니다[30]. 로테논 및 MPTP와 같은 복합 I의 기능을 방해하는 억제제는 PD를 유발합니다. MPTP는 선조체에 있는 3,{9}}디하이드록시페닐아세트산(DOPAC) 및 호모바닐산(HVA)을 포함하는 도파민과 그 대사물을 현저히 낮췄습니다[15]. PD에서 MPTP 생성은 미토콘드리아 이상으로 인해 발생합니다. 그것은 내부 미토콘드리아 막(IMM) 탈분극, 손상된 산화적 인산화, 상승된 ROS 출력, 미토콘드리아 기질 팽창, IMM 크리스타 전개, Ca2의 손실 및 항상성, 및 외부 미토콘드리아 막을 통한 세포자멸사 단백질의 방출과 같은 일련의 사건을 포함합니다. OMM), 결국 세포 사멸을 초래합니다[14]. Complex III는 Complex I과 유사하게 미토콘드리아에서 ROS의 원천입니다[12,13]. 이 계통에서 PD 관련 독소 MPTP, 로테논, 피리다벤, 트리클로로에틸렌 및 펜피록시메이트는 미토콘드리아 효소/복합체의 정상적인 기능을 방해하여 신경 세포에 손상을 줍니다[25]. 미토콘드리아 에너지 생산 과정에서 ROS도 생성되는데, 이는 뉴런 세포의 정상적인 기능에 영향을 미칩니다[25].

시스탄체 보디빌딩
또한, 미토콘드리아 및 신경 세포 게놈의 돌연변이는 또 다른 관련 파괴 메커니즘입니다. 따라서 미토콘드리아 DNA에서 12SrRNA 및 G11778A의 돌연변이에 이어 PINK1(PTEN-유도 키나제 1), PARK2(파킨), DJ{6}} 및 LRRKS(류신이 풍부한 반복 키나아제)는 ROS 생산을 유도합니다. 이 과정은 미토콘드리아와 ROS 사이의 불균형, 산화 스트레스에 대한 세포 보호의 상실, 미토콘드리아의 자가포식, α-시누클레인 비율의 증가로 인한 것입니다[8,25].
다른 메커니즘 중에서 미토콘드리아 분열 및 융합의 이상이 PD에서 중요한 역할을 합니다. 미토콘드리아 기능 장애는 PD에서 잘 알려져 있지만 미토콘드리아 분열, Drp1 및 융합 불균형의 역할은 아직 알려지지 않았습니다. Drp1 단백질(미토콘드리아 단편화에 관여하는 핵분열 단백질)과의 불규칙한 미토콘드리아 상호작용은 미토콘드리아 분열 및 PD에 관여하는 관련 조절 장애 단백질의 원인이 됩니다[8].
반면에 Drp1의 향상된 생산은 근육 기능 장애를 예방합니다. 또한 PINK1 돌연변이는 유전 PD와 관련이 있습니다. 미토콘드리아 분열은 PINK1/파킨 경로에 의해 자극되었고, 관련 돌연변이는 미토콘드리아 분열 감소를 통해 미토콘드리아와 조직 안정성을 조절하지 못합니다. synuclein, Parkin, PINK1 및 DJ1 단백질의 돌연변이는 PD의 신경 미토콘드리아 기능 장애와 관련이 있습니다[8]. SH-SY5Y 세포에서 PINK1 균형의 녹다운은 미토콘드리아 활성과 자가포식의 붕괴를 일으켰으며, 이는 PINK1에 대한 RNA 간섭(RNAi) 내성 플라스미드가 재도입되었을 때 모두 뒤집혔습니다. 또한, 미토콘드리아 형태 변화는 PINK1 돌연변이와 미토콘드리아 융합 프로모터, 미토푸신 2(Opa1) 및 융합 1(Mfn2)에 의해 유발됩니다[8]. LRRK2, EIF4G1, VPS35 및 PARK7은 PD에서 중요한 역할을 하는 다른 유전 관련 요인입니다. -synuclein의 A30P, E46K 및 A53T missense 돌연변이는 -synuclein 단백질이 LB를 결합하고 형성하는 -sheet를 구성하는 경향을 향상시킵니다. 이 돌연변이 유전자의 여러 사례가 PD의 다양한 유전 사례에서 발견되었습니다[26]. 또한 PD에 걸리기 쉬운 다른 요인으로는 독소와 식사 중 철분 결핍이 있습니다[26].
Nrf2는 신체가 산화 스트레스를 견디도록 돕는 해독 유전자의 중요한 조절자입니다[15]. 놀랍게도, 새로운 연구에 따르면 폴로 유사 키나아제 2(PLK2)의 생성은 글리코겐 합성 효소 키나아제 3(GSK-3)을 인산화하여 항산화 신호를 촉진하여 Nrf2의 핵 전달을 촉진하여 항산화 반응 요소(ARE)를 활성화합니다. . 이 PLK2는 미토콘드리아 기능을 조절하는 데 필수적인 역할을 할 수 있습니다[15].
레보도파는 파킨슨병에 사용되는 주요 약물 중 하나로 도파민을 대사 전구체로 공급하는 역할을 합니다[31]. 레보도파 및 기타 기존 치료법 외에도 천연물 및 2차 대사산물에 대한 관심도 증가했습니다[19,25,31]. PD의 기존 치료는 뉴런에서 도파민의 파괴, 공급 및 저장 메커니즘을 기반으로 합니다[31]. 최근 몇 년 동안 식물 이차 대사 산물은 PD에 중점을 둔 신경 퇴행성 질환 퇴치에 중요한 대체 요법입니다.
3. 식물 이차 대사 산물과 미토콘드리아
앞서 언급한 바와 같이 식물의 2차 대사산물은 다양한 신경계 질환의 조절 및 치료와 관련하여 서로 다른 특성을 가지고 있습니다[19]. 이차 대사 산물의 사용은 신경 세포 기능 장애를 조절하는 메커니즘을 방해할 수 있습니다[13]. 기계론적 관점에서 볼 때, 이러한 대사산물은 신경퇴행성 질환을 제어하고 예방하는 미토콘드리아 사건과 상호 연결된 다양한 항산화, 항염 및 항세포자멸 효과를 보여줍니다[26]. 또한 이러한 대사 산물의 섭취와 미토콘드리아를 표적으로 하여 신경퇴행성 질환을 개선하는 것 사이에는 상당한 관계가 있습니다[21].
미토콘드리아를 보호하고 세포자멸사 및 산화 스트레스의 위험을 방지하려는 노력은 파이토케미칼의 ROS 관련 경로에 의해 영향을 받습니다[18,32](그림 1). 식물 2차 대사산물은 또한 Sirtuin1(SIRT1), peroxisome proliferator-activated receptor gamma coactivator 1-alpha(PGC{8}})를 통해 미토콘드리아 생합성을 자극하여 신경 세포의 미토콘드리아 복합체/효소에 항산화 및 조절 효과가 있습니다. , 전사 인자 A, 미토콘드리아(TFAM) 및 Nrf1 경로가 미토콘드리아 분열을 차단하고 [33], 막 안정성을 유지한다[32].

4. 미토콘드리아 표적화를 통한 파이토케미칼에 의한 PD 조절
이차 대사 산물은 미토콘드리아를 표적으로 삼아 신경퇴행성 질환, 특히 PD에 대한 유망한 효과를 보여주었습니다[19,25,34]. PD는 미토콘드리아 기능 장애, 산화 스트레스 및 신경 염증을 특징으로 하는 복잡한 신경 퇴행성 질환입니다. 이 라인에서 폴리페놀, 테르펜/테르페노이드 및 알칼로이드의 효과는 다양한 메커니즘을 통해 PD의 미토콘드리아에 강조 표시됩니다.
4.1. PD의 미토콘드리아에 대한 폴리페놀 효과
폴리페놀은 PD 동안 미토콘드리아를 조절하는 주요 2차 대사 산물입니다. 이 2차 대사산물은 플라보노이드, 리그난, 스틸벤 및 페놀산의 4가지 주요 범주를 포함하여 페닐 고리를 기반으로 하는 구조를 가지고 있습니다[6,13,25]. 플라보노이드는 차례로 플라보놀, 플라본, 플라바논, 플라바노놀, 플라바놀, 안토시아닌 및 이소플라본을 포함하는 7개의 서브유닛을 가지고 있습니다[13,35]. 폴리페놀은 미토콘드리아 기능 장애로 인한 산화 스트레스, 세포 사멸 및 염증 과정을 완화할 뿐만 아니라 -synuclein 잘못 접힌 응집의 생성을 방지합니다[21].
바이칼레인은 Scutellaria baicalensis 뿌리의 주요 활성 플라본 요소이며 6-하이드록시도파민(6-OHDA)[36,37]에 의해 유도된 생체 내 및 시험관 내 실험에서 미토콘드리아 기능 장애를 감소시킵니다. 격리된 뇌 미토콘드리아에서 바이칼레인 처리는 로테논 유도 ROS 생성, ATP 부족 및 미토콘드리아 팽창을 감소시켰습니다. 놀랍게도, 바이칼레인은 고립된 미토콘드리아에서 미토콘드리아 호흡 작용을 증가시켰습니다. 이러한 발견은 바이칼레인이 로테논 유도 신경독성에 대한 예방 특성을 갖는 미토콘드리아 표적화를 갖는 적절한 항산화제임을 암시한다[38].
푸에라리아 톰소니에서 얻은 이소플라본인 푸에라린은 1-메틸{1}}페닐피리디늄(MPP plus) 유도 PD의 시험관 내 모델의 독성을 감소시켜 미토콘드리아에 대한 치료 효과를 나타냈습니다[36]. PC12 세포와 1차 쥐 중뇌 뉴런에서 푸에라린은 미토콘드리아 기능 장애의 선택적 조절을 위해 미토콘드리아 효소 아르기나제{6}}를 상향 조절함으로써 PD에서 산화질소(NO) 매개 신경독성을 감소시켰습니다[39]. 또한, 뉴런에서 유비퀴틴-프로테아좀 시스템의 오작동은 PD를 악화시키는 것으로 광범위하게 확립되었습니다. 푸에라린은 또한 세포 생존을 증가시키고 형태학적 변화를 강화하며 유비퀴틴-프로테아좀 시스템을 조절하여 세포자멸사 속도를 감소시켜 MPP 플러스 유도 SH-SY5Y 세포에서 세포자멸사를 방지했습니다[40]. 다른 연구에서 플라보노이드는 미토콘드리아 효소 복합체 I(예: 루테올린, 피세틴, 로비넷, 미리세틴, 람네틴, 바이칼레인) 및 III(예: 히스피둘린 및 유파폴린)에 대한 치료 가능성을 나타냈습니다[13]. 또한, 플라보노이드는 PD에서 도파민 고갈 및 ROS 개시를 방어했습니다[25].
적포도주에 함유된 케르세틴과 레스베라트롤과 같은 폴리페놀 물질도 세포자멸사를 억제하여 미토콘드리아에 대한 치료 가능성을 보였다[13,20]. 레스베라트롤 치료는 또한 SH-SY5Y 세포에서 로테논 유도 미토콘드리아 막 전위를 회복시키고 미토콘드리아 역학을 변경하며 단편화된 미토콘드리아를 연장했습니다[41]. 케르세틴은 또한 미토콘드리아 생합성을 촉진하는 데 필수적인 역할을 했습니다[42]. MPP 플러스 또는 지질다당류(LPS)에 노출된 SH-SY5Y 세포에서 케르세틴으로 전처리하면 미토콘드리아 손상이 크게 감소했습니다. 티로신 수산화효소와 미토콘드리아 조절 단백질은 모두 케르세틴에 의해 상향 조절되었습니다[43]. 이전에 설명한 바와 같이 PD는 미토콘드리아 기능 장애와 미토파지 부족으로 인해 발생합니다. 6-OHDA 처리된 PC12 세포에서 케르세틴 투여는 미토콘드리아 품질 관리를 강화하고 산화 스트레스를 줄였으며 미토파지 마커의 수준을 높였습니다. 또한, PD가 있는 쥐에서 케르세틴은 6-OHDA로 유발된 PD 유사 운동 이상 진행을 완화하고 신경 세포 사멸을 감소시키며 미토콘드리아 기능 장애를 감소시켰습니다[44]. 추가 연구에 따르면 케르세틴의 분석은 미토콘드리아 ETC 이상을 복구하고 상향 조절되는 것으로 가정했습니다. 이 활동은 미토콘드리아 신경독에 의한 파킨슨병에서 나타나는 신경보호의 기초이다[45]. 케르세틴 3-o-갈락토사이드인 Hyperoside는 시험관 내 실험에서 PC12 세포에서 미토콘드리아 세포자멸사 신호를 감소시키는 플라보놀 배당체입니다[46].
실리범 마리아눔(Silybum marianum)에서 추출한 플라보놀리그난인 실리비닌은 생쥐의 MPTP 유도 PD 모델에 대한 생체 내 실험에서 미토콘드리아 막 전위(MMP)에 대한 조절 역할을 보여주었습니다[47]. 실리비닌의 신경 보호 메커니즘에는 미토콘드리아 손상 감소 및 산화 방어 시스템 강화가 포함됩니다. 도파민성 신경 보호는 손상된 미토콘드리아의 해로운 결과를 제거하는 미토파지를 자극함으로써 달성됩니다. 이러한 데이터는 실리비닌이 PD의 치료 옵션으로 추가로 탐색될 가능성이 있음을 암시합니다[48]. 다른 연구에서 실리비닌은 MPTP에 의해 유발된 운동 장애와 도파민성 신경 변성을 유의하게 감소시켰습니다. 이 연구 결과는 실리비닌이 미토콘드리아 막 전위의 안정성을 증가시켜 달성한 PD의 MPTP 유도 모델에서 이러한 이점이 있음을 시사합니다[49]. 리그난 계열의 또 다른 구성원인 schisandrin은 ROS 수준을 낮추고 Ca2 plus의 영향을 줄이며 미토콘드리아 막 투과 능력을 회복했습니다[25].
플라바논인 나린제닌은 뉴런에서 조절 효과를 보여 미토콘드리아의 기능을 완화시켰다. 이 효과는 Sprague Dawley 쥐의 뇌 뉴런에 대한 시험관 내 실험에서 Nrf2/ARE 경로에 영향을 주어 MMP를 증가시키고 ROS를 감소시킴으로써 발휘되었습니다. 또한, 나린제닌은 Nrf2/GSH 경로를 통해 인간 신경모세포종 SH-SY5Y 세포에서 메틸글리옥살로 인한 미토콘드리아 관련 생체 에너지 및 산화 환원 기능 장애를 억제했습니다[51]. 글리코실화된 나린제닌인 Naringin은 동물 모델에서 PD를 방어하는 것으로 나타났습니다. 쥐의 선조체 및 흑색질 콤팩트(SNpc)에서 나린진은 로테논 유도 도파민성 독성을 감소시켰습니다. 세포 내인 naringin은 Nrf{9}}매개 경로를 통해 동물의 SNpc에서 미토콘드리아 기능, 안정성 및 생체 에너지의 로테논 유도 감소를 감소시켰습니다[52].
Isoliquiritigenin은 Glycyrrhizae uralensis에서 얻은 chalcone fflavonoid입니다. Isoliquiritigenin 전처리는 ROS의 생성과 MMP의 소산 및 세포질 내 cytochrome c의 존재를 완전히 억제했습니다[53]. 감초의 이소리퀴리티게닌과 같은 Nrf2/ARE 경로의 유도제는 산화 스트레스 및 신경퇴행성 질환 모델에서 미토콘드리아 기능의 잠재적 보존을 보여주었고 노화 관련 신경퇴행성 장애, 특히 PD를 예방하고 치료하기 위한 독특한 전략을 제공했습니다 [23] .

ellagic acid 및 ferulic acid를 포함한 페놀의 하위 집합인 페놀산은 미토콘드리아에 영향을 미치고 ROS 관련 경로로부터 보호합니다. Protocatechuic aldehyde는 Salvia miltiorrhiza의 뿌리에서 얻은 또 다른 페놀산으로, 시험관 내 실험에서 평가된 MPP와 배양된 SH-SY5Y 세포에서 ROS 생성을 차단하고 complex I의 활성을 유지하여 미토콘드리아에 보호 효과가 있습니다[15] . 이 계통에서 차, 와인, 커피 등에서 얻은 또 다른 페놀산인 카페인산은 ROS 생성을 차단하고 6-OHDA로 유도된 PD의 SH-SY5Y 세포 모델에서 미토콘드리아의 활성을 정상화했습니다. [54]. PD의 MPTP 동물 모델에서 caffeic acid phenethyl ester는 도파민성 신경변성과 도파민 손실을 감소시켰다. 또한, 시험관 내에서 MPP 플러스로 유도된 신경독성을 감소시켰고 MPP 플러스로 유도된 미토콘드리아 시토크롬 c 및 세포자멸사를 효과적으로 방지했습니다. 결과적으로 카페인산은 PD의 진행을 지연시키거나 멈추는 데 도움이 될 수 있습니다[55].
버진 올리브 오일에 함유된 주요 항산화제는 페놀릭 제품이며, 양적으로는 세코이리도이드 계열이 올리브 오일에 가장 풍부합니다[6]. 올류로핀(Oleuropein)과 리그스트로사이드(ligstroside)는 올리브 오일에서 발견되는 두 가지 주요 세코이리도이드이며 히드록시티로솔과 티로솔에 대해 생산할 수 있습니다. Oleuropein은 미토콘드리아에서 슈퍼옥사이드 음이온의 비율을 감소시켰습니다[56]. 생쥐의 용해된 뇌 세포에서 히드록시티로솔은 미토콘드리아 막 전위 탈분극을 방지하고 미토콘드리아 복합체 I, II 및 IV의 기능을 감소시켰습니다. Tyrosol은 도파민성 뉴런에서 MPP 플러스에 대한 방어 기능을 보였다[6]. 이에 따라 녹차와 홍차 폴리페놀은 뇌에 있는 미토콘드리아의 막 조각에 대해 믿을 수 없을 정도로 강력한 항산화 라디칼 소거 효과를 가지고 있습니다[18]. 차 폴리페놀은 DA 관련 손상을 극적으로 억제하고, DA 산화를 억제하고, DA 퀴논과 결합하고, ROS를 소거하고, 항산화 신호 경로 Nrf{6}}Keap1 및 PGC를 조절하여 도파민 뉴런을 보존할 수 있습니다.{8}} [57 ]. Nrf2의 조절에 따라 프로폴리스의 플라보노이드인 pinocembrin은 ERK1/2와 Nrf2의 감쇠를 억제하여 미토콘드리아와 세포의 안전성을 제공합니다[58].
Curcuma longa에서 얻은 폴리페놀인 Curcumin은 in vivo 및 in vitro 실험에서 MPP plus 및 ROS 생성의 활성을 차단하고 PD에서 미토콘드리아 막 손상을 방지하여 PD의 미토콘드리아 기능을 보호했습니다[18,19 ,34]. 정확한 메커니즘을 표적으로 하는 페놀성 알데히드인 바닐린은 SH-SY5Y 세포에서 로테논 유도 ROS 생성과 미토콘드리아 기능 장애를 감소시켰습니다[54]. 또 다른 페놀 화합물로 들깨의 익은 종자에서 얻은 루테올린도 ROS 생성을 예방하는 역할을 하고 미토콘드리아의 활성을 정상 수준으로 유지했습니다[46,60]. 또 다른 페놀 화합물인 에피갈로카테킨 갈레이트(Epigallocatechin Gallate, EGCG)는 녹차에서 얻은 카테킨의 일종으로 AMPK(AMP-activated protein kinase) 경로의 자극을 통해 미토콘드리아 기능 장애를 억제했습니다[61].
감귤류에서 자주 관찰되는 플라보노이드 배당체인 헤스페리딘은 생쥐에 대한 생체 내 실험에서 미토콘드리아 복합체 I, IV, V를 조절하여 미토콘드리아에 대한 보호 효과를 나타냈습니다[62]. 플라보노이드/페놀 화합물의 화학 구조는 그림 2에 나와 있습니다.

따라서 여러 연구에서는 플라보노이드와 페놀 화합물이 MMP, ROS, Nrf2/ARE, NO, JNK, p38MAPK, Bcl을 포함한 미토콘드리아 및 관련 세포자살/산화 매개체를 표적으로 하여 PD의 예방/치료에 유용할 수 있다고 주장했습니다.{2} }/Bax 비율, PI3K/Akt, 핵인자 카파-B(NF-κB), PGC-1 및 복합체 I, II 및 IV의 활성.
4.2. PD의 알칼로이드와 미토콘드리아
알칼로이드는 질소 원자를 포함하는 1차 파이토케미컬이며, 일반적으로 순환 시스템의 일부로 또는 조합되어 있습니다. 이 종류의 파이토케미컬은 다양한 질병, 특히 PD[63,64]에서 인간 생활의 사회 생활, 경제적 지위 및 건강 측면에 영향을 미칩니다. 니코틴은 Nicotiana tabacum 뿌리와 잎에서 발견되는 자연 발생 알칼로이드입니다. 또한 감자, 토마토, 가지, 고추와 같은 가지과의 다양한 종류의 소량에도 주로 존재합니다. 니코틴은 NADH에서 복합체 I로의 ETC를 억제하고 NADH-유비퀴논 환원효소의 작용을 차단하여 미토콘드리아에 의한 산소 섭취량을 측정 가능한 수준으로 감소시킵니다. 복합 I을 억제함으로써 니코틴은 전자 고갈을 줄이고 결과적으로 ROS 생성을 줄였습니다[65]. 또 다른 연구에서 니코틴은 미토콘드리아 세포자살 경로를 방해하고 산화 스트레스로 인한 세포자멸사로부터 뉴런을 보호합니다[32]. Xie et al.이 제공한 바와 같이 니코틴은 파킨슨병 발병 가능성을 낮추는 것과 관련이 있습니다. 니코틴은 MPP 플러스 및 칼슘 유도 미토콘드리아 고진폭 부종 및 SH-SY5Y 세포의 온전한 미토콘드리아로부터의 시토크롬 c 방출을 억제했습니다. 그들의 결과는 니코틴이 PD 동안 MPP plus, 칼슘 유도 미토콘드리아 및 시토크롬 c를 약화시킴으로써 수용체 독립적인 신경 보호 효과를 나타냈다는 것을 나타냅니다[66]. 또 다른 보고서는 니코틴이 미토콘드리아 역학을 매개하고 미세소관으로부터 미토콘드리아 결합에 영향을 미치고 IP3 수용체 클러스터링을 크게 증가시키고 미토콘드리아-소포체 통신을 조절하며 배양된 해마 뉴런에서 미토콘드리아 생물 발생을 증가시킨다는 것을 보여주었습니다[67]. 니코틴은 또한 생체 내 및 시험관 내에서 소량으로 미토콘드리아에 영향을 미쳐 쥐의 CNS에서 미토콘드리아 기능을 유지하는 것으로 나타났습니다[68]. 이러한 발견에 따르면 니코틴은 7개의 니코틴성 아세틸콜린 수용체(7-nAChR)를 자극하여 미토콘드리아 경로를 통해 H2O{17}}유도 성상교세포의 세포자멸사를 억제했으며, 면역학적 반응과 연결된 성상세포는 PD와 관련이 있습니다. 또한 성상교세포에서 발현되는 {{20}nAChR의 능력을 고려할 때 신경퇴행성 질환에 대한 잠재적인 치료적 접근이 될 수 있습니다[69].
카페인(1,3,{2}}트리메틸 크산틴)은 커피, 차, 코코아 식물에서 발견되는 자연 발생 알칼로이드입니다[70]. 카페인은 ROS 생성을 차단하고 미토콘드리아의 활동을 향상시킬 수 있습니다. 또한 미토콘드리아 생합성과 관련된 Nrf{4}}keap1 및 PGC{6}}를 자극하고 항산화 및 항염 기전을 상호 연결하여 미토콘드리아 형성을 증가시킵니다. 또한 카페인은 세포 사멸, 세포 주기 조절, 산화 스트레스, 미토콘드리아 기능 관련 유전자 발현과 같은 다양한 활동에 관여하는 전사 유전자를 회복시킨다[70].
Berberine은 다양한 약용 식물, 특히 Berberis 속에 속하는 식물에서 발견되는 이소퀴놀린 알칼로이드입니다. PD의 동물 모델에서 베르베린은 신경 보호 특성을 갖는 것으로 나타났습니다. 이를 위해 연구자들은 PD의 세포 모델과 형광 표지된 베르베린 유도체를 사용하는 제브라피쉬 PD 모델에서 베르베린의 세포내 국소화 및 혈액뇌장벽(BBB) 투과성을 조사했습니다[72,73]. 그들의 연구에서 베르베린의 유도체는 BBB를 쉽게 통과하여 항PD 작용을 나타냈습니다. 또한 세포 내 국소화 분석에 따르면 PC12 세포의 미토콘드리아에 빠르고 정확하게 축적되었습니다. 또한 6-OHDA로 인한 세포 사멸을 방지하고 MPTP로 인한 PD 유사 행동을 완화하며 PD에 영향을 받는 zebrafish의 뇌에서 도파민성 뉴런 손실을 증가시킵니다[72].
Embelin은 Lysimachia punctata(Primulaceae)와 Embelia ribes Burm(Myrsinaceae)의 열매에서 발견되는 천연 식물 제품입니다[74]. 이 발견은 MPP 플러스 유도 산화 스트레스 및 세포 사멸로부터 보존된 N27 도파민성 세포를 시작한다는 것을 입증합니다. Embelin 처리된 세포는 더 높은 수준의 pAMPK, SIRT1 및 PGC1을 나타내어 개선된 미토콘드리아 생물 생성을 나타냅니다. 또한 엠블린은 MPTP에 의해 유도된 선조체 도파민 및 미토콘드리아 생합성 경로의 감소에 대한 생체 내 보호를 제공했습니다[75].
Isorhynchophylline은 신경 장애를 완화하기 위해 동아시아에서 여러 세대에 걸쳐 사용되는 중국 약초 치료제 Uncaria rhynchophylla에서 확인된 중요한 4환식 oxindole 알칼로이드입니다[76]. 이 연구는 이소린코필린이 PC12 세포에서 MPP+유도 세포자멸사 세포사를 상당히 감소시켰고 MPP+유도 소포체 스트레스 반응을 크게 감소시켰으며, 이 둘은 PD의 도파민성 신경세포 사멸과 관련이 있음을 발견했습니다[77]. 또 다른 연구에서 Herba Leonuri(중국 전통 의학)에서 얻은 독특한 알칼로이드 레오닌은 PD의 미토콘드리아에 보호 효과가 있고 산화 스트레스를 차단하는 것으로 나타났습니다[78].
앞서 언급한 연구는 PD를 예방하고 치료하기 위해 미토콘드리아를 표적으로 하는 알칼로이드의 가능한 적용을 암시합니다. 따라서 알칼로이드는 ROS, Nrf{0}}keap1, PGC-1 , pAMPK, 7-nAChR 및 SIRT1을 비롯한 여러 신호/매개체를 조절합니다.
4.3. PD의 테르펜과 미토콘드리아
테르펜은 미토콘드리아 관련 경로를 조절하여 신경 보호 효과를 갖는 식물 2차 대사 산물입니다. 테르펜/테르페노이드는 이소프렌 단위 또는 변형된 구조로 만들어집니다. 분자 구조의 이소프렌 단위 수에 따라 테르펜/테르페노이드는 모노테르펜, 세스퀴테르펜, 디테르펜, 트리테르펜 및 테트라테르펜으로 분류됩니다[79].
카로티노이드는 식물의 광합성 색소에 풍부하며 분자 구성은 테트라테르펜({0}이소프렌 중합체)입니다. 천연 카로티노이드인 리코펜은 Bax를 억제하면서 미토콘드리아 구조막 능력과 ATP 비율을 개선하고 Bcl{1}} 수치의 관련 감소는 신경 세포의 염증 및 산화 스트레스에 대한 보호를 제공했습니다[32]. 또 다른 연구에서 리코펜 치료는 미토콘드리아의 탈분극과 뉴런의 시토크롬 c 방출을 감소시켜 미토콘드리아 막의 완전성이 보존되었음을 시사합니다[80]. 또한, 리코펜은 MPP 플러스로 유도된 미토콘드리아 ROS 생성과 미토콘드리아 형태학적 변화를 감소시켰습니다. 그들의 연구에서 리코펜은 MPP 플러스로 유도된 미토콘드리아 투과성 전환(MPT) 기공의 개방을 억제했습니다. MPP와 함께 유도된 세포독성에 대한 리코펜의 예방적 이점은 미토콘드리아 활성 강화에 관여하기 때문일 수 있습니다. 이러한 발견은 리코펜이 PD에 대한 유용한 치료적 접근이 될 수 있음을 의미합니다[81].
Kaur et al. 또한 라이코펜은 미토콘드리아에서 시토크롬 c의 방출을 억제한다고 보고했습니다. 이 발견은 산화 스트레스를 조절함으로써 신경퇴행성 질환에 유익한 효과를 보인 로테논 유도 PD에서 리코펜 보충제의 치료 가능성을 뒷받침합니다[82]. 미세조류 Haematococcus Pluvialis의 케토 구조 카로티노이드인 Astaxanthin은 생체 내 및 시험관 내 실험에서 미토콘드리아 기능 장애를 예방하고 ROS 생성을 조절했습니다[83]. docosahexaenoic acid-acylated astaxanthin ester는 MPTP로 유도된 마우스 모델에서 PD의 진행을 실질적으로 억제했습니다. JNK 및 p38MAPK 경로뿐만 아니라 미토콘드리아 매개 경로를 통해 뇌에서 도파민성 신경 세포 사멸을 조절하는 잠재적인 역할을 보여주었다[84].
SH-SY5Y 세포에서 Asiatic acid라고 하는 5환 트리테르페노이드는 H2O2 또는 로테논으로 인한 세포 손상 및 미토콘드리아 기능 장애를 방어합니다. 전압 의존적 음이온 채널 및 미토콘드리아 막 전위 분산의 로테논 유도 증가는 아시아산에 의해 차단되었습니다. 또한, 미토콘드리아 막의 안정성을 위해 Asiatic acid는 Bax 생성을 감소시키고 Bcl-xL 수준을 증가시켰다[85]. 로테논 유도 세포 모델에서 아시아산은 산화적 손상과 세포자멸사로부터 미토콘드리아를 구출했습니다. 아시아산은 또한 분리된 미토콘드리아 모델에서 MMP를 증가시켜 막 무결성과 ATP 생성을 보존했습니다. 연구 결과는 미토콘드리아가 파킨슨병에 필수적이며 아시아산은 파킨슨병 예방 및 치료를 위한 유망한 옵션임을 보여줍니다[86].
디테르페노이드 락톤인 Andrographolide는 생체 내 및 시험관 내 모델 모두에서 ATP 수준의 균형을 유지하여 ROS 생성을 차단하고 미토콘드리아 기능 장애를 조절함으로써 미토콘드리아에 대한 보호 효과를 보여주었습니다. Andrographolide는 또한 파킨 의존성 경로를 통해 탈분극된 미토콘드리아의 삭제를 향상시켰습니다[87]. MPTP에 노출된 쥐에서 안드로그라폴라이드 치료는 행동 장애를 완화하고 도파민성 신경 세포 손실을 줄였으며 시험관 내에서 로테논으로 인한 세포 사멸을 감소시켰습니다. PD 동안, andrographolide는 과도한 미토콘드리아 분열과 신경 손상을 방지했습니다[88].
로즈마리의 디테르펜인 카르노식산은 미토콘드리아 융합 단백질인 미토푸신 1 및 2(MFN1 및 MFN2) 및 시신경 위축 1(OPA1)을 자극했습니다. 또한 핵분열 단백질 다이너민 관련 단백질 1(DRP1)을 차단했습니다. 또한 파킨은 IKK/NF-κB 경로를 활성화하고 carnosic acid에 의한 OPA1 단백질 생산을 증가시켰습니다[89]. 이 라인에서 carnosic acid는 PD의 paraquat 모델이 미토콘드리아 활동에 미치는 부정적인 영향을 줄이면서 ROS/반응성 질소 종(RNS) 생성을 줄였습니다. 결과적으로 carnosic acid는 PI3K/Akt 경로를 조절하여 SH-SY5Y 세포에서 Nrf2를 자극하여 더 높은 항산화 효소를 생성합니다[90]. 6-OHDA 처리 후 MMP가 교란되었고 전압 의존성 음이온 채널 1(VDAC1) 단백질이 차단되었으며 세포질 시토크롬 c가 SH-SY5Y 세포에서 증가했습니다. 그러나 carnosic acid는 그러한 효과를 방지했습니다. PINK1/파킨 매개 미토파지를 자극함으로써 carnosic acid는 6-OHDA의 신경독성을 완화시키는 것으로 보입니다[91]. 결과적으로 carnosic acid는 미토콘드리아 관련 경로를 통해 PD를 치료하기 위한 신경 보호 약물로 간주될 수 있습니다.
Boswellia 속의 pentacyclic triterpenes 그룹인 Boswellic acid는 인터루킨(IL)-6/신호 변환기 및 전사 활성제-3를 억제하여 로테논 유발 미토콘드리아 기능 장애를 줄이는 것으로 나타났습니다 )/NF-κB 신호 전달 경로 [92]. Torment acid는 Rosa rugosa 및 Potentilla Chinensis를 포함한 약용 식물에서 발견되는 트리테르펜으로 SH-SY5Y 세포에서 MPP 플러스에 의해 유도된 ROS의 세포내 응집 및 Bax/Bcl{6}} 비율을 현저하게 억제합니다. 이 효과는 주로 PI3K/Akt/GSK{10}} 신호 전달 경로의 자극을 통해 발휘되었습니다. 그들의 결과는 torments acid가 PD의 예방 및 치료에 관한 더 많은 전임상 연구를 위한 가능한 경쟁자가 될 수 있음을 보여줍니다[93].
Rehmannia glutinosa Libosch의 뿌리에서 추출한 iridoid glucoside인 Catalpol은 ATP 생성을 감소시키고 MPP 플러스 수준을 향상시켜 미토콘드리아 기능 장애를 줄였습니다. 또한 신경 세포의 칼슘 입력, ROS 축적 및 MPT 공극을 감소시켰습니다[94,95].
다른 테르페노이드 중 인삼의 효능에 주도적인 역할을 하는 트리테르페노이드인 ginsenosides-Rg1은 생체 내 실험에서 미토콘드리아 기능 장애에 대한 산화 스트레스 예방 효과가 있을 수 있다[96,97]. Panax 종(Araliaceae)의 뿌리인 인삼은 중국의 전통 약재이자 현대에 널리 사용되는 천연 약재입니다. 진세노사이드는 인삼의 주요 약리 활성 성분으로 대부분의 인삼 작용과 관련이 있다[98]. Ginsenosides-Rg1(G-Rg1)은 시험관 내 및 생체 내 독성이 낮으면서 치료 효과가 있는 것으로 나타났습니다. 또한 다양한 신경 장애, 특히 PD와 같은 진행성 신경퇴행성 질환에 도움이 됩니다. ginsenosides-Rg1의 이러한 효과에는 항염증, 항산화 및 항세포사멸 역할의 강화가 포함됩니다. 그것은 또한 흥분 독성과 Ca2 플러스 뉴런으로의 과잉 유입을 억제하고 세포 ATP 농도를 유지하며 뉴런 구조적 완전성을 보호할 수 있는 가능성을 보여주었습니다. 반응성이 높은 철 농도에 의해 생성된 과도한 과산화수소 및 기타 ROS는 미토콘드리아 기능 장애 및 도파민 대사 향상을 초래할 수 있습니다. Ginsenosides-Rg1(G-Rg1)은 MPTP 처리 생쥐의 SN에서 철 염색 세포의 수를 감소시켰다[96]. 또한 진세노사이드 Rb1(10M)은 MMP를 회복하고 Ca2와 미토콘드리아로의 과잉 유입을 줄여 대조군에 비해 세포 생존을 상당히 향상시켜 1차 배양된 도파민성 마우스 뉴런에서 미토콘드리아에 의해 생성된 에너지를 증가시키는 것으로 밝혀졌습니다. 또한, 진세노사이드 Re는 최적의 NO 신호 전달의 복원을 통해 샤페론 LRPPRC, Hsp90 및 Hsp60의 발현 수준을 증가시켜 PINK null 도파민성 세포주의 특정 미토콘드리아 복합체 IV 결핍을 복구하고 상쇄하는 것으로 밝혀졌습니다. P. notoginseng에서 분리한 notoginsenoside인 Notoginsenoside R2(NGR2)는 MEK1/2–ERK1/2 경로를 통해 SH-SY5Y 세포에서 미토콘드리아 사멸을 감소시키고 6-OHDA 유발 산화 스트레스를 억제합니다. P. 인삼 뿌리의 물 추출물은 또한 감소된 Bax/Bcl-2 비율인 시토크롬에서 알 수 있듯이 ROS 과잉 합성을 감소시키고 미토콘드리아 의존적 세포자멸사 경로를 억제하여 MPP와 SH-SY5Y 세포의 세포 사멸을 억제했습니다. c 릴리스 및 caspase{45}} 활동 [100]. 알칼로이드/테르페노이드의 화학 구조는 그림 3에 나와 있습니다.

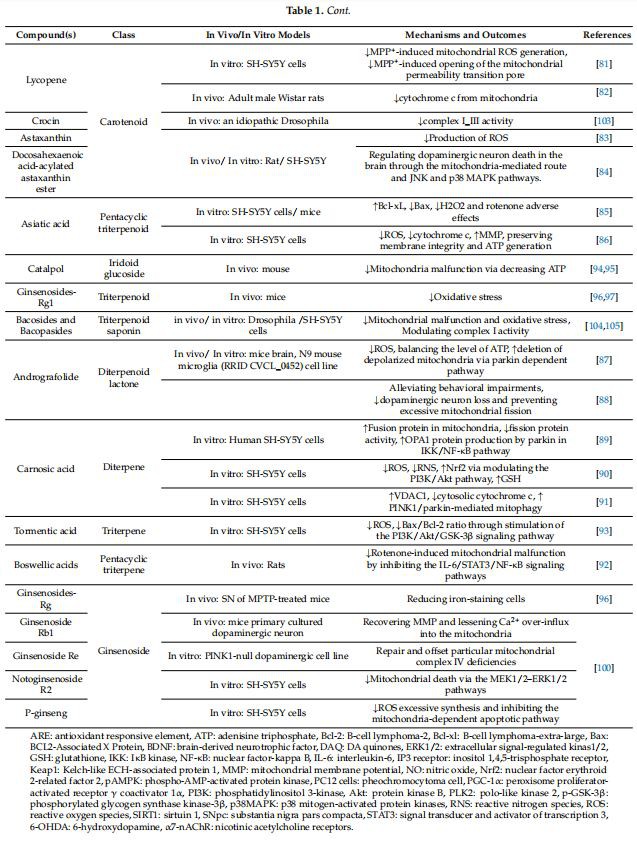
전체적으로 테르펜/테르페노이드는 미토콘드리아를 표적으로 하여 상서로운 항PD 효과를 나타내어 복잡한 I–III 활성, PINK1/파킨, ROS, Bax, JNK/p38MAPK, IKK/NF-κB, VDAC1, PI3K/Akt/GSK를 억제합니다{{ 6}} 및 IL-6/STAT3/NF-κB. 표 1은 PD 예방/치료에 대한 미토콘드리아 및 상호 연결된 매개체에 대한 식물 2차 대사 산물의 조절 효과를 보여줍니다.


5. 결론
미토콘드리아는 여러 신경퇴행성 질환, 특히 PD와 싸우는 유망한 표적입니다. 미토콘드리아의 복합체/효소 및 상호 연결된 산화/세포자멸 매개체가 PD에서 중요한 역할을 하기 때문에 이 질병에 대한 다중 표적 요법을 제공하면 유망한 치료법을 찾는 새로운 길을 열 수 있습니다. 식물 이차 대사 산물은 항염증, 항 세포 사멸 및 항산화 효과를 사용하여 신경 퇴행과 싸우는 다중 표적 제제입니다. 미토콘드리아와 상호 연결된 매개체를 동시에 표적화하는 식물화학물질의 잠재력은 PD 치료의 길을 열 수 있습니다. 이 라인에서 복합체 IV, MIMP의 활성. PINK1/파킨, ROS. 아니요 Bc-2/Bax 비율, PGC-1, pAMPK, -nAChRs 및 SIRT1, Nrf2/ARE, INK/p38MAPK, IKK/NF-KB, PI3K/Akt/GSK-3 , VDACl 및 STAT3/NF-kB는 PD의 치료/예방을 향해 미토콘드리아를 통과하는 식물화학물질에 의해 조절됩니다(그림 4).

그들의 효과에도 불구하고, 파이토케미칼은 낮은 생체이용률, 불안정성/용해성/선택성, 빠른 대사, 그리고 PD에서의 혈장 농도 및 치료 적용을 제한하는 제거로 고통받습니다. 따라서 파이토케미칼에 대한 적절한 전달 시스템(예: 나노입자, 미셀, 리포솜 및 고체-지질 나노입자)에 대한 조사는 신경보호 식물의 세포 흡수, 생체이용률, 효능 및 특이성을 증가시켜 PD 퇴치에 대한 응용 프로그램의 한계에 대응할 수 있습니다. 파생된 이차 대사 산물 [79].
그림 4. 파이토케미컬은 미토콘드리아를 통과하는 PD의 치료에 여러 메커니즘을 사용합니다. 그들의 효과에도 불구하고, 파이토케미칼은 낮은 생체이용률, 불안정성/용해성/선택성, 빠른 대사, 그리고 PD에서의 혈장 농도 및 치료 적용을 제한하는 제거로 고통받습니다. 따라서 파이토케미칼에 대한 적절한 전달 시스템(예: 나노입자, 미셀, 리포솜 및 고체-지질 나노입자)에 대한 조사는 신경보호 식물 유래의 세포 흡수, 생체이용률, 효능 및 특이성을 증가시켜 PD 퇴치에서의 응용 프로그램의 한계를 상쇄할 수 있습니다. 이차 대사 산물 [79]. 현재의 연구는 미토콘드리아 관련 경로를 통과하는 PD와 싸우는 데 있어 페놀성 화합물, 알칼로이드, 테르페노이드 및 기타 식물화학물질의 잠재력을 강조합니다. 향후 보고서에는 파킨슨병에서 미토콘드리아의 중요한 표적화를 밝히기 위한 추가적인 전임상 연구와 파이토케미컬을 효과적인 치료법으로 평가하기 위한 잘 통제된 임상 시험이 포함되어야 합니다. 또한 PD의 전임상 및 임상 징후에서 미토콘드리아의 직접적인 역할과 식물 이차 대사 산물의 유익한 효과를 밝히는 것이 매우 중요할 것입니다. 이러한 보고서는 PD의 예방, 관리 및 치료에 있어 파이토케미칼의 잠재력을 더욱 강조할 것입니다.
