조절된 세포 사멸 및 종양 면역에서 GTPase 활성화 단백질의 역할
May 05, 2023
추상적인
GTPase-활성화 단백질(GAP)은 활성 GTPase-GTP 형태의 GTPase-GDP 형태로의 전환을 촉진하는 것으로 생각되는 GTPase 단백질의 음성 조절자입니다. GTPase 단백질 및 기타 도메인을 조절하는 능력을 기반으로 GAP는 다양한 세포 요구 과정에 직간접적으로 관여합니다. 우리는 조절된 세포 사멸(RCD), 주로 아폽토시스 및 자가포식, 일부 새로운 RCD를 조절하는 GAP의 기존 증거를 질병, 특히 암과의 연관성에 특히 주의하여 검토했습니다. 우리는 또한 GAP가 종양 면역에 영향을 미칠 수 있다고 생각하고 GAP, RCD 및 종양 면역을 연결하려고 시도했습니다. 이러한 과정을 조절하기 위한 GAP에 대한 더 깊은 이해는 병리학적 세포 손실을 피하거나 암 세포 사멸을 중재하기 위한 새로운 치료 표적의 발견으로 이어질 수 있습니다.
조절 세포 사멸은 면역계에서 조절 세포 부류의 활성 사멸을 말하며, 이에 따라 면역 반응의 강도와 기간을 조절합니다. 조절세포에는 조절T세포, 조절B세포 등이 있으며 면역계의 항상성 유지에 중요한 역할을 한다. 조절 세포 사멸과 면역 사이에는 밀접한 관계가 있습니다. 조절 세포 사멸은 면역 반응의 강도와 기간, 따라서 면역 수준에 영향을 미칠 수 있습니다. 한편으로 조절된 세포 사멸은 면역 반응을 강화하고 병원균 제거를 촉진할 수 있습니다. 한편, 과도한 조절 세포 사멸은 면역력을 약화시켜 감염 및 자가 면역 질환에 대한 감수성을 유발할 수 있습니다. 요약하면 조절 세포 사멸은 면역과 밀접한 관련이 있습니다. 적절한 조절 세포 사멸은 면역 반응을 강화하고 병원체 제거를 촉진할 수 있지만 과도한 조절 세포 사멸은 면역을 약화시켜 신체가 감염에 취약해지고 자가 면역 질환이 발생할 수 있습니다. 따라서 면역력 향상에 세심한 주의를 기울여야 합니다. Cistanche는 면역력을 향상시킬 수 있습니다. Cistanche는 비타민 C, 비타민 C, 카로티노이드 등과 같은 다양한 항산화 물질이 풍부합니다. 이러한 성분은 자유 라디칼을 제거하고 산화 스트레스를 줄이며 면역력을 향상시킬 수 있습니다. 면역 체계 저항.

키워드:
GTPase-활성화 단백질, 조절된 세포 사멸, 종양 면역.
소개
작은 구아노신 트리포스파타아제(작은 GTPases)의 인간 Ras 슈퍼패밀리(모노머 GTPases)는 150개 이상의 구성원으로 구성되며[1] 일반적으로 Ras, Rho, Rab, Arf 및 Ran 패밀리의 5가지 주요 패밀리로 나뉩니다[2]. 그들은 신호 전송, 물질 수송 및 세포질 골격의 구성을 포함한 다양한 세포 과정과 관련이 있습니다[3]. 작은 GTPase는 두 가지 다른 형태 상태를 가지며 이들 사이에서 앞뒤로 순환합니다.
활성화된 상태에서는 GTP에 구속되며 GDP의 경우 그 반대입니다. 이 상태 전이는 구아닌 뉴클레오타이드 교환 인자(GEF), 구아닌 뉴클레오타이드 해리 억제제(GDI) 및 GTPase 활성화 단백질(GAP)의 세 가지 조절자에 의해 관리됩니다[4]. 이 중 GEF는 GTP와의 결합을 촉진하여 GTPase를 활성화시키는 양성 인자이고, GDI와 GAP는 각각 GTP를 격리시키고 가수분해하여 GTPase를 비활성화시키는 음성 인자이다[3, 4].
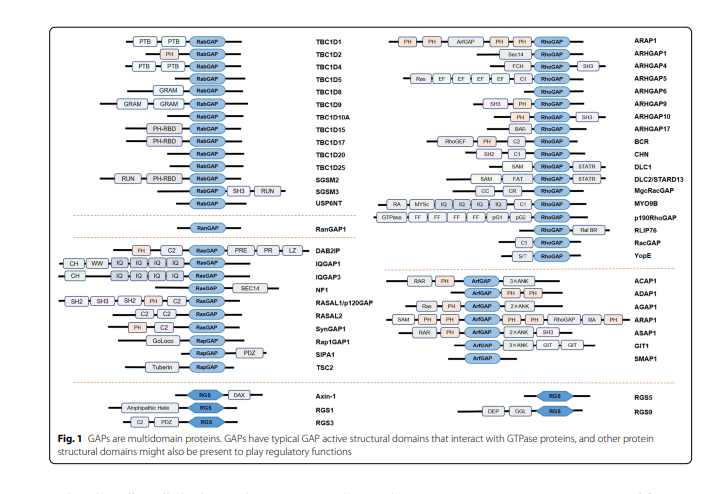
GAP는 크기가 50~250kDa인 다중 구조 도메인 단백질(그림 1)입니다[5]. GTPases의 Ras 수퍼패밀리에 해당하는 GAP는 Ras-GAPs, RhoGAPs, Rab-GAPs, Arf-GAPs 및 Ran-GAPs 패밀리의 5가지 주요 패밀리로 나눌 수도 있습니다. Ras 수퍼패밀리의 GAP와 달리 G 단백질 신호 조절자(RGS)라고 불리는 GAP 클래스는 이종삼량체 G 단백질에 작용합니다[5, 6]. 일단 GDP 결합 구조에 들어가면 GAP는 일반적으로 GTP를 가수분해하여 해당 다운스트림 신호 캐스케이드를 종료할 수 있습니다. GTP 가수분해 반응은 매우 느리지만 GAP는 가수분해 속도를 높이기 위해 분해 단계를 몇 배나 촉진할 수 있습니다. RasGTP 가수분해 동안 전통적인 GAP는 아르기닌 손가락 또는 아스파라긴 엄지손가락을 표적 GTPase의 뉴클레오티드 결합 홈에 삽입하여 가수분해를 자극합니다[7, 8]. 반면 RGS 단백질은 G 단백질 결합 수용체의 활성 G 서브유닛에 직접 결합합니다. (GPCR)을 사용하여 가수분해를 유도합니다[6].
생리학적으로 세포 사멸은 조직과 기관의 기능과 크기를 조절하고 유지하는 항상성 메커니즘입니다. 우발적 세포 사멸(ACD)과는 현저하게 다른 외부 환경 교란의 결과인 조절된 세포 사멸(RCD)은 유전적으로 간섭될 수 있는 내인성 유전적으로 암호화된 분자 구조 신호 캐스케이드 및 메커니즘을 활성화하는 생리학적 또는 병리학적 골칫거리에 필요합니다. 나 약리학 . RCD는 세포사멸과 비세포사멸의 두 가지 마스터 유형으로 분류할 수 있습니다. Apoptosis는 프로그램화된 세포 사멸(PCD)의 가장 흔한 형태이며, necroptosis, autophagy, mitotic catastrophe, pyroptosis, ferroptosis, methuosis, proptosis, parthanatos, lysosome-dependent cell death, entosis, oncosis도 주목을 받고 있다[9, 10].
이러한 다양한 유형의 세포 사멸은 형태학적 변화와 사멸 자극으로 인한 생화학적 특징에 의해 구별되지만 일부 형태의 세포 사멸은 세포 사멸 및 자가포식 세포 사멸과 같은 분자 특성의 특정 교차점을 통해 다른 세포 사멸과 완전히 독립적이지 않습니다[11 ]. 정상적인 세포 사멸의 규칙에 관계없이 암 세포는 대체로 RCD를 우회하기 위해 세포 사멸 신호의 전달에 영향을 미치는 관련 유전적 돌연변이 또는 후생유전적 변형을 생성함으로써 생존합니다.
GAP에 의한 GTPase 활동의 조절은 일련의 신호 변화, 특히 세포 성장, 증식 및 사망을 유발하며, 우리는 RCD 및 종양 면역 측면에서 관찰할 수 있는 것을 구성하여 이 세 가지 사이의 연결을 탐색했습니다. 이 검토에서는 먼저 다양한 RCD에 대한 GAP의 분자 메커니즘에 대한 이해를 논의하고 많은 개별 사례(표 1)를 설명하고 마지막으로 GAP에 의한 종양 면역 조절에 중점을 둘 것입니다. . 이 지식을 요약함으로써 우리는 이러한 과정의 GAP 조절의 병태생리학적 의미에 대해 더 자세히 설명하고 이러한 새로운 발견에 비추어 유망한 암 치료 접근법을 강조할 것입니다.

아폽토시스
Apoptosis는 PCD의 한 형태이며 염색질 응축 및 세포 수축(pyknosis)의 형태학적 특성 때문에 '수축 괴사'라고도 합니다[12]. 또한 그 특징에는 DNA 단편화(karyorrhexis), apoptosome 형성 및 막 수포가 포함됩니다[9]. 두 가지 일반적인 신호 경로는 세포 사멸을 유도합니다. 하나의 경로는 미토콘드리아 막 전위 및 외막 투과성의 변화로 인한 내인성 경로이며, 이후 시토크롬 c와 같은 미토콘드리아 단백질의 방출을 촉진하여 caspase 3를 활성화하고 apoptosome을 형성합니다[13 ]. 이 과정은 주로 proapoptotic 단백질(BAX, BAK, BIM, PUMA 및 BID) 및 antiapoptotic 단백질(BCL-2, BCL-XL 및 MCL1)인 BCL-2 계열의 단백질에 의해 조절됩니다. 14]. 다른 경로는 Fas, 종양 괴사 인자(TNF) 수용체 및 TNF 관련 세포 사멸 유도 리간드와 같은 사망 유도 신호 복합체(DISC) 및 사망 수용체(세포막 단백질)에 의해 개시되는 외인성 세포 사멸 경로입니다. (TRAIL) 수용체는 궁극적으로 세포 사멸의 실행자인 caspase protease 계열을 활성화하고 세포 사멸을 유도합니다[13, 15].
세포사멸 장애는 자가면역질환, 신경퇴행성 질환 및 종양의 발생 및 발달과 밀접한 관련이 있습니다. 예를 들어, 암세포는 종종 세포사멸을 억제하여 무제한적인 증식을 보장하는 특성을 가지고 있습니다.
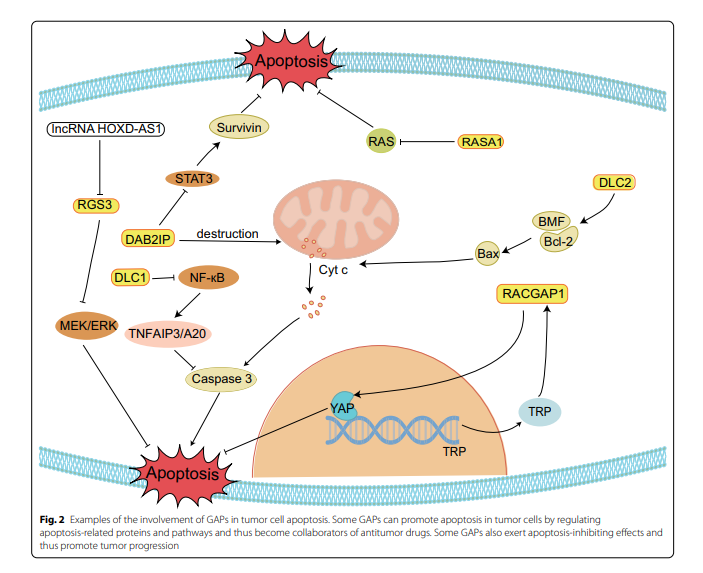
신흥 연구에 따르면 GAP는 세포 사멸 진행과 밀접한 관련이 있습니다 (그림 2). 일부 GAP는 유기체를 보호하기 위해 종양 세포의 세포사멸을 촉진할 수 있습니다. p120RasGAP, 간암 1(DLC1)에서 결실된 G-단백질 신호 3(RGS3)의 조절인자, DOC-2/DAB2 상호작용 단백질(DAB2IP) 및 STARD13은 5개의 GAP가 균형에 영향을 미칠 수 있기 때문에 대표적인 예입니다. 항아폽토시스 단백질 및 프로아폽토시스 단백질 및/또는 아폽토시스를 유도하는 상응하는 신호 전달 경로. RAS의 고전적인 GAP인 p120RasGAP(RASA1이라고도 함)는 전사 조절이 억제될 때 Ras 의존성 종양 형성을 유도합니다. 간세포 암종(HCC)의 표적 제제인 소라페닙은 종양 세포의 세포사멸을 유도할 수 있습니다. 연구에 따르면 그것의 중요한 경로는 p120RasGAP의 발현과 안정성을 증가시키기 위해 뇌하수체 homeobox 1(PITX1)의 인산화를 촉진함으로써 치료 효과를 위해 p120RasGAP의 수준을 상향 조절하는 것으로 나타났습니다[16]. 그러나 성공적으로 세포사멸을 유도할 수 있는지 여부는 신호 전달 경로의 활성 정도에 달려 있습니다. Caspase-3는 p120RasGAP를 두 조각으로 절단하여 세포 사멸을 막고 세포 생존을 촉진하는 보다 약하게 활성화됩니다. 그것의 N-말단 조각은 PI3k/Akt 경로를 활성화하고 caspase의 과활성화만이 세포사멸 세포 사멸을 촉진할 것입니다[17, 18].
HCC에서 RGS3의 발현은 발암성 lncRNA HOXD-AS1에 의해 영향을 받으며, 이는 RGS3의 mRNA 수준을 감소시키고 MEK/ERK 신호 경로를 활성화하여 세포사멸을 방지합니다[19]. HOXD-AS1은 또한 ARHGAP11A(RhoGAP)의 발현을 상향 조절하고 경쟁하는 내인성 RNA(ceRNA) 역할을 하고 miR19를 억제함으로써 전이를 유도합니다[19]. HOXD-AS1과 유사하게 STARD13(DLC2, a RhoGAP) 3'UTR은 ceRNA로 작용하고 유방암에서 miR-125b와 경쟁적으로 결합하여 Bcl-2 변형 인자(BMF) 발현을 증가시킵니다.
한편, STARD13 3'UTR은 BMF/Bcl-2의 상호작용을 촉진하여 Bax와 사이토크롬 c를 방출하여 세포자살의 고유 경로를 활성화할 수 있습니다[20]. DLC1 및 DAB2IP는 해당 경로 및 표적 단백질에 직접 영향을 주어 세포 사멸을 유도합니다. 예를 들어, DLC1(RhoGAP)은 TNFAIP3/A20의 발현을 완화하고 BCL211/BIM 및 caspase-3의 발현을 상향 조절하여 혈관육종에서 NF-κB 신호를 비활성화하여 세포 사멸을 유도합니다[21]. 세포사멸 촉진에 대한 DAB2IP의 효과는 암에서 다중 신호 전달 경로를 포함합니다[22]. 전립선암(PCa)에서 DAB2IP는 세포사멸에 영향을 미치는 이중 역할을 합니다. 첫째, DAB2IP는 STAT3와 직접 상호 작용하여 인산화(티로신 705 및 세린 727) 및 전사 활성화를 억제하여 pro-apoptotic gene(Bax) 및 anti-apoptotic 유전자(surviving, Bcl-2 및 Bcl)의 균형 잡힌 발현을 방해합니다. -xL) 및 세포사멸 촉진. 둘째, DAB2IP는 미토콘드리아 막 전위의 파괴 및 사이토크롬 c, Omi/HtrA2 및 Smac의 방출을 포함하는 고유 경로를 활성화하여 궁극적으로 카스파제 캐스케이드를 활성화합니다[23].
RACGAP1은 세포사멸을 억제함으로써 암의 전이와 발달을 촉진할 수 있습니다. RACGAP1은 Rho 계열의 작은 G 단백질에 작용하여 GTP 가수분해를 자극하고 CDC42 및 RAC1을 조절합니다. RACGAP1의 발현 및 안정성은 STAT3 및 상피 세포 형질전환 서열 2(ECT2)에 의해 영향을 받습니다. HCC에서 RACGAP1의 전사 인자인 STAT3는 RACGAP1의 발현을 상향 조절할 수 있으며, 그 다음 RACGAP1은 F-액틴의 축적을 통해 Hippo 신호 전달 경로를 감소시켜 전사 보조 활성화 인자 YAP(yes-associated protein)를 활성화합니다. YAP를 사용하면 뉴클레오포린 전위 프로모터 영역(TPR)의 전사가 상향 조절됩니다. 차례로 TPR은 중앙 스핀들에서 RACGAP1의 인산화 및 국소화를 조절할 수 있습니다. 그 결과 세포사멸은 억제되고 종양 세포의 성장은 촉진된다[24]. 작은 GTPase에서 구아닌 뉴클레오티드 교환의 촉매제인 ECT2[25]는 RacGAP1과 상호 작용합니다. HCC에서 한편으로 ECT2는 RacGAP1 단백질 안정성을 촉진하고 다른 한편으로 RacGAP1은 ECT2-매개 RhoA 활성화 및 HCC 세포 전이를 촉진합니다[26]. 기저 유사 유방암(BLBC)에서 녹다운 RACGAP1 세포는 또한 세포질분열에 실패하고 세포사멸의 개시를 유발하는 것으로 나타났습니다[27].
확실히 GAP는 암을 제외한 다른 세포 사멸 관련 질병에서도 중요한 역할을 합니다. 시기 적절하지 않은 부적절한 세포 사멸은 심혈관 질환의 발생률을 높일 것입니다. 모세혈관 기형-동정맥 기형 환자의 70%는 RASA1 유전자에 비활성화된 돌연변이를 가지고 있습니다. RASA1의 절단된 N-말단 단편이 세포자살 억제를 매개하는 기능에 기초하여, RASA1 결핍은 림프관(LV) 내피 세포의 세포자멸사를 유발하여 좌심실 판막의 손상된 형성을 유발합니다[28].
또한 RGS5는 proapoptotic protein, antiapoptotic protein, caspase-3의 활성을 조절할 뿐만 아니라 JNK1/2와 p38 신호전달 경로를 억제하여 심근허혈-재관류에 존재하는 심근세포의 세포사멸을 억제한다[29] ]. 불필요한 아폽토시스는 신경계 질환 및 시신경병증과도 관련이 있습니다. 연구자들은 apoptosis signal-regulating kinase1-interacting protein-1이라는 새로운 이름을 가진 DAB2IP의 과발현이 대뇌 내피 세포의 -amyloid-induced apoptosis를 매개함으로써 알츠하이머병 발병을 촉진할 수 있다고 제안합니다. TBC1D17의 과발현은 시신경병증을 달성하기 위해 망막 세포 사멸을 촉진할 것입니다[30, 31].
요약하면, 전술한 GAP는 표적 단백질 또는 신호 전달 경로와 상호 작용하여 세포 사멸 신호 경로를 활성화 또는 억제하고 세포 사멸에 영향을 미침으로써 질병의 발병에 영향을 미칩니다. 지속적으로 학자들은 종양의 메커니즘과 치료 전략에 많은 관심을 기울여 왔습니다. 여기서 우리는 병리학적 과정을 밝히고 종양의 치료 효과를 향상시키기 위해 세포 사멸에 영향을 미치는 일부 GPA를 소개합니다. 물론 GAP 연구는 다른 병리학적 과정의 특수한 메커니즘도 밝혀내어 설계에 대한 더 나은 이해를 제공하고 특수 대상에 대한 효과적인 치료법을 개발하는 데 도움을 줍니다.

비세포 사멸 RCD
이 섹션에서는 GAP와의 연관성을 설명하기 위해 autophagy 의존적 세포 사멸뿐만 아니라 ferroptosis, pyroptosis 및 기타 비공식 유형과 같은 새로운 형태의 세포 사멸도 다룹니다(그림 3).
자가포식 의존 세포 사멸
신체적 항상성과 건강을 유지하기 위해서는 세포의 중복되고 유해한 성분을 제거하기 위해 자가포식을 활성화하는 것이 필요합니다. Autophagy는 항상 여러 단계로 나누어지는 중요하고 보존된 정상적인 세포 과정입니다: phagophores의 유도, autophagosomes 및 autolysosomes의 형성, 내강 내용물의 분해 및 재순환. 주요 특징은 phagophores, autophagosomes 및 autolysosomes를 포함한 특수한 막 구조입니다. Autophagy는 세포 생존 메커니즘으로 간주되지만 autophagy가 세포의 능력 이상으로 과활성화되면 autophagy-dependent cell death (ADCD)라고하는 세포 사멸로 이어집니다. ADCD의 확인은 autophagic 활성의 증가와 다른 형태로 인한 세포 사멸의 배제라는 특징을 필요로 하며, autophagy 인자의 유전적 및/또는 약리학적 억제에 의해 변형될 수 있다[32].
그러나 ADCD의 개념은 여전히 논란의 여지가 많습니다. 한편으로 autophagy와 apoptosis와 같은 다른 RCD 사이의 혼선의 존재는 관련 분자 및 형태학적 마커에 의해서만 ADCD를 독립적인 세포 사멸 과정으로 정의하기 어렵게 만들고 다른 한편으로는 치명적인 치명적이지 않은 autophagy는 결정하기 어렵습니다 [33, 34]. 종양에서 autophagy의 역할은 양면적일 수 있습니다. autophagy의 손실이 마우스 모델에서 종양 진행을 촉진하지만 autophagy가 종양 특정 염증 반응을 억제하고 영양소가 제한된 미세 환경에서 종양 세포 대사 활동을 지원하여 종양 성장을 촉진할 수 있다는 더 많은 증거가 있습니다[35, 36]. resveratrol 및 arsenic trioxide와 같은 일부 항암제는 ADCD를 유도할 수 있으며[37-39], ADCD는 다른 cotransformed 유전자가 없는 발암성 Ras 발현 세포에서 발생하지만[40], 다양한 종양에서의 역할은 여전히 연구되어야 합니다. 따라서 여기서는 autophagy에서 GAP의 역할에 대한 제한된 소개만 제공합니다.
Autophagosomes는 autophagy의 형태학적 마커인 반면 autophagy(ATG) 관련 단백질은 autophagosome 형성의 핵심이며 autophagy의 분자 마커입니다. RAB GTPase는 세포내 소포의 수송을 제어할 수 있으며[41] 자가포식소체 성숙을 지정할 수 있습니다[42]. 약 10개의 RAB 단백질이 자가포식에서 명확한 기능을 합니다[43]. 따라서 TBC(TRE2-BUB2-CDC16) 도메인을 포함하는 RABGAP를 포함한 RABGAP도 자가포식에 관여합니다. RAB33B는 Atg12-Atg5-Atg16L1 복합체를 식세포로 모집하여 자가포식소체의 형성에 영향을 미치며 Atg16L1은 RAB33B의 결합 단백질입니다[44].
한 연구에서는 OATL1이 RAB33B에 작용하는 GAP이며, 그것의 과발현이 자가포식소체와 리소좀 사이의 융합을 조절함으로써 자가포식소체 성숙을 지연시킬 수 있음을 보여주었습니다[45]. Ras GTPase 계열의 구성원인 RalA/B(A/B와 같은 RAS)도 소포 수송의 주요 조절자입니다[46]. 포유류 세포 모델에서 RalB와 이펙터 단백질인 Exo84는 자가포식소체 형성에 필요한 ULK1-Beclin1-VPS34 어셈블리를 함께 유도합니다. 영양소 제한이 없는 실험 조건에서 RalGAP의 감소는 RalB를 활성화하고 autophagy의 증가를 유도할 수 있습니다. Drosophila를 모델로 사용한 또 다른 실험에서 연구자들은 Ral GTPase가 ADCD로 간주될 수 있는 PCD[48]의 맥락에서 자가포식을 조절한다는 것을 발견했습니다.
라파마이신의 기계적 표적(mTOR)은 성장 인자와 영양 신호를 통합하여 자가포식을 억제합니다. mTOR을 주성분으로 하는 신호 전달 복합체인 mTORC1은 충분한 영양소가 있을 때 ULK1(키나아제 1과 유사하지 않음)의 인산화를 촉진합니다[49]. AKT 및 AMPK 신호 키나아제의 조절 하에서 결절성 경화증 복합체 1/2(TSC1/2)는 Rheb(뇌에 풍부한 Ras 상동체)의 GAP 역할을 하여 GTP 결합 Rheb의 형성을 억제하고 조절에 참여합니다. autophagy를 촉진하기 위한 Rheb-mTORC1-ULK1 신호 전달 경로[49–51]. Tsc1/2 결핍은 환자에게 여러 장기 시스템의 종양 발생에 소인이 되는 상염색체 우성 질환인 결절성 경화증 복합체(TSC)의 발생에 책임이 있습니다[52]. 따라서 TSC의 결함 있는 자가포식은 비정상적인 단백질과 세포 소기관을 포함한 자가포식 기질의 축적으로 이어져 종양 형성을 촉진할 수 있습니다. 연구에 따르면 RalGAP의 결실은 mTORC1 활성의 증가를 유도하여 자가포식을 감소시키는 것으로 나타났습니다.

한편, 췌장암에서 RalGAP는 mTORC1 신호를 통해 종양 세포 침윤을 억제합니다[53]. Autophagy는 화학 요법 및 방사선 요법에 대한 종양 세포의 저항성을 증가시킵니다. 교모세포종(GBM) 치료를 위한 테모졸로마이드(TMZ)는 자가포식을 유도하는 경향이 있으며 종양 세포가 약물에 저항성을 갖도록 만들 수 있습니다. DAB2IP는 Wnt/-catenin 신호 경로를 통해 ATG9B 발현을 부정적으로 조절하여 TMZ 유도 autophagy를 억제하고 GBM 세포에서 약물 감수성을 증가시키는 것으로 밝혀졌습니다[54]. 또한 DAB2IP는 PCa에서 autophagy 관련 방사선 저항의 음성 조절자인 것으로 나타났습니다. DAB2IP의 업스트림 조절기로서 miR-32는 3'-UTR을 표적으로 하고 번역을 억제함으로써 DAB2IP의 단백질 수준을 하향 조절합니다[55]. 결과적으로, 다운스트림 mTOR-S6K 경로가 활성화되지만 자가포식 활성이 강화되는데, 이는 Akt의 음성 피드백 억제의 결과일 수 있으며[56], 궁극적으로 PCa 세포의 방사선 저항성을 강화합니다[55, 57].
일부 GAP는 autophagy를 조절하여 신경계에 영향을 미칩니다. Rap GTPase-활성화 단백질인 SIPA1L2는 TrkB/Rap1 신호 및 autophagosomes와 TrkB-late endosomes의 융합 소기관인 amphisomes[58]와 연결된 신경 전달 물질 해방 과정을 조절하는 반면, TBC1D5 및 TBC1D15, 운동 신경 질환과 관련이 있으며, 이러한 GAP는 자가포식의 무질서 분해 과정과 독성 단백질의 응집을 유발합니다[59-63]. SGSM3/RABGAP5 및 TBC1D10A는 모두 해당 GTPase를 비활성화하여 자가포식을 종료하고 자가포식이 병원체를 제거하고 세포 소기관을 손상시킬 때 면역 체계에 영향을 미칩니다[64, 65]. GAP가 없으면 유 전적으로 이질적인 상 염색체 질환이 발생할 수 있습니다. 예를 들어, TBC1D20 단백질의 결실은 상염색체 장애이며 비정상적인 눈, 뇌 및 생식기 기능을 갖는 Warburg Microsyndrome 4의 사고율을 증가시킬 수 있습니다[66]. Autophagy는 또한 기아 또는 스트레스 중에 신진 대사를 유지하고 영양소를 재활용하는 본질적인 메커니즘입니다. TBC1D5는 LC3와 autophagic 구획을 결합 및 격리하고 원형질막에서 포도당 수송체 GLUT1/Slc2a1 발현을 증가시켜 포도당 흡수 및 당분해 플럭스를 촉진합니다[67].
결론적으로, 대부분의 GAP는 상응하는 GTPase 활동을 하향 조절하여 우리의 신체 기능에 영향을 미치는 autophagy를 직접 조절하지만, 그 목표를 달성하기 위해 autophagy를 간접적으로 조절하는 이펙터 역할을 하는 사람은 거의 없습니다. Autophagy는 신체적 항상성 및 건강과 밀접한 관련이 있습니다. 중요한 것은 GAP가 자가포식 과정에 영향을 미친다는 것입니다. 아쉽게도 ADCD 자체는 미연구 영역이 많고, 그 결과 ADCD와 GAP에 대한 연구는 거의 없는 실정이다. 우리는 autophagy와 GAP 사이의 연결로부터 ADCD에서 가능한 GAP의 역할을 추론할 수 있습니다. 따라서 GAP가 생리학적 및 병리학적 상황에서 ADCD를 조절하는 방법을 더 잘 이해하고 병리학적 발달을 올바르게 이해하며 치료 대상을 찾는 방법에 대한 추가 연구가 필요합니다.
페롭토시스
Ferroptosis는 지질 과산화수소에 대한 치명적인 철 의존성에 의해 결과가 축적되는 새로운 산화성 RCD입니다[68]. 그것의 과학적 관찰은 2003년에 엘라스틴 유도 선택적 세포 사멸 실험을 시작했으며 "ferroptosis"라는 용어는 2012년에 만들어졌습니다[69]. 그 후 학자들은 페롭토시스 연구를 급증시켰습니다. 그 형태의 독특한 특징은 작은 크기, 막 밀도의 변화, 미토콘드리아 크리스타의 감소 또는 소실, 외막의 파열을 포함하는 미토콘드리아 변화입니다[70]. Ferroptosis는 급성 신장 손상, 암 및 심혈관 질환을 포함한 다양한 질병과 관련이 있습니다. ferroptosis 유도의 일부는 RAS 의존적입니다 [71]. Ras 돌연변이 암 세포에서 RAS-RAF-MEK 경로를 차단하면 세포 사멸을 촉진하는 항종양제인 elastin에 의해 유도되는 ferroptosis가 억제됩니다[72]. 그러나 GAP와 ferroptosis 사이의 연관성에 대해서는 상대적으로 거의 알려져 있지 않습니다.
많은 수의 분자 마커와 경로가 페롭토시스의 가능한 과정으로 자가포식에 대해 설명되었습니다[9, 73]. autophagy에서 역할을 하는 GTPase와 GAP는 또한 ferroptosis의 조절인자가 될 수 있습니다. RAB7A는 autophagy에 의해 유도된 지질 방울(LDs)의 분해에 관여하며 동반된 지질 과산화는 ferroptosis를 악화시킵니다[74]. 따라서 TBC1D2는 RAB7A의 음성 조절자로서 RAB7A 의존적 방식으로 페롭토시스를 조절할 수 있습니다[75]. G3BP1(Ras-GTPase-활성화 단백질 결합 단백질 1)은 Ras 신호 전달 경로의 조정에 관여합니다. 그것으로 유도된 세포 사멸의 과정은 LSH와 p53에 의해 조절되는 긴 비암호화 RNA P53RRA와 연결되어 있습니다. 이 과정에서 P53RRA의 뉴클레오티드 1과 871은 G3BP1(aa 177-466)의 RNA 인식 모티프 상호작용 도메인과 직접 상호작용하여 P53RRA-G3BP1 복합체를 형성합니다. 세포질에서 P53RRA-G3BP1 상호작용은 G3BP1 복합체에서 p53을 대체하여 세포질에서 핵으로의 p53 전달을 통해 p53의 재분배를 유도하며, 이는 p53 신호 경로를 활성화하고 TIGAR와 같은 여러 대사 유전자의 발현에 영향을 미칩니다. 그리고 SLC7A11은 결국 세포 주기 정지를 일으켜 세포 사멸과 철근 증식을 유발합니다[76].
파이롭토시스
Pyroptosis는 염증성 RCD의 한 유형으로 병원체 침입에 저항하고 물리적 항상성을 유지하는 선천적 면역 메커니즘입니다[77]. Caspase-1/4/5/11 활성화는 가스더민 D의 절단 속도를 증가시키고 인터루킨-18 및 인터루킨-1과 같은 성숙한 염증성 사이토카인을 분비하는 일부 인플라마솜에 의해 유도됩니다[78 ]. 그 특징은 DNA 단편화, 세포 팽창 및 궁극적으로 원형질막을 파열시키는 거품입니다.
pyroptosis와 GAP 사이의 연결은 특정 미생물에 의해 유도된 세포 사멸에 반영됩니다. YopE는 Yersinia 외부 단백질(Yops)의 일종으로 Yersinia에서 GTP 결합 Rho GTPase를 비공유 방식으로 가수분해하여 Rho GTPase의 숙주 GAP로 작용할 수 있습니다. Yersinia 감염 및 세포 사멸 유도 동안 YopE는 Rho GTPase의 C-말단을 공유 분해하는 시스테인 프로테아제인 YopT라는 또 다른 협력자를 가지므로 Rho GTPase 해리 및 불활성화로 이어집니다. YopE 및 YopT는 본질적으로 Rho GTPase 불활성화와 다르지만 둘 다 숙주 세포 생리에 영향을 미치고 면역 반응을 회피하는 Rhomodifying 독소입니다. 이 과정은 pyrin의 활성 Ser205 및 Ser241 부위를 탈인산화하고 pyrin inflammasome을 형성하여 궁극적으로 pyroptosis를 일으키는 방식으로 직접 유도됩니다[79].
Entosis 세포 사멸
2007년에 연구자들은 종양 세포들 사이에서 관찰되는 세포-먹는 현상을 설명하기 위해 비세포 사멸 세포 사멸 과정 엔토시스를 기술했습니다[80, 81]. 살아 있는 세포가 동일하거나 다른 유형의 세포에 의해 소비될 때 "세포 내 세포" 구조가 발생하여 내부화된 세포(내부 세포)가 사멸합니다. 죽어가는 엔토시스 세포는 아폽토시스의 형태학적 및 분자적 특성을 갖지 않지만 리소좀 및 액포 막 자가포식 단백질 의존적 융합으로 엔토시스를 유도하는 자가포식 의존성을 나타냅니다[82, 83].
세포 부착 및 세포골격 재배열은 엔토시스의 핵심 과정이며 상피 카드헤린 및 Rho-ROCK 신호 전달에서는 정의할 수 없습니다[80]. 세포-세포 접합부에서 p190A RhoGAP의 모집은 Rho 경로의 활성을 억제하여 미오신 경쇄 인산화를 감소시켜 액토미오신 수축을 감소시키고 칼모듈린 수준을 억제합니다. p190A RhoGAP의 분극 분포로 인해 세포 접착의 원위 말단에서 액틴의 수축이 세포 접착 부위에서보다 훨씬 더 높습니다[84]. 또한 Rho는 세포 부착 말단에서 RhoGEF에 의해 활성화됩니다[85]. 따라서 RhoGAP와 RhoGEF는 Rho에 대해 개별적으로 작용하지만 케톤증 유도에는 상승적으로 작용합니다.

유사 분열 재앙
Mitotic catastrophe(MC)는 효과적인 항암 메커니즘 및 치료법이기도 한 비정상적인 유사분열 세포 사멸의 한 유형입니다[86]. 그 형태학적 특징은 일반적으로 다핵화 및/또는 소핵화를 나타내는 독특한 핵 변경입니다[87]. 정확히 말하면 MC는 autophagy와 마찬가지로 MC가 반드시 세포 사멸을 유발하는 것은 아니기 때문에 RCD의 한 유형이 아니며, 따라서 2018년 세포 사멸 명명 위원회에서는 이러한 유형의 사망의 이름으로 유사분열사라는 용어를 사용할 것을 권장합니다[10 ]. 더욱이 연구에 따르면 대부분의 MC 세포의 궁극적인 운명은 본질적인 세포사멸[10, 88]이며 둘 사이의 차이점과 연관성이 있습니다.
트리 유형의 GAP는 비정상적인 유사분열과 연결됩니다: RasGAP NF1, p190RhoGAP 및 RanGAP. NF1의 돌연변이는 RAS 관련 다운스트림 신호 경로를 활성화할 수 있습니다. 이 경우 PKC 관련 경로와 같은 다른 신호 경로의 조정은 RAS 과잉 활성화의 세포 교란을 조절하고 세포 생존을 보장하는 데 필요합니다. Nf1- 결핍 조건에서 내인성 단백질 키나아제 C(PKC)의 억제는 Akt(비정상 Ras의 다운스트림 이펙터 중 하나) 경로와 협력하여 Chk1을 활성화하고 유사분열 정지를 연장하며 이후 MC를 통해 세포자멸사를 유발합니다. [89]. T 세포 악성 종양 1(MCT-1)에서 다중 복제의 과발현은 PTEN 유전자의 제시에 직면하고 단백질의 안정성과 기능적 활성에 부정적인 영향을 미쳐 포스포이노시티드 3 키나제/AKT 신호를 활성화합니다. 또한 MCT-1는 p190RhoGAP를 하향 조절하고 Src에 결합하고 MCT-1와 상호 작용하며 Src/p190B 신호를 활성화하는 p190B의 발현을 상향 조절했습니다. 결국 MCT-1의 증가된 표현과 억제된 PTEN은 상승적으로 Src/p190B 경로를 증가시켜 RhoA 활동의 억제를 유발하고 MC의 발생률을 향상시킵니다[90].
위의 GAP에 대한 설명과 달리 RanGAP1의 키네토코어 및 스핀들 국소화는 주요 간기 핵 및 유사분열 진행의 벡터에 관여하는 조절인자인 임포트틴 1에 의해 영향을 받는 것 외에도 RanGAP1 sumoylation도 임포트틴과 관련이 있습니다. 1과 양의 상관관계를 보인다. 그 메커니즘은 RanBP2가 임포틴 1의 N-말단과 직접 상호작용하고, 내인성 RanBP2를 격리시키고, 임포틴 1과 임포틴 1을 감소시키고, 둘 다 확산시켜 비정상적인 스핀들 형성 및 손상된 염색체 정렬을 초래하여 궁극적으로 세포 사멸을 야기할 가능성이 가장 높습니다[91] . 요약하면, GAP에 의한 해당 GTPase 단백질 활성의 비정상적인 조절은 정상적인 신호 캐스케이드를 방해하고 결국 MC 사고율을 증가시킬 수 있습니다.
행동 양식
Methuosis는 RCD의 독특한 형태이며, 그 특별한 특징은 액포화, 소포의 축적(단일 막 및 마크로피노좀으로부터, autophagosomes의 이중 막 구조를 구별함), 그리고 결국에는 원형질막 파열입니다[92]. Methuosis는 GBM 및 위암종을 특징으로 하는 Ras 신호 전달 경로(지속적인 활성화)와 밀접한 관련이 있습니다[93].
GIT1은 GTP를 가수분해하여 방법에 영향을 주어 Arf6를 비활성화하는 GAP 역할을 합니다. 그 과정에서 과잉 활동적인 H-Ras는 Rac1 GEF를 활성화하여 Rac1-GTP의 양을 증가시킵니다. Rac1 및 CIE(clathrin-independent endocytosis)의 활성화에 의해 강화된 Micropinocytosis는 후기 엔도좀(Rab7 및 LAMP1)의 일부 특징을 얻습니다. 한편, 과잉 활성 Rac1이 Rac1-GTP가 GIT1과 직접 상호 작용하여 Arf6의 활성을 감소시키고 CIE의 재활용을 손상시키며 리소좀과 융합하지 못하게 하는 피드백 메커니즘이 있습니다. 마지막으로, 이러한 결과는 CIE의 축적으로 이어지고 후기 엔도솜 소포가 합쳐져 더 큰 유체로 채워진 세포질 액포를 형성하고 궁극적으로 원형질막을 파열시키고 세포 사멸을 유발합니다[94, 95]. 그러나 위의 결과는 Arf6(Q67 L) 활동이 H-Ras(G12V)를 발현하는 세포에서 액포 형성을 촉진한다는 Shliom과 동료들의 자금 지원과 모순됩니다[96]. 이 현상에 대한 가장 적절한 설명은 발생하는 액포에 영향을 미친다는 것입니다.
GAP는 종양 면역을 조절합니다.
RCD와 면역은 밀접한 관련이 있습니다.
RCD는 처음에 면역-관용원성 사건, 특히 세포사멸로 생각되었습니다[97]. 그러나 이후의 증거와 면역원성 세포사(ICD) 개념의 도입으로 점차 RCD에서 면역 활동의 역할이 확립되었습니다. ICD는 독립적인 죽음의 방식이 아니며 스트레스 유발 세포 죽음에 대한 반응으로 세포 독성 T 림프구(CTL)의 활성화에 의해 구동되는 적응 면역의 존재를 갖는 RCD 유형을 말합니다[97, 98]. ICD의 발달은 죽은 세포에서 중심 내성에 포함되지 않는 항원의 존재와 DAMP(손상 관련 분자 패턴)의 노출 및 방출이 각각 항원성 및 보조성이라고 하는 핵심 구성 요소인 복잡한 과정입니다[98 ]. DAMP는 항원 제시 세포(APC)의 모집 및 성숙을 촉진하여 CTL 의존성 면역 반응을 유발합니다[99]. 일부 기존 화학요법제, 종양 용해 바이러스, 표적 항암제, 특정 방사선 요법 양식 및 기타 요인이 ICD의 유도제가 될 수 있습니다[100, 101].
이 연구 결과를 바탕으로 2013년 연구자들은 ICD 유도제와 다른 면역 조절제를 병용하면 효과적인 항종양 효과를 나타낼 수 있다고 제안했고[99], 후속 연구에서는 세포독성 T-림프구 관련 항원 4(CTLA-4), 프로그램된 세포 사멸-1(PD-1) 및 이에 상응하는 리간드 PD-L1은 ICD의 좋은 협력자입니다[102-104]. 최근 ICD를 유도하기 위해 나노기술과 결합된 암 면역요법도 새로운 가능성을 보여주고 있다[105, 106]. 물론 다른 RCD는 세포의 끝이 아니라 면역 반응 또는 ICD의 시작일 수 있습니다[107]. 또한, 이러한 RCD는 항종양 면역에도 관여합니다[108, 109]. 예를 들어, T 세포와 ferroptosis는 종양에서 서로 매개합니다. 면역요법으로 활성화된 CD8 + T 세포는 종양 세포에서 지질 과산화를 강화했으며, 이는 차례로 증가된 페롭토시스를 동반한 면역요법의 항종양 효능에 기여했습니다[110]. 이 증거는 RCD가 면역 활동 및 면역 요법과 불가분의 관계가 있음을 입증하기에 충분합니다.

GAP는 면역 미세 환경에 기여합니다.
다중 면역 세포의 형성 및 기초 기능은 GAP에 의해 영향을 받습니다(그림 4A). T 세포는 항종양 면역의 주축입니다. 미성숙 이중 양성(DP) 흉선 세포는 양성 선택 후 CD4 플러스 또는 CD8 플러스 단일 양성(SP) T 세포로 부분적으로 분화되는 반면, 다른 DP T 세포는 세포 사멸을 겪습니다. Ras-MAPK 경로가 이 과정을 조절하는 메커니즘은 잘 연구되었습니다[111, 112].
RASA1- 결핍 흉선에서 DP 세포는 세포사멸에 대한 감수성이 증가했지만 CD4 SP 대 DP 비율의 증가는 RASA1 결실이 양성 선택을 촉진하고 Ras-MAPK 신호 경로 활성화와 관련될 수 있음을 시사합니다[113]. 또한 DAB2IP의 proapoptotic 효과로 인해 CCR4-NOT 복합체는 DAB2IP를 하향 조절하여 흉선 세포의 양성 선택에 참여합니다[114]. 흥미롭게도 또 다른 연구에서는 NF1이 암컷 HY TCR Tg 마우스에서 흉선 세포의 양성 선택을 촉진하지만 그 메커니즘은 불분명하다는 것을 보여주었습니다[115]. T 세포 조절의 또 다른 예는 ARHGAP19가 T 림프구 분열에 필요한 세포골격 리모델링을 조정하고 RhoA를 조절하여 염색체 분리를 조절한다는 것입니다[116]. ARHGAP45는 RHO를 조절하여 나이브 T 세포의 세포골격 변화를 조율하고 변형 및 림프절(LN)로의 이동을 증가시키며 T 세포 전구체의 흉선 파종을 촉진할 수 있습니다[117].
또한 Rab35와 그 GAP EPI64C(TBC1D10C)는 T 세포-APC 상호 작용의 일부인 면역 시냅스(IS) 형성에 필요합니다[118]. 대식세포는 죽은 세포를 삼켜 면역 반응의 하류에서 중요한 역할을 합니다. 이전 연구에서는 Rho GTPase 구성원인 Rac1 및 Cdc42를 액틴 세포골격 조직을 제어하여 Fc 수용체 매개 식세포 작용을 조절하는 분자 스위치로 특징지었습니다[119, 120]. Sh3BP1, ArhGAP12, ArhGAP25는 시간과 공간에서 Rac와 Cdc42를 협력적으로 불활성화하여 대식세포의 대식세포가 세포사멸 세포와 같은 큰 입자에 대한 식균작용을 종료시킵니다[121]. 대식세포 분극화, 운동성 및 세포 퍼짐 특성은 p190RhoGAP 전좌의 RASA1-매개 조절과 관련이 있습니다[122]. 대식세포에서 또 다른 RhoGAP 미오신 Myo9b 결실은 세포 형태를 변경하고 이동 능력을 손상시키는 것으로 나타났습니다[123]. Roland Csépányi-Kömi 등이 검토한 바와 같이 호중구에서 RhoGAP 계열의 역할은 보다 광범위하며 주로 호중구 모양 변화, 부착, 화학주성 및 식균작용을 포함합니다. [124].

종양 미세 환경의 참여로 종양 세포는 면역 체계의 감시를 피할 수 있으므로 발달 과정에서 면역 공격에서 살아남을 수 있습니다. neurofibromin을 암호화하는 NF1은 종양 면역 미세 환경에서 GAP의 역할을 설명하는 좋은 예입니다(그림 4B). Neurofibromin은 RAS 활동을 하향 조절하는 GTPase 활성화 단백질이므로 NF1의 돌연변이는 RAS 관련 다운스트림 신호 경로를 활성화할 수 있습니다. 신경섬유종증 1형(NF1)은 신경섬유종 단백질인 GAP의 활성 상실로 인해 발생하는 신경계의 유전 질환입니다[125]. 침윤성 염증 비만 세포와 같은 면역 세포는 NF1의 구성 요소이며 면역 세포에서 NF1 유전자의 돌연변이도 이 질병에 필수적입니다 [126]. 연구원들은 NF1fox/−를 설계했습니다. Krox20- NF1-/- Schwann 세포와 NF1 plus /- 비만 세포가 있는 Cre 마우스는 Schwann 세포 증식뿐만 아니라 대규모 비만 세포 침윤이 있는 마우스가 대조군 마우스에 비해 얼기형 신경섬유종을 발생시키는 것을 발견했습니다. 이 발견은 NF1 비만 세포의 haploinsufficiency가 종양에 유리한 NF1 + /- 면역 미세 환경을 만든다는 사실을 입증합니다[127].
또한 NF1-/- Schwann 세포는 PIK-3 경로의 c-kit 매개 활성화를 통해 줄기 세포 인자(SCF) 및 탈과립에 의한 Nf1 haploinsufficiency 비만 세포 이동을 향상시킵니다[128-130]. 정상인에 비해 NF1 환자는 중추신경계 종양이 발생하기 쉽습니다. 저등급 신경아교종(LGG)에서 연구원들은 핵심 신경면역 축을 발견했는데, 이는 NF1 돌연변이 뉴런이 미드킨을 생성하여 T 세포가 미세아교세포를 활성화하여 LGG의 성장을 촉진하는 인자인 CCL5를 생성하도록 유도함을 시사합니다[131]. 유사한 결과가 GBM에서 발견되었습니다.
최근 연구에 따르면 Nf1 및 Pten의 코드집합과 EGFRVIII의 과발현이 있는 종양 모델은 면역 제거 및 고도의 면역 억제 미세 환경을 피할 수 있으며 Nf1 손실이 핵심 사건입니다[132]. 흥미롭게도 NF1 대립유전자의 불완전한 돌연변이가 종양의 원인이지만 일부 연구자들은 T 세포에 NF1이 없으면 T 세포 활동을 증가시켜 종양의 물리적 면역 모니터링 메커니즘을 강화하고 악성 이동을 억제할 수 있다는 모순을 제시합니다. 이러한 발견과 일치하게, NF1과 관련된 대부분의 종양이 비악성인 NF1 환자의 임상 현상은 NF1 유전자 돌연변이에 대한 우리의 인식을 개조합니다[133].
또한 연구에 따르면 Ras protein activator-like 1 단백질(Rasal1)은 T 세포의 P21Ras-ERK 경로를 부정적으로 조절하여 T 세포의 활성화를 억제하여 T 세포의 항종양 면역을 감소시키는 반면, RASAL1 녹다운은 나타났습니다. B16 흑색종 및 EL-4 림프종에서 T 세포의 항종양 활성을 향상시키기 위해 [134]. G 단백질의 GAP로서 RGS 계열은 면역 활동의 조절에 여러 방식으로 관여하며 표적 면역 요법의 잠재력을 가지고 있습니다[135]. 최근 연구에 따르면 RGS1은 T1 세포와 CTL의 종양으로의 수송을 억제하여 유방암에서 '차가운 종양'의 형성을 촉진하고 항종양 면역을 손상시키는 것으로 나타났습니다[136]. 한편, 마우스 실험은 PD-L1과 함께 RGS1 녹다운이 있는 종양 특이적 CTL의 전이가 유방암에 대한 유망한 면역 치료 전략이 될 수 있음을 입증했습니다[136].
결론 및 관점
질병, 특히 암의 GAP에 대한 연구는 최근 몇 년 동안 증가했습니다. 일부 GAP는 암세포 증식, 이동, 약물 내성 및 악성 변형에 영향을 미치는 요인이 될 수 있으며 암에 대한 새로운 치료 표적 및 예후 지표가 될 수도 있습니다. RCD와 관련된 신호 경로는 이 과정에서 GAP에 의해 조정될 수 있습니다. 가장 전형적인 예는 RASGAP에 의한 RAS 관련 경로의 억제로 암 세포의 세포 사멸 과정을 조절하는 것입니다. GAP에 의한 종양 면역 조절에 관한 연구는 제한적이다. 여기에서 RCD 조절에 있어 GAP의 광범위한 역할을 요약함으로써 우리는 GAP가 RCD 관련 면역 활동 또는 보다 정확하게는 ICD 유발 항종양 면역 반응에 존재할 수 있다고 추측합니다. 또한, 면역세포에서 발현되는 GAP는 면역세포의 생리기능을 유지하는데 필수적이며, 면역세포를 조절하여 면역회피 및 항종양면역에 관여한다.
발암성 RAS 단백질의 활성화 특징 중 하나는 무제한 증식을 얻기 위해 암 세포의 세포사멸을 억제하는 능력입니다. 발암성 RAS는 RASGAP에 의해 유발되는 가수분해 억제에 저항하는 돌연변이를 가질 수 있습니다.
RAS-GTP 가수분해를 촉진하기 위해 GAP와 동등한 역할을 할 수 있는 소분자 약물에 대한 검색이 오랫동안 제안되었지만 낙관적인 진전은 이루어지지 않았습니다. 세마포린 4D는 GAP 활성 수용체 Plexin-B1에 작용하여 R-Ras를 비활성화하여 인테그린 활성화 및 세포 이동을 조절하는 것으로 나타났습니다[137]. 특정 GAP 활동 규제에 대한 추가 사례가 있습니다. 예를 들어, 합성 단백질 반발 유도 분자 A(RGMA) 수용체 네오게닌은 p120GAP 활성을 상향 조절하여 Ras 및 그 다운스트림 이펙터 Akt를 억제합니다[138]. RASGAP의 기능 억제는 암에도 존재할 수 있습니다. 그러나 전형적으로 연관된 NF1 질병에 대한 치료 양식은 여전히 매우 어려우며 현재의 전략은 대부분 RAS/MEK 경로의 억제를 포함합니다[139]. 요약하면, GAP의 기본 기능은 잘 알려져 있지만 GAP가 생물학적 과정을 조절하는 방법을 더 잘 이해하고, 병리학적 발달을 올바르게 이해하고, 치료 대상을 식별하기 위해서는 추가 연구가 필요합니다.
약어
GAP: GTPase-활성화 단백질; RCD: 조절된 세포 사멸; GEF: 구아닌 뉴클레오티드 교환 인자; GDI: 구아닌 뉴클레오티드 해리 억제제; RGS: G 단백질 신호 전달 조절자; GPCR: G-단백질 결합 수용체; ACD: 우연한 세포 사멸; PCD: 프로그램된 세포 사멸; DISC: 사망 유도 신호 복합체; TNF: 종양 괴사 인자; TRAIL: TNF 관련 세포사멸 유도 리간드; RGS3: G-단백질 신호 전달 3 조절자; DLC1: 간암 1에서 삭제됨; DAB2IP: DOC-2/DAB2 상호작용 단백질; PITX1: 뇌하수체 호메오박스 1의 인산화; HCC: 간세포 암종; ceRNA: 경쟁하는 내인성 RNA; PCa: 전립선암; ECT2: 상피 세포 형질전환 서열 2; YAP: 예 관련 단백질; TPR: 전위된 프로모터 영역; BLBC: 기저 유사 유방암; LV: 림프관; ADCD: Autophagy 의존적 세포 사멸; mTOR: 라파마이신의 기계적 표적; TMZ: 테모졸로마이드; GBM: 교모세포종; G3BP1: Ras-GTPase활성화 단백질 결합 단백질 1; Yops: Yersinia 외부 단백질; MC: 유사분열 재앙; MCT-1: T 세포 악성종양 1의 여러 사본; ICD: 면역원성 세포 사멸; CTL: 세포독성 T 림프구; DAMP: 손상 관련 분자 패턴; APC: 항원 제시 세포; DP: 이중 양성; NF1: 신경섬유종증 유형 1; SCF: 줄기 세포 인자; LGG: 저등급 신경아교종; Rasal1: Ras 단백질 활성제 유사 1 단백질.
감사의 말
그림과 원고를 검증해 주신 Yongguang Tao 교수와 Li Xie 박사, Wenbing Liu에게 감사드립니다.
저자의 기여
YJ와 LC는 검토의 개념과 디자인에 기여했습니다. HH와 SW는 원고를 썼습니다. JH와 HH는 수치와 표를 준비했습니다. SJ, LL, YL은 참고 문헌을 수집하고 토론에 참여했습니다. 모든 저자는 최종 원고를 읽고 승인했습니다.
펀딩
이 작업은 중국 국립자연과학재단(81802785[YJ], 82100490[LC]), 중국 후난성 자연과학재단(2020JJ5382[YJ], 2020JJ5381[LC]), 후난성 보건 과학 연구 프로젝트의 지원을 받았습니다. 위원회(20200763[WL]) 및 창사 과학 기술국의 기본 연구 프로젝트(kq2004127[LX]).

데이터 및 자료의 가용성
적용되지 않습니다.
선언
윤리 승인 및 참여 동의
적용되지 않습니다.
게시 동의
적용되지 않습니다.
경쟁 관심
저자는 경쟁 이익이 없다고 선언합니다.
저자 세부 정보
1 중화인민공화국 후난성 창사 410013 후난성 후난성 모델 동물 및 줄기 세포 생물학의 핵심 실험실. 중화인민공화국 후난성 창사 410013 호남사범대학교 의과대학 2호. 3 중화인민공화국 창사 410013 중남대학교 샹야 의과대학 부속암병원 두경부외과. 중화인민공화국 창사 410078 중남대학교 기초의학대학 샹야병원 병리학과 교육부 발암 및 암침습 핵심 연구실 4.
참조
1. Wennerberg K, Rossman KL, Der CJ. Ras 수퍼패밀리 개요. J 셀 사이언스 2005;118(Pt 5):843–6.
2. Takai Y, Sasaki T, Matozaki T. 소형 GTP 결합 단백질. Physiol Rev. 2001;81(1):153–208.
3. Bos JL, Rehmann H, Wittinghofer A. GEF 및 GAP: 작은 G 단백질 제어에 중요한 요소. 셀. 2007;129(5):865–77.4. Cherfls J, Zeghouf M. GEF, GAP 및 GDI에 의한 작은 GTPase의 규제. Physiol Rev. 2013;93(1):269–309.
5. Ligeti E, Welti S, Schefzek K. GTPase 활성화 단백질에 의한 생리적 반응의 억제 및 종료. Physiol Rev. 2012;92(1):237–72.
6. 로스 EM, 윌키 TM. heterotrimeric G 단백질에 대한 GTPase 활성화 단백질: G 단백질 신호(RGS) 및 RGS 유사 단백질의 조절자. Annu Rev Biochem. 2000;69:795–827.
7. Schefzek K, Ahmadian MR, Kabsch W, Wiesmuller L, Lautwein A, Schmitz F, Wittinghofer A. Ras-RasGAP 복합체: 발암성 Ras 돌연변이에서 GTPase 활성화 및 손실에 대한 구조적 기초. 과학. 1997;277(5324):333–8.
8. Schefzek K, Shivalingaiah G. Ras 특정 GTPase 활성화 단백질 구조, 메커니즘 및 상호 작용. 콜드 스프링 Harb Perspect Med. 2019;9(3):a031500.
9. Tang D, Kang R, Berghe TV, Vandenabeele P, Kroemer G. 조절된 세포 사멸의 분자 기계. 셀 해상도 2019;29(5):347–64.
10. Galluzzi L, Vitale I, Aaronson SA, Abrams JM, Adam D, Agostinis P, Alnemri ES, Altucci L, Amelio I, Andrews DW, Annicchiarico-Petruzzelli M, Antonov AV, Arama E, Baehrecke EH, Barlev NA, Bazan NG, Bernassola F, Bertrand MJM, Bianchi K, Blagosklonny MV, Blomgren K, Borner C, Boya P, Brenner C, Campanella M, Candi E, Carmona-Gutierrez D, Cecconi F, Chan FK, Chandel NS, 외. 세포 사멸의 분자 메커니즘: 세포 사멸 2018에 관한 명명법 위원회의 권장 사항. 세포 사멸은 다릅니다. 2018;25(3):486–541.
11. Maiuri MC, Zalckvar E, Kimchi A, Kroemer G. Self-eating and self-killing: autophagy와 apoptosis 사이의 혼선. Nat Rev Mol Cell Biol. 2007;8(9):741–52.
12. 커 JF. 수축 괴사: 뚜렷한 세포 사멸 방식. J 파톨. 1971;105(1):13–20.
13. Carneiro BA, 엘-데이리 WS. 암 치료에서 표적 세포 사멸. Nat Rev Clin Oncol. 2020;17:395–417.
14. Czabotar PE, Lessene G, Strasser A, Adams JM. BCL-2 단백질 계열에 의한 세포사멸 제어: 생리학 및 치료에 대한 함의. Nat Rev Mol Cell Biol. 2014;15(1):49–63.
15. Seyrek K, Ivanisenko NV, Richter M, Hillert LK, Konig C, Lavrik IN. DED 단백질의 번역 후 변형을 통한 세포 사멸 제어. 트랜드 셀 바이오. 2020;30(5):354–69.
16. Tai WT, Chen YL, Chu PY, Chen LJ, Hung MH, Shiau CW, Huang JW, Tsai MH, Chen KF. Protein tyrosine phosphatase 1B는 간세포 암종에서 PITX1을 탈인산화하고 p120RasGAP를 조절합니다. 간장학. 2016;63(5):1528–43.
17. Vanli G, Sempoux C, Widmann C. caspase-3/p120 RasGAP 스트레스 감지 모듈은 간암 발병률을 감소시키지만 감마선 조사 및 발암 물질 처리 마우스의 전체 생존에는 영향을 미치지 않습니다. 몰 카시노그. 2017;56(6):1680–4.
18. Yang JY, Michod D, Walicki J, Murphy BM, Kasibhatla S, Martin SJ, Widmann C. 온화한 스트레스 조건에서 세포 생존을 위해서는 caspases에 의한 RasGAP의 부분 절단이 필요합니다. Mol Cell Biol. 2004;24(23):10425–36.
19. Lu S, Zhou J, Sun Y, Li N, Miao M, Jiao B, Chen H. 비암호화 RNA HOXD-AS1은 인간 간세포 암종에서 전이 및 세포사멸 표현형의 중요한 조절자입니다. 몰 암. 2017;16(1):125.
20. Guo X, Xiang C, Zhang Z, Zhang F, Xi T, Zheng L. BMF에 의한 Bax의 변위는 STARD13 3' UTR 유도 유방암 세포 세포사멸을 miRNA 의존 방식으로 중재합니다. 몰팜. 2018;15(1):63–71.
21. Sánchez-Martín D, Otsuka A, Kabashima K, Ha T, Wang D, Qian X, Lowy DR, Tosato G. DLC1 결핍이 내피 세포 접촉 성장 억제 및 혈관 육종 진행에 미치는 영향. J Natl Cancer Inst. 2018;110(4):390–9.
22. Bellazzo A, Di Minin G, Collavin L. 블락 원, 언리쉬 백. 암에서 DAB2IP 비활성화의 메커니즘. 세포 죽음은 다릅니다. 2017;24(1):15–25.
23. Zhou J, Ning Z, Wang B, Yun EJ, Zhang T, Pong RC, Fazli L, Gleave M, Zeng J, Fan J, Wang X, Li L, Hsieh JT, He D, Wu K. DAB2IP 손실 부여 STAT3 활성화 및 세포 사멸 억제를 통한 안드로겐 박탈 요법에 대한 전립선 암의 저항. 세포 사멸 Dis. 2015;6:e1955.
24. Yang XM, Cao XY, He P, Li J, Feng MX, Zhang YL, Zhang XL, Wang YH, Yang Q, Zhu L, Nie HZ, Jiang SH, Tian GA, Zhang XX, Liu Q, Ji J, 주 X, 시아 Q, 장 ZG. Rac GTPase 활성화 단백질 1의 과발현은 히포 신호를 감소시켜 세포분열을 촉진함으로써 암세포의 증식에 기여합니다. 위장병학. 2018;155(4):1233–49.
25. Tatsumoto T, Xie X, Blumenthal R, Okamoto I, Miki T. Human ECT2는 Rho GTPase의 교환 인자이며 G2/M 단계에서 인산화되고 세포질분열에 관여합니다. 제이셀바이오. 1999;147(5):921–8.
26. Chen J, Xia H, Zhang X, Karthik S, Pratap SV, Ooi LL, Hong W, Hui KM. ECT2는 Rho/ERK 신호 전달 축을 조절하여 인간 간세포 암종의 조기 재발을 촉진합니다. J 헤파톨. 2015;62(6):1287–95.
27. Lawson CD, Fan C, Mitin N, Baker NM, George SD, Graham DM, Perou CM, Burridge K, Der CJ, Rossman KL. Rho GTPase 전사체 분석은 기저 유사 유방암에서 rho GTPase 활성화 단백질에 대한 발암성 역할을 밝혀줍니다. 암 해상도 2016;76(13):3826–37.
28. Lapinski PE, Lubeck BA, Chen D, Doosti A, Zawieja SD, Davis MJ, King PD. RASA1은 마우스에서 림프관 판막의 기능을 조절합니다. 제이클린 인베스트 2017;127(7):2569–85.
29. Wang Z, Huang H, He W, Kong B, Hu H, Fan Y, Liao J, Wang L, Mei Y, Liu W, Xiong X, Peng J, Xiao Y, Huang D, Quan D, Li Q, Xiong L, Zhong P, Wang G. G-단백질 신호 전달 조절기 5는 JNK1/2 및 P38 신호 경로를 모두 억제하여 생쥐의 시험관 내 심장 허혈 재관류 동안 세포 사멸로부터 심근 세포를 보호합니다. Biochem Biophys Res Commun. 2016;473(2):551–7.
30. Wang H, Fan L, Wang H, Ma X, Du Z. 아밀로이드 베타는 AIP1의 발현과 기능을 조절합니다. J Mol Neurosci. 2015;55(1):227–32.
31. Sirohi K, Swarup G. 옵티뉴린의 녹내장 관련 돌연변이로 인한 autophagy의 결함. 특급 안구 해상도. 2016;144:54–63.
32. Shen HM, Codogno P. Autophagic cell death: Loch Ness 괴물인가 멸종위기종인가? 자가 포식. 2011;7(5):457–65.
33. Kriel J, Loos B. The good, the bad and the autophagosome: autophagy-dependent cell death에 대한 답이 없는 질문 탐구. 세포 죽음은 다릅니다. 2019;26(4):640–52. 34. Lindqvist LM, Simon AK, Baehrecke EH. autophagy의 현재 질문 및 가능한 논쟁. 세포 사멸 발견 2015;1:1–7.
35. Amaravadi R, Kimmelman AC, White E. 암에서 autophagy의 기능에 대한 최근 통찰력. 진 데브. 2016;30(17):1913–30.
36. Kimmelman AC, White E. Autophagy 및 종양 대사. 세포 메타. 2017;25(5):1037–43.
37. Kanzawa T, Kondo Y, Ito H, Kondo S, Germano I. 삼산화비소에 의한 악성 신경아교종 세포에서의 자가포식 세포 사멸 유도. 암 해상도 2003;63(9):2103–8.
38. Dasari SK, Bialik S, Levin-Zaidman S, Levin-Salomon V, Merrill AH Jr, Futerman AH, Kimchi A. Signalome-wide RNAi 스크린은 GBA1을 자가포식 세포 사멸의 양성 중재자로 식별합니다. 세포 죽음은 다릅니다. 2017;24(7):1288–302.
39. Zein L, Fulda S, Kogel D, van Wijk SJL. 약물 유발 autophagy 의존성 세포 사멸의 소기관 특이 적 메커니즘. 매트릭스 비올. 2021;100–101:54–64.
40. Elgendy M, Sheridan C, Brumatti G, Martin SJ. Noxa 및 Beclin-1의 발암성 Ras 유도 발현은 자가포식 세포 사멸을 촉진하고 clonogenic 생존을 제한합니다. 몰셀. 2011;42(1):23–35.
41. Stenmark H. Rab GTPases는 소포 교통의 조정자입니다. Nat Rev Mol Cell Biol. 2009;10(8):513–25.
42. Hyttinen JM, Niittykoski M, Salminen A, Kaarniranta K. autophagosomes 및 endosomes의 성숙: Rab7의 핵심 역할. Biochim Biophys 액타. 2013;1833(3):503–10.
43. Szatmari Z, Sass M. Rab 소형 GTPases 및 해당 상류 조절기의 자가포식 역할: 검토. 자가 포식. 2014;10(7):1154–66.
44. 팬텀 S, 콘스탄티니디스 G, 보스 S, 한 H, Hofnagel O, 리 Z, 우 YW. RAB33B는 비정규 RAB 결합 단백질을 통해 ATG16L1 복합체를 phagophore에 모집합니다. 자가 포식. 2020. https://doi.org/10.1080/15548627.2020.1822629.
45. 새로운 autophagosome 상주 Rab33B-GAP 인 Itoh T, Kanno E, Uemura T, Waguri S, Fukuda M. OATL1은 autophagosomal 성숙을 조절합니다. 제이셀바이오. 2011;192(5):839–53.
46. Moskalenko S, Henry DO, Rosse C, Mirey G, Camonis JH, White MA. exocyst는 Ral efector complex입니다. Nat Cell Biol. 2002;4(1):66–72.
For more information:1950477648nn@gmail.com






