신장 질환의 요로 족세포 표지자
Mar 23, 2022
자세한 정보:ali.ma@wecistanche.com
Lingfeng Zeng 외
추상적인
족세포는 신장 기능의 유지에 중요한 역할을 하며 많은 사람들의 주요 초점입니다.신장질병. 족세포 손상은 족세포 유래 세포 단편과 족세포 특이적 분자 표적을 소변으로 흘리게 하며, 이는 다음의 바이오마커 역할을 할 수 있습니다.신장질병. 살아 있거나 죽은 온전한 족세포 및 족세포 유래 미세소포는 다양한 원심분리, 시각화 및 배양 방법을 통해 소변에서 정량화될 수 있습니다. 핵, 세포질, 슬릿-횡격막, 사구체 모세혈관 기저막, 세포골격의 족세포 특이적 단백질 표적과 소변에서 상응하는 전령 RNA(mRNA)는 웨스턴 블롯팅, ELISA 또는 정량적 중합효소로 정량화할 수 있습니다. 연쇄 반응. 이러한 기술 중 일부는 현재 비용이 많이 들거나 노동 집약적일 수 있지만 기술 및 자동화의 향상으로 인해 미래에 널리 사용 가능해질 수 있습니다. 의 적용비뇨기족세포다양한 진단 및 모니터링을 위한 마커신장질병그러나 이 분야에서 발표된 데이터는 충분히 체계적이지 않고 외부 검증이 부족합니다. 추가 연구는 실험실 방법을 표준화, 비교 및 자동화하고 일상적인 임상 테스트에 대한 부가가치를 정의하는 데 중점을 두어야 합니다.
키워드:족세포, 바이오마커, mRNA, miRNA, 네프린, 포도신, 포도칼릭신, 시냅토포딘,만성병 환자신장질병

Cistanche 줄기는 만성 신장 질환을 치료할 수 있습니다
1. 소개
1.1. 만성신장질환의 역학
만성병 환자신장질병(CKD)는 중요하고 비용이 많이 드는 비전염성 질병입니다[1]. 신대체 요법이 가능해지면서 CKD 치료에 사용되는 의료비가 (C만성신장질병)1960년대 이후 급격히 증가하였다[2,3]. 2015년 전 세계적으로 신대체 요법을 받는 환자는 250만 명이 넘었으며, 이 숫자는 2030년까지 두 배로 증가할 것으로 예상됩니다[4]. 진단, 치료 및 모니터링을 위한 효과적인 수단신장질병많이 필요합니다.
1.2. 신장 질환의 초점으로서의 족세포
신장의 주요 기능은 대사 폐기물과 과도한 체수분의 배설이며[5], 이는 세 가지 과정에 의해 달성됩니다. (2) 신세뇨관을 통한 유용한 물질의 선택적 재흡수; (3) 세뇨관주위 모세혈관에서 세뇨관액으로 다른 대사성 폐기물을 선택적으로 분비[6]
신장은 섬세한 3-차원 구조로 배열된 여러 세포 유형으로 구성되어 있지만 족세포는 정상적인 신장 기능을 유지하는 데 핵심적인 역할을 하며 많은 세포의 주요 초점입니다.신장질병. 족세포는 내피 세포 및 사구체 모세관 기저막(GCBM)과 함께 사구체 여과 장벽을 구성하는 고도로 특이적인 말단 분화 세포입니다[7]. 족세포는 하부 족세포 공간에 의해 GCBM과 분리된 부피가 큰 세포체를 가지고 있습니다[8]. 세포체는 GCBM 쪽으로 확장되고 광범위한 발 돌기에 의해 후자에 부착되는 긴 일차 돌기를 발생시킵니다[8].
족세포에는 몇 가지 생리적 기능이 있습니다. 그들은 사구체 혈관 루프 형태를 유지하고 사구체 여과를 조절하며 국소 면역 및 염증 반응에 참여합니다. 또한, 족세포는 부분적으로 GCBM의 합성 및 전환[9] 뿐만 아니라 내피 세포의 투과성 및 증식 조절에 중요한 혈관 내피 성장 인자(VEGF)와 같은 측분비 인자의 생성을 담당합니다. [10]. 족세포 기능 장애는 많은 질병의 발병 및 진행에서 중추적인 역할을 합니다.신장질병. 다양한 족세포 관련 유전자의 돌연변이는신장질병, 일반적으로 임상적으로는 스테로이드 내성 신증후군으로, 조직학적으로는 국소 사구체 경화증(FGS)으로 나타납니다. 반면에 족세포 수 또는 밀도 감소 및 족세포 족돌기 융합을 포함한 후천적 족세포 기능 장애는 이차 내피 및 GCBM 손상, GCBM 음전하 소실, 열공막 단백질 이상 및 다양한 기전을 통해 최종적으로 단백뇨를 유발합니다. 11,12].
족세포 손상의 특징적인 결과는 GCBM과의 약화된 상호작용이며, 이는 GCBM에서 족세포의 분리로 누적됩니다. 족세포는 재생 및 기능적 보상 능력이 제한되어 있기 때문에 나머지 족세포는 GCBM의 기계적 및 전하 장벽 기능을 유지할 수 없으며, 이는 비가역적으로 손상되며 최종 결과는 단백뇨이다[13]. 모욕의 정도에 따라 족세포 손상은 발 돌기의 손실, 액포 및 가낭 형성, 탈분화 및 세포자멸사로 이어질 수 있습니다. 측벽 상피 세포의 증식, GCBM의 수축, 사구체 모세혈관 응회암의 소실, 최종적으로 사구체 경화증을 포함하는 인접 구조가 후속적으로 영향을 받을 것입니다[14].
1.3. 문헌 검토 방법
"발세포", "발세포 관련 분자" 또는 "바이오마커"를 포함하는 검색어로 문헌 검토를 수행했습니다.만성병 환자신장질병", "급성 신장 손상", "사구체신염", "당뇨병성 신병증" 또는 "당뇨병신장질병", Medline, Embase 및 Cochrane Library에서 관련 문헌을 검색하는 데 사용되었습니다. 관련 출판물의 참고 문헌에서 추가 잠재적 논문을 조사했습니다. 적격 연구에는 2020년 7월 이전에 출판된 인간 및 동물 연구가 포함되었습니다. 족세포 생물학, 막 생리학 및 족세포의 분자 조작은 제외되었습니다.
1.4. 바이오마커로서의 족세포 특이적 표적
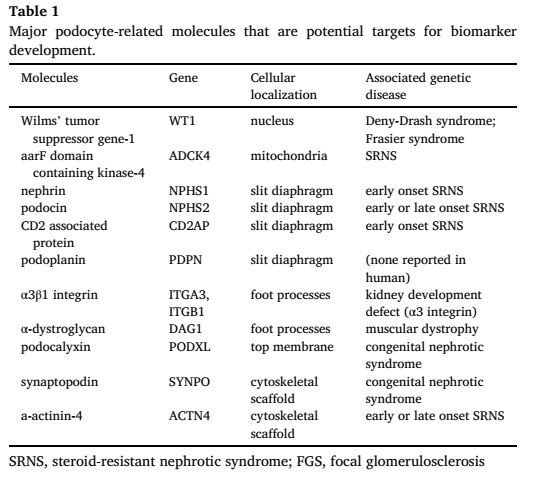
족세포 손상은 다양한 족세포 유래 분자를 요로로 흘리게 하고 다음의 바이오마커 역할을 할 수 있습니다.신장질병(그림 1). 족세포의 세포체는 해부학적으로나 기능적으로 구분되는 세 부분으로 나눌 수 있습니다: 기저부, 상부, 슬라이드-횡격막(SD) 부분[15]. 특정 세포막 단백질은 각 부분에 존재하며, 세포질 세포골격계와의 상호작용은 족세포 구조 및 기능의 안정성을 담당합니다[16]. 바이오마커 개발의 잠재적 표적인 주요 족세포 유래 분자는 표 1에 요약되어 있습니다.

그림 1. 소변에서 족세포 손상 및 잠재적 족세포 유래 마커. 족세포의 손상은 형태학적 변화, 세포자멸사 및 분리의 3가지 상호 관련된 병리학적 과정을 초래합니다. 족세포는 생존할 수 있지만 단백뇨 및 세뇨관간질 섬유증과 같은 기능적 다운스트림 결과를 갖는 형태학적 변화로 나타날 수 있습니다. 족세포 아폽토시스는 축적된 형태학적 변화의 결과로 또는 특정 모욕으로부터 직접 발생할 수 있습니다. 사구체에서 족세포의 손실(즉, 족혈구감소증)은 사구체 모세혈관 루프의 구조적 변화를 초래하고 사구체 경화증을 초래합니다. 3 1 인테그린 손실로 인한 세포자멸사 또는 생존 가능한 족세포는 요강으로 분리되어 소변에서 식별되고신장질병. 손상되거나 apoptotic podocytes에서 파생된 vesicles, microparticles 또는 podocyte-specific 분자도 소변에서 감지되어 바이오마커 역할을 할 수 있습니다. (GCBM, 사구체 모세혈관 기저막; AgII, 안지오텐신 II; TGF-, 변형 성장 인자-베타, ROS, 활성 산소 종).
1.5. 핵 및 세포질 표적
Wilms의 종양 억제 유전자-1(WT1)는 족세포 핵의 징크 핑거 유사 전사 인자이며 아마도 조직학적 연구에 가장 일반적으로 사용되는 족세포 특이적 마커일 것입니다[17]. WT1 유전자는 10개의 엑손으로 구성되며, 그 중 엑손 7~10은 DNA 결합 도메인의 4개의 징크 핑거를 암호화합니다. WT1은 족세포에서 특이적으로 발현되며 아마도 네프린의 발현을 조절하는 것으로 보인다[18]. WT1 유전자의 엑손 8과 9에 이형접합 돌연변이가 발생하면 Denys-Drash 증후군이 나타나며, 이는 신증후군, 남성 가자성동염, Wilms 종양을 나타냅니다[19].
족세포의 다른 핵 및 세포질 단백질은 바이오마커로서 잘 연구되지 않았습니다. aarF 도메인 함유 키나제{1}}(ADCK4)는 쥐 족세포의 족돌기 내 미토콘드리아에 특이적으로 존재합니다[20]. ADCK4는 CoQ 복합체를 안정화시키는 역할을 하며 정상적인 족세포 항상성 기능에 필요합니다[20]. 마우스에서 족세포 특이적 ADCK4 제거는 족돌기 소실, 여과 슬릿의 해체, 미토콘드리아 확대 및 기능 장애, CoQ10 감소를 초래하고[21] 치료하면 CoQ10, 미토콘드리아 기능, 족세포 형태 개선, 족돌기 소실 방지[21]가 회복됩니다. ,22].
1.6. 슬릿 다이어프램 단백질 복합체
족세포 슬릿-횡격막의 단백질 성분은 다음의 바이오마커로 광범위하게 연구되었습니다.신장질병. 이 그룹의 주요 단백질에는 네프린, 포도신, CD{0}}연관 단백질(CD2AP) 및 포도플라닌이 있습니다[23]. 네프린은 슬릿 횡격막의 핵심을 형성하는 세포외 도메인이 있는 막횡단 단백질입니다. 그것은 물리적 체 장벽과 신호 발판 역할을 합니다[24]. nephrin 유전자의 돌연변이는 인간에서 선천성 신증후군의 첫 번째 보고된 원인이었습니다[25]. 포도신과 CD2AP는 네프린을 세포막 아래의 액틴 세포골격에 연결하는 역할을 합니다. Podocin은 stomatin family의 hairpin-like protein이며 podocytes에서만 발현된다[26]. 이는 8개의 엑손으로 구성되고 염색체 1q{10}}q31 영역에 위치한 NPHS2 유전자에 의해 인코딩됩니다[27]. NPHS2 유전자의 돌연변이는 소아 및 성인 환자 모두에서 상염색체 열성 스테로이드 내성 신증후군을 유발합니다[27,28]. CD2AP는 섬유상 액틴 및 기타 세포막 단백질과 직접 상호작용하는 스캐폴딩 분자이며 동적 액틴 리모델링 및 막 수송에 연루되어 있습니다[29]. 포도플라닌은 많은 수의 O-글리코사이드 사슬을 가진 작은 막횡단 당단백질입니다. 족세포에서 포도플라닌의 선택적 손실은 단백뇨를 유발하고, 이어서 자발적인 단백뇨의 쥐 모델에서 족세포 형태의 변경이 뒤따릅니다[30].

시스턴스가 신장에 좋다
1.7. GCBM에 연결된 표적
족세포 기저 영역의 주요 단백질 성분은 3 1 인테그린과 -디스트로글리칸(-DG)입니다. 이 단백질은 족세포를 GCBM에 고정시키고 족세포의 정확한 위치와 여과막의 무결성을 유지하는 데 중요한 역할을 합니다[31,32]. 3 1 인테그린은 세포외 도메인이 GCBM에서 라미닌 521의 라미닌 G 유사 도메인 G(LG)에 연결된 막횡단 단백질이며, 세포질 영역은 -액티닌{{{{ 9}}. 글리코실화된 단백질 -DG는 유트로핀을 통해 세포골격에 연결되고, 라미닌 521과의 상호작용을 통해 족세포 및 GCBM에 연결됩니다.
1.8. 상단 멤브레인의 표적
Podocalyxin은 족세포의 꼭대기 쪽에 있는 주요 막횡단 단백질입니다. 이것은 사구체 여과의 전하 장벽에 기여하는 음전하를 띤 시알산 단백질입니다 [33]. 포도칼릭신에는 세 가지 기능이 있습니다. (1) 음전하를 띤 단백질이 소변으로 누출되는 것을 방지합니다. (2) 인접한 족세포의 분리를 유지하기 위해; (3) 상피 세포와 모세관 루프 사이의 접착을 방지하기 위해 [34]. 포도칼릭신은 에즈린과 나트륨 양성자 교환 조절 인자 2(NHERF2)에 의해 액틴 세포골격에 연결됩니다.
1.9. 액틴 관련 표적
많은 족세포 특이적 단백질이 액틴 세포골격에 연결되어 족세포의 3-차원 구조를 유지합니다. 이 그룹에서 가장 잘 연구된 대상은 synaptopodin과 -actinin-4입니다. 둘 다 역방향-1(MAGI{7}})으로 막 관련 구아닐레이트 키나아제와 상호작용하여 액틴 골격에 결합합니다[35]. Synaptopodin은 SYNPO 유전자에 의해 암호화된 프롤린이 풍부한 선형 단백질이며[36] 발 돌기가 발달할 때 분화하는 족세포에서 발현됩니다. 그 결과 시냅토포딘은 성숙한 족세포의 표지자로 간주된다[37].
2. 연구 방법
2.1. 사구체 내 족세포 마커
이 리뷰의 초점은비뇨기족세포마커의 경우 신장 조직에서 이러한 마커의 검출을 간략하게 논의하는 것이 논리적입니다. 족세포 고갈은 절대적(족세포 손실) 또는 상대적(사구체 부피당 족세포 수 감소)일 수 있습니다[38]. 신장에서 족세포를 정량화하는 황금 표준 방법은 입체 방법론(광 또는 전자 현미경, 공초점 레이저 주사 현미경, 초음파, 컴퓨터 단층 촬영 또는 자기 공명 영상)이다[39]. 그러나 모두 시간이 많이 걸리고 노동 집약적입니다. 최근 Venkatareddy et al. 등은 단일 파라핀 포매 포르말린 고정 절편으로 족세포 밀도를 추정하는 방법을 평가했으며, 여기서 족세포 핵은 WT1에 대한 항체 또는 분할의 트랜스듀신 유사 인핸서를 사용한 간접 면역형광에 의해 가시화되었습니다[40]. 후속 연구는 이 방법이 선택적 족세포 고갈의 형질전환 마우스 모델에서 정확한 족세포 계수를 제공함을 보여주었으며, 이 접근법이 전체 사구체에서 족세포 고갈 분석을 위한 효율적인 정량적 도구를 제공함을 확인시켜주었습니다[41]. 그럼에도 불구하고 이 방법은 여전히 신장 생검이 필요하므로 연속 모니터링에는 적합하지 않습니다.
2.2. 소변 족세포 정량화 및 배양
족세포는 발 돌기에 의해서만 생리적 위치에 고정되기 때문에 소변에서 생존 가능한 세포로 소실되기 쉽다[42]. 사실, 온전한 족세포는 건강한 사람과 환자의 소변에서 감지할 수 있습니다.신장질병[43], 그리고 요실금은 아마도 CKD가 진행되는 동안 족세포 고갈의 주요 기전일 것입니다.(C만성신장질병)[42]. 소변에서 족세포를 식별하는 전통적인 방법은 cytospin 기술과 특정 항-podocalyxin 항체를 사용한 면역형광 연구를 포함하며 [44], 자동화가 부분적으로 가능합니다. 그러나 이 기술은 요도 침전물에서 세포 파편을 오염시키기 때문에 민감도와 특이도가 제한적입니다.
대안적으로, 족세포는 탠덤 질량 분석(LC-MS/MS)과 결합된 액체 크로마토그래피로 족세포 특이적 트립신 펩티드의 검출에 의해 식별될 수 있다. 이 기술의 장비 비용은 높지만 조작자 독립적이고 재현성이 높다는 장점이 있으며[45] 임상 실험실 실습에서 응용 가능성이 증가할 것입니다.
이전 연구에 따르면 cytospin 면역형광 기술을 사용하면 건강한 사람은 0.5 podocytes/mg creatinine 미만을 배출하는 반면 활동성 사구체 질환이 있는 환자는 400 podocytes/mg creatinine을 배출합니다[43]. 대다수비뇨기족세포propidium iodide 배제 및 TUNEL 염색으로 테스트할 때 생존 가능합니다[43]. 이론적으로, 생체 외에서 생존 가능한 족세포의 배양은 따라서 죽은 세포 및 비특이적 세포를 제거함으로써 족세포 식별의 특이성을 향상시킬 것입니다. 그러나 족세포는 일반적으로 생체 내에서 증식하지 않으며 생체 외에서 배양하려면 특별한 실험 조건이 필요합니다[46]. 이전 보고서에서는 발세포가 먼저 불멸화된 족세포가 복제되는 성장 허용 조건에서 성장할 수 있음을 보여주었습니다[46]. 이 목적을 위한 세포 배양 배지는 일반적으로 Roswell Park Memorial Institute(RPMI) 1640 또는 Dulbecco의 변형된 Eagle 배지로 구성되며, 10% 태아 소 혈청에 20-100U/ml의 마우스 인터페론-감마(INF-)가 보충되고, 배양 접시는 일반적으로 족세포 증식을 촉진하기 위해 유형 I 콜라겐으로 코팅됩니다[46]. 이 방법은 번역 연구 및 치료 대상 식별에 큰 가치가 있지만 일상적인 임상 사용에는 너무 복잡합니다.

Cistanche는 신장 기능을 향상시킬 수 있습니다
2.3. 소변 족세포 유래 단편
세포외 소포(EV)는 다양한 세포 유형에 의해 방출되는 구형 막체입니다[47]. 비뇨기 계통에서 정점막과 세포내액을 포함하는 EV는 족세포, 신세뇨관 상피 세포 및 요상피 세포를 포함한 모든 네프론 세그먼트에서 소변으로 배출됩니다. 소변 EV는 신장 기능 장애 및 구조적 손상의 단백질 마커를 포함합니다. 최근 연구에서는 EV가 세포간 통신과 관련이 있을 수 있다고 제안합니다[48]. 또한, 이전 연구에서도 손상된 족세포에서 정단 세포막 조각이 소변으로 흘러나와[49] 전자현미경에 의해 포도칼릭신 양성 과립 구조(PPGS)로 식별될 수 있음을 보여주었습니다[49]. 당뇨병 마우스 모델에서 족세포의 요 엑소좀은 직렬 원심분리에 의해 분리될 수 있고 마이크로입자는 아넥신 V 항체(모든 마이크로입자를 검출함)를 사용한 유세포분석에 의해 정량화될 수 있으며, 이어서 포도칼릭신 또는 포도플라닌(족세포 유래 마이크로입자를 구체적으로 식별함)에 대한 항체가 뒤따를 수 있습니다. [50,51]. 추가 광산란 분석을 사용하여 미세 입자의 크기를 추가로 결정할 수 있습니다[52]. 이러한 정교한 기술로 족세포 유래 미세입자는 고혈당에 노출된 생쥐[51]와 알부민뇨가 발병하기 전의 당뇨병 생쥐[52]에서 증가하는 것으로 나타났습니다. 전자의 경우, 이상은 Rho-kinase 억제제에 의해 억제되었으며, 이는 세포골격 재구성이 미세입자 방출의 주요 유발인자임을 나타냅니다[51]. 그러나 이러한 기술을 인간에게 적용하면신장질병탐구되지 않았습니다.
최근에는 소변에서 족세포 유래 EV와 미세입자의 수와 크기를 측정하는 것보다 소변 엑소좀에서 족세포 특이적 분자를 측정하는 데 관심이 높아지고 있다. 예를 들어, 소변 EV의 족세포 유래 신호 전달 인자(PDSTF)는 족세포 손상 평가의 잠재적 후보로 제안되었습니다[52]. 그러나 그들의 임상 응용 프로그램은 아직 개발 중입니다.
2.4. 소변 족세포 특이적 단백질 표적
여러 족세포 특이적 단백질 표적의 소변 수준을 쉽게 측정할 수 있으며 이들의 생물학적 지표로서의 역할신장질병연구되었습니다. 소변의 포도칼릭신 수치는 간접 면역형광법, ELISA 또는 유세포 분석법으로 측정할 수 있으며[53],비뇨기족세포세다. 그러나 이전 연구에서 소변의 포도칼릭신은 온전한 족세포가 요로 파쇄된 것이 아니라 손상된 족세포의 정단막에서 대부분 유래한 것으로 나타났으며, 초기 신장 손상 시 그 수치가 증가한다[49]. 소변에서 또 다른 중요한 족세포 특이적 단백질 표적인 포도칼릭신(Podocalyxin)과 네프린(nephrin)은 건강한 사람의 소변에서는 전통적인 Western blotting으로 검출할 수 없지만[54] 전자간증 환자에서 전통적인 ELISA로는 검출할 수 있습니다[55]. 더욱이, 요중 네프린 수치는 단백뇨의 중증도[56] 및 신장 기능[57]과 상관관계가 있습니다. 혈장 네프린 수치도 측정할 수 있지만[57] 생물학적 또는 임상적 관련성은 확인되지 않았습니다. 발세포 특이적 단백질 표적의 소변 수준을 임상 바이오마커로 사용하는 주요 문제는 낮은 농도(보통 ng/ml 범위)와 소변 농도 희석의 교란 효과입니다.
2.5. 소변 족세포 특이적 mRNA
측정비뇨기족세포-특정 mRNA 수준은 소변 족세포 수 측정을 위한 대체 방법으로 제안되었습니다. 소변에서 족세포 특이적 mRNA의 양은 일반적으로 전통적인 노던 블롯 연구에 충분하지 않지만 실시간 정량적 중합효소 연쇄 반응(RT-QPCR)에 의해 쉽게 측정됩니다. 이전의 두 연구에서는 소변의 네프린 mRNA 수준이 소변의 족세포 수와 밀접한 상관관계가 있음을 보여주었습니다[56,58]. 일련의 신장 생검을 이용한 항사구체 기저막 질환의 마우스 모델에서,비뇨기족세포-특정 mRNA 수준은 사구체 족세포 손실 속도와 상관관계가 있습니다[52].
그러나 최근 연구에서는 족세포 스트레스 또는 상대적 족세포 손상에 대한 대리 마커로서 파생된 요 mRNA 지수에 초점을 옮겼습니다. 쥐 모델에서 진행성 사구체 질환은 podocin mRNA 수준과 비교하여 감소된 nephrin과 관련이 있었고 요중 podocin-to-nephrin mRNA 비율은 조직학적 진행의 중증도와 상관관계가 있었습니다[59]. 후속 연구에서 건강한 사람들의 평균 동맥압은 소변의 포도신 mRNA 대 크레아티닌 비율(족세포 분리의 지표), 포도신 대 네프린 mRNA 비율(발세포 스트레스의 지표) 및 소변의 포도신과 상관관계가 있는 것으로 나타났습니다. -to-aquaporin-2 mRNA 비율(상대 족세포 손상 대 세뇨관 손상의 마커) [60]. 사구체 손상은 특히 요중 포도신 대 아쿠아포린{11}} 및 네프린 대 아쿠아포린{14}} mRNA 비율 증가와 관련이 있습니다[61].
2.6. 족세포에 특이적인 소변 miRNA 마커
마이크로 RNA(miRNA)는 특정 mRNA를 표적으로 하여 많은 생물학적 경로를 조절하는 짧은 비암호화 RNA입니다[62]. mRNA와 유사하게 소변 miRNA는 RT-qPCR에 의해 쉽게 정량화됩니다[63]. 바이오마커 개발의 관점에서 miRNA는 분해에 강하다는 장점이 있어 임상적 활용과 아카이브 샘플 연구에 용이하다[63]. 많은 특정 miRNA 변화가 관찰되었습니다.신장질병[9]. 예를 들어, miR-23b, miR-24 및 miR-26a를 포함한 기능적 miRNA의 족세포 특이적 손실은 빠른 사구체 및 세뇨관 손상을 초래하는 것으로 밝혀졌습니다[64]. 특히 miR{6}}b는 아데노신 수용체 2B를 표적으로 하여 족세포 생존을 조절합니다[65]. 유사하게, 요 중 miR-21, miR{10}} 및 miR{11}} 수치는 신장 기능 장애(알부민뇨 및 추정 GFR)의 중증도와 상관관계가 있는 것으로 보고되었습니다.비뇨기족세포당뇨병 환자의 표지자(nephrin, synaptopodin 및 podocalyxin)[66]. 최근 연구에서는 여러 miRNA에 대한 특정 다운스트림 경로를 추가로 확인했는데, 이는 발병 또는 진행과 관련이 있을 수 있습니다.신장질병. 특히 miR{0}}a는 족세포 분화에 영향을 미치고[67] 사구체 질환의 발병기전에 역할을 할 수 있는 WT{1}}의 발현을 억제합니다[68]. 한편, miR-21은 금속단백분해효소 3(TIMP3)의 조직 억제제[69,70]의 발현을 억제하고, miR{9}}a는 형질전환 성장인자 베타{10}}(TGF-1 11}}) 발현 [71,72], miR{14}}b는 Ras GTPase 활성화 단백질 SH3 도메인 결합 단백질 2(G3BP2)를 표적으로 하고, miR-29c는 Sprouty 상동체 1(Spry1)을 표적으로 합니다. ) [74]; 이들 모두는 당뇨병성 신병증의 진행에 관여합니다.

신장 기능 개선을 위한 시스탄체
그러나 족세포는 소변 miRNA의 작은 부분에만 기여합니다. 족세포에서 관찰된 특정 miRNA 변화는 소변에서 쉽게 식별할 수 없는 반면, 소변 miRNA 수준의 변화는 다른 신장 세포 유형의 병리학적 변화를 반영할 수 있습니다[75,76]. 예를 들어, miR-155, miR{3}} 및 miR-1915의 소변 수준은 FGS 또는 최소 변화 신병증(MCN) 환자와 건강한 대조군 사이에 유의하게 다르지만 [77] miR-155, miR-663 또는 miR-1915이 특히 족세포에서 유래하는 것으로 나타나지 않았습니다. N-아세틸{10}}D-글루코사미니다제(NAG) 및 신장 손상 분자{12}}(KIM{13}})의 뇨 수준을 포함하여 많은 miRNA 수준과 세뇨관 손상 마커 사이의 유의한 상관관계[66], 보고되기도 했다. 즉, 족세포 손상 마커로서의 특이성을 확인하기 어렵다. 이 규칙의 주목할만한 예외는 miR{15}}a입니다. 최근 연구에 따르면 비뇨기 엑소좀 miR{16}} 수준은 건강한 대조군보다 루푸스 신염에서 유의하게 더 높았으며, miR{17}}a는 정상 C57BL/6 마우스의 사구체에서 가장 풍부하게 발현된 miRNA였으며, miR{20}} 족세포 분화 및 세포골격 완전성의 조절을 담당했습니다[78]. 그럼에도 불구하고 족세포 특이적 마커로서의 요 miR{22}}의 역할은 검증이 필요합니다.
2.7. 순환 족세포 마커
위에서 언급한 많은 족세포 마커, 특히 족세포 특이적 단백질 표적 및 mRNA는 전신 순환에서 측정될 수 있으며[56,79,80],신장질병탐구되었다[55,81-84]. 그러나 이 주제에 대한 전체 토론은 이 검토의 범위를 벗어납니다. 위에서 언급한 방법론의 주요 장점과 단점은 표 2에 요약되어 있습니다.

3. 특정 신장 질환의 요로 족세포 표지자
3.1. 당뇨병성 신장 질환
당뇨병 환자신장질병(DKD)는 CKD의 가장 흔한 원인입니다.(C만성신장질병)전 세계적으로 다양한 활용에 관한 풍부한 문헌이 있습니다.비뇨기족세포DKD의 진단 및 모니터링을 위한 마커. 예를 들어 Jim et al[14]은 알부민뇨가 있는 모든 DKD 환자에서 요중 네프린 수치를 감지할 수 있지만 알부민뇨가 없는 환자에서는 54%만 검출할 수 있다고 보고했습니다. 요중 네프린 수치는 알부민뇨 수치와 상관관계가 있고, 신장 기능과 반비례합니다[14]. Ma et al은 DKD에서 소변의 angiopoietin-like-4(Angptl4) 수치가 증가했다고 보고했습니다[85]. 소변 포도칼릭신 수치는 미세단백뇨가 발병하기 전에 당뇨병 환자에서 증가했으며 아마도 미세단백뇨보다 DKD의 조기 발견에 더 민감했을 것입니다[86]. 확립된 DKD에서 소변 포도칼릭신 수치는 HbA1c 수치 및 알부민 대 크레아티닌 비율과 양의 상관관계가 있었습니다[87,88]. 종합하면, 이용 가능한 결과는 여러 족세포 특이적 표적의 소변 수준이 DKD의 초기 지표이며, 이와 관련하여 소변의 포도칼릭신 수준이 가장 유망한 지표임을 나타냅니다[54].
개별 소변 성분에서 족세포 특이적 표적의 수준도 조사되었습니다.소변족세포유세포 분석에 의해 결정된 미세 입자 수준은 건강한 대조군보다 제1형 당뇨병에서 더 높았고, 그 수준은 고혈당 클램프로 더 증가했습니다[89]. 요중 엑소좀 WT-1 수치는 당뇨병 환자의 단백뇨, 신장 기능, 사구체 손상 및 신장 기능 저하의 중증도와 상관관계가 있었습니다[58,90]. 또 다른 연구에서, 요로 박리 세포의 글리코겐 합성효소 키나제(GSK)3 수준은 진행성 신장 손상이 있거나 없는 당뇨병 환자를 구별하는 데 알부민뇨보다 더 정확했습니다[91]. 그러나 이 분석의 방법론은 번거롭고 일상적인 임상 실습에 적용되지 않을 수 있습니다.
소변의 족세포 특이적 mRNA 마커와 관련하여 이전 연구에서는 nephrin, podocin, synaptopodin, WT{1}} 및 -actin-4의 소변 mRNA 수준이 정상 대조군보다 DKD 환자에서 더 높은 것으로 나타났습니다. [92]. 다양한 중증도의 알부민뇨를 가진 당뇨병 환자에서 nephrin, podocin, -actinin-4 및 CD{7}}관련 단백질의 소변 mRNA 수준에는 유의한 차이가 있었습니다[93]. nephrin, podocin, synaptopodin, WT{9}} 및 -actin{11}}의 소변 mRNA 수준은비뇨기족세포수, 요중 네프린 수치, 알부민뇨, 신장애의 중증도[93]. 보다 최근에는 제2형 당뇨병 환자에서 소변의 족세포 특이적 mRNA 수준이 미세알부민뇨 발병보다 먼저 발견되었으며[94], 족세포 박리의 표지자인 소변의 포도신 mRNA-대-크레아티닌 비율은 후속 비율과 유의한 상관관계가 있었습니다. 신장 기능 저하 [94]. 또한, 12주 동안 ACE 억제제와 안지오텐신 수용체 차단제(ARB)를 병용 투여한 후 소변 시냅토포딘 mRNA 수치가 ACE 억제제 단독 요법에 비해 낮아졌다[95]. 종합하면, 이용 가능한 증거는 소변에서 족세포 특이적 mRNA 수준의 측정이 DKD에서 위험 계층화 및 치료 반응 모니터링에 유용할 수 있음을 시사합니다.
3.2. 신병증 및 국소 사구체 경화증의 최소 변화
MCN과 FGS는 종종 족세포 질환으로 간주되며,비뇨기족세포대상이 테스트되었습니다. Zhou et al. [96]은 면역블롯팅 기술로 측정한 요로 엑소좀 WT{1}} 수치가 스테로이드에 민감한 신증후군(SSNS) 환자나 건강한 지원자보다 FGS 환자에서 유의하게 더 높았다고 보고했습니다. 비뇨기 엑소좀 WT-1 수치는 코르티코스테로이드 치료와 FGS 또는 SSNS의 관해 후에 유의하게 감소했습니다[96]. 또 다른 연구에서는 기존의 ELISA 분석으로 측정한 요로 네프린 수치가 신증후군의 다른 원인보다 FGS가 있는 성인에서 유의하게 더 높았습니다[97].
족세포 특이적 mRNA의 소변 수준도 연구되었습니다. 초기 연구에 따르면 요중 nephrin과 podocin mRNA 수준은 MCN 환자와 건강한 지원자 사이에 유의한 차이가 없었으며 그 수준은 DKD 환자보다 유의하게 낮았습니다[98]. 후속 연구에서 요중 nephrin과 podocin mRNA 수치는 FGS 또는 건강한 대조군보다 MCN 환자에서 더 낮았으며 감소 정도는 단백뇨의 정도와 상관관계가 있었습니다[99]. 이 연구에서 소변 시냅토포딘 mRNA 수준은 FGS 환자의 신장 기능 감소의 후속 속도와 상관관계가 있는 것으로 밝혀졌으며[99], 이는 FGS 족세포의 질적 변화가 소변에서 식별될 수 있음을 시사합니다.
3.3. 막성 신증
막성 신병증(MGN)의 주요 병리학적 변화는 상피하 공간에 면역 복합체가 침착되어 사구체 여과 장벽의 변화를 초래하지만,비뇨기족세포MGN의 마커는 부족합니다. MGN에서 nephrin, podocin 및 synaptopodin의 요침사 mRNA 수준은 유의하게 증가했지만 수준은 MGN을 신증후군의 다른 원인과 확실하게 구별했습니다[98]. 보다 최근에 Lu et al[100]은비뇨기족세포- 면역억제제 치료 후 임상변수의 개선과 동시에 유도된 미세입자가 감소하여 MGN 모니터링에 역할을 함을 시사한다.
3.4. IgA 신증
면역글로불린 A 신병증(IgAN)은 주로 간질 질환이지만,비뇨기족세포바이오마커로서의 카운트가 탐색되었습니다. 특히 Shen et al[101]은 IgAN 환자가 요로 족세포 손실이 증가하고 사구체에서 족세포가 더 적으며 신장 생검 표본에서 더 심각한 족돌기 융합이 있음을 발견했습니다. 본 연구에서는 podocalyxin의 간접 면역형광 연구를 통해 소변 족세포를 동정하였으며,비뇨기족세포혈청 크레아티닌 및 단백뇨와 상관관계가 있는 수 [101]. 후속 연구에서 분절 경화증이 있는 IgAN 환자의 요 족세포 수가 분절 경화증이 없는 환자보다 더 많았다[102]. IgAN 또는 Henoch-Sch¨ 온라인 자반병 신염이 있는 소아에서 Hara 등[103]은 소변에서 족세포의 누적 손실이 신장 생검에서 조직학적 손상의 중증도 및 사구체 경화증의 정도와 상관관계가 있음을 보여주었습니다.비뇨기족세포배설은 빠른 조직학적 진행을 보였다.
IgAN의 바이오마커로서 소변의 족세포 특이적 분자에 대한 연구는 단편적이고 불완전합니다. 요중 포도칼릭신 수치는 성인 IgAN에서 급성 모세혈관 외 병변의 중증도와 유의한 상관관계가 있었습니다[102]. 소변 포도신 mRNA 수준은 신장 생검에서 활성 사구체 손상의 심각성을 반영하고 단백뇨 수준에 상보적인 예후 정보를 제공하는 것으로 보고되었습니다[104]. IgAN은 전 세계적으로 가장 흔한 원발성 사구체신염이기 때문에 이 분야에 대한 더 많은 연구가 확실히 필요합니다.
IgAN의 역할 외에도비뇨기족세포마커는 다른 혈관간 사구체 병증에서 탐색되었습니다. 예를 들어,비뇨기족세포유전성 및 후천성 형태의 미만성 메산지움 경화증에서 손실이 현저하게 증가합니다[102]. 그럼에도 불구하고, 이 영역은 병리학적 분류의 이질성 때문에 잘 연구되지 않았습니다.
3.5. 루푸스 신염
소변족세포루푸스 신염에서의 흘리기가 연구되었습니다. 이전 보고서에 따르면 주요비뇨기족세포활동성 루푸스 신염 환자에서 생존 가능하지만 역분화되었고, 소변에서 apoptotic podocytes의 비율은 건강한 대조군보다 유의하게 낮았습니다[105]. 이 연구에서 소변 포도칼릭신, 시냅토포딘, 포도신, 네프린, WT{1}} 수치(웨스턴 블롯팅으로 측정)는 전신성 루푸스, 특히 활동성 루푸스 신염에서 유의하게 증가했으며, 그 수치는 중증도 단백뇨와 유의한 상관관계가 있었습니다. 및 조직학적 활성 [105]. 후속 연구에서 nephrin, podocin 및 synaptopodin의 소변 mRNA 수준이 활동성 루푸스 신염 환자에서 활동성 루푸스 신염 환자에서 유의하게 더 높았다고 보고했습니다[106]. 구체적으로, 요중 nephrin mRNA 수준은 단백뇨 및 전신 질환 활성과 상관관계가 있었지만 조직학적인 lupus nephritis와는 관련이 없었고, 요 podocin mRNA 수준은 이후의 신기능 저하의 독립적인 예측인자였습니다[107].
3.6. 항호중구 세포질 항체(ANCA) 관련 혈관염
족세포는 ANCA 관련 사구체신염에서 신장 손상의 주요 표적이 아니지만 사구체 내 족세포 밀도는 특징적으로 감소합니다[108]. Zou et al[108]은 소변에 대한 족세포 박리율이 ANCA 관련 사구체신염에서 후속적인 신장 기능 손실을 예측한다는 것을 발견했으며 Minakawa et al[109]은 사구체 내 족세포의 대리 마커인 뇨 podocin 대 nephrin mRNA 비율을 보고했습니다. 응력, 초승달 형성 비율과 상관관계 [109]. 후자의 연구에서 높은 수치의 환자는비뇨기족세포-유도된 mRNA는 아마도 더 나은 사구체 족세포 비축과 가역성 가능성으로 인해 유리한 신장 결과를 보였다[109].
3.7. 기타 CKD
의 유용성비뇨기족세포특정 마커신장질병표 3에 요약되어 있습니다. 소변의 많은 족세포 특이적 마커도 CKD의 일반 마커로 탐색되었습니다.(C만성신장질병). 예를 들어,비뇨기족세포유세포 분석에 의해 정량화된 세포외 미세소포는 신장 기능이 손상된 고혈압 환자에서 신장 장애가 없는 환자보다 유의하게 증가했습니다[110]. Western blotting으로 측정한 소변 시냅토포딘 수치는 당뇨병 및 비당뇨 CKD 모두에서 신장 기능과 상관관계가 있습니다.(C만성신장질병), 알부민뇨의 정도에 관계없이 소변 시냅토포딘이 족세포 손상의 일반적인 표지자임을 시사합니다[110]. 족세포 특이적 요 mRNA 표적 패널 중 BDNF(요뇌 유래 신경영양 인자) mRNA 수준은 제네릭 마커인 요로 신장 손상 분자-1(KIM{4}})와 가장 높은 상관관계를 보였습니다. 신장 손상 [111]. miRNA 표적의 경우, 족세포 손상 및 CKD 동물 모델에서 소변 엑소좀 miR{6}} 수준이 증가했습니다.(C만성신장질병)환자 [112], 그러나 miR{1}}의 세포 기원은 이 연구에서 결정되지 않았습니다.

그럼에도 불구하고 모두가 아니라는 점에 유의하는 것이 중요합니다.신장질병족세포 손상이 있다. 증가비뇨기족세포소실은 다양한 사구체 질환에서 보고되었지만 상염색체 우성 다낭성 질환에서는 보고되지 않았습니다.신장질병(ADPKD) [113]. 더 중요하게는, 족세포뇨와 단백뇨 사이의 연관성은 사구체 질환에 따라 현저하게 달랐습니다.비뇨기족세포마커는 질병 특이적으로 더 잘 간주되어야 합니다[113].
4. 결론
족세포 손상은 많은 질병의 발병 및 진행에 중요한 역할을 합니다.신장질병. 소변의 족세포 유래 세포 단편 및 족세포 특이적 분자 표적은 다음의 진단 및 모니터링을 위한 바이오마커로 개발될 큰 잠재력을 가지고 있습니다.신장질병. 바이오마커 개발의 과정은 특정 마커의 식별, 측정 방법론의 결정, 적용을 위한 임상적 맥락의 결정을 포함한다(Fig. 2). 족세포 생물학에 대한 이해의 발전과 새로운 기술의 가용성으로,비뇨기족세포마커는 새로운 표적의 식별과 정량화를 위한 새로운 방법의 개발로 인해 적용 범위가 확장될 것으로 예상됩니다. 그 대가로, 요로 족세포 마커의 검증은 다음의 병태생리학에 대한 우리의 이해를 밝힐 수 있습니다.신장질병. 소변에서 족세포 및 다양한 족세포 특이적 마커의 정량화를 위한 풍부한 방법이 있습니다. 향후 10년 동안 연구 노력은 실험실 방법을 표준화, 비교 및 자동화하고 일상적인 임상 테스트에 대한 부가가치를 정의하는 데 중점을 두어야 합니다.
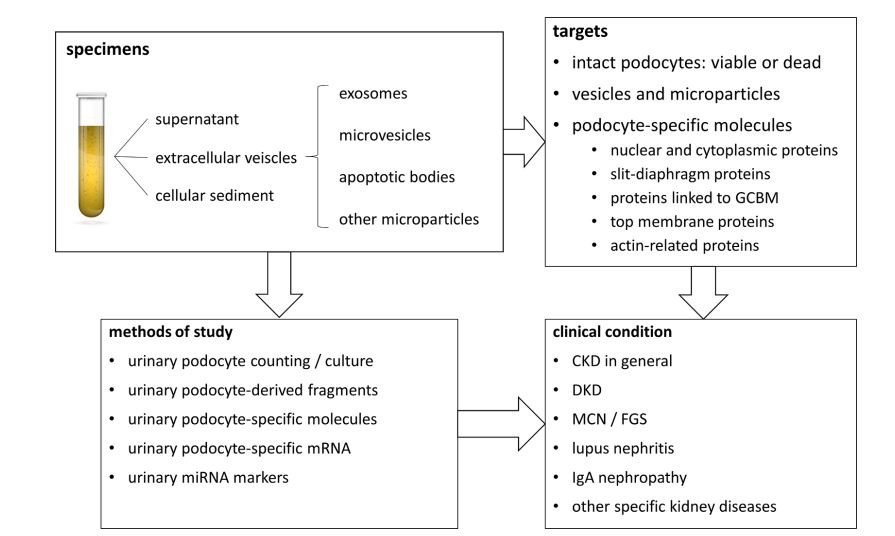
그림 2. 요로 족세포 관련 바이오마커 개발 시 고려해야 할 사항신장질병. (GCBM, 사구체 모세혈관 기저막; CKD,만성병 환자신장질병; DKD, 당뇨병신장질병; FGS, 국소 사구체 경화증).
경쟁 이익 선언
저자는 이 문서에 보고된 작업에 영향을 미칠 수 있는 경쟁적인 재정적 이해관계나 개인적 관계가 없음을 선언합니다.
승인
이 연구는 Richard Yu Chinese University of Hong Kong(CUHK) PD 연구 기금과 CUHK 연구 계정 6905134 및 8601286의 지원을 받았습니다. 기금 제공자는 연구 설계, 데이터 수집 및 분석, 출판 결정 또는 원고 준비에 아무런 역할도 하지 않았습니다. 저자는 다른 이해 상충을 선언하지 않습니다. 이 논문에 제시된 결과는 이전에 전체 또는 일부가 발표되지 않았습니다.

신장 질환 개선{0}}Cistanche acteoside
From: '소변 족세포 마커신장질병' 에 의해Lingfeng Zeng 외
---Clinica Chimica Acta 523(2021) 315–324
