새로운 미백제로 산화 그래핀 나노리본은 멜라닌 생성 메커니즘을 억제합니다
Mar 25, 2022
연락하다:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Hsin-Yu Chou, Hui-Min David Wang,* Chia-Heng Kuo, Pei-Hsuan Lu, Lin Wang, Wenyi Kang, Chia-Liang Sun*
요약:멜라닌 합성 과정에서 산화 반응은 필수적인 역할을 하며, 산화 스트레스를 줄여 멜라닌 생성을 억제하는 좋은 전략입니다. 풀러렌과 그 유도체 또는 복합체는 강력한 자유 라디칼 제거제로 간주되었으며 다층 sp2 나노카본을 추가로 적용하여멜라닌합성 억제 메커니즘. 본 연구에서 우리는 멜라닌 생성을 조절하기 위한 항산화제로 다중벽 탄소나노튜브(MWCNT), 쇼트형 MWCNT, 그래핀 옥사이드 나노리본(GONR) 및 쇼트형 GONR과 같은 새로운 나노물질을 사용했습니다. 결과는 GONR이 다른 것보다 세포 내 및 세포 외 산화 스트레스 분석 플랫폼에서 더 나은 항산화 능력을 가짐을 보여주었습니다. 우리는 GONR에 산소 함유 작용기가 있다고 제안했습니다. 2',7'-디클로로디히드로플루오레세인 디아세테이트 분석에서 우리는 GONR이 금속 이온을 킬레이트화하여 활성 산소 종을 제거할 수 있음을 발견했습니다. 분자 통찰력 관점에서 우리는 이러한 나노 물질이 소안증 관련 전사 인자 관련 유전자 발현을 감소시켜 멜라닌 합성을 하향 조절하고 단백질 발현에서 유사한 결과가 있음을 관찰했습니다. 요약하자면, GONR은 새로운 항산화제 및 피부 미백 화장품 재료로서 잠재적인 작용제입니다.

씨스탄체도소설로서의 잠재적 대리인항산화제그리고 피부 미백미용 재료.
1. 소개
피부는 인체의 외부 표면을 덮고 있는 기관입니다. 인터페이스는 환경과 접촉하기 때문에 피부층은 병원체로부터 신체를 보호하고 과도한 수분 손실을 방지하며 체온을 조절하는 등 중요한 역할을 합니다. 멜라닌 세포는 피부 표피의 기저막에서 자라며 세포 함량의 5~10%를 차지합니다. 그들은 가늘고 긴 줄무늬 모양의 수상돌기와 가지가 있는 단세포 "샘"으로 특징지어집니다. 멜라닌 세포는 인접한 표피 세포를 통해 이동하여 각 멜라닌 세포 주위에 표피 세포의 집합을 만듭니다. 피부 노화의 내부 및 외부 원인에는 여러 가지가 있으며, 그 중 하나는 햇빛으로부터의 자외선(UV)입니다.1 자외선에 노출되면 피부의 활성산소(ROS) 수치가 급격히 증가하는데, 이를 산화 스트레스라고 합니다. 살충제, 사염화탄소, 중금속, 방향족 아민, 미립자 물질 2.5(PM2.5)와 같은 여러 환경 독성 요인도 피부에 대한 산화 스트레스를 증가시킵니다. 효소 시스템, ROS로 변환하여 멜라닌 생성 경로를 유발합니다.3
ROS 외에도 영향을 미치는 많은 요소가 있습니다.멜라닌 생성, 유전자 발현, 염증, 내분비 변화 및 색소 흡수를 포함합니다.1 멜라닌 생성의 첫 번째 단계에서 티로시나제는 티로신을 페노멜라닌 및 유멜라닌으로 촉매하는 역할을 합니다. 두 안료 제조 메커니즘은 유사하며, L-티로신 하이드록실화에서 3,{3}}디하이드록시-L-페닐알라닌(L-DOPA) 및 L-DOPA가 도파퀴논으로 산화됩니다. 다음 단계에서 도파민은 소안구증 관련 전사 인자( MITF) 멜라닌을 형성합니다. 마지막으로, 멜라닌은 성숙되어 각질층 내에서 침전됩니다.4,5 이들은 기저층의 인접한 케라티노사이트에 침투하여 UV로 인한 돌연변이 또는 변형으로부터 DNA를 보호합니다. 멜라노솜 내의 성숙한 멜라닌은 각질형성세포 6-9로 옮겨지고 마침내 오래 지속되는 색소 침착으로 이어집니다. 흑점, 주근깨, 갈색/검은 반점은 때때로 남성과 여성에게 사회적 문제를 일으킵니다. 산화 스트레스를 차단하거나 티로시나제 활성을 억제하는 것은 과다 색소 침착 및 피부 질환의 증후군을 하향 조절하는 한 가지 전략입니다. 항산화제는 ROS로 인한 과다색소침착 및 세포 손상을 치료합니다. 따라서 합성된 항산화제 화합물은 스킨케어 분야에서 많은 생물학적 기능을 합니다.

그림 1.(a) 저배율파이양이온 및 고배율파이MWCNT 및 GONR의 양이온 TEM 사진. (b) 4개의 나노카본의 라만 스펙트럼. 압축 해제 후 GONR의 D 밴드는 MWCNT의 밴드보다 높습니다. (c,d) 4개의 나노카본의 X선 광전자 분광 스펙트럼을 표시합니다.
풀러렌(C60), 탄소나노튜브(CNT), 그래핀 및 그래핀 나노리본(GNR)은 전 세계적으로 널리 연구되고 있는 4가지 종류의 sp2 나노카본입니다.12 풀러렌 및 그 유도체 또는 복합체는 강력한 것으로 간주되었습니다.자유 라디칼 청소부오랫동안. Yodh et al. 수용성 C60을 이화 스트레스 유발 변성에 대한 보호제로 사용했습니다. Inject et al. C60(OH)24는 산화 스트레스가 너무 높을 때 강력한 항산화 화합물이라고 결론지었습니다. Okuda et al. C60 복합체가 NO 매개 세포 손상을 예방할 수 있다고 제안했습니다.13,14 Tong et al. C60복합체는 증가된 수준의 과산화물로 인한 뇌 관련 질병을 치료하기 위한 유망한 후보가 될 수 있음을 보여주었습니다. 실제로 일본 회사는 2006년에 화장품 용도로 강력한 항산화 활성을 가진 풀러렌을 확인했습니다. Lucente-Schultz et al. 기능화된 단일벽 CNT(SWCNT)의 산소 라디칼 소거 능력이 수지상 C60.15-19 Fenoglio et al.보다 거의 40배 더 크다는 것을 입증했습니다. 다중벽 CNT(MWCNT)가 하이드록실 또는 슈퍼옥사이드 라디칼의 외부 소스와 접촉하여 놀라운 라디칼 소거 능력을 가지고 있음을 관찰했습니다. 밀도 기능 이론 계산은 또한 자유 라디칼 소거제로서의 SWCNT 모델을 밝혔습니다. 2004년 Novoselov et al. 그래핀이 강한 양극성 전기 효과를 나타내며 전자 응용 분야에 유망할 수 있음을 처음으로 보여주었습니다. 그 후, 그들은 그래핀이 Dirac 방정식에 의해 설명된 입자의 2D 기체에 대해 독특한 전자 특성을 가지고 있음을 계속 보여주었습니다.22,23 이 두 가지 획기적인 논문에서 그래핀 기반 연구에 점점 더 많은 관심이 주어졌습니다.24-30 예를 들어, Qiu et al. 2014년에 산화 그래핀과 소수층 그래핀이 상당한 항산화 활성을 나타내며 다양한 생체 분자를 산화로부터 보호할 수 있음을 보여주었습니다.31 Han et al. 2007년에 실험적으로 GNR의 에너지 갭은 리본 폭을 변경함으로써 리소그래피 공정 동안 제어될 수 있음을 입증했습니다. 우리가 아는 한, 산화 그래핀 나노리본(GONR)의 항산화 특성에 대한 연구는 거의 없습니다. 따라서 이 연구에서 우리는 MWCNT, 짧은 MWCNT, GONR 및 짧은 GONR을 주의 깊게 준비하고 이들의 항산화 특성과 관련 결과를 체계적으로
2. 결과 및 논의
2.1. MWCNT 및 GONR의 형태.
Figure 1a shows the low- and high-magnification transmission electron microscopy (TEM) images of MWCNTs and short MWCNTs. Following acidic cutting under ultrasonication, the length of MWCNTs could be shortened from >10 μm ~ 2−3 μm. 동시에 질산 처리는 매끄러운 관 표면을 거칠게 하는 것으로 관찰되었습니다. 고배율 사진에는 일부 노치와 불규칙한 모양이 표시됩니다. 또한, 마이크로웨이브 반응을 통해 MWCNT 및 짧은 MWCNT를 사용하여 각각 GONR 및 짧은 GONR을 얻습니다. 우리는 또한 GONR과 짧은 GONR의 저배율 및 고배율 TEM 사진을 보여주었습니다. 주요 세로 압축 풀기 및 약간의 가로 절단으로 인해 GONR이 MWCNT보다 짧은 것으로 보입니다. 반면, 고배율 사진에서는 MWCNT보다 GONR의 직경이 0.11−0.18 μm 더 크게 나타나 압축 해제가 성공적임을 알 수 있었다. 유사하게, 짧은 GONR은 짧은 MWCNT보다 더 짧은 길이와 더 큰 직경을 나타냈다. 우리의 새로운 압축 해제 프로세스의 공기 압축기에서 GONR의 얇은 층 구조는 더 두꺼운 중앙 MWCNT를 유지하면서 250W의 동일한 마이크로파 전력에 대한 초기 보고서에서 얻은 것보다 적습니다.12 이는 코어-쉘 MWCNT를 의미했습니다. /GONR 이종 구조는 새로운 프로세스에서 모든 마이크로파 전력을 통해 완전히 압축 해제된 나노리본 구조 대신 나타날 가능성이 더 큽니다. 이전 연구의 짧은 GONR과 비교하기 위해34 더 높은 마이크로파 전력은 리본 측면에 더 많은 노치를 생성하고 멋지고 매끄러운 리본 가장자리를 형성하지 않았습니다. 그림 1a에서 두 가지 다른 종류의 Cu 그리드를 사용했습니다. 충분한 길이의 MWCNT 및 GONR의 경우 탄소로 안정화된 레이스 형태의 Gu grid(제품 번호 01881-F, Ted Pella, Inc., USA)가 사용되었습니다. 레이시 탄소 필름의 열린 구멍은 나노카본과 탄소 필름 사이의 중첩 투과 이미지를 방지했습니다. 짙은 회색 네트워크는 레이스 탄소 필름에 속합니다. 그러나 짧은 MWCNT 및 짧은 GONR에는 탄소로 안정화된 formvar가 있는 Gu 그리드(제품 번호 01800-F, Ted Pella, Inc., USA)가 필요했습니다. 이는 레이시 카본 필름의 큰 구멍으로 인해 짧은 MWCNT와 짧은 GONR을 효율적으로 유지하는 데 문제가 발생했기 때문입니다. 그림 1에서 볼 수 있듯이 짧은 MWCNT와 짧은 GONR 아래의 밝은 회색 대비는 가벼운 탄소층입니다. 이 탄소 층은 열 및 전기 전도성 특성을 통해 전자빔에 노출된 formvar 필름을 안정화했습니다.

그림 2.압축을 풀고 자르는 프로세스 다이어그램은 MWCNT를 GONR 및 짧은 GONR로 표시했습니다.
2.2. MWCNT 및 GONR의 결합 구성.
4개의 나노카본의 라만 스펙트럼은 그림 1b에 나와 있습니다. 압축 해제 후 GONR의 D 밴드는 MWCNT의 밴드보다 높았다. 이는 MWCNT에 비해 GONR의 더 높은 산화 수준과 더 많은 수의 에지 구조에 기인합니다. 이 현상은 2{8}}11.12에서 관찰한 것과 유사합니다. 높은 흑연화 수준으로 인해 MWCNT의 G 밴드는 최대 반값의 전체 너비가 가장 낮았습니다. 4개의 나노카본의 ID/IG 비율은 각각 {{1{12}}}.{14}}76, 0.502, 0.483, 0.700이었습니다. 간단히 말해서, 감소된 길이와 표면 산화는 결함 수준을 증가시켜 ID/IG 비율을 더 높게 만들었습니다. D' 피크는 모든 결함 있는 그래핀에 존재하며 품질의 척도로 간주됩니다.35 그림 1b에서 볼 수 있듯이 4개의 스펙트럼에서 D' 피크는 절단 또는 압축 해제 과정 후에 더 두드러져 파괴적임을 시사합니다. 많은 결함을 도입하는 프로세스. 그림 1c,d는 4개의 나노카본의 X선 광전자 분광 스펙트럼을 표시합니다. 분명히 D' 피크는 짧은 GONR에서 가장 명확합니다. 그림 1c에서 볼 수 있듯이 O 수준은 산성 환경에서 KMnO4의 강력한 산화 능력으로 인해 7.6%(MWCNT)에서 19.9%(GONR)로 크게 증가했습니다. 반면, O 수준은 MWCNT에서 short MWCNT로 0.8% 소폭 증가하였다. 중요하게도, 가장 높은 O 수준은 짧은 GONR의 경우 38.3%이며, 이는 나노리본의 끝이 평면 sp2 표면보다 산소 작용기를 부착하기 더 쉬울 것임을 의미합니다. MWCNT와 짧은 MWCNT의 압축 해제 과정 후 더 큰 전체 너비의 최대 수와 C 1s 피크의 높은 결합 에너지로의 이동이 그림 1d에 나와 있습니다. 그래핀 옥사이드의 경우, 결합 에너지가 높은 쪽의 deconvoluted 피크는 C−C(CC), C−O, CO 및 COOH 결합에 할당될 수 있습니다.36 우리는 2013년에 GONR(200W)을 특성화했습니다. ,37 및 본 연구 결과와 유사한 결과를 보였다. 이 연구는 라만 스펙트럼의 현상을 결론지었습니다. 즉, 튜브에서 리본으로의 변환 동안 더 많은 산소 함유 작용기가 생성되었음을 의미합니다(그림 2).
2.3. MWCNT 및 GONR의 항산화 특성.
2.3.1. 1,1-디페닐-2-피크릴히드라질 자유 라디칼 소거 활성 분석의 측정.
1,{1}} Diphenyl-2-picrylhydrazyl(DPPH) 자유 라디칼 소거 활성은 항산화 능력을 감지하기 위해 적용된 항산화 플랫폼입니다. 4개의 나노카본에 대한 결과는 표 2에 설명되어 있습니다. DPPH 분석에서 1{14}}0μM 농도의 비타민 C를 양성 대조군으로 사용했습니다. MWCNT, short MWCNT, GONR 및 short GONR의 항산화 활성을 테스트하기 위해 1, 5 및 1{22}} mg/L의 용량을 반응 용액에 인큐베이션하여 특성을 측정했습니다. MWCNT, 짧은 MWCNT, GONR 및 짧은 GONR은 10 mg/L(19.2 ± 0.3, 12.1 ± 0.3, 26.8 ± 0.3 및 30.0 ± 0.4%), 비타민 C는 억제에 대해 100μM(93.4 ± 0.1%)에서 유사한 조건을 보였습니다.

표 1. 이 연구에서 사용된 프라이머의 뉴클레오티드 서열
2.3.2. 이온 킬레이트화 활성 분석.
산화 스트레스 상황 내에서 페로진은 Fe2 플러스와 착물을 형성하여 정량적으로 측정할 수 있습니다. 킬레이트 매개체의 존재하에 착물이 파괴되어 철 이온이 Fe2 플러스 착물의 암적색에서 환원되도록 합니다. 우리는 EDTA를 양성 대조군으로 사용했습니다. 표 2는 MWCNT, 짧은 MWCNT, GONR 및 짧은 GONR이 10 mg/L(29.2 ± {{1{14}}}}.8, 28.7 ± 0 .7, 69.7 ± 0.6 및 68.9 ± 0.3%) 반면 양성 대조군은 100μM(93.4 ± 0.1%)에서 유사한 조건을 보였습니다.
2.3.3. 제2철 환원 항산화력 측정.
제2철 환원 전위 분석은 Fe(III)-페리시안화물 복합 합성을 정량화하는 데 사용되는 간단하고 신뢰할 수 있는 테스트입니다. 이 분석에서 Fe(III)-TPTZ 철 복합체를 생성하는 4개의 나노카본의 환원력은 노란색에서 녹색 및 파란색으로 용액의 색상 변화에 의해 감지되었습니다. 표 2는 MWCNT, short MWCNT, GONR 및 short GONR의 환원력이 10 mg/L에서 광학 밀도(OD) 1.11, 1.13, 1.15 및 1.11임을 보여줍니다.
2.3.4. MWCNT 및 GONR은 세포 내 ROS 축적을 억제합니다.
많은 보고에 따르면 ROS는 세포막과 핵막을 포함한 세포막의 구조적 완전성을 파괴하여 세포 손상과 정상적인 기능 상실을 초래한다는 것을 보여주었습니다.38-40 또한 ROS는 티로시나제 형성을 촉매하는 중요한 요소 중 하나입니다 멜라닌, ROS 생성 억제는 멜라닌 합성을 하향 조절하는 좋은 전략입니다. 이 연구에서 우리는 MWCNT 및 GONR 처리 세포에서 세포 내 산화 스트레스 수준을 분석하기 위해 2',7'-디클로로디히드로플루오레세인 디아세테이트(DCFDA) 염색 분석을 사용했습니다. Phorbol 12-myristate 13-acetate(PMA)는 MWCNT 및 GONR 그룹에서 산화 자극을 유도하여 음성 대조군으로 사용했습니다.41 PMA의 농도가 20ng/mL일 때 산화 스트레스를 유도하여 증가 값을 38%로 설정합니다. GONR과 MWCNT를 처리한 후, ROS의 수준은 정상 수준으로 하향 조절되었습니다. 데이터는 두 재료 모두 산화 스트레스 수준을 억제했으며 GONR의 항산화 효과가 MWCNT보다 더 높음을 보여주었습니다(그림 3). 표 1은 유사한 결과 목록을 보여줍니다. 우리는 새로운 발견에 대한 세 가지 이유가 있다고 주장했습니다. 첫째, 이러한 재료의 용해도 순서는 다음과 같습니다. 짧은 GONR > GONR > 짧은 MWCNT > MWCNT, 즉 짧은 GONR의 접촉 면적이 가장 컸으므로 다음과 같았습니다. ROS 소거에 탁월합니다. 둘째, GONR과 MWCNT는 부가물 형성이나 전자 전달을 통해 ROS 전기를 파괴할 수 있는 sp{13}}탄소 구조였습니다.42 우리는 나노리본 구조의 항산화 효과가 나노튜브 구조의 항산화 효과보다 우수함을 발견하여 나노리본이 나노튜브보다 전자를 전달하기 쉽다. 마지막으로, 그림 1b에서 GONR sp{16}}탄소 부위에는 MWCNT보다 더 많은 산소 작용기가 포함되어 있고, 카르복실산기는 금속 이온을 킬레이트할 수 있으며, 히드록실기는 ROS 및 멜라닌 생성을 억제합니다.
2.4. 인간 진피 섬유아세포에서 치료된 MWCNT 및 GONR의 세포독성.
{{0}}(4,5-Dimethylth-iazol-2-yl)-2,5-diphenyltetrazolium bromide(MTT) 방법을 적용하여 Hs68 세포에 대한 GONR의 세포독성 특성(그림 3) 및 세포를 1, 5 및 10ug/mL의 다양한 용량에서 배양했습니다. 우리는 MWCNT의 세포 생존율이 1, 5 및 10 mg/L의 농도에서 각각 100.7 ± 3.7, 99.8 ± 4.9 및 94.1 ± 4.7%임을 조사했습니다. 짧은 MWCNT에 대한 생존율은 같은 순서로 계산되었으며 93.9 ± 2.2, 86.4 ± 3.0 및 98.9 ± 2.1%인 것으로 나타났습니다. 우리는 B16-F10 세포가 고농도에서 배양되었고 Hs68 세포의 세포 생존이 80% 이상임을 관찰하여 MWCNT와 짧은 MWCNT가 인간 진피 섬유아세포에 독성 효과가 없음을 시사합니다. GONR 및 short GONR의 세포 생존율은 86.24 ± 2.1, 90.87 ± 3.5, 88.58 ± 2.5, 89.03 ± 3.6, 90.71 ± 2.8 및 90.64 ± 2.5%였습니다. 또한 그림 4a에서 GONR과 짧은 GONR이 HS68 세포에 대해 식별 가능한 세포독성 효과를 나타내지 않았음을 지적합니다. 이전 보고서에서 미용 목적으로 테스트되지 않은 나노 물질의 사용은 의심스러운 것으로 간주될 수 있으며43,44 이는 일반적으로 나노 입자가 세포에 들어간 후 DNA의 공격 때문이었습니다. 세포 독성 시험 결과 우리 물질이 정상 피부 세포에 독성을 일으키지 않는 것으로 나타났습니다. 우리는 나노 물질이 세포에 들어간 후 나노 물질이 산화 스트레스를 감소시키고 금속 이온을 킬레이트함으로써 멜라닌 생성을 억제하고 미토콘드리아 또는 DNA를 손상시키지 않는다는 결론을 내렸습니다. 이는 MWCNT 및 GONR이 사용하기에 안전하다는 것을 의미합니다.
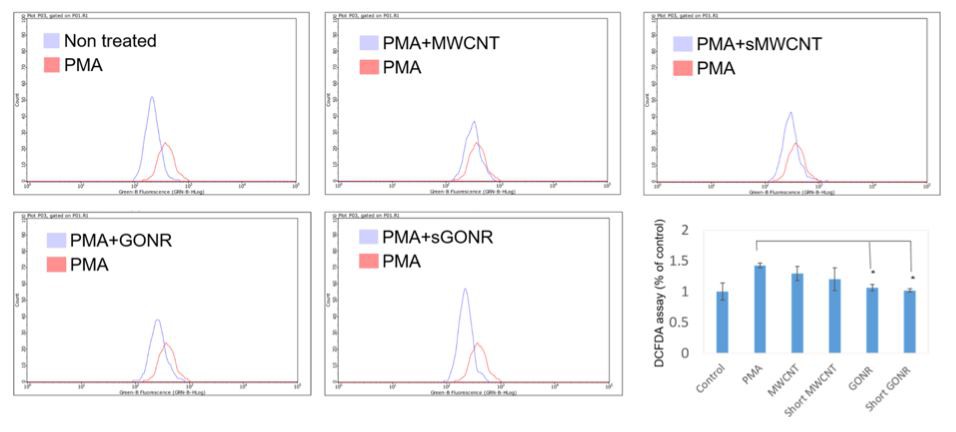
그림 3.MWCNT 및 GONR 처리가 B16 F10 세포에서 ROS 생성을 감소시켰음을 보여주는 DCFDA 분석 결과.
2.5. B16-F10 세포 티로시나아제 활성 및 멜라닌 함량에서 두 가지 유형의 MWCNT 및 GONR.
멜라닌 합성 경로에서 티로시나아제는 중요한 역할을 합니다. Tyrosinase는 일련의 생화학적 반응을 통해 산화되고 유멜라닌과 페오멜라닌을 형성합니다. GONR과 MWCNT가 tyrosinase의 활성을 억제하고 멜라닌 생성을 감소시키는지 확인하기 위해 B16-F10 세포에서 tyrosinase 활성을 분석했습니다. 우리는 MWCNT와 짧은 MWCNT가 10mg/L에서 약 17.1%와 23%까지 티로시나제 활성을 억제한다는 것을 발견했습니다. GONR과 짧은 GONR은 다른 GONR에 비해 동일한 농도에서 tyrosinase 활성을 억제하는 데 더 나은 효과를 보였습니다. 그들은 또한 그림 4b와 같이 용량 의존적 방식으로 티로시나제 활성의 49.8%와 44.7%를 억제했습니다.
멜라닌은 인체에 없어서는 안될 색소이지만 멜라닌의 과발현은 종종 일련의 질병을 유발합니다. 이전 연구에서 Xiao et al. 유사한 물질인 Radical Sponge(풀러렌 나노입자)를 항멜라닌 제제로 사용했습니다.45 몇 가지 좋은 결과가 있었습니다. 멜라닌 생성의 약 2{11}}%가 억제될 수 있습니다. 효율성을 향상시키기 위해 그림 4c와 5와 같이 멜라닌의 억제율과 분자 메커니즘을 측정하는 시험 물질을 더욱 개선했습니다. MWCNT와 짧은 MWCNT는 멜라닌 함량을 17.6 ± 5.5 및 13.2 ± {{ 16}} 10 mg/L에서 용량 의존적 방식으로 0.2%. GONR 및 짧은 GONR은 10mg/L에서 값을 32.0 ± 2.3 및 35.3 ± 3.4%로 강력하게 하향 조정했습니다. 실험 결과 4가지 유형 모두 멜라닌 합성을 억제할 수 있으며 GONR이 더 강력한 효과를 나타냅니다. 반면에, 우리는 짧은 GONR이 멜라닌 생성을 억제하는 데 더 나은 효과가 있음을 관찰했습니다. 우리는 짧은 GONR이 더 많은 작용기를 가지며 금속 이온 촉매 티로시나아제를 효과적으로 방지하여 멜라닌 생성을 더욱 억제할 수 있다고 결론지었습니다(그림 2). 표 1에서 우리는 금속 이온 킬레이트 짧은 유형의 노력이 일반 유형보다 높은 것을 관찰합니다. 이것은 이러한 짧은 GONR이 잠재적으로 화장품 분야에서 스킨 케어 제제로 적용될 수 있음을 의미합니다.
2.6. MWCNT 및 GONR의 메커니즘은 B16-F10 세포의 멜라닌 함량을 억제합니다.
세포는 단백질 발현을 조절하여 외부 산화 스트레스에 반응합니다. B16-F10 세포는 c-myc 유전자 발현을 향상시키고 AMPK를 상향 조절하여 산화 수준을 감소시키며, 이 연구에서 MITF는 분자 멜라닌 합성 신호 경로를 조절하는 티로시나제의 특정 전사 인자입니다.47-49 그림에서 도 5a에서 볼 수 있듯이, MWCNT와 GONR은 산화 스트레스를 감소시켜 소안구증 관련 전사 인자를 하향 조절한 다음, 다운스트림 유전자 TRP{10}}와 TRP{11}}도 하향 조절했습니다. 단백질 수준의 경우 MWCNT와 GONR이 MITF 관련 멜라닌 생성 경로를 하향 조절한 다음 최종적으로 멜라닌 함량을 감소시키는 유사한 현상이 발견되었습니다(그림 5b).
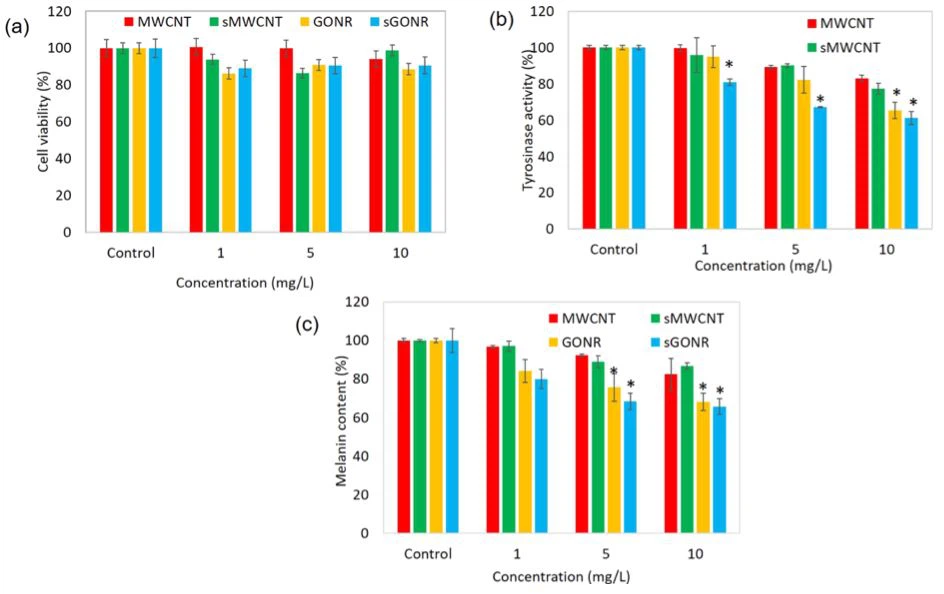
그림 4.
3. 실험 재료 및 방법
3.1. MWCNT 및 GONR의 준비.
GONR을 만드는 관련 공정은 이전 논문에 보고되었습니다.12 MWCNT(0.{13}}5g)를 9:1 H2SO4/H3PO4에 현탁시키고 마이크로파 반응기(CEM-Discover)로 처리했습니다. 2분 동안 250W로 설정된 전력으로. 용액에 KMnO4(0.25g)를 첨가한 후, 용액을 65도에서 4분 동안 동일한 마이크로파 전력으로 처리했습니다. 그런 다음 공기 압축기를 사용하여 8분의 더 짧은 2단계 마이크로파 시간을 사용하여 이 프로세스를 수정했습니다. 여기서 공기 압축기는 공정 중 마이크로파 반응기의 온도를 제어하는 데 사용됩니다. 마이크로파 전력은 예비 테스트에서 250W로 설정되었습니다.
3.2. 짧은 MWCNT 및 짧은 GONR의 준비.
짧은 GONR을 만드는 관련 프로세스는 이전 논문에서 보고되었습니다.34 산성 처리 시간은 8시간으로 선택되었습니다. 마이크로파 전력은 GONR을 얻는 것과 동일한 250W로 설정되었습니다.
3.3. DPPH 라디칼 소거 활동.
DPPH는 시료의 소거 능력과 항산화 특성을 결정하는 데 자주 사용되었습니다.50 DPPH는 자유 라디칼이 분석물로 전달되면 색상이 보라색에서 노란색으로 변하는 보라색 시약입니다. 적절한 농도의 긍정적인 항산화 샘플을 용액에 첨가하고 샘플을 517 nm에서 30분 동안 분석했습니다. 우리는 이전 DPPH 라디칼을 감소시키는 데 필요한 항산화제의 양을 측정하기 위해 테스트 샘플 외에 나머지 DPPH의 백분율을 사용했습니다. 100μM의 비타민 C를 양성 대조군으로 사용했습니다. 소거 활성(%)은 다음과 같이 측정되었습니다.
소거 능력(백분율)=(Asample - Ablank) / (Acontrol - Ablank) × 100%(1)
3.4. 금속 킬레이트화 활동.
금속 이온은 지질 과잉 산화를 일으키는 요인이며 Fe2 plus는 가장 영향을 미치는 이온 중 하나입니다. (10 μL), 그런 다음 페로진(5 mM, 20 μL)에 로드했습니다. 혼합물을 69 μL 멘톨과 완전히 혼합하고 실온에서 10분 동안 유지했습니다. 그 후, 샘플 반응 용액은 562 nm에서 관찰되었다. EDTA는 100 μM에서 양성 대조군으로 사용되었으며 금속 킬레이트 활성 계산식은 eq 1을 기반으로 하였다.

그림 5.다양한 농도(0, 15, 10)로 처리된 B16 F1{2}} 세포의 멜라닌 생합성과 관련된 RNA 및 단백질 발현μg/mL) MWCNT 및 GONR.
3.5. 전력 감소.
환원력 계산은 이전 연구를 기반으로 합니다.50 먼저 2.5μL 그래핀 재료를 PBS 버퍼(67mM, pH 6.8) 및 K3Fe(CN)6(2.5μL, 20%)와 혼합한 다음 50도에서 배양했습니다. 20분 동안 그런 다음, 10% 트리클로로 아세트산(160μL)을 300g의 시약과 혼합하고 20분 동안 원심분리했습니다. 25 μL FeCl3(2%)와 혼합한 후 700 nm에서 흡수 길이를 측정했습니다. 부틸화 하이드록시아니솔(BHA)은 100μM에서 사용되었습니다.
3.6. 세포 증식 검사.
인간 진피 섬유아세포 세포주 HS68을 사용하여 세포 증식 비율을 분석하였다. HS68은 10% 소태아혈청과 1% 페니실린과 스트렙토마이신이 혼합된 Dulbecco의 변형된 Eagle 배지(DMEM)에서 배양되었습니다.50,51 다양한 농도의 샘플로 처리한 후 MTT를 적용하여 세포 증식 비율을 측정했습니다. 8000개의 세포를 96-웰 플레이트에 파종하고 24시간 동안 샘플로 처리했습니다. 상등액을 제거하고 MTT 용액을 사용하여 37도에서 2시간 동안 배양하였다. 인큐베이션 후 MTT가 포함된 배지를 제거하고 DMSO(디메틸 설폭사이드)로 용해했습니다. 용액은 OD 590 nm에서 판독되었고 속도는 eq 1에 의해 계산되었습니다.
3.7. 세포 멜라닌 함량 평가.
우리는 이전 분석을 기반으로 약간 수정된 방법을 사용했습니다.52,53 Bioresource Collection and Research Center(BCRC, CRL 6323, Hsinchu, Taiwan)의 B16-F10 세포 펠렛을 2.0 혼합물에 용해했습니다. N NaOH 및 10% DMSO. 이어서 샘플을 90도에서 1시간 동안 가열하고 10.g에서 추가로 10분 동안 원심분리하여 맑은 상층액을 얻었다. 멜라닌 수는 475 nm에서 상청액의 OD를 모니터링하여 결정되었습니다.
3.8. B16-F10 세포성 티로시나제 활성.
B16−F10 세포성 티로시나제 활성에 대해서는 일부 수정된 이전 작업을 참조했습니다. 50세포는 각 웰에 105개 세포의 12-웰 플레이트에서 배양되었습니다. 샘플로 처리한 후 세포를 1% Triton X{6}}/PBS 및 2mM L-티로신(50μL)에서 3시간 동안 용해했습니다. 배양 후 배지를 제거하고 OD 590 nm에서 흡광도를 읽었습니다. 티로시나아제 활성 공식은 식 1에 의해 계산되었습니다.

Cistanche는 티로시나제 억제제입니다.
3.9. DCFDA 염색에 의한 ROS 검출.
이전 연구를 참조하면{0}}.{1}}.105 B16−F10 세포를 6-웰 플레이트에 파종하고 다양한 농도의 샘플로 처리했습니다. 세포를 PBS에 현탁시킨 다음 37도에서 30분 동안 비페놀 레드 DMEM에 DCFDA(5μM)를 로딩하였다. DCFDA의 형광 신호를 검출하기 위해 유세포 분석기(Guava, Merck, Germany)를 사용하였다. DCFDA의 여기 및 방출 파장은 각각 488 및 535 nm였습니다.
3.10. 정량적 실시간 중합효소 연쇄 반응.
우리는 Lin et al.의 방법을 따랐습니다. (2018).1 실시간 정량적 역전사 중합효소 연쇄 반응(qRT-PCR)은 형광을 생성하는 전용 프라이머 프로브로 구성되었습니다. 7500 qRT-PCR System(Applied Biosystems, USA)을 사용하여 각 주기를 감지하는 형광 검출 기술을 사용했습니다. 방출된 형광량을 기준으로 주기를 감지하고 생성된 함량에 대해 주기별 곱을 계산하여 실시간 정량적 목적을 달성하였다. Trizol(Invitrogen, USA)을 사용하여 제조업체가 제공한 지침에 따라 폐 조직의 완전한 RNA를 추출했습니다. 이어서 역전사 키트(Takara, Japan)를 사용하여 DNA를 생성하였다. 표 1에 나열된 프라이머를 사용한 qRT-PCR에서 먼저 샘플을 가열하여 단일 가닥의 DNA를 형성했습니다. 그런 다음 프라이머 결합이 발생하여 이중 가닥 DNA(dsDNA)를 형성한 후 SYBR Green dsDNA를 결합하여 SYBR 녹색 플러스 시약 키트(Roche, Basel, Swiss)를 사용하여 형광을 방출했습니다. 결과물을 형광 검출 시스템에 통과시켰다. 형광 신호의 검출은 각 주기의 신장 또는 어닐링 단계 동안 발생했습니다. 검출 후, 검체 내용물은 검출된 형광 강도에 의해 back-push되었다. 표적 유전자의 발현 수준은 2-ΔΔCt 방법을 사용하여 -tubulin 수준으로 정규화되었다.

미리세틴
3.11. 웨스턴 블롯 테스트.
B16-F10 세포는 protease inhibitor가 들어있는 radioimmunoprecipitation assay buffer(Thermo Scientific Co., USA)를 이용하여 4도에서 밤새 용해시켰다. bicinchoninic acid protein assay kit(BCA, Sigma-Aldrich Corp., USA)를 이용하여 단백질 양을 정량하였다. 샘플 단백질을 10% 나트륨 도데실 설페이트-폴리아크릴아미드 겔에서 분리하고 폴리비닐리덴 디플루오라이드(PVDF) 멤브레인(PALL Life Science, Ann Arbor, MI, USA)으로 옮겼습니다. PVDF 막을 차단 완충액(Thermo Scientific)으로 1시간 동안 차단하고 특정 1차 항체와 함께 4도에서 밤새 인큐베이션하였다. 다음으로, 막을 Tris 완충 식염수-Tween 20 완충액으로 두 번 세척하고 이차 항체와 함께 1.5시간 동안 인큐베이션했습니다. 그 후, 막을 화학발광 검출 시약(Thermo Scientific)에 담그고 MiniChemi 화학발광 이미저(Beijing Sage Creation Science, 중국)로 분석했습니다. 항체 공급원에는 토끼 항-MITF, 토끼 항-TRP{14}}, 토끼 항-TRP{16}} 및 -액틴(Thermo Scientific)이 포함되었습니다.
3.12. 재료 분석.
TEM(JEOL JEM-1230, 100kV)을 이용하여 나노카본의 형태를 관찰하였다. 마이크로 라만 분광계(PTT, RAMaker)를 적용하여 나노카본의 공명 모드를 확인하였다. X선 광전자 분광법(XPS, Kratos Axis Ultra DLD) 측정도 구성 분석을 결정하기 위해 수행되었습니다.12,34
3.13. 통계 분석.
모든 샘플과 표준 실험은 적어도 세 번 반복되었습니다. 평균값 ± 표준편차의 평균값을 통계적으로 비교하여 표현하기 위해 Student's t-test를 적용하였다.
4. 결론
요약하면, 짧은 GONR이 다양한 생체 기능 특성으로 인해 스킨케어 제품의 잠재적 재료임을 관찰했습니다(그림 6). 결과는 나노카본이 세포외 및 세포내 항산화제 역할을 한다는 것을 보여주었다. 한편, 나노카본은 티로시나아제 활성과 멜라닌 함량을 억제하여 색소 세포에 심각한 손상을 일으키지 않았습니다. 이 작업은 4가지 유형의 나노카본의 멜라닌 생성 방지 기능을 확립했습니다. 향후 연구에서는 멜라닌 성숙, 수송 및 축적과 관련된 특정 유전자 및 단백질 발현에 대한 이러한 화합물의 메커니즘을 조사할 것입니다.

