암의 APOBEC{0}}매개 돌연변이 유발:원인, 임상적 중요성 및 치료 가능성
Oct 17, 2023
추상적인
아포지단백질 B mRNA 편집 효소, 촉매 폴리펩티드(APOBEC)는 선천성 및 적응성 면역에 관여하는 시토신 탈아미노효소입니다. 그러나 일부 APOBEC 계열 구성원은 숙주 게놈을 제거하여 발암성 돌연변이를 생성할 수도 있습니다. 주로 시그니처 2와 13인 결과 돌연변이는 많은 종양 유형에서 발생하며 암에서 가장 흔한 돌연변이 시그니처 중 하나입니다. 이 검토에서는 APOBEC3을 주요 돌연변이원으로 암시하는 현재 증거를 요약하고 APOBEC3 발현 및 돌연변이 활동의 외인성 및 내인성 유발 요인에 대해 간략하게 설명합니다. 이 검토에서는 또한 APOBEC3- 매개 돌연변이 유발이 운전자 돌연변이 유도 및 종양 면역 미세 환경 조절을 포함하여 돌연변이 유발 및 비돌연변이 유발 경로를 통해 종양 진화에 어떻게 영향을 미치는지 논의합니다. 분자 생물학에서 임상 결과로 이동하면서, 검토는 암 유형 전반에 걸친 APOBEC3의 다양한 예후 중요성과 현재 및 미래의 임상 환경에서의 치료 잠재력을 요약함으로써 결론을 내립니다.
키워드 APOBEC, 암, 체세포 돌연변이, 생식계열 유전학, 종양 미세환경, 바이오마커, 면역요법

한약재 시스탄체 식물-항종양
배경
폴리펩티드(APOBEC)는 APOBEC1, AID(Activation-Induced Deaminase), APOBEC2, APOBEC3(A-H) 및 APOBEC4 등 11개의 주요 계열 구성원을 포함하는 시토신 탈아미노효소의 한 종류입니다. APOBEC3B, APOBEC3H 및 APOBEC3F의 대체 스플라이싱은 APOBEC 슈퍼패밀리를 더욱 다양화합니다[1-4]. 모든 APOBEC 계열 구성원은 보존된 촉매 도메인을 공유하지만 서로 다른 기능, 돌연변이 기질 및 조직 발현 패턴을 가지고 있습니다[5]. 예를 들어, AID는 활성화된 B 세포에서 발현되며 면역글로불린 유전자를 탈아미노화하여 항체 다양화를 촉진합니다[6]. 대조적으로, APOBEC1은 소장에서 발현되며 mRNA를 편집하여 잘렸지만 기능적으로 중요한 위장 단백질의 조직 특이적 발현을 가능하게 합니다[7-9]. APOBEC3은 인간 조직 전체에서 훨씬 더 광범위하게 발현되며 선천적 면역 반응의 일부로 바이러스 게놈을 탈아미노화하여 손상시킵니다[10]. APOBEC3은 바이러스 감염으로부터 세포를 보호하지만 숙주 DNA를 돌연변이에 취약하게 만듭니다. APOBEC3- 매개 돌연변이 유발은 시토신 탈아미노화로 시작되며, 모든 APOBEC3은 다양한 수준의 효소 활성을 통해 단일 가닥 DNA(ssDNA)를 탈아미노화할 수 있습니다[11-13]. APOBEC3에 대한 ssDNA 기질은 DNA 복제, 전사 및 게놈 복구와 같은 정상적인 세포 과정 중에 이중 가닥 게놈에서 일시적으로 발생할 수 있습니다. 예를 들어, APOBEC3A와 APOBEC3B는 모두 DNA 복제 중에 지연 가닥 주형을 제거할 수 있습니다[14-16]. APOBEC3A는 DNA 복제 중에 형성되는 헤어핀 루프에도 작용할 수 있는 반면, APOBEC3B는 전사 중에 R 루프를 우선적으로 제거합니다[17, 18]. APOBEC3G는 전사 중에, 특히 5' UTR 내에서 ssDNA에 유사하게 작용할 수 있습니다[15]. 또한 APOBEC3G는 펼쳐진 ssDNA와 느슨하게 접힌 ssDNA를 제거하는 것으로 나타났습니다(그림 1)[19].

그림 1 APOBEC3-매개 돌연변이 유발을 위한 메커니즘과 선호되는 기질. 상단 패널: APOBEC3은 ssDNA를 탈아미노화하여 DNA 주형에 우라실을 남깁니다. 잘못된 복제 및 복구 경로는 돌연변이 시그니처 2와 13을 생성할 수 있습니다. TLS(병변병변 합성) 폴리머라제 REVI에 의한 복구는 C-to-G 돌연변이(서명 13)를 생성하는 반면, DNA 폴리머라제 δ, DNA 폴리머라제와 같은 다른 효소에 의해 복구됩니다. ε, 그리고 TLS 중합효소 κ는 C에서 T로의 돌연변이를 생성합니다(서명 2)[20]. 하단 패널: APOBEC3 슈퍼패밀리 중 주요 돌연변이체는 주로 트리뉴클레오티드 컨텍스트와 ssDNA 2차 구조에 의해 정의되는 뚜렷한 기질 선호도를 가지고 있습니다.
ssDNA 내에서 다양한 APOEBC3은 서로 다른 삼중뉴클레오티드 상황에서 시토신을 탈아미노화합니다. 예를 들어, 주요 돌연변이체인 APOBEC3A 및 APOBEC3B는 티아민 선행 시토신(TpC) 모티프를 탈아미노화합니다. APOBEC3A는 피리미딘 다음으로 TpC 모티프에 우선적으로 작용하는 반면, APOBEC3B는 퓨린 다음으로 TpC 모티프를 제거하는 경향이 있습니다[20-23]. 탈아미노화 후, 다양한 세포 과정은 C-toT 및 C-to-G 돌연변이를 생성할 수 있으며, 이는 각각 COSMIC에서 시그니처 2 및 13으로 정의됩니다[24-26]. 이전의 C에서 T로의 전환은 더 일반적이며 우라실 함유 DNA 주형의 비정상적인 복제로 인해 발생하는 반면, 두 치환 모두 우라실 글리코실라제 활성에 의해 생성된 염기 부위의 잘못된 복구를 통해 발생할 수 있습니다(그림 1) [20, 27-29 ]. 이러한 전통적으로 정의된 APOBEC3-유발 돌연변이 시그니처 외에도 APOBEC3G는 TCC, GCC, CCC, CCT 및 GCG 모티프에서 C에서 T로의 전환을 일으킬 수 있습니다(그림 1)[30]. APOBEC3- 유발 돌연변이는 암 어디에나 존재하며 게놈 전체 또는 클러스터에 분산되어 발생할 수 있습니다. 종양 게놈에서 kataegis의 75% 이상이 APOBEC3 활성에 기인한 반면, 더 확산된 omikli 과돌연변이의 15%는 이에 기인합니다[31, 32]. 전체적으로, APOBEC3- 유발 돌연변이는 종양 돌연변이 부담의 최대 68%를 구성할 수 있으며 전체 종양의 절반 이상에서 발견됩니다. 연령 관련 서명만이 더 일반적입니다[26, 27, 33]. APOBEC3-에 의해 유발된 변형의 대부분은 종양 유전자 및 종양 억제 인자에 영향을 미치는 재발성이 높은 구동 돌연변이이며, APOBEC3은 종양 미세 환경의 면역 조절과 같은 비돌연변이 경로를 통해 질병 과정에 영향을 미칠 수도 있습니다.
풀 사이즈 테이블

APOBEC3은 면역 활성화 또는 면역 억제 표현형을 촉진할 수 있으며, 이는 암 유형에 따른 다양한 예후 중요성을 부분적으로 설명할 수 있습니다. 임상 연관성과 전임상 연구를 바탕으로 APOBEC3은 바이오마커로 사용될 수 있으며 치료법의 표적이 될 수 있습니다. 따라서 APOBEC3-매개 돌연변이 유발의 원인과 임상적 의미는 중요한 연구 분야이자 본 리뷰의 초점입니다.
암에서 APOBEC3의 발현
APOBEC3은 많은 건강한 조직에서 낮은 수준으로 발현되지만 종양에서는 종종 과발현됩니다. 대부분의 연구에서는 APOBEC3 발현을 검출하기 위해 RNA 기반 프로파일링을 사용했으며, 단백질 기반 분석은 더욱 제한적이었습니다(표 1). APOBEC3B는 일반적으로 다른 APOBEC3 계열 구성원보다 더 높은 수준으로 발현되며, 여러 암에 대한 분석을 통해 방광, 유방, 두경부, 폐 선암종, 폐 편평 세포 암종, 전립선, 투명 세포 신장, 암종 등 8가지 종양 유형에서 APOBEC3B가 농축된 것으로 확인되었습니다. 그리고 자궁 [34]. 건강한 조직은 비교할 수 없었지만 자궁경부암과 피부암에서도 높은 APOBEC3B 발현이 관찰되었습니다[34]. 마찬가지로 방광, 담관, 폐, 위, 식도, 신경내분비 및 난소 종양에서 높은 APOBEC3B 수준이 보고되었습니다[35-43]. 다른 APOBEC3의 발현도 암에서 조절 장애가 있을 수 있습니다. 예를 들어, APOBEC3G는 결장 및 췌장 종양에서 높은 수준으로 발견되었습니다[49, 50]. 유방암에서 연구에 따르면 APOBEC3A, APOBEC3B 및 APOBEC3H의 농축이 발견되었습니다[27, 48]. 다발성 혈액암에서도 높은 APOBEC3 발현이 관찰되었습니다. 예를 들어, APOBEC3A 농축은 백혈병에서 나타났고, APOBEC3B와 APOBEC3C는 모두 원발성 삼출성 림프종에서 높은 수준으로 발견되었습니다[45, 52].

cistanche tubeulosa-항종양의 장점
주요 돌연변이 원인 APOBEC3A 및 APOBEC3B
여러 연구에서 APOBEC3 발현과 시그니처 특이적 돌연변이 부담 사이의 상관관계가 확인되었으므로 APOBEC3 과발현은 돌연변이 유발을 촉진할 가능성이 높습니다(표 1). 여러 종양 유형의 결합 분석에서 APOBEC3B 발현은 더 높은 APOBEC3-유발 돌연변이 부하와 강력하게 연관되어 있었습니다. APOBEC3A, APOBEC3F, APOBEC3G는 유사하지만 약한 상관관계를 보였습니다[27]. 높은 APOBEC3B 발현은 또한 폐암에서 더 많은 APOBEC3- 유도 돌연변이와 관련이 있는 반면, APOBEC3A 및 APOBEC3B 수준은 모두 유방암에서 APOBEC3- 유도 돌연변이와 상관관계가 있었습니다[22, 47, 53, 54]. APOBEC3- 유발 돌연변이 부담이 가장 높은 방광암에서도 유사한 연관성이 관찰되었습니다[1, 27, 34, 46]. 담관암종에서는 APOBEC3A 발현만이 APOBEC{25}}유발 돌연변이 부담과 관련이 있었습니다[43]. 이러한 상관관계는 APOBEC3A와 APOBEC3B가 둘 다 돌연변이 유발에 기여한다는 것을 시사하지만 이들 계열 구성원의 상대적 중요성은 여전히 논란의 여지가 있습니다[47, 58]. APOBEC3B는 많은 종양에서 더 높은 발현을 보이기 때문에 종종 주요 돌연변이인 것으로 추정됩니다[22, 26, 34-36, 45, 48, 59]. 그러나 APOBEC3A는 더 큰 효소 활성을 가지므로 일반적으로 조직 발현이 낮음에도 불구하고 더 많은 돌연변이를 생성할 수 있습니다[47, 60]. 따라서 APOBEC3 녹아웃 세포주를 비교하면 APOBEC3A 결핍이 돌연변이 유발에 가장 큰 영향을 미치는 것으로 나타났습니다 [58]. 이 결과는 처음으로 APOBEC3A 및 APOBEC3B에 의해 유발된 돌연변이를 구별하고 전자가 종양 게놈에 더 풍부하다는 것을 발견한 효모의 초기 연구 결과를 확증합니다[23]. APOBEC3A가 주요 돌연변이인 것으로 더 암시되어 APOBEC3B의 5' UTR에 융합된 APOBEC3A 코딩 영역의 키메라를 생성하는 APOBEC3B 생식계열 결실은 일부 암에서 더 많은 APOBEC 유발 돌연변이와 연관되어 있습니다[61-64]. 다른 APOBEC3 계열 구성원은 APOBEC3A와 APOBEC3B를 모두 제거했음에도 불구하고 시그니처 2와 13의 획득이 크게 감소했지만 계속해서 시험관 내 분석에서 감지됨에 따라 돌연변이를 유도할 가능성이 높습니다[58]. APOBEC3H는 특히 강력한 효소 활성과 증가된 핵 위치를 갖는 APOBEC3H 일배체형 I이 있는 암에서 이러한 잔류 돌연변이 유발에 기여할 수 있습니다[65]. APOBEC3G는 발현이 뚜렷한 돌연변이 특징과 연관되어 있기 때문에 돌연변이를 일으킬 수도 있습니다[30]. 따라서 다중 APOBEC3은 암에서 돌연변이를 유도할 수 있으며, 가장 중요한 돌연변이는 종양에 따라 잠재적으로 다양합니다.
APOBEC3 매개 돌연변이 유발의 외인성 및 내인성 유발 요인
바이러스 감염
APOBEC3s는 폴리오마바이러스, 파보바이러스, 헤르페스바이러스, B형 간염 바이러스를 포함한 다양한 바이러스에 의해 유도되는 인터페론 자극 유전자입니다[66]. 따라서 많은 바이러스 관련 암은 돌연변이 시그니처 2와 13의 부하가 높습니다. 예를 들어 자궁경부암은 95% 이상의 사례에서 인유두종 바이러스(HPV)에 의해 발생하며 APOBEC3-으로 인한 돌연변이가 풍부합니다[67 , 68]. APOBEC에 의해 유발된 돌연변이는 두경부 편평 세포 암종(HNSCC)에서도 흔하며, HPV 양성과 돌연변이 특징 2와 13 사이에 강한 상관관계가 있습니다[69]. 바이러스 감염은 전통적으로 바이러스와 관련된 것으로 이해되지 않는 일부 암에서 APOBEC3-매개 돌연변이 유발에 기여할 수도 있습니다. "뺑소니" 가설에 따르면, 바이러스 감염은 종양 형성 초기에 APOBEC3 활성을 유발할 수 있지만 종양이 발견되기 전에 제거됩니다[70]. BK 폴리오마바이러스(BKPyV) 양성 소변의 병력이 방광암 위험 증가와 연관되어 있기 때문에 이 가정은 일부 방광암 사례와 관련이 있을 수 있습니다[71]. BKPyV 감염은 또한 정상적인 인간 요로 상피의 시험관 내 모델에서 APOBEC3 발현 및 탈아미노화 활성을 유도하는 것으로 나타났습니다[72]. BKPyV로 인한 방광암 발생의 잠재적 위험은 특히 면역 저하 집단, 특히 장기 이식 수혜자에서 높을 수 있습니다. 따라서 BKPyV 바이러스혈증 또는 기타 폴리오마바이러스 관련 합병증은 신장 이식 후 방광암 위험이 4배 더 높은 것과 관련이 있습니다[73-77].
장기 이식 수혜자의 방광 종양 게놈에 대한 심층 시퀀싱을 통해 BKPyV 통합도 밝혀졌습니다 [78-80]. 특정 바이러스 감염이 일부 전통적으로 비바이러스성 암에서 APOBEC3-매개 돌연변이 유발에 기여할 수 있지만, 종양 진화 후반 및 아마도 감염 제거 이후에 APOBEC{4}}유발 돌연변이가 지속적으로 획득된다는 점을 고려하면 추가 요인이 중요할 가능성이 높습니다. [22, 56, 81, 82]. 이러한 비바이러스 요인은 뺑소니 바이러스 병인이 타당하지 않은 암에서 APOBEC{10}}유도 돌연변이의 유병률을 설명할 수도 있습니다.

남성의 면역체계 강화를 위한 시스탄체의 효능
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
염증
수많은 요인이 염증을 유발할 수 있으며, 이는 주요 염증 경로인 NF-κB 신호 전달을 통해 APOBEC3 발현을 증가시킬 수 있습니다. 이 가설을 뒷받침하는 것은 APOBEC3B 프로모터에서 3개의 NF-κB 결합 부위가 발견되었으며, 표준 NF-κB 경로의 일부인 p65/p50 및 p65/c-Rel 이종이합체가 APOBEC3B 전사에 중요한 것으로 입증되었습니다[83] . APOBEC3B 프로모터에는 RelB 결합 부위가 포함되어 있으므로 비표준 NF-κB 신호 전달은 APOBEC3 발현을 조절할 수도 있습니다. LPS 및 IL-4과 같은 여러 알려진 APOBEC3 유도물질도 강력한 NF-κB 활성화제이며, 이는 염증 동안 NF-κB가 APOBEC3의 전사 동인으로 작용한다는 것을 더욱 의미합니다[84]. NF-κB 신호전달은 또한 전염증 매개체의 전사를 통해 APOBEC3 발현을 간접적으로 증가시킬 수 있습니다. 예를 들어, NF-κB 표적 유전자 IL-6는 JAK/STAT 신호 전달을 통해 간세포 암종에서 APOBEC3B 발현을 유도하는 것으로 나타났습니다[85, 86]. 유사하게, TNF-는 각질세포에서 APOBEC3A 발현을 촉진하는 것으로 밝혀졌습니다[87, 88]. 이러한 발견을 뒷받침하는 담관암종 및 담낭암에 대한 연구에서는 IL{35}} 및 TNF 노출에 따라 APOEBC3A 및 APOBEC3B가 모두 상향 조절되는 것으로 나타났습니다[43]. 추가적으로, IFN-은 방광 종양 및 폐 선암종에서 APOBEC3B 발현의 동인으로 연루되어 있습니다[46, 89]. APOBEC3 전사를 통해 직접적으로 작용하고 다른 염증 매개체를 통해 간접적으로 작용할 수 있는 NF-κB 신호전달은 따라서 암에서 APOBEC{44}}매개 돌연변이 유발의 동인일 가능성이 높습니다(그림 2). NF-κB의 이러한 APOBEC{46}}유도 역할은 염증이 매우 심한 미세 환경을 갖는 면역학적으로 "뜨거운" 종양에서 특히 중요할 수 있습니다.
약물 노출 및 복제 스트레스
특정 약물에 대한 노출은 APOBEC{0}}매개 돌연변이 유발을 유발할 수도 있으며, 블레오마이신, 시스플라틴, 에토포사이드, 5-플루오로우라실, 젬시타빈, 하이드록시우레아, 아피디콜린, 캄프토테신과 같은 화학요법은 모두 암에서 APOBEC3 발현을 유도하는 것으로 나타났습니다. 세포주 [1, 61, 90, 91]. NF-κB 신호전달은 이러한 약물 중 일부에 대한 반응으로 APOBEC3 유도를 중재할 가능성이 높지만 복제 스트레스와 PI3K 신호전달도 중요한 역할을 할 수 있습니다(그림 2) [1, 90, 92, 93]. APOBEC3 발현을 증가시키는 것 외에도 유전독성 약물은 게놈 손상을 유도하여 ssDNA 기질을 생성함으로써 APOBEC3- 매개 돌연변이 유발을 더욱 촉진할 수 있습니다(그림 3). 유전독성 약물이 없더라도 암세포는 축적된 DNA 손상과 특정 발암성 돌연변이로 인해 복제 스트레스를 유발하는 APOBEC3-를 경험할 수 있습니다. 예를 들어 유방암에서는 PTEN 고갈과 HER2 증폭이 복제 스트레스를 유도하고 시험관 내에서 APOBEC3B 활성을 증가시키는 것으로 나타났습니다[90]. 폐암에서 복제 스트레스를 유발하는 일반적인 유전적 변형인 FHIT1의 소실은 APOBEC3-으로 인한 돌연변이 부담의 증가와 관련이 있었습니다[53]. 이러한 복제 스트레스 유발 돌연변이는 바이러스 감염 또는 약물 노출 후 보다 일시적인 APOBEC3 유도와 대조적으로 지속적인 세포 변화를 일으키기 때문에 APOBEC3- 매개 돌연변이 유발의 특히 강력한 유발 요인이 될 수 있습니다. 양성 피드백 루프에서 APOBEC3 발현 증가는 추가적인 DNA 손상, 복제 분기 속도 저하 및 세포 주기 정지로 인해 복제 스트레스를 악화시킬 수 있습니다[52, 97-99]. 복제 스트레스의 맥락에서 APOBEC3, 특히 APOBEC3B는 특히 더 확산된 돌연변이 패턴보다는 카타에기스를 유발하는 경향이 있을 수 있습니다. 따라서 APOBEC3B는 텔로미어 위기 동안 암 세포주에서 카타에기스를 유도하는 것으로 나타났습니다[94]. APOBEC3B는 p53-결핍 세포주에서 kataegis와 유사하게 연관되어 있으며 범암 분석에서는 APOBEC3B 발현이 kataegis와 양의 상관관계가 있음을 발견했습니다[31, 99].

cistanche tubeulosa - 면역 체계를 향상시킵니다.
체세포 및 생식계열 변경
여러 유전자의 체세포 돌연변이는 APOBEC{0}}매개 돌연변이 발생의 증가와 연관되어 있지만, 전체 게놈 시퀀싱 분석에서는 APOBEC3의 코딩 또는 조절 영역에서 재발성 체세포 단일 뉴클레오티드 변이체를 발견하지 못했습니다[100, 101]. 따라서 APOBEC3의 탈아미노화 활성을 증가시키는 체세포 돌연변이는 가능성이 낮으며, 증가된 프로모터 또는 인핸서 활성을 통해 APOBEC3 발현을 변경하는 돌연변이도 마찬가지입니다. 그러나 암에서 복제수 증폭으로 인해 APOBEC3 발현이 증가할 수 있습니다. 한 가지 암 유형에서만 언급되었지만, APOBEC3 복제수 변이는 폐 종양의 ~30%에서 발견되었습니다[36, 102]. 이러한 유전적 변화는 APOBEC3B 발현 증가 및 APOBEC 유발 돌연변이 부담 증가와 관련이 있었습니다[36]. APOBEC3 유전자좌의 생식 계열 변이체는 더 흔한 것으로 보이며 APOBEC3 발현 및 암 위험에 영향을 줄 수 있습니다. 예를 들어, APOBEC3 유전자 클러스터의 상류에 위치한 단일 염기 다형성(SNP) rs1014971은 APOBEC3B 발현 증가, APOBEC{21}}유발 돌연변이 강화 및 방광암 위험 증가와 관련이 있습니다[61, 63, 103]. 유방암에서 APOBEC3A/B 키메라를 생성하는 결실 다형성은 질병 위험 증가, APOBEC{26}} 유도 돌연변이 증가 및 종양 분화 불량(음성 예후의 징후)과 관련이 있습니다[47, 61, 62, 64 , 104, 105]. 동일한 결실 다형성은 급성 림프구성 백혈병에서 APOBEC3-유도된 과다돌연변이에 기여할 수 있습니다[62]. 폐암에서 APOBEC3H 일배체형 I을 정의하는 6개 SNP의 조합은 질병 위험 증가와 관련이 있습니다[65](표 2). 이 일배체형 내의 유전적 변이는 폐암 위험을 더욱 증가시킬 수 있습니다[106]. 또한, 변종 rs2267401은 담낭암 및 간세포 암종 위험을 증가시키는 것으로 나타났습니다. 이는 강화된 프로모터 활성 및 IL{41}} 반응을 통해 발생하는 APOBEC3B 발현 증가로 인해 발생하는 것으로 보입니다[43, 86]. 대조적으로, 동일한 SNP rs2267401은 담관암종의 위험 감소 및 이 종양 유형에서 APOBEC3B 프로모터 활성 감소와 관련이 있었는데, 이는 아마도 전사 억제인자 TFAP2A의 과발현으로 인한 것일 수 있습니다[43]. 또 다른 변종인 rs12157810은 APOBEC3A 프로모터 활성을 증가시키는 것으로 밝혀졌지만 담관암종 및 담낭암 위험을 낮추는 것과 관련이 있는 것으로 나타났습니다[43]. 신장암에서도 일치하는 결과가 관찰되었습니다[108]. 또 다른 SNP rs139293은 폐암 위험 감소와 관련이 있습니다[107]. 엑손에 위치한 이 변이체는 APOBEC3H에서 잠재적으로 활성을 감소시키는 아미노산 변화를 생성하고 APOEBC3H 및 APOBEC3C의 발현을 낮출 수 있습니다[107](표 2).

그림 2 APOBEC3 유전자의 전사 조절. NF-κB 신호 전달은 내인성 및 외인성 APOBEC3 유발 요인에 대한 공유 경로입니다. APOBEC3을 유도하기 위해 NF-κB 신호전달은 APOBEC3의 전사를 통해 직접적으로 작용하고 다른 염증 매개체의 전사를 통해 간접적으로 작용합니다. 주요 염증 매개체에는 인터페론, TNF- 및 IL-6이 포함되며, 이는 NF-κB 및 JAK/STAT 신호 전달을 통해 APOBEC3 전사를 유도할 수 있습니다. 또한 복제 스트레스는 PI3K/Akt를 통해 NF-κB 신호 전달을 활성화하여 APOBEC3 발현을 촉진할 수 있습니다.

그림 3 APOBEC3-매개 돌연변이 유발에 대한 2요인 모델. 2요인 모델에서 APOBEC3-매개 돌연변이 유발에는 APOBEC3 발현 유도와 ssDNA 가용성이 모두 필요합니다. 약물 노출, 텔로미어 위기 및 DNA 복구 과정과 같은 요인은 ssDNA를 생성할 수 있는 반면, 전사 유발 요인은 APOBEC3 발현을 상향 조절할 수 있습니다 [94-96]
레트로트랜스포존 활동, 텔로미어 위기 및 DNA 손상
암세포는 일반적으로 다양한 경로를 통해 APOBEC3-매개 돌연변이 유발을 촉진할 수 있는 불안정한 게놈을 가지고 있습니다. 특히, 게놈 불안정성은 레트로트랜스포존 활성을 촉진하여 APOBEC3-매개 돌연변이 유발의 일시적 폭발을 유발할 수 있습니다[112]. 게놈 불안정성은 APOBEC3B에 의해 탈아미노화된 ssDNA 중단점을 생성하는 것으로 밝혀진 텔로미어 위기 및 색소침착과도 연관되어 있습니다[94](그림 3). APOBEC3-매개 돌연변이 유발은 DNA 손상으로 인한 복제 스트레스 및 ssDNA 중간체를 생성하는 비상동 말단 결합(NHEJ) 및 상동 재조합(HR)과 같은 관련 불일치 복구 프로세스 동안 APOBEC3의 상향 조절에 의해 촉발될 수 있습니다[90 , 95, 96, 113–116] (그림 3). APOBEC3은 지체 가닥 주형을 제거할 수 있기 때문에 빠르게 분열하는 암세포는 ssDNA에 자주 노출되어 APOBEC{17}} 매개 돌연변이 유발을 촉진할 수 있습니다[14]. 암세포의 이러한 내인성 과정은 외인성 유발 요인에 노출되지 않고 종양 진화 후반에 APOBEC3- 유도 돌연변이의 지속적인 획득을 유도할 수 있습니다[81]. DNA 손상과 ssDNA 기질 가용성의 중요성은 APOBEC3이 많은 건강한 조직에서 낮은 수준으로 발현되고 일반적으로 상당한 종양 게놈 유사 돌연변이 패턴을 유발하지 않는 이유를 설명할 수도 있습니다. 유의미한 APOBEC3- 유발 돌연변이 부하가 건강한 식도 또는 자궁내막 조직에서는 발견되지 않았지만, 비암성 장 선와 및 기관지 상피 세포의 하위 집합에서는 낮은 수준의 그러한 돌연변이가 발견되었습니다[59, 117-120 ]. 따라서 APOBEC3 활성에 대한 2인자 모델은 APOBEC{32}}매개 돌연변이 유발에 필요한 APOBEC3 발현 증가와 기존 DNA 손상 둘 다와 함께 많은 암에서 타당합니다(그림 3).
흡연?
흡연은 APOBEC3-으로 인한 돌연변이 부하가 높은 여러 암의 주요 위험 요소입니다. 예를 들어 흡연은 방광암 위험의 50% 이상을 차지하며 폐종양의 80~90%를 유발하는 것으로 추정됩니다[121, 122]. 흡연은 돌연변이 시그니처 4, 5 및 29와 가장 밀접하게 연관되어 있지만, 담배 노출이 APOBEC3- 유도 시그니처 2 및 13과도 연관되어 있는지 여부를 여러 연구에서 테스트했습니다[24-26, 123, 124]. 그러나 결과는 모순되었습니다. 폐 선암종 분석에서 시그니처 2와 13은 흡연자의 종양에서 농축되었습니다[123]. 방광암의 경우 시그니처 13은 이전 흡연자의 종양에서 강화되었습니다[125]. 그러나 근육 침윤성 방광 종양에 대한 별도의 분석에서는 시그니처 13이 비흡연자에서 풍부하고 시그니처 5와 음의 상관 관계가 있음이 밝혀졌습니다[124]. 또한 정상 인간 요로상피를 대상으로 한 in vitro 연구에서는 담배연기의 발암물질인 벤조[a]피렌에 대한 노출이 시그니처 2나 13을 유발하지 않는 것으로 나타났습니다. 담배 연기에는 약 60종의 발암물질이 포함되어 있습니다[126]. 흡연이 APOBEC3- 매개 돌연변이 유발을 증가시키는 경우, 그 효과는 ssDNA 기질 가용성을 증가시키는 일반화된 DNA 손상으로 인한 것일 가능성이 높습니다[123]. 담배의 니코틴 성분이 염증과 NF-kB 신호 전달을 유발할 수 있지만 담배 연기가 APOBEC3 발현을 직접적으로 증가시킨다는 증거는 없습니다. 비소세포폐암에 대한 단일 연구에서 이 가설을 테스트했지만 흡연과 APOBEC3B mRNA 발현 사이에는 연관성이 발견되지 않았습니다[54]. 그러나 APOBEC3-매개 돌연변이 유발이 광범위하게 작동하는 암의 일반적인 위험 요소인 흡연의 확산으로 인해 흡연과 APOBEC3 사이의 상호 작용을 식별하기 어려울 수 있습니다.
풀 사이즈 테이블

표 2 (계속)
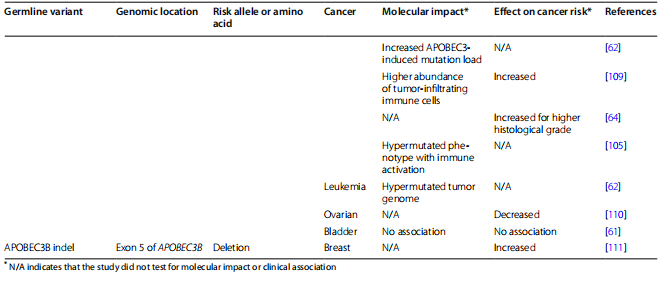
돌연변이 유발성 및 비돌연변이성 경로를 통한 APOBEC3의 영향 APOBEC3에 의해 유발된 발암성 코딩 돌연변이
APOBEC3-으로 인한 돌연변이는 암 어디에나 존재하며 종양 유전자를 활성화하거나 종양 억제 인자를 비활성화하여 발암을 촉진할 수 있습니다(표 3). 예를 들어, APOBEC3-유발 FGFR3 S249C 돌연변이(방광암에서 가장 흔한 FGFR3 돌연변이)는 암호화된 성장 인자 수용체의 구성적 활성화를 유발하여 세포 증식을 촉진합니다[127, 128]. 다른 종양 유형에서는 덜 재발하지만, S249C는 폐암, 자궁경부암, 두경부암에서도 발견되었습니다[129-132]. 수용체 활성화 외에도, APOBEC3- 유도 돌연변이는 하류 신호 전달 경로에 영향을 주어 발암성이 높은 돌연변이 시너지 효과를 생성할 수 있습니다. 예를 들어, Te APOBEC3- 유도 PIK3CA E545K 돌연변이는 성장 촉진 PI3K 경로의 비정상적인 활성화를 유발하고 방광, 유방, 자궁경부, 대장, 식도, 두경부 및 폐 종양에서 발견되었습니다[39, 132–137]. 매우 유사한 PIK3CA E542K 돌연변이가 방광암, 유방암, 자궁경부암, 결장직장암, 식도암, 두경부암, 폐암에서 발견되었습니다[39, 132, 133, 135, 137-140]. APOBEC3- 유도 및 기타 종양유전자 활성화 돌연변이는 종양 억제 유전자에 추가 돌연변이가 있는 경우 암세포가 확인되지 않은 채 증식하도록 허용할 수 있습니다. 이 중 일부는 APOBEC3-매개 돌연변이 유발에서 발생합니다. 예를 들어, 비활성화된 R505G FBXW7 돌연변이는 APOBEC3s에 기인하며 HNSCC, 상부 소화관암, 요로암 및 폐암에서 검출되었습니다[132, 143]. 서브클론 APOBEC3- 유도 돌연변이는 방광, 유방, 두경부 및 폐 종양의 종양 억제 유전자 PTEN 및 TP53에서도 관찰되었습니다[148]. 다른 돌연변이 과정도 종양 억제인자를 비활성화할 수 있으며, 높은 APOBEC3 활성은 그러한 돌연변이를 선호하는 선택적인 압력을 생성할 수 있습니다. APOBEC3은 전반적인 종양 돌연변이 부담을 높이므로 종양 억제 돌연변이로 인해 DNA 손상 반응(DDR)이 손상된 세포는 세포사멸을 피하고 계속해서 증식할 가능성이 더 높습니다. 따라서 대부분 비APOBEC3- 유도된 TP53 돌연변이는 APOBEC3- 유도 돌연변이 부담이 높은 방광암, 폐 선암종 및 B 세포 림프종 세포주에서 더 흔했습니다[46, 89 , 149]. 마찬가지로, 높은 APOBEC3B 발현은 유방암 및 부신피질 암종에서 더 많은 p53 돌연변이와 연관되어 있습니다[22, 44]. 선택 압력 외에도 p53이 p21 및 DREAM 단백질을 통해 APOBEC3B 전사를 억제할 수 있기 때문에 p{53}}돌연변이 종양에서 APOBEC3 발현이 높아짐에 따라 이러한 경향이 발생할 수 있습니다[150].
표 3 암에서 재발성 APOBEC3-유발 체세포 돌연변이 및 복제수 변경

재발성 APOBEC3에 의해 유발된 비암호화 돌연변이
난소 영역은 또한 재발성이 높으며 암 관련 유전자의 발현을 조절하여 종양 발달에 기여할 수 있습니다(표 3). 예를 들어, 많은 방광 및 유방 종양에는 PLEKHS1 및 TBC1D12의 프로모터에 APOBEC3-유도된 "쌍둥이 돌연변이 핫스팟"이 있으며, 이는 침습성 질환 및 불량한 예후와 관련된 잠재적인 종양 유전자입니다[33, 144, 147, 151, 152 ]. 혈관신생과 관련된 APOBEC3-유발 ADGR6/GPR126 인핸서 돌연변이는 방광암에서도 발견되었습니다[33, 145]. 방광암에서 APOBEC3에 기인하는 비암호화 돌연변이가 있는 다른 유전자에는 LEPROTL1 및 잠재적으로 종양 억제 인자인 WDR74가 포함됩니다[144, 153, 154]. 또한, 많은 T세포 급성 림프구성 백혈병에는 종양유전자 LMO1의 전사 시작 부위 상류에 APOBEC{24}}유발 돌연변이가 있습니다[146]. 몇몇 그러한 돌연변이는 유방암에서 기능적이며 잠재적인 발암성 역할을 하는 것으로 밝혀졌습니다[155]. 그러나 비코딩 유전자간 및 프로모터 영역에서 APOBEC3- 매개 돌연변이 유발을 유발하는 요인은 발견되지 않았지만 DNA 복제 및 전사 개시 중에 발생할 가능성이 높습니다.
조절 영역에서 점 돌연변이를 생성하는 것 외에도, APOBEC3은 종양 유전자 카피 수의 증가를 촉진하여 유전자 발현 조절을 더욱 어렵게 할 수 있습니다(표 3). 예를 들어, APOBEC3 발현이 높을수록 신경교종에서 ATP2B4, MAKAPK2 및 USP15와 같은 여러 Ras/MAPK 조절 유전자의 복제수 변이 증가와 관련이 있습니다[51]. 종양 유전자로 알려진 EGFR 및 CDK4의 증폭도 APOBEC3-고교교종에서 관찰되었습니다[51]. APOBEC3이 복사 번호 변경을 촉진하는 메커니즘은 아직 알려지지 않았습니다. 그러나 APOEBC3-유발 kataegis가 염색체 불안정성과 이중 가닥 절단을 촉진하여 복제수 변경 기회를 생성한다는 것은 타당합니다[156, 157].

cistanche tubeulosa-항종양의 장점
종양 진화
Although some APOBEC3-induced mutations are likely important for initial tumor formation, many occur later in tumor evolution. Supporting this paradigm, episodic bursts of APOBEC3-mediated mutagenesis were observed during prolonged culture of numerous cancer cell lines [81, 112]. This repeated APOBEC3 activity can create a high overall tumor mutation burden and fuel subclone heterogeneity in a tumor context. Accordingly, APOBEC3s have been identified as primary drivers of subclonal mutations in bladder, breast, head neck, and lung cancers [48, 148]. In bladder cancer, over 45% of subclonal mutations in driver genes may be attributable to APOBEC3s [148]. Additionally, APOBEC3-induced mutation load has been strongly associated with tumor heterogeneity in metastatic thoracic cancers [89]. APOBEC3-induced tumor heterogeneity can promote resistance to cancer therapies. While the continued acquisition of signatures 2 and 13 is often part of natural tumor evolution, chemotherapy treatment may further fuel APOBEC3-mediated mutagenesis by triggering APOBEC3 expression and inducing DNA damage [1, 81, 90, 91]. Specific therapy resistance mutations can also arise due to APOBEC3 activity. For example, the APOEBC-induced MEK2 L46F mutation may confer resistance to BRAF inhibitors such as vemurafenib and dabrafenib in melanoma [82, 142]. In lung cancer, the potentially APOBEC3-induced C>T EGFR T790 돌연변이는 EGFR 억제제인 게피티닙(gefitinib)과 엘로티닙(erlotinib)에 대한 내성을 촉진할 수 있습니다[82, 141]. 마찬가지로, 재발성 난치성 다발성 골수종에서 관찰되는 일부 APOEBC3-유발 돌연변이는 치료 저항성을 획득하는 데 기여할 수 있습니다[158]. 비돌연변이 경로 APOBEC3-에 의해 유도된 돌연변이는 종양 형성의 중요한 동인이지만, APOBEC3은 비돌연변이 경로를 통해 암에서도 역할을 할 수 있습니다. 이러한 경로의 중요성을 보여주는 간세포 암종 연구에서는 촉매적으로 비활성인 APOBEC3B의 과발현이 시험관 내에서 세포 증식, 세포 이동 및 세포 침입을 증가시키는 것으로 나타났습니다[159]. K-Ras 돌연변이가 있는 경우, APOEBC3A는 췌장관 선암종의 마우스 모델을 기반으로 STING 의존성 전이 및 염색체 불안정성을 촉진할 수도 있습니다[157]. 촉매적으로 비활성인 APOBEC3B의 과발현은 또한 더 빈번한 "G1 탈출"과 연관되어 있으며, 이는 APOBEC3B가 세포 주기 조절 장애에 기여한다는 것을 시사합니다[159]. 유사한 APOBEC3B 매개 세포 주기 진행이 방광암에서도 관찰되었습니다[159, 160]. APOBEC3s는 또한 여러 메커니즘을 통해 세포 사멸을 억제할 수 있습니다. APOBEC3G는 췌장암에서 Akt 활성화를 통해 아노이키스를 억제하는 것으로 나타났으며, APOBEC3B는 PDCD2 기능을 억제하고 ATM 및 Chk1/2 활성을 낮춤으로써 위암에서 세포 사멸을 감소시킬 수 있습니다[38, 49]. 또한, APOBEC3은 후성유전학적 결합 메커니즘을 통해 종양 유전자 및 종양 억제 인자의 발현에 영향을 줄 수 있습니다. 예를 들어, APOBEC3B는 일시적인 염색질 리모델링을 통해 유방암에서 에스트로겐 수용체(ER) 과발현을 유도하는 것으로 나타났습니다[161]. APOBEC3-매개 후생적 조절에 대한 추가 증거를 제공하는 높은 APOBEC3B 발현은 식도암에서 더 큰 LINE1 메틸화(전체 DNA 메틸화의 프록시)와 연관되어 있습니다[39].
종양 면역 미세 환경의 조절
APOBEC3은 또한 종양 면역 미세환경을 형성하는 비돌연변이 경로를 통해 종양 성장에 영향을 미칠 수 있습니다(표 4). APOBEC3은 일부 암에서 면역억제제이며, APOBEC3B 발현이 높을수록 부신피질 암종 및 위암에서 면역 세포 침윤이 감소하는 것과 관련이 있습니다[37, 162]. APOBEC3 발현은 또한 간세포 암종의 마우스 모델에서 골수 유래 억제 세포(MDSC) 및 종양 관련 대식세포(TAM)와 같은 면역억제 매개체의 더 큰 침윤과 관련이 있는 것으로 나타났습니다[163]. 다른 암 유형에서는 반대 효과가 관찰되었으며, APOBEC3은 면역 활성화를 촉진합니다. 범암 분석에서 높은 APOBEC3B 발현은 피부 흑색종 및 유방암에서 증가된 면역 활성화와 관련이 있었습니다[162]. 유방암에 대한 추가 연구에서도 비슷한 결과가 나타났습니다. 높은 APOBEC3B 발현은 더 많은 종양 팽창 림프구와 연관되어 있으며, APOBEC3B 유도는 마우스 모델에서 강력한 T 세포 매개 면역 반응을 유도했습니다[164, 165]. APOBEC3C-H 수준은 또한 종양 미세환경에서 더 많은 CD{23}} T 세포, 증가된 T 세포 수용체 다양성 및 더 큰 세포용해 활성과 상관관계가 있었습니다[48, 64]. 유사한 면역 활성화가 방광암에서도 관찰되었으며, 여러 연구에서 APOBEC3-고 종양에서 증가된 면역 신호 및 인터페론 신호 전달을 감지했습니다[35, 46, 160]. 폐암에서 T 세포 매개 면역 활성화는 높은 APOBEC3B 발현 또는 높은 APOBEC{32}}유발 돌연변이 부하와 연관되어 있습니다[36, 166]. 난소암에서 APOBEC3B 및 APOBEC3G 발현 증가는 면역 세포 침윤 증가와 관련이 있습니다[41, 167]. 종양 자체에서는 아니지만, 증가된 APOBEC3A 발현은 대식세포 분극화를 전염증성, 면역 활성화 상태로 전환시키는 것으로 나타났습니다[168].
표 4 암 유형별 APOBEC3의 면역 조절 효과

암에서 APOBEC3의 임상적, 치료적 중요성
여러 암에서 나쁜 예후와의 연관성
면역억제는 일부 암에서 APOBEC3-매개 돌연변이 유발과 시너지 효과를 발휘하여 발암성 돌연변이가 축적되어 종양 발생을 유도하는 동시에 숙주 면역 반응을 방지할 수 있습니다. 이 모델에 따르면, APOBEC3s로 면역억제를 나타내는 부신피질암종과 위암에 대한 연구에서는 APOBEC3B 발현이 높을수록 생존기간이 짧아지는 것과 상관관계가 있음을 발견했습니다(표 4 및 5)[37, 38, 44]. APOBEC3 발현의 증가는 비인두 암종, 투명 세포 신장 암종 및 신경내분비 종양의 불리한 임상 결과와도 연관되어 있지만, 이들 암에서의 APOBEC{9}}매개 면역 효과에 대해서는 알려진 바가 거의 없습니다(표 5) [55, 169] . 높은 APOBEC3 발현 또는 유도된 돌연변이 부담은 유방암의 불리한 결과를 예측할 수도 있지만 일부 보고서에서는 일관성 없는 결과가 발견되었습니다(표 5). APOBEC3은 유방암에서 면역 활성화를 유도하기 때문에 종양 형성을 촉진하려면 추가적인 요인이 이러한 고조된 면역 반응을 극복해야 합니다(4). 더 큰 에스트로겐 수용체 활성화(ER)는 APOBEC3B가 유방암에서 ER 과발현을 촉진하는 것으로 나타났기 때문에 가능성 있는 메커니즘입니다[161]. 따라서, 높은 APOBEC3B 발현과 불리한 임상 결과 사이의 연관성은 ER+ 질환에서 더 강력합니다(표 5).
표 5 APOBEC3 발현 및 APOBEC3-유발 돌연변이와 암 유형별 임상 결과의 연관성
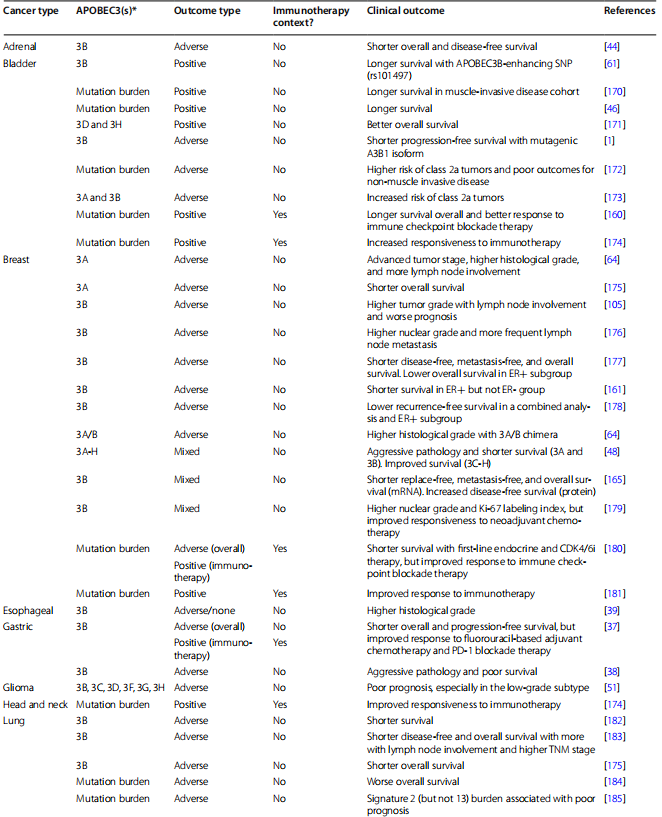
표 5 (계속)


그림 4 APOBEC3- 유발 요인이 예후에 미치는 영향은 암 유형에 따라 다릅니다. APOBEC3은 돌연변이 유발 및 비돌연변이 경로를 통해 종양 형성에 영향을 미칠 수 있으며, 이는 질병 과정에 반대 효과를 줄 수 있습니다. 이러한 효과의 상대적인 강도는 APOBEC3의 예후적 중요성을 결정할 수 있으며, 이는 암 유형에 따른 APOBEC3의 다양한 임상적 영향을 설명합니다(표 5). 특정 암 유형의 예가 표시됩니다.
APOBEC3은 전통적으로 치료된 폐암에도 마찬가지로 해로운 영향을 미칩니다. 면역요법 맥락 밖에서, 여러 연구에서 APOBEC3B 발현 또는 유도된 돌연변이 부담이 공격적인 질병 또는 불량한 예후와 연관되어 있음이 밝혀졌습니다(표 5). 폐암에서는 치료 저항성을 촉진하는 APOBEC3-유발 돌연변이와 같은 추가 요인이 APOBEC3-매개 면역 활성화보다 더 커서 임상 결과가 좋지 않을 수 있습니다[141](그림 4).
유리한 면역요법 및 백금 기반 치료 결과와의 연관성
폐암에서 APOBEC3-매개 면역 활성화는 면역 체크포인트 차단 요법에 대한 반응성 개선과 관련이 있는 것으로 나타났습니다(표 5). 유방암, 방광암 및 폐암의 면역요법 반응에 대해서도 유사한 결과가 관찰되었으며, 모두 APOBEC3에 의한 면역 활성화를 나타냈습니다(표 4 및 5). 이러한 암에서 APOBEC3-매개 면역 활성화는 높은 APOBEC3-유도 신생항원 부하와 시너지 효과를 발휘하여 면역요법 반응성을 촉진할 가능성이 높습니다(그림 4)[164, 187]. APOBEC3은 또한 위암의 면역요법에 대한 향상된 반응과 관련이 있지만, 이 암 유형은 역설적으로 APOBEC3에 의해 면역억제를 나타냈습니다[37]. 현재 데이터는 다소 불분명하지만, APOBEC3은 전통적인 화학요법으로도 방광암 생존율을 향상시킬 수 있습니다(표 5). 방광암은 종종 DNA 알킬화제인 시스플라틴으로 치료되는데, 이는 APOBEC3이 있을 때 활성이 강화될 수 있습니다. 기계적으로 APOBEC3은 약물 유발 나선외 시토신을 탈아미노화하여 시스플라틴 반응을 중재할 수 있으며, APOBEC3B는 화학 요법으로 유발된 불일치 복구 중에 추가 유전독성 효과를 유도할 수 있습니다[188]. 또한 APOBEC3은 세포를 추가적인 시스플라틴 유발 DNA 손상에 민감하게 만드는 높은 배경 돌연변이 부하를 생성할 수 있습니다. 그러나 방광암에서 APOBEC3의 임상적 이점은 더 높은 APOBEC3B 발현이 비근육 침습성 질환에서 근육 침습성 질환으로의 진행에 기여할 수 있기 때문에 후기 질환으로 제한될 수 있습니다[1]. APOBEC3은 백금 기반 치료법인 시스플라틴과 카보플라틴을 사용하여 방광암처럼 치료되는 난소암의 임상 결과 개선과 유사하게 연관되어 있습니다(표 5). 예를 들어, 높은 APOBEC3- 유발 돌연변이 로드는 투명 세포 난소 암종 환자의 무진행 및 전체 생존율 향상과 관련이 있었습니다[186]. 높은 APOBEC3 발현은 고급 장액성 난소 종양 아형에서 향상된 생존율과 상관관계가 있었습니다[41, 42, 167]. 방광암과 마찬가지로 난소암에서도 이러한 APOBEC{42}}관련 생존 혜택은 면역 활성화와 백금 기반 치료법에 대한 반응성 증가로 인해 발생할 가능성이 높습니다(그림 4).
바이오마커로서의 APOBEC3
APOBEC3 발현 및 APOBEC3-유발 돌연변이 부담은 여러 암 및 치료 상황에서 임상 결과와 연관되어 있으며, 이는 예후 바이오마커로서의 사용을 합리화합니다(표 5). 시스플라틴/카보플라틴으로 치료된 암에 대한 여러 연구에서 APOBEC3과 유리한 결과 사이의 연관성이 보고되었으므로 APOBEC3은 이 일반적인 화학 요법에 대한 바이오마커로 추가 평가할 가치가 있습니다[41, 46, 61, 167, 170, 186]. APOBEC3은 또한 폐암, 방광암 및 유방암에 대한 기존 데이터를 고려할 때 면역요법을 위한 바이오마커로 사용될 수 있습니다[37, 160, 166, 174, 180, 181]. 이러한 임상 연관성 외에도 여러 전임상 연구에서 APOBEC3가 잠재적인 백금 기반 치료법 및 면역요법 바이오마커로서의 사례를 뒷받침했습니다(표 6). 더욱이, APOBEC3은 표적 치료에 특히 유용한 바이오마커가 될 수 있습니다(표 6). 높은 APOBEC3B 발현은 신경교종에서 Raf 억제제에 대한 불량한 반응과 연관되어 있으며 특정 APOBEC3- 유도 돌연변이는 각각 다발성 골수종 및 폐암에서 Raf 억제제 및 EGFR 억제제에 대한 내성을 예측할 수 있습니다[82, 158]. ER+ 유방암에서 높은 APOBEC3B 발현은 내분비 요법인 타목시펜에 대한 내성을 예측할 수 있습니다[192]. 전임상 연구에 따르면, APOBEC3은 세포 독성 DNA 손상을 유발하는 합성 취약성으로 인해 표적 복제 체크포인트 및 DDR 억제제에 대한 유리한 반응을 예측할 수도 있습니다 [52, 99, 157, 191]. 전반적으로, APOBEC3 발현 또는 유도된 돌연변이 부담에 대해 환자 종양을 테스트하는 것이 치료 결정을 안내할 수 있다는 강력한 증거가 있습니다. 그러나 실험실과 진료소 사이에는 상당한 격차가 있으며, "APOBEC 양성"을 정의하는 의미 있는 매개변수를 설정하는 것이 필수적입니다. 이를 위해 향후 연구에서는 최종적으로 임상시험에 사용될 수 있는 APOEBC3 발현이나 돌연변이 시그니처 점수를 평가해야 할 것입니다. PD-L1/PD1 및 전반적인 종양 돌연변이 부담에 대한 채점 및 프로파일링 시스템을 지침으로 사용할 수 있습니다[195-199].
암 치료제를 위한 APOBEC3 억제
APOBEC3은 돌연변이 유발 경로가 아닌 돌연변이 유발 경로를 통해 종양 형성을 유도할 수 있으므로, 특정하지만 가능성이 높은 발암성 상황에서 APOBEC3를 억제하는 것이 유익할 수 있습니다(표 6). 예를 들어, APOBEC3 억제제는 비근육 침습성 방광암이 APOBEC3-유발 돌연변이 부담이 더 높은 근육 침습성 질환으로 진행되는 것을 잠재적으로 예방할 수 있습니다[1, 200]. APOBEC3 억제제는 또한 특히 새로운 STING 억제제와 결합하여 STING 의존성 전이를 늦출 수 있습니다[157, 201]. APOBEC3G를 억제하면 APOBEC3이 이러한 형태의 세포 사멸을 방해하는 것으로 나타났기 때문에 아노이키스를 지원할 수도 있습니다[49]. 또한, APOBEC3 억제제는 특히 APOBEC3이 나쁜 예후를 예측하는 암에서 종양 진화, 서브클론 이질성 및 화학요법 저항성을 제한하는 데 사용될 수 있습니다[82, 148]. APOBEC3 억제제는 현재 임상 용도로 사용할 수 없지만 APOBEC3 효소의 분자 구조를 해결하는 최근의 발전은 이 약물 계열의 최종 개발을 위한 중요한 토대를 마련했습니다[202]. 카테콜 부분을 가진 여러 화합물은 APOBEC3G를 억제하는 것으로 나타났으며 화학적 변형은 APOBEC3A의 보다 제한된 표적화를 지원합니다[203]. AID, APOBEC3A 및 APOBEC3B의 촉매 포켓을 표적으로 삼을 수 있는 최근 확인된 소분자 억제제도 보고되었으며 각 APOBEC 효소에 특이적인 억제제의 설계를 안내할 수 있습니다[205]. 소분자 억제제 외에도 APOBEC3 활성을 감소시키는 다른 잠재적 전략에는 유전자 침묵 치료법, ssDNA 함유 2'-데옥시제불라린 유사체 및 대체 스플라이싱 조절제가 포함됩니다[204]. 후자의 접근법은 일부 APOBEC3 이소형이 돌연변이를 유발하지 않고 SF3B1 억제가 엑손 5 스키핑을 유도하여 돌연변이를 유발하지 않는 APOBEC3B 이소형으로 발현을 이동시키는 것으로 나타났기 때문에 가능합니다[1]. 추가적으로, 뉴클레오시드 보충 및 chk1 억제를 통한 복제 스트레스의 완화는 시험관 내에서 APOBEC3B 발현을 감소시키는 것으로 나타났습니다[90].
표 6 APOBEC3의 바이오마커 및 치료 가능성

표 6 (계속)

암 치료제를 위한 APOBEC3의 활성화
APOBEC3를 억제하는 것이 많은 암에 도움이 될 수 있지만, 특정 상황에서 APOBEC3 활동을 증가시키는 겉보기에 반직관적인 전략은 독특한 치료 기회를 제공할 수 있습니다. 예를 들어, APOEBC3의 표적화된 과발현은 면역요법제를 사용하는 경우 유리할 수 있습니다. 이러한 접근법을 뒷받침하는 APOBEC3B 유도는 흑색종 및 유방암의 마우스 모델에서 면역 체크포인트 차단 요법에 대한 반응성을 증가시키는 것으로 나타났습니다[164, 187]. 이러한 APOBEC3-유발 감작은 여러 시너지 경로를 통해 발생할 수 있습니다(그림 5). 첫째, APOBEC3은 전체 종양 돌연변이 부담을 높여 일부 종양 유형에서 네오에피토프 형성 및 면역 활성화를 일으킬 수 있습니다[187]. 둘째, APOBEC{10}}매개 PD-L1 발현 증가는 면역요법 반응을 향상시킬 수도 있습니다[64, 171, 189]. 기계적으로 APOBEC3은 JNK/c-JUN 신호 전달을 활성화하는 DNA 손상을 통해 PD-L1 발현을 촉진할 수 있습니다. APOBEC3s와 IFN- 사이의 시너지 효과는 암세포에서 PD-L1 발현을 추가로 증가시키고 추가로 면역요법에 대한 민감성을 향상시킬 수 있습니다[206, 207]. APOBEC3은 높은 수준의 DNA 손상을 유발하기 때문에 암세포에서 이들의 표적 과발현은 세포독성을 일으킬 수도 있습니다[208]. APOBEC3A의 활성화는 APOBEC3 중 가장 높은 탈아미노화 활성을 갖기 때문에 특히 시험관 내에서 세포사멸을 유발할 수 있습니다[43, 108]. 더욱이, APOBEC3의 표적화된 과발현은 우라실 글리코실라제 기능이 손상되거나 염기성 부위 센서인 HCES(합성 취약성을 생성하는 돌연변이)의 상실이 있는 종양에 특히 세포독성이 될 수 있습니다[209, 210]. APOBEC3-활성화 치료법은 또한 유전독성 약물의 사용을 효과적으로 만들 수 있습니다. 예를 들어, APOBEC3 유도제는 백금 기반 화학요법과 DDR 억제제에 반응하도록 종양을 준비시킬 수 있습니다. 개념 증명으로, 시험관 내 유방암 연구에서는 기준선 발현이 낮은 세포주에서 APOBEC3를 유도하면 시스플라틴에 대한 반응성이 유의하게 증가한다는 사실이 밝혀졌습니다[188]. APOBEC3의 과발현은 또한 급성 골수성 백혈병 및 골육종 세포주에서 표적 ATR 및 Chk1/2 억제제에 대한 반응성을 증가시키는 것으로 나타났습니다[52, 191]. 유사하게, APOBEC3B 과발현은 p{47}}결핍 세포를 CHEK1/2, WEE1 및 PARP 억제에 민감하게 만들었습니다[99]. PARP 억제제에 대한 민감도 증가는 췌장암 세포의 APOBEC3A 상향 조절에서도 관찰되었습니다[157]. 일부 상황에서 치료 가능성이 있음에도 불구하고, APOBEC3 유도는 모든 암, 특히 더 높은 APOBEC3 발현이 면역억제와 연관된 종양에서 면역치료 반응을 촉진하지 못할 수 있습니다(표 4). APOBEC3-증강 약물은 새로운 동인 돌연변이, 종양 이질성 증가 및 화학요법 내성의 위험을 고려하여 주의 깊게 탐색해야 합니다. 그럼에도 불구하고, APOBEC3 활성의 활성화 및 억제는 모두 미래의 임상 환경을 위한 새로운 치료 옵션을 창출할 수 있는 유망한 접근법입니다.

그림 5 면역치료에 대한 반응을 향상시키기 위한 APOBEC3의 활성화. APOBEC3 활성 증가는 마우스 모델을 사용한 연구에서 입증된 바와 같이 네오에피토프 형성, PD-L1 발현 증가 및 면역 활성화를 통해 면역치료 반응을 증가시킬 수 있습니다.
결론
APOBEC3은 암의 주요 돌연변이 유발 요인이며, APOBEC3A 및 APOBEC3B는 APOBEC3 슈퍼패밀리 중에서 가장 중요한 돌연변이 유발 요인일 가능성이 높습니다. APOBEC3A와 APOBEC3B는 많은 암에서 과발현되며 이들의 발현은 더 높은 APOBEC3-유발 돌연변이 부담과 상관관계가 있습니다. 그러나 두 가족 구성원을 녹아웃시킨 후 잔류 탈아미노화 활동이 감지된 것은 다른 APOBEC3도 활성 돌연변이원임을 시사합니다. 각각의 APOBEC3이 암에 어떻게 기여하는지에 대한 이해가 향상되면 종양 병인을 더 명확하게 밝힐 수 있으며 APOBEC3을 표적으로 삼는 데 치료적으로 관련성이 높아질 수 있습니다.

그림 6 암에서 APOBEC3-매개 돌연변이 유발의 원인, 결과 및 임상적 측면. 다양한 외인성 및 내인성 요인이 APOBEC3을 유도할 수 있으며, 이는 돌연변이 유발성 및 비돌연변이성 경로를 통해 암 성장에 영향을 미칠 수 있습니다. 이러한 APOBEC3-매개 효과는 임상 결과를 형성하고 현재와 미래의 치료 환경 모두에 관련될 수 있습니다.
APOBEC3-매개 돌연변이 유발을 유발하는 요인에 대한 보다 포괄적인 이해는 향상된 암 예방 전략으로 이어질 수도 있습니다. 현재 알려진 APOBEC3 발현 유발 요인에는 바이러스 감염, 염증 및 특정 유전독성 약물이 포함되지만, 발현 증가만으로는 높은 수준의 돌연변이 유발이 발생하지 않을 수 있습니다(그림 6). 2요인 모델에서 유전독성 약물 노출, 게놈 불안정성 등으로 인해 발생할 수 있는 ssDNA는 APOBEC3에 대한 주요 돌연변이 기질을 생성하고 돌연변이 유발을 촉진합니다. 돌연변이 유발은 암에서 APOBEC3 역할의 핵심이지만, APOBEC3은 세포 주기 조절, 후생적 조절, STING 의존성 전이 및 세포 사멸 억제와 같은 비돌연변이 경로를 통해 종양 형성에도 기여할 수 있습니다(그림 6). 또한 APOBEC3은 암 유형에 따라 효과가 달라지면서 종양 면역 미세 환경을 조절할 수 있습니다. APOBEC3은 유방암, 폐암 및 방광암에서 면역 활성화와 관련이 있는 반면, APOBEC{12}}매개 면역억제는 간암, 위암 및 부신피질 암종에서 관찰되었습니다. APOBEC3의 면역 조절 효과는 질병 경과에 영향을 미칠 가능성이 있지만, APOBEC3- 매개 면역 활성화가 항상 개선된 임상 결과로 해석되는 것은 아닙니다. 왜냐하면 운전자 돌연변이 및 세포 사멸 억제와 같은 다른 요인이 반대 효과를 가질 수 있기 때문입니다. APOBEC3- 매개 면역 활성화, 증가된 네오에피토프 부하 및 더 높은 PD-L1 발현은 시너지 효과를 발휘하여 면역요법에 대한 반응을 향상시킬 수 있습니다(그림 6). APOBEC3은 또한 백금 기반 치료법에 대한 반응성을 촉진할 수 있습니다. 전임상 연구와 함께 여러 임상 연관성은 APOBEC3이 현재 사용 가능한 면역요법 및 화학요법의 바이오마커로 사용될 수 있는 반면, APOBEC3 활성화를 위한 새로운 전략은 치료 반응 증가를 위해 특정 종양을 준비시킬 수 있음을 시사합니다(그림 6).

시스탄체 튜불로사의 장점-면역체계 강화
대조적으로, APOBEC3를 억제하면 종양 진화를 늦추고, 서브클론 이질성을 감소시키며, 일부 암과 특정 치료 유형에 대한 치료 저항성을 예방할 수 있습니다. APOBEC3은 매우 다양하고 높은 비율의 인간 종양에서 조절 장애가 있으므로 이 분야에 대한 연구는 큰 잠재력을 갖고 있으며 많은 암 유형에 대한 새로운 치료 옵션으로 이어질 수 있습니다.
참고자료
1. Rouf Banday A, Onabajo OO, Lin SHY, Obajemu A, Vargas JM, Delviks Frankenberry KA 등 APOBEC3B의 자연적인 접합 가소성을 표적으로 삼으면 발현과 돌연변이 유발 활성이 제한됩니다. 커뮤니얼바이올.
2. 2021;4(1):386. Ebrahimi D, Richards CM, Carpenter MA, Wang J, Ikeda T, Becker JT, 외. APOBEC3H 대체 접합, 레트로바이러스 제한 및 HIV{6}} 프로테아제에 의한 반작용에 대한 유전적 및 기계적 기초. 냇 커뮤.
3. 2018;9(1):4137. Harari A, Ooms M, Mulder LCF, Simon V. 다형성 및 스플라이스 변형은 인간 APOBEC3H의 항레트로바이러스 활성에 영향을 미칩니다. J 비롤. 2009;83(1):295–303.
4. Lassen KG, Wissing S, Lobritz MA, Santiago M, Greene WC. HIV-1 항바이러스 활성을 나타내고 Vif*에 대한 민감도를 대조하는 두 개의 APOBEC3F 스플라이스 변이체 식별. J Biol Chem. 2010;285(38):29326–35.
5. 솔터 JD, 베넷 RP, 스미스 HC. APOBEC 단백질 계열: 구조적으로 통합되어 있으며 기능이 다양합니다. 동향 생화학 과학. 2016;41(7):578–94.
6. Chaudhuri J, Evans T, Kumar R, DiMenna L. 활성화 유발 시티딘 데아미나제(AID)의 생물학적 기능. Biomed J. 2014;37(5):269.
7. Chen SH, Habib G, Yang CY, Gu ZW, Lee BR, Weng SA 등. 아포지단백질 B-48는 기관 특이적 인프레임 정지 코돈이 있는 메신저 RNA의 산물입니다. 과학. 1987;238(4825):363–6.
8. Powell LM, Wallis SC, Pease RJ, Edwards YH, Knott TJ, Scott J. 조직 특이적 RNA 처리의 새로운 형태는 장에서 아포지단백질-B48을 생성합니다. 셀. 1987;50(6):831–40.
9. 히라노 K, 민 J, 후나하시 T, Baunoch DA, 데이비슨 NO. 인간 호기성-1 유전자의 특성 분석: 새로운 절단형 펩타이드 생산과 교대 스플라이싱에 의해 결정되는 위장 조직에서의 발현. J 지질 입술. 1997;38(5):847–59.
10. 해리스 RS, 더들리 JP. APOBEC 및 바이러스 제한. 바이러스학. 2015;479–480:131–45.
11. 실바스 T, 캘리포니아주 쉬퍼. APOBEC3s: DNA 편집 인간 시티딘 탈아미노효소. 단백질 과학. 2019. https://doi.org/10.1002/pro.3670.
12. Yu Q, König R, Pillai S, Chiles K, Kearney M, Palmer S 등. APOBEC3G의 단일 가닥 특이성은 HIV 게놈의 마이너스 가닥 탈아미노화를 설명합니다. Nat Struct Mol Biol. 2004;11(5):435–42.
13. Chan K, Sterling JF, Roberts SA, Bhagwat AS, Resnick MA, Gordenin DA. 단일 가닥 DNA 내의 염기 손상은 유비쿼터스 환경 인자에 의해 유발된 생체 내 과다 돌연변이의 기초가 됩니다. PLoS Genet. 2012;8(12):e1003149.
14. Hoopes JI, Cortez LM, Mertz TM, Malc EP, Mieczkowski PA, Roberts SA. APOBEC3A 및 APOBEC3B는 DNA 복제 중에 지연 가닥 주형을 우선적으로 제거합니다. 셀 담당자 2016;14(6):1273–82.
15. Lada AG, Kliver SF, Dhar A, Polev DE, Masharsky AE, Rogozin IB 등. 전사 보조활성제 Sub1의 파괴는 활성 효모 유전자에서 APOBEC에 의해 유도된 클러스터 돌연변이의 게놈 전체 재분배를 유도합니다. PLoS Genet. 2015;11(5):e1005217.
16. Seplyarskiy VB, Soldatov RA, Popadin KY, Antonarakis SE, Bazykin GA, Nikolaev SI. 인간 암에서 APOBEC에 의해 유발된 돌연변이는 복제 중에 지연 DNA 가닥에 강력하게 농축됩니다. 게놈 해상도. 2016;26(2):174–82.
17. Buisson R, Langenbucher A, Bowen D, Kwan EE, Benes CH, Zou L, 외. APOBEC3A 및 중규모 게놈 특징에 의해 유발되는 암의 승객 핫스팟 돌연변이. 과학. 2019;364:6447.
18. McCann JL, Cristini A, Law EK, Lee SY, Tellier M, Carpenter MA 등. DNA 시토신 데아미나제 APOBEC3B에 의해 촉진되는 R-루프 항상성 및 암 돌연변이 유발. bioRxiv [인터넷]. 2021;2021.08.30.458235. 출처: http://biorxiv.org/content/early/2021/08/30/2021.08.30.458235.abstract.
19. 홀츠 CM, 새들러 HA, 맨스키 LM. APOBEC3G 시토신 탈아미노화 핫스팟은 서열 맥락과 단일 가닥 DNA 2차 구조 모두에 의해 정의됩니다. 핵산 해상도. 2013;41(12):6139–48.
20. 해리스 RS. 유방암에서 APOBEC3B가 촉매하는 돌연변이 유발의 분자 메커니즘과 임상적 영향. 유방암 입술. 2015;17(1):8.
21. Refsland EW, 해리스 RS. APOBEC3 계열의 역요소 제한 인자. 베를린: 스프링거; 2013.p. 1~27.
22. Burns MB, Lackey L, Carpenter MA, Rathore A, Land AM, Leonard B 등 APOBEC3B는 유방암의 효소적 돌연변이 원인입니다. 자연. 2013;494(7437):366–70.
23. Chan K, Roberts SA, Klimczak LJ, Sterling JF, Saini N, Malc EP 등. APOBEC3A 과돌연변이 시그니처는 인간 암에서 APOBEC3B에 의한 배경 돌연변이 유발 시그니처와 구별됩니다. 냇 제넷. 2015;47(9):1067–72.
24. 우주. 2022.
25. Alexandrov LB, Kim J, Haradhvala NJ, Huang MN, Tian Ng AW, Wu Y, 외. 인간 암의 돌연변이 시그니처 레퍼토리. 자연. 2020;578(7793):94–101.
26. Alexandrov LB, Nik-Zainal S, Wedge DC, Aparicio SAJR, Behjati S, Biankin A, 외. 인간 암의 돌연변이 과정의 특징. 자연. 2013;500(7463):415–21.
27. Roberts SA, Lawrence MS, Klimczak LJ, Grimm SA, Fargo D, Stojanov P 등. APOBEC 시티딘 데아미나제 돌연변이 유발 패턴은 인간 암에 널리 퍼져 있습니다. 냇 제넷. 2013;45(9):970–6.
28. Zou J, Wang C, Ma X, Wang E, Peng G. APOBEC3B, 인간 암의 돌연변이 유발 분자. 셀바이오사이. 2017;7(1):29.
29. Taylor BJ, Nik-Zainal S, Wu YL, Stebbings LA, Raine K, Campbell PJ 등 DNA 탈아미노효소는 유방암 kataegis에서 APOBEC3B 및 3A의 의미와 함께 중단 관련 돌연변이 소나기를 유도합니다. 엘라이프. 2013;16:2.
30. Liu W, Newhall KP, Khani F, Barlow L, Nguyen D, Gu L, 외. 시티딘 데아미나제 APOBEC3G는 방광암의 암 돌연변이 유발 및 클론성 진화에 기여합니다. 암 입술. 2022;26:2651.
31. Aaltonen LA, Abascal F, Abeshouse A, Aburatani H, Adams DJ, Agrawal N 등 전체 게놈의 범암 분석. 자연. 2020;578(7793):82–93.
32. Bergstrom EN, Luebeck J, Petljak M, Khandekar A, Barnes M, Zhang T, 외. 암에서 클러스터된 돌연변이를 매핑하면 cDNA의 APOBEC3 돌연변이 유발이 드러납니다. 자연. 2022;602(7897):510–7.
33. Langenbucher A, Bowen D, Sakhtemani R, Bournique E, Wise JF, Zou L 등. 암의 확장된 APOBEC3A 돌연변이 서명. 냇 커뮤. 2021;12(1):1602.
34. 번즈 MB, 테미즈 NA, 해리스 RS. 여러 인간 암에서 APOBEC3B 돌연변이 유발에 대한 증거. 냇 제넷. 2013;45(9):977–83.
35. Kim H, Kim O, Lee MA, Lee JY, Hong SH, Ha US, et al. 전이성 요로상피암종에서 APOBEC3B 발현의 예후 영향 및 종양 침윤 세포독성 T 세포와의 연관성. 현재 Oncol. 2021;28(3):1652–62.
36. 왕 S, Jia M, He Z, Liu XS. 비소세포폐암에서 면역요법 반응에 대한 잠재적인 예측 마커로서의 APOBEC3B 및 APOBEC 돌연변이 시그니처. 종양 유전자. 2018;37(29):3924–36.
37. Xia S, Gu Y, Zhang H, Fei Y, Cao Y, Fang H, 외. APOBEC3B 강화에 의한 면역 불활성화는 위암의 화학요법에 대한 반응과 생존을 예측합니다. 종양면역학. 2021. https://doi.org/10. 1080/2162402X.2021.1975386.
38. 장 J, 웨이 W, 진 HC, 잉 RC, 주 AK, 장 FJ. 위암에서 APOBEC3B의 역할. Int J Clin Exp Pathol. 2015;8(5):5089-96.
39. 코스미 K, 바바 Y, 이시모토 T, 하라다 K, 나카무라 K, 오후치 M, 외. APOBEC3B는 식도 편평 세포 암종에서 분자 변형의 효소적 원천입니다. 메드온콜. 2016;33(3):26.
40. Feng C, Zheng Q, Yang Y, Xu M, Lian Y, Huang J, 외. 위장췌장 신경내분비 종양에서 APOBEC3B의 높은 발현 및 림프 전이와의 연관성. Appl Immunohistochem Mol Morphol. 2019;27(8):599-605.
41. Rüder U, Denkert C, Alisa Kunze C, Jank P. 고급 장액성 난소 암종 환자의 APOBEC3B 단백질 발현 및 mRNA 분석. 히스톨 히스토파톨. 2019;34:405–17.
42. Du Y, Tao X, Wu J, Yu H, Yu Y, Zhao H. APOBEC3B 상향 조절은 난소암 예후를 독립적으로 예측합니다: 코호트 연구. 암세포 Int. 2018;18(1):78.
43. Liu W, Ji H, Zhao J, Song J, Zheng S, Chen L 등. 전사 억제와 세포사멸은 다음의 효과에 영향을 미칩니다.
44. Gara SK, Tyagi MV, Patel DT, Gaskins K, Lack J, Liu Y 등. GATA3 및 APOBEC3B는 부신피질 암종의 예후 지표이며 APOBEC3B는 GATA3에 의해 직접 전사적으로 조절됩니다. 온코타겟. 2020;11(36):3354–70.
45. Wagener R, Alexandrov LB, Montesinos-Rongen M, Schlesner M, Haake A, Drexler HG 등. B 세포 림프종 세포주의 엑솜의 돌연변이 시그니처를 분석하면 APOBEC3 계열 구성원이 원발성 삼출성 림프종의 발병에 관여하는 것으로 나타났습니다. 백혈병. 2015;29(7):1612–5.
46. Glaser AP, Fantini D, Wang Y, Yu Y, Rimar KJ, Podojil JR 등. 요로상피암종에서 APOBEC 매개 돌연변이 유발은 생존율 향상, DNA 손상 반응 유전자의 돌연변이 및 면역 반응과 관련이 있습니다. 온코타겟. 2018;9(4):4537–48.
47. Cortez LM, Brown AL, Dennis MA, Collins CD, Brown AJ, Mitchell D 등. APOBEC3A는 유방암에서 두드러진 시티딘 데아미나제입니다. PLoS Genet. 2019;15(12):e1008545.
48. Asaoka M, Patnaik SK, Ishikawa T, Takabe K. DNA 돌연변이 원인 APOBEC3 계열의 다양한 구성원은 유방암 환경과 반대되는 연관성을 가지고 있습니다. Am J Cancer Res. 2021;11:5111.
49. Wu J, Pan TH, Xu S, Jia LT, Zhu LL, Mao JS 등. 바이러스 유도 단백질 APOBEC3G는 췌장암 세포에서 Akt 키나제의 활성화를 통해 아노이키스를 억제합니다. 과학 대표. 2015;5(1):12230. 50. Ding Q, Chang CJ, Xie X, Xia W, Yang JY, Wang SC 등. APOBEC3G는 대장암의 동소이식 마우스 모델에서 간 전이를 촉진하고 인간 간 전이를 예측합니다. J 클린 조사. 2011;121(11):4526–36.
51. Luo C, Wang S, Liao W, Zhang S, Xu N, Xie W, 외. APOBEC3 계열의 상향 조절은 불량한 예후와 관련이 있으며 저등급 신경교종에서 Raf 억제제에 대한 치료 반응에 영향을 미칩니다. Int J Mol Sci. 2021;22(19):10390.
52. Green AM, Budagyan K, Hayer KE, Reed MA, Savani MR, Wertheim GB 등 시토신 데아미나제 APOBEC3A는 백혈병 세포를 DNA 복제 체크포인트 억제에 민감하게 만듭니다. 암 입술. 2017;77(17):4579–88.
53. Waters CE, Saldivar JC, Amin ZA, Schrock MS, Huebner K. FHIT 손실로 인한 DNA 손상은 최적의 APOBEC 기질을 생성합니다: APOBEC 매개 돌연변이 유발에 대한 통찰력. 온코타겟. 2015;6(5):3409–19.
54. 사사키 H, 스즈키 A, 타테마츠 T, 시타라 M, 히코사카 Y, 오쿠다 K, 외. 비소세포폐암에서의 APOBEC3B 유전자 과발현. Biomed Rep. 2014;2(3):392–5.
55. Feng C, Zhang Y, Huang J, Zheng Q, Yang Y, Xu B. 비인두 암종에서 APOBEC3B 및 PD-L1/PD-1의 예후적 중요성. Appl Immunohistochem Mol Morphol. 2021;29(3):239–44.
56. Leonard B, Hart SN, Burns MB, Carpenter MA, Temiz NA, Rathore A 등. 장액성 난소암종의 APOBEC3B 상향조절 및 게놈 돌연변이 패턴. 암 입술. 2013;73(24):7222–31.
57. Heller M, Prigge ES, Kaczorowski A, von Knebel Doeberitz M, Hohen Fellner M, Duensing S. 음경 편평 세포 암종에서의 APOBEC3A 발현. 병리생물학. 2018;85(3):169–78.
58. Petljak M, Dananberg A, Chu K, Bergstrom EN, Striepen J, von Morgen P 등. 인간 암세포에서 APOBEC3 돌연변이 유발 메커니즘. 자연. 2022;607(7920):799–807.
59. Petljak M, Maciejowski J. 암에서 APOBEC 관련 돌연변이의 분자 기원. DNA 복구(Amst). 2020;94:102905.
60. 목수 MA, Li M, Rathore A, Lackey L, Law EK, Land AM 등. 외래 DNA 제한 효소 APOBEC3A에 의한 메틸시토신 및 정상 시토신 탈아미노화. J Biol Chem. 2012;287(41):34801–8.
61. Middlebrooks CD, Banday AR, Matsuda K, Udquim KI, Onabajo OO, Paquin A, 외. APOBEC3 영역의 생식선 변이체와 암 위험의 연관성 및 종양의 APOBEC 서명 돌연변이 강화. 냇 제넷. 2016;48(11):1330–8.
62. Nik-Zainal S, Wedge DC, Alexandrov LB, Petljak M, Butler AP, Bolli N 등. APOBEC3A 및 APOBEC3B의 생식선 카피수 다형성과 유방암에서의 추정 APOBEC 의존 돌연변이의 연관성. 냇 제넷. 2014;46(5):487–91.
63. 마츠다 K, 다카하시 A, 미들브룩스 CD, Obara W, Nasu Y, Inoue K, 외. 게놈 차원의 연관성 연구에서는 일본 인구의 방광암 위험과 관련된 15q24의 SNP가 확인되었습니다. 흠 몰 제넷. 2015;24(4):1177–84.
64. 김 Y, 선 DS, 윤 J, 고 YH, 원 HS, 김 JS. 유방암 환자에서 APOBEC3A 및 3B 발현의 임상적 의미. PLoS ONE. 2020;15(3):e0230261. 65. Starrett GJ, Luengas EM, McCann JL, Ebrahimi D, Temiz NA, Love RP 등 DNA 시토신 데아미나제 APOBEC3H 일배체형 I은 유방암 및 폐암 돌연변이 유발에 기여할 가능성이 높습니다. 냇 커뮤. 2016;7(1):12918.
66. Stavrou S, 로스 SR. 바이러스 면역의 APOBEC3 단백질. J Immunol. 2015;195(10):4565–70.
67. Bosch FX, Lorincz A, Munoz N, Meijer CJLM, Shah K. 인간 유두종 바이러스와 자궁 경부암 사이의 인과 관계. J 클린 파톨. 2002;55(4):244–65.
68. Revathidevi S, Murugan AK, Nakaoka H, Inoue I, Munirajan AK. APOBEC: 자궁경부암 발병의 분자 동인. 암 레트. 2021;496:104–16.
69. Riva G, Albano C, Gugliesi F, Pasquero S, Pacheco SFC, Pecorari G 등. HPV와 APOBEC의 만남: 두경부암 분야의 새로운 플레이어. Int J Mol Sci. 2021;22(3):1402.
