PRRSV 계통과 같은 NADC30-에 감염된 돼지에서 엑소좀 MiRNA 발현 프로필의 체계적 식별 및 비교
Dec 27, 2023
간단한 요약:엑소좀은 바이러스 감염, 항원 제시, 신체 면역 억제/증진에서 독특한 역할을 합니다. 돼지생식기호흡기증후군 바이러스(PRRSV)는 양돈 산업에서 가장 피해가 큰 병원체 중 하나입니다. 여기서 우리는 CHsx1401 균주와 같은 PRRSV NADC30-를 사용하여 42-일령 돼지를 인공적으로 감염시키고, 혈청 엑소좀을 분리하고, 감염군과 대조군 사이에서 33개의 유의하게 차별적으로 발현된(DE) 엑소좀 miRNA를 식별했습니다. PRRSV 감염 및 면역과 관련된 18개의 DE miRNA가 엑소좀에 의한 PRRSV 바이러스 감염 조절에 관여하는 잠재적 기능 분자로 스크리닝되었습니다.
추상적인:엑소좀은 세포간 의사소통의 중재자 역할을 하며 바이러스 감염, 항원 제시 및 신체 면역 억제/증진에서 독특한 역할을 하는 세포에 의해 분비되고 방출되는 생물학적 소포입니다. 돼지 생식기 호흡기 증후군 바이러스(PRRSV)는 양돈 산업에서 가장 피해가 큰 병원체 중 하나이며 모돈의 생식 장애, 돼지의 호흡기 질환, 성장 성능 저하 및 돼지 사망으로 이어지는 기타 질병을 일으킬 수 있습니다. 본 연구에서는 PRRSV NADC30-유사 CHsx1401 균주를 사용하여 42-일령 돼지에 인공 감염시키고 혈청 엑소좀을 분리했습니다. 높은 처리량 시퀀싱 기술을 기반으로 감염 전후의 혈청 엑소좀에서 305개의 miRNA가 확인되었으며, 그 중 33개의 miRNA가 그룹 간에 유의미하게 차별적으로 발현되었습니다(13개는 상대적으로 상향 조절되고 20개는 상대적으로 하향 조절됨). CHsx1401 게놈의 서열 보존 분석을 통해 8개의 보존 영역이 확인되었으며, 그 중 총 16개의 차별적으로 발현된(DE) miRNA가 3에 가장 가까운 보존 영역에 결합할 것으로 예측되었습니다.0 CHsx에 결합할 수 있는 5개의 DE miRNA를 포함하는 CHsx1401 게놈의 UTR1401 30 UTR(ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR-486, ssc-miR-6529). 추가 분석에 따르면 차별적으로 발현된 miRNA의 표적 유전자는 엑소좀 기능 관련 및 선천성 면역 관련 신호 전달 경로와 18개의 DE miRNA(ssc-miR-4331-3p, ssc-miR-744)에 광범위하게 관여하는 것으로 나타났습니다. PRRSV 감염 및 면역과 관련된 , ssc-miR-320, ssc-miR-10b, ssc-miR-124a, ssc-miR-128 등)을 검사했습니다. 엑소좀에 의한 PRRSV 바이러스 감염 조절에 관여하는 잠재적인 기능 분자입니다.

시스탄체 식물의 면역 체계 증가
키워드:PRRSV; 혈청 엑소좀; miRNA
1. 소개
돼지 생식기 및 호흡기 증후군 바이러스(PRRSV)는 Nidovirales 목, Arteriviridae 계통, Betaarterivirus 속에 속하는 외피 구조를 갖는 단일 가닥 양성 가닥 RNA 바이러스입니다[1,2]. 동결전자현미경으로 보면 직경이 50~65nm인 구형 또는 타원형이다[3,4]. PRRSV 게놈은 길이가 약 15kb이고 50개의 캡과 30개의 폴리A-꼬리가 있으며 50번과 30번 말단 모두에서 번역되지 않은 영역(UTR) 옆에 최소 10개의 ORF(오픈 리딩 프레임)가 포함되어 있습니다[5,6]. 뉴클레오캡시드 단백질로 둘러싸여 있으며 지질 이중층 코팅으로 바이러스 입자를 형성합니다. 엑소좀은 단층막 구조를 갖는 소포에 속하며 세포와 동일한 위상적 구조를 가지고 있다[7]. 전자현미경으로 보면 모양은 "컵 모양" 또는 "디스크 모양"입니다[8,9]. 엑소좀은 순환계에 오랫동안 존재할 수 있으며, 엑소좀에 들어 있는 물질은 인접한 세포나 멀리 있는 수용체 세포에 흡수된 후 수용체 세포를 조절하여 세포 간 유전물질 교환에 참여할 수 있다[10,11]. 이들은 주로 세포 표면 수용체, 막 단백질, 수용성 단백질, 지질, RNA(mRNA, miRNA, lncRNA 및 바이러스 RNA 등), 게놈 DNA, 미토콘드리아 DNA를 포함하여 막 표면 물질과 운반 내용물로 구성됩니다. ]. 마이크로RNA(miRNA)는 진화적으로 보존된 18~25개 뉴클레오티드(nt)의 내인성 비암호화 단일 가닥 소형 RNA로, 표적 mRNA의 분해를 유도하거나 표적 mRNA의 30UTR과 결합하여 번역 과정을 억제합니다. 전사 후 유전자 침묵에 이어 전사 후 수준에서 유전자 발현을 조절합니다 [15-17]. miRNA는 전사 후 포유동물 유전자의 60% 이상을 조절하는 것으로 추정됩니다[18,19]. MiRNA는 세포 간 통신에서 중요한 역할을 하며 질병 및 바이러스 감염, 전염 및 방어를 위한 잠재적인 기능 분자로도 사용될 수 있습니다[20]. 점점 더 많은 연구에서 miRNA가 타액, 소변, 모유 및 혈액과 같은 체액에 존재할 수 있으며 신체의 체액 순환 시스템을 통해 작용한다는 사실이 밝혀졌습니다 [21,22]. 엑소좀 miRNA는 유전자 발현 및 대사의 내인성 조절자로 간주되며 다양한 병리학적 상태를 나타낼 수 있습니다[23,24].

cistanche tubeulosa - 면역 체계를 향상시킵니다.
지난 20년 동안 miRNA는 면역 세포 발달, 선천성 면역 반응 및 후천성 면역 반응의 조절에 중요한 역할을 하는 것으로 나타났습니다. 일부 다른 miRNA는 다음과 같은 방법을 통해 PRRSV 감염을 손상시키는 것으로 보고되었으며, PRRSV 게놈 또는 PRRSV 수용체를 직접 표적으로 삼거나 숙주의 선천적 면역 반응을 조절하는 역할을 합니다. miR-26 계열은 바이러스 복제를 심각하게 손상시킬 수 있으며, miR-26a는 I형 인터페론(IFN)을 조절하여 돼지 폐포 대식세포(PAM)에서 1형 및 2형 PRRSV 계통의 복제를 억제할 수 있습니다. 이는 miR-26b[25,26]보다 더 효율적인 경로입니다. miR-30c 및 miR-125b는 각각 I형 IFN 경로 및 NF-κB 경로를 표적으로 하여 숙주 선천적 면역 반응을 조절하는 것으로 확인되었습니다[27-29]. MiR-23, miR-378 및 miR{14}}은 PRRSV를 표적으로 하는 항바이러스 숙주 인자이며 제2형 PRRSV 변종에 보수적인 표적 부위를 가지고 있습니다[30]. 동시에, 호스트 miR-506은 MARC-145 세포에서 PRRSV 수용체 CD151을 직접 표적으로 삼아 PRRSV 복제를 억제하는 것으로 확인되었습니다[31]. miR-181은 또한 혈액 단핵구 및 PAM에서 PRRSV 수용체 CD163을 하향 조절하여 PRRSV 복제를 간접적으로 억제할 수 있습니다[32]. 또한 miRNA는 기본 세포 생리를 방해하여 PRRSV 복제를 촉진할 수 있습니다. MiR-24-3p 및 miR-22은 PRRSV 감염 중에 HO-1의 30 UTR을 직접 표적으로 삼아 헴 산소화효소-1(HO-1)의 억제를 피합니다. PRRSV에 대한 열 충격 단백질(HSP32라고도 함)[33,34] 돼지는 PRRSV에 더 취약하고 이 병원체가 유기체로 유입되는 것에 대해 자신을 방어할 능력이 떨어지는 것으로 알려져 있습니다[35]. 본 연구에서는 현장에서 유행하는 균주를 이용하여 이 바이러스에 감염된 돼지의 선천면역과 획득면역을 분자수준에서 연구하였다. 혈청 엑소좀 분리 키트, 투과전자현미경(TEM), 나노입자 추적 분석(NTA), 웨스턴 블롯(WB)을 이용하여 PRRSV 감염 전후의 혈청 엑소좀을 분리 및 동정한 후 작은 RNA 염기서열 분석, 동정, 여러 PRRSV 관련 혈청 엑소좀 miRNA를 얻기 위해 생물정보학 방법을 사용하여 차등 발현 결과를 분석한 후 정량적 실시간 PCR(qRT-PCR)을 사용하여 데이터 결과를 식별합니다.
2. 재료 및 방법
2.1. 동물 실험
격리, 건강 관리 및 환경 적응을 위해 PRRSV 항원 및 항체 이중 음성 건강한 42-일령 대형 백돈 6마리를 돼지 청정 급이 시스템에 배치했습니다. 모든 돼지는 제한 없이 자유롭게 먹고 마실 수 있었습니다. 격리기의 조건에 익숙해졌을 때, 이전 연구자들이 언급한 CHsx1401과 같은 2mL 105 TCID50/mL PRRSV NADC30-를 돼지의 비강으로 접종했습니다[36,37]. 혈청 분리를 위해 바이러스 접종 전(대조군, n=6) 및 7일 후(처리군, n=6) 돼지의 혈액을 전대정맥에서 수집했습니다. 혈청 내 세포 잔해물을 3000g에서 15분간 원심분리하여 제거했습니다. 본 연구의 모든 동물 실험은 중국 농업과학원(CAAS)(중국 베이징), IAS2022-130의 동물 과학 연구소 동물 윤리 위원회의 승인을 받았습니다.
2.2. 혈청 엑소좀의 분리 및 정제
제조사의 프로토콜에 따라 exoEasy Maxi 키트(QIAGEN, Hilden, Germany, 카탈로그 번호 76064)를 사용하여 엑소좀 분리 및 정제를 수행했습니다.
2.3. 투과전자현미경(TEM)
추출된 엑소좀 현탁액을 formvar carbo-코팅된 구리 메쉬 위에 스폿팅하고, 엑소좀을 PBS로 헹구고 실온에서 3분 동안 표준 우라닐 아세테이트 염색을 실시했습니다. 실온에서 몇 분 동안 건조시킨 후, 투과전자현미경(HT-7700, Hitachi-High Tech, Tokyo, Japan)을 사용하여 그리드를 시각화하고 100 kV에서 사진을 찍었습니다.
2.4. 나노입자 추적 분석(NTA)
추출된 엑소좀을 1×PBS로 10μL에서 30μL로 변화시켜 희석하였다. 샘플을 테스트한 후, 제조사의 지침(NanoFCM, Xiamen, China)에 따라 N30E flow nano-analyzer로 혈청 엑소좀의 농도와 크기를 분석했습니다.
2.5. 웨스턴 블롯
추출된 엑소좀 샘플을 프로테아제 억제제(Invitrogen, Waltham, MA, USA)와 페닐메틸설포닐 플루오라이드(PMSF)가 혼합된 RIPA 용해물에 첨가하여 엑소좀 단백질을 추출한 후 얼음 위에서 30분간 용해시켰습니다. 그런 다음 Bradford 키트의 지침에 따라 혈청 엑소좀 단백질의 농도를 정량화했습니다. 엑소좀 단백질은 열 변성을 겪었습니다. 동일한 양의 단백질을 12% SDS-PAGE 겔에서 분리한 후 폴리비닐리덴 플루오라이드(PVDF) 멤브레인(Millipore, Burlington, MA, USA)으로 옮겼습니다. 5% 탈지분유를 함유한 TBST에 담그고 실온에서 1시간 동안 밀봉하였다. 우리는 희석된 1차 항체(항-CD9 항체, Abcam, Boston, MA, USA, #ab92726; 항-CD81 항체, Abcam, Boston, MA, USA, #ab109201)에 막을 4℃에서 밤새 담가두었고 회복시켰습니다. 1차 항체. 희석된 2차 항체에 막을 담그고 실온에서 1시간 동안 배양한 후 2차 항체를 회수했습니다. 세척된 PBST 필름을 신선 유지 필름 위에 놓고 동일한 부피의 혼합 ECL a/b 발색 용액을 추가한 후 이를 화학발광 이미저에 배치했습니다.

남성의 면역체계 강화를 위한 시스탄체의 효능
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2.6. 엑소좀 소형 RNA 염기서열 분석 및 데이터 분석
제조업체의 지침에 따라 Trizol을 사용하여 엑소좀의 전체 RNA를 추출했습니다. 그런 다음 RNA 농도와 광학 밀도(OD) 값을 감지하고 1% 아가로스 겔 전기영동으로 RNA의 분해와 순도를 감지했습니다. 한편, Agilent Bioanalyzer 2100은 RNA의 무결성을 감지하는 데 사용되었습니다. 품질검사 후 엑소좀의 total RNA를 사용하였습니다. 제조업체의 지침에 따라 Illumina®(Illumina, San Diego, CA, USA)용 NEB NEXT 다중 소형 RNA 라이브러리 준비 세트를 사용했습니다. 키트는 작은 RNA cDNA 라이브러리를 준비하고 이를 서열 분석하여 Illumina Novaseq 6000 플랫폼을 통해 5{14}} nt 단일 말단 판독을 생성했습니다. 작은 RNA 라이브러리 준비를 위한 모든 절차는 Novogene(중국 베이징)에 의해 수행되었습니다. 품질 관리 후 데이터는 bowtie를 사용하여 돼지 참조 게놈(Sus scrofa 11.1)에 정렬되었습니다. 알려진 miRNA는 miRbase(v22.0) 데이터베이스[38](https://www.mirbase.org, 2022년 1월 14일 액세스), miRdeep2(v0.0.5)[39] 및 miRevo(v1.1)에 의해 식별되었습니다. ) [40] 새로운 miRNA를 예측하는 데 사용되었습니다. 동시에, miRNA에 대한 차등 발현 분석은 DESeq(v1.24.0)[41]에 의해 수행되었으며, |배 변화|가 필요했습니다. > 1.6 및 p < 0.05. MEGA(V11)[42]를 사용하여 정렬을 수행한 후 PHAST(v1.6.9)[43]를 사용하여 단일 염기 점수를 매기고 WUH3(GenBank 등록 번호 HM853973), VR2332( GenBank 접근 번호 U87392), JXA1(GenBank 접근 번호 EF112445), CH{41}}a(GenBank 접근 번호 AY032626), NADC30(GenBank 접근 번호 HN654459), HUN4(GenBank 접근 번호 EF635006), HLJZD 22-1812(GenBank 접근 번호 MN648450), SC/DJY(GenBank 접근 번호 MT075480) 및 Lelystad(GenBank 접근 번호 M96262.2). RNAhybrid(V2.0)[44]는 CHsx1401 바이러스 게놈의 3 0 UTR에 대한 확인된 miRNA 서열의 결합을 예측하는 데 사용되었습니다. Miranda(v3.3a)와 RNAhybrid는 표적 유전자 예측에 사용되었습니다. 클러스터 프로파일[45] R 패키지는 표적 유전자의 GO(Gene Ontology) 기능 강화 분석 및 KEGG(Kyoto Encyclopedia of Genes and Genomes) 경로 강화 분석에 사용되었습니다.
2.7. RT-qPCR에 의한 miRNA 발현 검증
제조사의 프로토콜에 따라 Trizol (Invitrogen, Shanghai, China)을 사용하여 혈청 엑소 좀으로부터 총 RNA를 분리했습니다. 분리된 RNA는 샘플(그룹당 n{1}})에서 RT-qPCR로 확인되었습니다. cDNA는 miRNA 1차 가닥 cDNA 합성(by 스템-루프) 키트(Vazyme, Nanjing, China)의 지시에 따라 합성하였고, 형광 정량은 ABI 7500에 따라 수행하였다. miRNA universal SYBR qPCR 마스터 믹스 지침(Vazyme, Nanjing, China). 사용된 열주기 매개변수는 다음과 같습니다: 첫 번째 단계: 30초 동안 95 ◦C; 2단계: 5초 동안 95°C, 34초 동안 60°C, 40주기; 3단계: 15초 동안 95°C, 1분 동안 60°C, 15초 동안 95°C. U6 유전자인 miRNA의 프라이머 서열은 참조 자료로 사용되었으며 [46] 보충 표 S1에 나열되어 있습니다. 모든 qRT-PCR 검증은 3개의 생물학적 복제와 각 샘플에 대한 3개의 복제를 사용하여 수행되었습니다. 전사체의 상대적 풍부함은 2-Ct 방법으로 계산되었으며, 데이터 분석 및 매핑에는 SPSS(v22.0) 및 GraphPad Prism(v8.0)이 각각 사용되었습니다. p < 0.05는 차이가 통계적으로 유의하다는 것을 의미합니다.
3. 결과
3.1. 바이러스 접종 후 항원과 항체의 상대값
챌린지 전(0일) 및 챌린지 후(7일) PRRSV 항원 및 항체 테스트 결과는 표 1에 나와 있습니다. 챌린지 전 PRRSV 항원 및 항체의 혈청학적 검출은 음성이었고 항원은 챌린지 후 양성 반응을 보였으며 이는 돼지가 CHsx1401에 성공적으로 감염되었음을 나타냅니다.
3.2. 혈청 엑소좀의 분리 및 식별
혈청에서 분리된 소포는 TEM에 의해 발견되었습니다. 대부분의 소포는 중앙에 있는 오목한 접시 모양 또는 디스크 모양의 엑소좀을 볼 수 있습니다. 엑소좀의 막 가장자리가 보이고 형태가 비교적 완전합니다(그림 1A, B). 나노입자 추적 분석에 따르면 엑소좀의 95.73%는 직경이 30~150nm(주로 약 72.25nm)이며 평균 직경은 76.22nm로 엑소좀의 크기 특성과 일치하는 것으로 나타났습니다(그림 1C). 이 크기 범위는 TEM에 의해 검출된 것과 유사했으며 이러한 소포가 엑소솜으로 확인되었음을 추가로 확인했습니다. 웨스턴 블롯 분석은 혈청 샘플에서 분리된 소포가 CD9 및 CD81 단백질에 대해 양성인 것으로 나타났습니다(그림1D). 위의 특성은 ISEV(International Society for Extrace Vesicles)가 MISEV2018에서 제정한 엑소좀 식별 기준에 부합합니다[47].
표 1. 챌린지 바이러스에 대한 (0일) 및 (7일)의 항원 및 항체.


그림 1. 혈청 엑소좀의 주요 특성. (A, B)는 TEM을 통해 소포의 형태학적 특성을 보여줍니다. 스케일 바는 각각 500nm와 100nm입니다. (C) NTA는 대부분의 소포의 직경과 농도를 보여줍니다. (D) 웨스턴 블롯은 혈청 엑소좀에 엑소좀 마커 CD81 및 CD9의 존재를 보여주었습니다. 참고: Mix in WB 결과는 exoEasy Maxi 키트로 분리된 샘플 혼합 현탁액입니다.
3.3. 혈청 엑소좀의 작은 RNA 서열 분석
각 샘플에 대해 순수 데이터는 0.5Gb에 도달했고 Q30 기본 비율은 96.20%를 초과했습니다. 각 샘플의 깨끗한 판독값은 돼지 참조 게놈과 정렬되었습니다. 12개 샘플 중 대조군은 각각 10,920,887, 10,248,696, 10,109,117, 10,655,494, 9,217,285 및 9,782,523개의 읽기를 얻었습니다. 치료 그룹은 각각 11,889,518, 10,593,504, 10,593,504, 12,846,080, 10,105,325, 11,729,451 및 9,789,542 읽기를 얻었습니다. 평균적으로 전체 클린 리드의 77.96%는 길이가 19-22개의 뉴클레오티드(nt)로 구성되었습니다(그림 2A). 품질 관리 후 판독이 전체 판독의 92.59% 이상을 차지했습니다. 처리된 클린 리드는 돼지 참조 게놈에 정렬되었으며 게놈에서 12개 라이브러리의 매핑된 비율은 92.30% 이상이었고 매핑된 비율은 94.98%였습니다(그림 2B). 이는 구축된 혈청 엑소좀 miRNA 라이브러리가 고품질이고 추가 분석에 적합하다는 것을 나타냅니다. 자세한 내용은 보충 표 S2에 나열되어 있습니다.

그림 2. 작은 RNA 전사체 데이터 개요. (A) 혈청 엑소좀 샘플의 판독 수의 길이 분포(nt=뉴클레오티드); (B) 참조 게놈에 매핑된 12개 샘플의 비율
3.4. miRNA의 차등 발현 분석
확인된 miRNA 발현을 정량적으로 분석한 후, 섹션 2.6에서 이전에 설명한 임계값을 기준으로 miRNA를 스크리닝했습니다. CHsx1401 균주(대조군, n= 6; 처리군, n{5}}) 접종 전후에 총 305개의 miRNA가 얻어졌다. 두 그룹 사이에서 총 33개의 차별적으로 발현된(DE) miRNA가 확인되었으며, 13개의 DE miRNA가 상향 조절되었으며, 치료 그룹에서 20개의 DE miRNA가 하향 조절되었습니다(그림 3 및 보충 표 S3).
3.5. miRNA 표적 유전자의 기능 강화 분석
33개의 DE miRNA에 의해 총 7283개의 표적 유전자가 예측되었으며, 표적 유전자의 기능은 주로 MAPK 캐스케이드의 양성 조절, 지질 대사 과정, 세포 내 신호 전달 조절, ERK1 및 ERK2 캐스케이드 등에 집중되었습니다 (그림 4A). ). 분자 기능 측면에서 차별적으로 발현되는 miRNA 표적 유전자는 주로 GTP 효소 조절 활성, 키나제 활성, 뉴클레오시드 트리포스파타제 조절 활성 및 신호 전달 및 에너지 대사와 관련된 기타 기능에 중점을 둡니다(그림 4B). 또한 세포 구성요소 중 표적 유전자는 주로 초분자 고분자, 골지체, 자가포식소체, 세포 표면, 초기 엔도솜 등의 생물학적 기능에 참여한다(그림 4C). 이러한 구성 요소의 기능은 엑소좀 형성과 밀접하게 관련되어 있으며 이는 또한 서열 분석의 정확성을 설명합니다. KEGG 경로 농축 분석에서는 표적 유전자가 세포내이입, MAPK 신호 전달 경로, Rap1 신호 전달 경로, 스핑고지질 신호 전달 경로 및 PI3K Akt 신호 전달 경로에서 상당히 풍부하다는 것을 보여주었습니다(p < 0.05)(그림 5A) ). 동시에 강화된 경로를 분류하고 분석했습니다. 결과는 표적 유전자의 KEGG 경로가 주로 환경 정보 처리, 인간 질병 및 생물학적 시스템에서 풍부하다는 것을 보여주었습니다(그림 5B).

그림 3. 엑소좀에서 miRNA의 차등 발현. (A) 대조군과 치료군 사이의 miRNA의 화산 플롯; (B) 대조군과 치료군 사이의 DE miRNA의 계층적 클러스터링 히트맵.

그림 4. DE miRNA 표적 유전자의 GO 기능 농축 분석. (A) DE miRNA 표적 유전자의 생물학적 과정; (B) DE miRNA 표적 유전자의 분자 기능; (C) DE miRNA 표적 유전자의 세포 구성요소

그림 5. 표적 유전자의 KEGG 경로 농축 분석. (A) DE miRNA의 표적 유전자를 갖는 상당히 강화된 KEGG 경로; (B) 상당히 풍부한 KEGG 경로의 분류.
3.6. 혈청 엑소좀 miRNA 및 PRRSV CHsx1401 게놈의 표적화 예측
PHAST에 의한 정렬 후 단일 염기의 phastCons 점수에 따르면, 바이러스 게놈 중에서 총 8개의 가장 잘 보존된 세그먼트(피크 맵 위의 검은색 밴드)가 얻어졌습니다(그림 6). 보존된 세그먼트에 결합된 miRNA를 예측함으로써 총 31개의 DE miRNA가 보존된 세그먼트에 결합하는 것으로 밝혀졌습니다. 그 중 CHsx1401 게놈의 30 UTR(14,870~15,020)에 가장 가까운 보존 영역(14,644~15,020nt)에서는 5개의 miRNA(ssc-miR-34)를 포함하여 16개의 DE miRNA가 결합할 것으로 예측됩니다. c, ssc-miR-375, ssc-miR-378, ssc-miR-486 및 ssc-miR-6529)은 CHsx1401의 30 UTR에 바인딩할 수 있습니다. 이러한 miRNA 중 ssc-miR-223만이 감염 후 상향 조절되었고 다른 miRNA는 감염 후 하향 조절되었습니다. 자세한 내용은 보충 표 S4를 참조하십시오.

그림 6. PHAST에 의해 예측된 CHsx1401 균주 게놈의 보존된 세그먼트
3.7. 엑소좀 기능 및 PRRSV와 관련된 DE miRNA 스크리닝
표적 유전자의 기능적 농축 분석을 통해 엑소좀과 PRRSV의 기능과 관련된 다양한 차별적으로 발현되는 miRNA가 발견되었습니다. 그 중 ssc-miR-4331-3p, ssc-miR-744 및 ssc-miR-320과 같은 11개의 DE miRNA가 엑소좀 흡수에 관여하며, 이들의 표적 유전자는 주로 다음에 집중되어 있습니다. Ras 유전자 계열, 아넥신 계열 및 ADP 리보실화 유전자 계열. sscmiR-10b, ssc-miR-124a 및 ssc-miR-128을 포함한 18개의 DE miRNA는 면역 관련 경로에 참여하며 이들의 표적 유전자는 주로 MAPK에 집중되어 있습니다. 유전자 가족, PIK3 유전자 가족 및 단백질 포스파타제 유전자 가족. 11개의 DE miRNA가 바이러스 침입에 관여하지만 관련 표적 유전자는 주로 MAPK 유전자 계열과 단백질 포스파타제 유전자 계열에 집중되어 있습니다. 또한 새로운 _102와 같이 차등적으로 발현되는 여러 miRNA가 있습니다. 6개의 DE miRNA(ssc-miR-320, ssc-miR-423-5p, ssc-miR-4331-3p,ssc-miR-7137-3p 및 ssc-miR{{ 포함) 25}}는 그림 7과 같이 엑소좀 기능, PRRSV 바이러스 침입 및 면역 관련 경로에서 공동 발현됩니다. 자세한 내용은 보충 표 S5에 나와 있습니다.
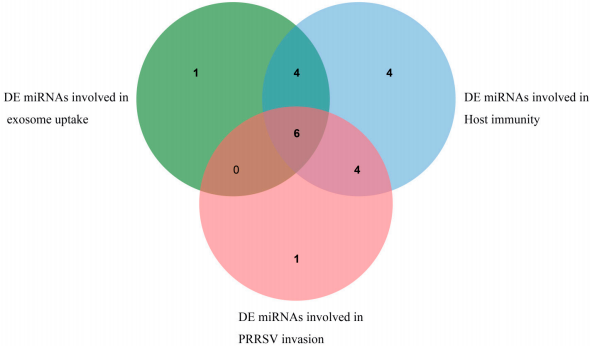
그림 7. 엑소좀 흡수, PRRSV 침입 및 면역과 관련된 DE miRNA
3.8. 두 그룹 간의 DE miRNA에 대한 QRT-PCR 분석
검증을 위해 5개의 DE miRNA가 무작위로 선택되었습니다. qRT-PCR 결과에 따르면 처리군에서는 ssc-miR-19a와 ssc-miR-32의 발현이 증가한 반면, ssc-miR-124a, ssc-miR{ {8}} 및 ssc-miR-34c는 시퀀싱 데이터와 일치하게 대조군에서 더 높은 발현을 나타냈습니다(그림 8).

그림 8. qRT-PCR로 검증된 5개의 DE miRNA
4. 토론
PRRSV는 여전히 전 세계 돼지 산업에서 완고한 병원체로 전 세계적으로 막대한 경제적 손실을 초래하고 있습니다. 현재 예방접종은 주로 PRRSV를 예방하고 통제하기 위해 사용되며, 그 중 MLV(Modified Live) 바이러스 백신이 가장 널리 사용됩니다[48]. 이 백신은 PRRS 발생 및 발생률을 줄이는 데 효과적이었지만 바이러스의 유전적 변이와 다양성을 크게 증가시켰으며 현장에서 야생 백신 바이러스와 살아있는 백신 바이러스 간의 바이러스 재조합을 유도했습니다[49,50]. 최근 몇 년간 PRRSV 변종과 같은 재조합 바이러스 NADC30-의 확산과 유병으로 인해 중국에서 돼지 생식기 및 호흡기 증후군이 여러 차례 발생했습니다. 본 연구에 사용된 CHsx1401과 NADC30의 유사성은 92.2~99.1%로 유지되었습니다. 그 이후로 중국에서는 전염병이 되었습니다. 엑소좀은 세포 소통의 매개체로서 다양한 체액에서 널리 발견되며 질병 진단 및 치료에 독특한 이점을 가지고 있습니다 [51,52]. 이전 보고에 따르면 엑소좀은 항원 제시[53], 면역 반응[53,54], 바이러스 복제[54], 암[55], 신경변성 질환[56], 혈관 신생[57], 종양 세포에서 중요한 의사소통 역할을 한다. 이주[58], 침입[59] 등이 연구 가치가 높다.
본 연구에서는 혈청 엑소좀의 miRNA 발현 프로파일을 구축하기 위해 high-throughput sequencing 기술을 사용하였고, 33개의 DE miRNA가 확인되었습니다. 우리 모두 알고 있듯이, 숙주에 코딩된 miRNA는 바이러스 게놈과 결합한 후 바이러스의 복제, 합성 및 방출을 조절하여 감염을 제한하고 병리학적 과정에 영향을 미칠 수 있습니다[15]. 바이러스 게놈을 표적으로 하는 miRNA에 대한 연구도 동물에서 반복적으로 보고되었습니다. 닭 전염성 윤활낭 질환에서 gga-miR-454 및 gga-miR-130b는 바이러스 게놈을 표적으로 삼아 바이러스 복제를 억제할 수 있는 반면, gga-miR-21는 바이러스 단백질 VP1을 직접 표적으로 삼아 억제할 수 있습니다. 바이러스 성 단백질 번역 [60,61]. PRRSV 연구에서 ssc-miR-181은 바이러스 게놈 ORF4 하류의 고도로 보존된 영역에 특이적으로 결합하여 PRRSV 복제를 강력하게 억제합니다[62]. 본 연구에서는 두 그룹 간의 ssc-miR-181의 발현 차이가 유의한 수준에 도달하지 못했습니다. 우리 연구에서는 9개의 서로 다른 PRRSV 바이러스의 게놈을 CHsx1401 균주의 게놈과 비교하여 가장 잘 보존된 8개의 세그먼트를 확인했습니다. 31개의 DE miRNA가 CHsx1401의 가장 잘 보존된 8개 세그먼트에 결합할 수 있고, 16개의 DE miRNA가 CHsx1401의 30 UTR에 가까운 보존된 서열에 결합할 수 있는 것으로 예측되었습니다. 그중에는 5개의 DE miRNA(ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR-486 및 ssc-miR{{)이 있습니다. 36}}) 동시에 CHsx1401 30 UTR에 바인딩할 수 있습니다. 또한, ssc-miR-223의 상향조절된 발현은 PRRSV 게놈의 30 UTR 표적에 결합할 것으로 예측되었습니다. 결과는 바이러스 게놈의 보존된 서열이 바이러스의 병원성에 중요한 역할을 할 수 있으며, 서로 다른 PRRSV 균주의 게놈 사이에 보존된 서열에 결합할 수 있는 miRNA가 바이러스의 병원성을 제어하는 데 중요한 의미를 가질 수 있음을 보여주었습니다. ssc-miR-10b[63], ssc-miR-378[30]을 포함하여 일부 차등적으로 발현된 miRNA는 이전 연구를 통해 PRRSV와 관련이 있고 심지어 PRRSV의 규제에 직접적으로 관여하는 것으로 입증되었습니다. , ssc-miR-124a [64], let-7f-5p [65], ssc-miR-744 [66] 및 ssc-miR{{57 }}a[67].
PRRSV는 선천성 면역 반응을 방해하여 숙주 방어를 회피할 수 있습니다. 이 과정은 MAPK 신호 경로, PI3K Akt 신호 경로, 자가포식, 케모카인 및 TNF 신호 경로를 포함한 많은 신호 경로에 의해 조절됩니다. 현재 MAPK 신호 전달 경로에는 ERK1/2, JNK 및 p38 경로의 세 가지 주요 경로가 포함됩니다. MAPK 캐스케이드의 활성화는 숙주 세포의 세포사멸을 촉진하고 바이러스가 숙주 면역 방어 반응을 피하도록 돕고 PRRSV 복제를 촉진할 수 있습니다. 더욱이, c-Jun N-말단 키나제(JNK) 및 p38의 활성화는 염증 인자 IL-10 [68-70]의 방출을 촉진하고 염증 효과를 향상시킬 수도 있습니다. 세포사멸을 유도하는 것 외에도 PRRSV는 PRRSV 복제를 촉진할 수 있는 자가포식을 유도할 수도 있습니다. PI3K/Akt의 활성화는 바이러스 진입과 바이러스 복제 촉진에 필요하며, PRRSV 활성화 Akt는 JNK 경로를 음성적으로 조절하여 숙주 세포의 세포사멸을 억제합니다[71]. TNF는 다른 염증 인자와 함께 염증 반응의 유도 및 조절에 중요한 역할을 할 수 있지만, TNF 발현은 PRRSV 복제의 음성 조절에 의해 영향을 받습니다[72]. 본 연구에서는 miRNA(ssc-miR-10b, ssc-miR-122-5p, ssc-miR-124a, ssc-miR-128, ssc-miR{ {24}}a-5p 등) 이러한 경로가 풍부한 것은 PRRSV 유발 세포사멸, 자가포식 및 염증에 관여하며 바이러스 면역 반응, 면역 회피 및 복제와 밀접하게 연관되어 있습니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
세포 원형질막에는 다양한 지질 뗏목이 풍부하며, 스핑고지질과 콜레스테롤이 풍부한 스핑고지질(스핑고미엘린 및 글리코스핑고지질)은 지질 뗏목의 핵심 분자입니다. 바이러스의 일부 단백질에 의한 지질 인식은 바이러스 침입에 필요한 조건일 수 있습니다[73]. 외피 바이러스는 바이러스 진입 단계에서 바이러스 외피 당단백질을 지질 래프트에 삽입하거나, 지질 래프트에 위치한 수용체와 상호 작용하거나, 자연 상태에서 활성화된 형태로 변화하여 바이러스 내재화/융합을 시작하거나 촉진합니다(예: HSV, SARS 코로나바이러스 및 새끼 돼지 전염병 설사 바이러스 [73,74]. 이전 연구에서는 MARC{5}} 세포 표면에서 콜레스테롤을 제거하면 PRRSV 감염이 크게 감소하는 것으로 나타났으며, 이는 PRRSV 감염 억제가 세포 콜레스테롤 제거에 의해 구체적으로 매개된다는 것을 입증합니다. 세포막 콜레스테롤의 고갈은 바이러스 침입, 특히 바이러스 부착 및 방출을 크게 억제했습니다[75]. 스핑고지질 대사는 막 구조와 접착을 조절할 수 있으며 이는 PRRSV 바이러스 침입에 매우 중요합니다. 세포내이입은 이 연구에서 가장 중요한 농축이었습니다. 세포내이입은 표적 세포에 의한 엑소좀 흡수의 중요한 메커니즘입니다. 이전 연구에서는 엑소좀 흡수가 에너지를 요구하고 세포골격에 의존하는 과정이라는 것이 밝혀졌으며, 이는 이 과정에서 세포내이입의 잠재적인 역할을 강조합니다[76]. 식세포작용, 거대음작용, 클라트린 등을 포함한 여러 경로가 이 과정을 중재할 수 있다는 것이 입증되었으며[77,78], 이로 인해 세포내이입된 물질의 분류와 역할이 달라졌습니다. 이 경로에서 차등적으로 발현된 엑소좀 miRNA의 농축은 엑소좀이 PRRSV 감염에서 중요한 역할을 하며 엑소좀의 내용물 수송 및 흡수 조절이 표적 세포 및 기관의 병태생리학적 변화로 이어질 수 있음을 나타냅니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
5. 결론
본 연구에서는 PRRSV에 감염된 돼지의 혈청 엑소좀 miRNA 식별 및 생물정보학 분석을 통해 ssc-miR-4331-3p, ssc-miR{{과 같은 다양한 PRRSV 관련 경로와 차별적으로 발현된 miRNA를 얻었습니다. 5}}, sscmiR-320, ssc-miR-10b, ssc-miR-124a, ssc-miR-128 등은 PRRSV에서 잠재적인 기능적 역할을 합니다. - 유도된 면역 반응, 침입 및 엑소좀 흡수. 또한 단일 miRNA는 여러 유전자를 표적으로 삼을 수 있고 단일 유전자도 여러 miRNA에 의해 조절되므로 여러 miRNA가 위 경로에서 여러 기능을 수행합니다. ssc-miR-10b, ssc-miR-378, miR-124a와 같은 일부 miRNA는 주요 수용체에 작용하거나 바이러스 게놈을 직접 표적으로 삼아 PRRSV 감염을 조절하는 것으로 확인되었습니다. let-7f-5p, ssc-miR-744, ssc-miR-19a 등. 한편, 본 연구에서는 결합할 수 있는 다양한 miRNA도 예측했습니다. ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR{{34}을 포함하여 CHX1401 바이러스 게놈의 30 UTR 중 가장 보존된 단편 } 및 ssc-miR-6529은 바이러스 병원성을 조절하는 데 중요할 수 있습니다.
참고자료
1. 스니더, EJ; 키커트, M.; Fang, Y. Arterivirus 분자생물학 및 발병기전. J. 비롤 장군. 2013, 94 Pt 10, 2141–2163. [상호참조] [PubMed]
2. 루, Y.; 장 Y.; 시앙, X.; 샤르마, M.; 리우, K.; 웨이, J.; 샤오, D.; 리, 비.; 통, G.; 매사추세츠주 올셰프스키; 외. 노치 신호전달은 돼지 폐포 대식세포에서 고병원성 돼지 생식기 및 호흡기 증후군 바이러스(HP-PRRSV) 감염에 의해 유도된 염증성 사이토카인의 발현에 기여합니다. 개발. 비교. 면역. 2020, 108, 103690. [CrossRef] [PubMed]
3. 데아, S.; 소이어, N.; 알랭, R.; Athanassious, R. 허용성이 높은 MARC-145 세포 클론에서 전파되는 돼지 생식기 및 호흡기 증후군 바이러스의 미세 구조적 특성 및 형태 형성. 고급 특급. 메드. Biol. 1995, 380, 95-98. [펍메드]
4. Dokland, T. PRRSV의 구조 생물학. 바이러스 해상도. 2010, 154, 86–97. [상호참조] [PubMed]
5. 존슨, CR; 그릭스, TF; 그나난다라자, J.; Murtaugh, MP 모든 동맥바이러스에 존재하는 대체 ORF5에 의해 암호화된 돼지 생식기 및 호흡기 증후군 바이러스의 새로운 구조 단백질. J. 비롤 장군. 2011, 92편 5, 1107-1116. [상호참조] [PubMed]
6. 이, 사우스캐롤라이나; 이석수; 유기광; 최화우; 아니, YH; 박, CE; 신진호; 윤이지; 강시윤; Lee, C. 배양된 돼지 폐포 대식세포에서 연속 계대 후 약화된 돼지 생식기 및 호흡기 증후군 바이러스 균주의 표현형 및 유전형 분석. J. 수의사. 과학. 2018, 19, 358-367. [상호참조] [PubMed]
7. Zebrowska, A.; Skowronek, A.; Wojakowska, A.; 위드락, P.; Pietrowska, M. 엑소좀의 대사체: 암세포에 의해 방출되고 인체 체액에 존재하는 소포에 중점을 둡니다. 국제 J.Mol. 과학. 2019, 20, 3461. [상호참조]
8. 베벨만, 의원; 스미트, MJ; 페그텔, DM; Baglio, SR 암에서의 세포외 소포의 생합성 및 기능. Pharmacol. 거기. 2018, 188, 1–11. [상호참조]
9. 자보로프스키(Zaborowski) 의원; 발라지, L.; 브레이크필드, XO; Lai, CP 세포밖 소포체: 구성, 생물학적 관련성 및 연구 방법. 생명과학 2015, 65, 783-797. [상호참조]
10. 알무글리크, FB; 고와이큐; 페이리스, HN; 바스와니, K.; 홀랜드, 오.; 마이어, S.; JR 로슈; 버크, CR; 매사추세츠주 크룩켄덴; 아라치게, BJ; 외. 순환하는 엑소좀은 대사 장애 위험이 있는 소의 바이오마커를 식별할 수 있습니다. 과학. 2019, 9, 13879. [상호참조]
11. 장, RC; 두, WQ; 장, JY; 유, SX; 루, FZ; 딩, HM; 쳉, YB; 렌, C.; Geng, DQ 말초 신경 손상에 대한 중간엽 줄기 세포 치료: 서사적 검토. 신경 재생. 결의안. 2021년 16월 2170~2176년. [펍메드]
12. 브리즈구노바, OE; 자리포프, MM; Skvortsova, TE; 렉치노프, EA; Grigor'eva, AE; 아이오와주 자포로즈첸코; 모로즈킨, ES; Ryabchikova, EI; 유르첸코, YB; 보이치츠키, VE; 외. 건강한 사람과 전립선암 환자의 소변에서 세포밖 소포체의 비교 연구. PLoS ONE 2016, 11, e0157566. [상호참조] [PubMed]
13. Camussi, G.; 데레기부스, MC; 브루노, S.; 그레인지, C.; 폰사토, V.; Tetta, C. 세포의 엑소솜/미세소포 매개 후성유전적 재프로그래밍. 오전. J. Cancer Res. 2011, 1, 98–110. [펍메드]
14. 탐코비치, SN; 투타노프, OS; Laktionov, PP 엑소좀: 생성, 구조, 수송, 생물학적 활동 및 진단 응용. 생화학. 모스크바. 공급 Ser. 회원. 셀바이올. 2016, 10, 163-173. [상호참조]
15. Bartel, DP MicroRNA: 유전체학, 생물 발생, 메커니즘 및 기능. 셀 2004, 116, 281–297. [상호참조]
16. 고르디노, G.; 코스타-페레이라, S.; 코레데이라, P.; 알베스, P.; 코스타, L.; 고메스, AQ; 실바-산토스, B.; Ribot, JC MicroRNA-181a는 Map3k2 및 Notch2를 표적으로 하여 인간 δ T 세포 분화를 제한합니다. EMBO Rep. 2022, 23, e52234. [상호참조]
17. 리우, B.; 얀, 엘.; 치, Y.; 선, Y.; Yang, X. Long 비코딩 RNA AFAP1-AS1은 miR-107/PDK4 축을 조절하여 난소암 진행을 촉진합니다. J. 난소 Res. 2021, 14, 60. [상호참조]
18. 김영수; 이DH; 박, SH; 전티; Jung, CH 비알코올성 지방간 질환의 자가포식 조절에서 마이크로RNA와 전사 인자의 상호 작용. 특급. 몰. 메드. 2021, 53, 548–559. [상호참조]
19. Kazmierczak, D.; 조펙, K.; Sterzynska, K.; 노비키, M.; 루신스키, M.; Januchowski, R. 시스플라틴 및 파클리탁셀 내성 난소암 세포주에서 약물 내성 유전자 조절에 있어서 microRNA 발현 및 잠재적인 역할의 프로필. 국제 J.Mol. 과학. 2022, 23, 526. [상호참조]
20. 공와이.; 웨이, X.; 썬, W.; 렌, X.; 첸, J.; 아웨야, JJ; 마, H.; 찬, KG; 장 Y.; Li, S. Exosomal miR-224은 갑각류의 박테리아 감염 중 혈림프 미생물군 항상성에 기여합니다. PLoS Pathog. 2021년 17월, e1009837. [상호참조]
21. 쳉, Y.; 코우, W.; 주, D.; 유, X.; Zhu, Y. 부신피질 암종의 진단, 예후 및 질병 모니터링의 미래 방향: 새로운 비침습적 바이오마커. 앞쪽. 내분비놀. 2022, 12, 811293. [CrossRef] [PubMed]
22. 갈로, A.; 탠든, M.; 알레비조스, I.; Illei, GG 혈청과 타액에서 검출 가능한 대부분의 마이크로RNA는 엑소좀에 집중되어 있습니다. PLoS ONE 2012, 7, e30679. [상호참조] [PubMed]
23. 팬, B.; 쵸프, M.; 장, ZG; Liu, XS 당뇨병성 신경병증에 대한 바이오마커 및 치료 표적으로서 마이크로RNA의 새로운 역할. 앞쪽. 뉴롤. 2020, 11, 558758. [CrossRef] [PubMed]
24. 웨이, H.; 첸, Q.; 린, L.; 샤, C.; 리, 티.; 리우, Y.; 음, X.; 쉬, Y.; 첸, 엘.; 가오, W.; 외. 엑소좀 생산 및 화물 분류 규제. 국제 J. Biol. 과학. 2021, 17, 163–177. [상호참조]
25. 지아, X.; 비, Y.; 리, J.; 시에, Q.; 양, H.; Liu, W. 세포 마이크로RNA miR-26a는 선천적 항바이러스 면역을 활성화하여 돼지 생식기 및 호흡기 증후군 바이러스의 복제를 억제합니다. 과학. 2015, 5, 10651. [상호참조]
26. 리, 엘.; 웨이, Z.; 저우, Y.; 장, Y.; 유, 엘.; 정, H.; 통, W.; 양, S.; 정, H.; 샨, T.; 외. 숙주 miR-26a는 I형 인터페론을 상향 조절하여 돼지 생식기 및 호흡기 증후군 바이러스의 복제를 억제합니다. 바이러스 해상도. 2015, 195, 86–94. [상호참조]
27. 리우, F.; 왕, H.; 두, L.; 웨이, Z.; 장, Q.; Feng, WH MicroRNA-30c는 인터페론-알파/베타 수용체 베타 사슬을 표적으로 삼아 제2형 PRRSV 감염을 촉진합니다. J. 비롤 장군. 2018, 99, 1671-1680. [상호참조]
28. 장, Q.; 황, C.; 양, Q.; 가오, L.; 리우, HC; 탕, J.; Feng, WH MicroRNA-30c는 JAK1을 표적으로 하여 돼지 생식기 및 호흡기 증후군 바이러스 감염을 촉진하기 위해 I형 IFN 반응을 조절합니다. J. Immunol. 2016, 196, 2272-2282. [상호참조]
29. 왕, D.; 카오, L.; 쉬, Z.; 팡, L.; 종 Y.; 첸, Q.; 루오, R.; 첸, H.; 리, K.; Xiao, S. MiR-125b는 NF-κB 경로를 부정적으로 조절하여 돼지 생식기 및 호흡기 증후군 바이러스 복제를 감소시킵니다. PLoS ONE 2013, 8, e55838. [상호참조]
30. 장, Q.; 구오, XK; 가오, L.; 황, C.; 리, N.; 지아, X.; 리우, W.; Feng, WH MicroRNA-23는 PRRSV RNA를 직접 표적으로 삼고 유형 I 인터페론을 상향 조절하여 PRRSV 복제를 억제합니다. 바이러스학 2014, 450-451, 182-195. [상호참조]
31. 우, J.; 펭, X.; 저우, A.; 챠오, M.; 우, H.; 샤오, H.; 리우, G.; 정, X.; 장, S.; Mei, S. MiR-506은 CD151을 통해 MARC-145 세포에서 PRRSV 복제를 억제합니다. 몰. 셀. 생화학. 2014, 394, 275-281. [상호참조]
32. 가오, L.; 구오, XK; 왕, L.; 장, Q.; 리, N.; 첸, XX; 왕 Y.; Feng, WH MicroRNA 181은 PRRSV 수용체 CD163을 표적으로 삼아 돼지 생식기 호흡기 증후군 바이러스(PRRSV) 감염을 억제합니다. J. 비롤. 2013, 87, 8808-8812. [상호참조]
33. 샤오, S.; 두, T.; 왕, X.; NIH : 국립보건원.; 얀, Y.; 리, N.; 장, C.; 장, A.; 가오, J.; 리우, H.; 외. MiR-22은 숙주 인자 HO-1를 표적으로 삼아 돼지 생식기 및 호흡기 증후군 바이러스 복제를 촉진합니다. 수의사. 미생물. 2016, 192, 226–230. [상호참조]
34. 샤오, S.; 왕, X.; NIH : 국립보건원.; 리, N.; 장, A.; 리우, H.; 푸, F.; 쉬, L.; 가오, J.; 자오, Q.; 외. MicroRNA miR-24-3p는 hemeoxygenase-1 발현 억제를 통해 돼지 생식기 및 호흡기 증후군 바이러스 복제를 촉진합니다. J. 비롤. 2015, 89, 4494-4503. [상호참조]
35. 버틀러, JE; 신코라, M.; 왕, G.; 스테파노바, K.; 리, Y.; Cai, X. 흉선세포 발달의 교란은 PRRS 전염병의 기초가 됩니다: 테스트 가능한 가설. 앞쪽. 면역. 2019, 10, 1077. [상호참조]
36. 저우, L.; 왕, Z.; 딩, Y.; 스테파노바, K.; 리, Y.; Cai, X. NADC30-와 같은 돼지 생식기 호흡기 증후군 바이러스 계통, 중국. 신흥. 감염. 디스. 2015, 21, 2256-2257. [상호참조]
37. 저우, L.; 양, B.; 쉬, L.; 진, H.; Ge, X.; 구오, X.; 한제이; Yang, H. 돼지 생식기 및 호흡기 증후군 바이러스 NADC30- 유사 계통에 대한 세 가지 변형 생 바이러스 백신의 효능 평가. 수의사. 미생물. 2017, 207, 108–116. [상호참조]
38. 웡, N.; Wang, X. miRDB: microRNA 표적 예측 및 기능 주석을 위한 온라인 리소스. 핵산 해상도. 2015, 43, D146–D152. [상호참조]
39. 프리드랜더, MR; 매코위악, SD; 리, N.; 첸, W.; Rajewsky, N. miRDeep2는 7개 동물 계통군에서 알려진 수백 개의 새로운 microRNA 유전자를 정확하게 식별합니다. 핵산 해상도. 2012, 40, 37–52. [상호참조]
40. 웬, M.; 센, Y.; 시, S.; Tang, T. miREvo: 차세대 염기서열 분석 실험을 위한 통합 microRNA 진화 분석 플랫폼입니다. BMC바이오인폼. 2012, 13, 140. [상호참조]
41. 앤더스, S.; Huber, W. 서열 수 데이터에 대한 차등 표현 분석. 게놈 바이오. 2010, 11, R106. [상호참조] [PubMed]
42. 타무라, K.; 스테처, G.; Kumar, S. MEGA11: 분자진화유전학 분석 버전 11. Mol. Biol. 진화. 2021, 38, 3022–3027. [상호참조] [PubMed]
43. 휴비스, MJ; 폴라드, 캔자스; Siepel, A. PHAST 및 RPHAST: 공간/시간 모델을 이용한 계통발생 분석. 짧은. 생물정보. 2011, 12, 41–51. [상호참조] [PubMed]
44. 크루거, J.; Rehmsmeier, M. RNAhybrid: microRNA 표적 예측이 쉽고 빠르며 유연합니다. 핵산 해상도. 2006, 34, W451–W454. [상호참조]
45. 유, G.; 왕, LG; 한영; He, QY ClusterProfiler: 유전자 클러스터 간의 생물학적 주제를 비교하기 위한 R 패키지입니다. 오믹스 2012, 16, 284-287. [상호참조]
46. 큐, R.; 딩, G.; 첸, J.; Cao, L. 췌장 선암종 환자의 혈청 엑소좀 마이크로RNA 및 임상병리학적 특징 분석. 세계 J. Surg. 온콜. 2013, 11, 219. [상호참조]
47. 테리, C.; 위트워, KW; 아이카와, E.; 알카라즈, MJ; 앤더슨, JD; 안드리안티토하이나, R.; 안토니유, A.; 아랍, T.; 아처, F.; Atkin-Smith, GK; 외. 세포외소포 연구를 위한 최소 정보 2018(MISEV2018): 국제세포외소포학회의 입장 성명 및 MISEV2014 지침 업데이트. J.엑스트라셀. Vesicles 2018, 7, 1535750. [CrossRef]
48. Lyoo, K.-S.; 최재영; 한, 대만; 박, KT; Kim, HK 변형 생돼지생식기호흡기증후군 바이러스 백신 접종이 포장 조건에서 비육돈의 성장 성능에 미치는 영향. J. 수의사. 메드. 과학. 2016, 78, 1533-1536. [상호참조]
49. 비안, T.; 선, Y.; 하오, M.; 조우, L.; Ge, X.; 구오, X.; 한제이; Yang, H. NADC30- 유사와 MLV 유사 사이의 재조합 2형 돼지 생식기 및 호흡기 증후군 바이러스: 새끼 돼지에 대한 유전적 특성 및 병원성. 감염. 그 가죽. 진화. 2017, 54, 279-286. [상호참조]
50. 리, Y.; 지지; 왕, J.; 탄, F.; 주앙, J.; 리, X.; Tian, K. 다른 균주와의 재조합을 특징으로 하는 NADC30-유사 돼지 생식기 및 호흡기 증후군 바이러스의 완전한 게놈 서열. 게놈 발표. 2016, 4, e00330-16. [상호참조]
51. 칼루리, R.; Lebleu, VS 엑소좀의 생물학, 기능 및 생물의학 응용. 사이언스 2020, 367, eaau6977. [상호참조] [PubMed]
52. Miao, XY 엑소좀에서 miRNA의 역할과 치료 가능성에 대한 이해가 최근 발전했습니다. J. 통합. 농업. 2017, 16, 753-761. [상호참조]
53. 셰노다, BB; Ajit, SK 항원 제시 세포에서 유래된 엑소좀에 의한 면역 반응의 조절. 클린. 메드. 인사이트 파톨. 2016, 9(Suppl. S1), CPath-S39925. [상호참조] [PubMed]
54. 리, S.; 리, S.; 우, S.; Chen, L. Exosomes는 HBV 감염에서 바이러스 복제 및 숙주 면역 반응을 조절합니다. BioMed 해상도. 국제 2019, 2019, 2103943. [상호참조]
55. 녹화, DW; 고팔, SK; 쉬, R.; 심슨, RJ; Chen, W. Exosomes 및 면역 조절 및 암에서의 역할. 세포 및 발달 생물학 세미나에서; 학술 출판물: 미국 매사추세츠주 케임브리지, 2015년; 40권, 72~81페이지.
56. 호위트, J.; Hill, 신경퇴행성 질환의 병리학에서의 AF 엑소좀. J. Biol. 화학. 2016, 291, 26589-26597. [상호참조]
57. 리베이로, MF; 주, H.; 밀라드, RW; Fan, G. Exosomes는 혈관신생 촉진 및 항혈관신생 기능을 합니다. 현재 혈관신생 2013, 2, 54-59. [상호참조]
58. 란, J.; 선, 엘.; 쉬, F.; 리우, L.; 후, F.; 송디; 허우, Z.; 우, W.; 루오, X.; 왕, J.; 외. M2 대식세포 유래 엑소좀은 대장암의 세포 이동과 침입을 촉진합니다. 암 입술. 2019, 79, 146–158. [상호참조]
59. 아가, M.; 벤츠, GL; 라파, S.; 토리시, MR; 콘도, S.; 와키사카, N.; 요시자키, T.; 파가노, JS; Shackelford, J. Exosomal HIF1은 비인두 암종 관련 LMP1-양성 엑소좀의 침습 가능성을 지원합니다. 종양 유전자 2014, 33, 4613-4622. [상호참조]
60. 푸, M.; 왕, B.; 첸, X.; 그, Z.; 왕 Y.; 리, X.; 카오, H.; Zheng, SJ gga-miR-454은 IBDV 게놈 세그먼트 B 및 SOCS6(사이토카인 신호 전달 6)의 세포 억제자를 직접 표적으로 삼아 감염성 윤활낭 질환 바이러스(IBDV) 복제를 억제합니다. 바이러스 해상도. 2018, 252, 29–40. [상호참조]
61. 푸, M.; 왕, B.; 첸, X.; 그, Z.; 왕 Y.; 리, X.; 카오, H.; Zheng, SJ MicroRNA gga-miR-130b는 바이러스 게놈의 표적화와 사이토카인 신호 전달의 세포 억제 인자를 통해 감염성 윤활낭 질환 바이러스 복제를 억제합니다. 5. J. Virol. 2018, 92, e01646-17. [상호참조]
62. 구오, XK; 장, Q.; 가오, L.; 리, N.; 첸, XX; Feng, WH microRNA 181의 발현 증가는 돼지 생식기 및 호흡기 증후군 바이러스 복제를 억제하고 바이러스 감염을 제어하는 데 영향을 미칩니다. J. 비롤. 2013, 87, 1159-1171. [상호참조] [PubMed]
63. 콩, 피.; 샤오, S.; 첸, Y.; 왕, L.; 가오, J.; 리, M.; 그, Z.; 구오, Y.; 자오, G.; 장, X.; 외. 돼지 폐포 대식세포(PAM 세포)의 통합된 miRNA 및 mRNA 전사체는 H-PRRSV 및 N-PRRSV 감염과 관련된 계통 특이적 miRNA 분자 시그니처를 식별합니다. 몰. Biol. 2014, 41, 5863-5875. [상호참조] [PubMed]
64. 리, 엔.; 황, K.; 첸, Y.; 황, Z.; 장 Y.; 렝, C.; 리우, Y.; 시, J.; 샤오, S.; Yao, L. MicroRNA ssc-miR-124a는 숙주 유전자 CD163의 억제를 통해 돼지 생식기 및 호흡기 증후군 바이러스에 대한 항바이러스 활성을 나타냅니다. 수의사. 미생물. 2021, 261, 109216. [CrossRef] [PubMed]
65. 리, 엔.; 두, T.; 얀, Y.; 장, A.; 가오, J.; 허우, G.; 샤오, S.; Zhou, EM MicroRNA let-7f-5p는 MYH9를 표적으로 삼아 돼지 생식기 및 호흡기 증후군 바이러스를 억제합니다. 과학. 2016, 6, 34332. [상호참조]
66. 젠, Y.; 왕, F.; 리앙, W.; 리우, J.; 가오, G.; 왕 Y.; 쉬, X.; 수, Q.; 장, Q.; Liu, B. Tongcheng의 돼지 폐포 대식세포와 PRRSV에 반응한 대형 백돈에서 차별적으로 발현된 비코딩 RNA의 확인. 과학. 2018, 8, 15621. [상호참조]
67. 저우 X.; 마이클, JJ; 지앙, Z.; Liu, B. 생체 내에서 PRRSV에 감염된 토착 중국 Tongcheng 돼지의 폐포 대식세포에서 MicroRNA 발현 프로파일링. J. Appl. 그 가죽. 2017, 58, 539-544. [상호참조]
68. 이영재; Lee, C. 돼지 생식기 및 호흡기 증후군 바이러스 복제는 세포외 신호 조절 키나제(ERK) 신호 전달 경로의 억제에 의해 억제됩니다. 바이러스 해상도. 2010, 152, 50–58. [상호참조]
69. 송S.; 비, J.; 왕, D.; 팡, L.; 장, L.; 리, F.; 첸, H.; Xiao, S. 돼지 생식기 및 호흡기 증후군 바이러스 감염은 돼지 폐포 대식세포에서 NF-κB 및 p38 MAPK 경로를 통해 IL{1}} 생산을 활성화합니다. 개발. 비교. 면역. 2013, 39, 265-272. [상호참조]
70. 음, S.; 후오, Y.; 동영; 팬, 엘.; 양, H.; 왕, L.; 닝, Y.; Hu, H. c-Jun NH(2)-말단 키나제의 활성화는 돼지 생식기 및 호흡기 증후군 바이러스 유발 세포사멸에 필요하지만 바이러스 복제에는 필요하지 않습니다. 바이러스 해상도. 2012, 166, 103–108. [상호참조]
71. Fan, L. PRRSV 감염 시 숙주 세포에서 세포사멸 유도 조절에 관여하는 신호 전달 경로. 바이러스 유전자 2019, 55, 433-439. [상호참조]
72. 로페즈-푸에르테스, L.; 캄포스, E.; 도메네크, N.; 에즈케라, A.; 카스트로, JM; 도밍게즈, J.; Alonso, F. PRRS(돼지 생식기 및 호흡기 증후군) 바이러스는 감염된 대식세포에서 TNF- 생산을 하향 조절합니다. 바이러스 해상도. 2000, 69, 41–46. [상호참조]
73. Teissier, É.; Pécheur, EI 지질은 바이러스 융합 단백질에 의해 매개되는 막 융합 조절제입니다. 유로. 생물 물리학. J. 2007, 36, 887-899. [상호참조]
74. 전재호; Lee, C. 돼지 니도바이러스 감염에는 세포 콜레스테롤이 필요합니다. 아치. 비롤. 2017, 162, 3753-3767. [상호참조]
75. 선, Y.; 샤오, S.; 왕, D.; 루오, R.; 리, 비.; 첸, H.; Fang, L. MARC-145 세포에서 돼지 생식기 및 호흡기 증후군 바이러스 진입 및 방출에는 세포막 콜레스테롤이 필요합니다. 과학. 중국 생명 과학. 2011, 54, 1011-1018. [상호참조]
76. 티안, 티.; 주, YL; 저우, YY; 리앙, GF; 왕, YY; 후, FH; Xiao, ZD clathrin 매개 세포내이입 및 거대음작용을 통한 Exosome 흡수 및 miR-21 전달 매개. J. Biol. 화학. 2014, 289, 22258-22267. [상호참조]
77. 루이지애나주 멀케이; 핑크, RC; Carter, DRF 경로 및 세포외 소포 흡수 메커니즘. J.엑스트라셀. Vesicles 2014, 3, 24641. [CrossRef]
78. 장, M.; 장, X.; 왕, M.; 리, Z.; 챠오, M.; 뭐.; Chen, D. 약물 전달을 위한 생체 영감 및 다용도 수단으로서의 엑소좀 기반 나노운반체: 최근 발전과 과제. J. Mater. 화학. B 2019, 7, 2421-2433. [상호참조]
