티로시나아제의 촉매 기반 특이적 검출 및 억제 및 그 응용 파트 1
May 09, 2023
추상적인
Tyrosinase는 멜라닌소체에서 멜라닌 형성을 조절하는 중요한 효소이며 모발과 피부의 색소 침착에 중요한 역할을 합니다. 티로시나제의 비정상적인 발현 또는 활성화는 백색증, 백반증, 흑색종 및 파킨슨병과 같은 여러 질병과 관련이 있습니다. 과도한 멜라닌 침착은 인체에 주근깨, 갈색반점 등의 질병을 유발할 수 있으며, 과일 및 채소의 갈변 및 곤충 탈피와도 밀접한 관련이 있습니다. 티로시나제의 활성을 검출하고 억제하는 것은 이러한 질병의 진단 및 치료 과정에서 매우 중요합니다. 따라서 많은 선택적 광학 검출 탐침 및 저분자 억제제가 개발되었으며 이러한 질병에 대한 기초 및 임상 연구에 크게 기여했습니다. 이 논문에서는 tyrosinase의 검출 및 억제와 미백 제품에 대한 적용을 검토하고 특히 형광 프로브 및 억제제 개발에 중점을 둡니다. 바라건대, 이 검토가 흑색종과 같은 질병에 대한 새로운 치료법을 밝히는 것뿐만 아니라 보다 효율적이고 민감한 티로시나제 프로브 및 억제제를 설계하는 데 도움이 되기를 바랍니다.
관련 연구에 따르면,담배"생명을 연장하는 기적의 허브"로 알려진 일반적인 허브입니다. 주요 구성 요소는시스타노사이드등의 다양한 효과가 있습니다.산화 방지제,항염증, 그리고면역 기능 촉진. cistanche와피부호분cistanche glycosides의 항산화 효과에 있습니다. 인간 피부의 멜라닌은 티로신의 산화에 의해 생성됩니다.티로시나아제, 산화 반응에는 산소의 참여가 필요하므로 체내의 산소가 없는 라디칼이 중요한 요소가 됩니다.영향을 미치는 멜라닌생산. Cistanche는 산화 방지제인 cistanoside를 함유하고 있으며 신체의 자유 라디칼 생성을 감소시킬 수 있습니다.억제멜라닌생산.

Cistanche Tubulosa 보충제를 클릭하십시오.
더 많은 정보를 위해서:
david.deng@wecistanche.com WhatApp:86 13632399501
키워드:
1. 소개
Tyrosinase(EC 1.14.18.1; catechol oxidase; polyphenol oxidase[1] 또는 diphenolase)는 멜라닌 형성에서 가장 중요한 구리 함유 효소로 간주됩니다. Tyrosinase는 분자 산소의 작용 하에서 하이드록실화 및 모노페놀 단위의 오르토퀴논으로의 후속 산화를 촉매할 수 있습니다. 그것은 멜라닌의 합성, 저장 및 수송 부위인 멜라노좀에서 발견됩니다. 약하고 심하게 멜라닌화된 멜라노솜의 pH 값은 각각 약 4.5와 3입니다. 티로시나제 활성의 최적 pH는 6.8입니다[2]. Raper[3]와 Mason[4]은 다양한 유기체에서 멜라닌 형성의 생합성 경로를 처음으로 규명했으며 최근 Schallreuter 등에 의해 장식되었습니다. [5] 및 Cooksey 외. (그림 1) [6].
Tyrosinase는 식물, 동물 및 미생물에서 널리 발견됩니다. 흑색종의 병인에 tyrosinase가 관여한다는 점을 감안할 때, 그 활성을 모니터링하고 약리학적으로 조절하는 것이 질병의 진단과 치료에 도움이 될 것입니다[7]. 탐침은 생리학적 환경에서 티로시나제 활성을 구체적으로 감지하기 위해 개발되었습니다. 티로시나제를 불활성화시킬 수 있는 억제제도 개발되었고, 그 중 일부는 질병 치료를 위해 임상적으로 사용되었습니다. 예를 들어 코지산과 알부틴[8]은 티로시나아제의 특정 억제제로서 미백 제품으로 임상적으로 활용되었습니다. 약물 발견이 발전함에 따라 티로시나제 활성을 감지/억제할 수 있는 효과적인 화합물의 수가 증가하면서 최근에 설계 및 합성되었습니다. 이는 비정상적인 멜라닌 생성으로 인한 질병의 진단 및 치료를 크게 촉진할 것입니다. 이 검토에서는 내인성 티로시나제 활성에 대한 저분자 기반 프로브 및 억제제 개발의 진행 상황에 대해 논의할 것입니다. 티로시나아제에 대해 더 많이 배우고 티로시나아제를 표적/조절하는 더 많은 기능성 화합물을 찾는 데 도움이 되기를 바랍니다.

2. 티로시나아제의 구조
티로시나제 활성 부위는 단백질의 히스티딘 잔기에 결합하는 두 개의 구리 이온으로 구성된 이중 코어 구리 중심 구조를 나타냅니다(그림 2). 두 개의 구리 이온 센터는 내인성 배위 브리지로 연결됩니다. 티로신 및 기타 물질은 효소의 활성 중심과 수산기 사이의 결합을 통해 효소와 복합체를 이룹니다. 멜라닌의 촉매 반응 과정에서 촉매 부위는 산화 상태(Eoxy), 환원 상태(Emet) 및 탈산소 상태(Edeoxy)의 세 가지 형태로 분류되며, 차이점은 이핵 구리 이온 활성 중심의 구조에 있습니다. (그림 2).
에폭시는 두 개의 정사각형 구리(II) 원자로 구성됩니다. 각 원자는 두 개의 강한 이퀘이터로 구성되며 리간드는 하나의 약한 축방향 NH[9]입니다. 외인성 산소 분자는 과산화물의 형태로 두 개의 구리 중심을 결합하고 연결합니다. CueCu 결합 길이는 약 0.35nm입니다. 산소 분자의 결합은 (m-h2:h2 -peroxo) 구조[10]의 형성을 유도하므로 Eoxy 활성 중심은 [Cu(II)eO2eCu(II)]로 쓸 수 있습니다. 과산화물의 전자 구조는 Eoxy의 생물학적 기능에 중요한 역할을 합니다. 강한 s* 억셉터 작용으로 인해 과산화물은 음전하가 적고 p 전자 수용체는 과산화물의 s* 오비탈에 있는 전자와 상호 작용하여 산소-산소 결합의 강도를 크게 약화시켜 핵을 생성합니다. 쉽게 부서질 수 있는 티로시나제 활성 센터의 [9]. Mettyrosinase(Emet)는 Eoxy와 유사하며 내인성 다리를 통해 결합된 두 개의 정방정계 구리(II) 원자도 포함합니다. 차이점은 구리 이온 간의 가교 리간드가 과산화물 대신 수산화물이라는 것입니다[2]. 산화 특성 측면에서 Emet과 Eoxy도 약간 다릅니다. Emet은 모노 페놀 화합물을 산화시킬 수 없습니다. 기질이 없으면 Emet은 유기체의 주요 형태로 존재합니다. Deoxytyrosinase(Edeoxy)는 deoxy hemocyanin과 유사하게 대칭적인 구조[(Cu(I)eCu(I)]를 가지고 있다. 이핵 구리 사이에는 과산화물이나 수산화물과 같은 가교 리간드가 없기 때문에 물 속의 수산화물은 필수적인 가교 리간드이다.
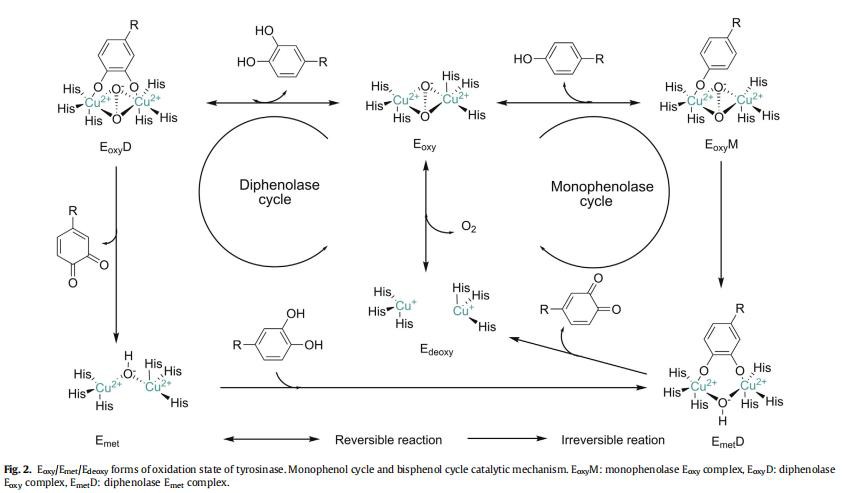
3. 티로시나아제의 작용기전
연구자들이 티로시나제 및 관련 단백질에 대한 심도 있는 연구를 수행했지만 촉매 반응의 메커니즘은 여전히 논란의 여지가 있습니다. 예를 들어, 티로시나아제의 동일한 활성 부위에서 촉매 활성이 다릅니다. 티로시나아제의 촉매 중심은 각각 Cu(A) 및 Cu(B)로 명명된 이핵 구리 중심을 포함합니다. 활성 중심의 각 구리 이온은 세 가지 다른 히스티딘 잔기와 배위됩니다. 마이코페놀레이트 활성과 디페놀라아제 활성에는 큰 차이가 있으며, 환원된 티로시나아제는 모노페놀과 반응할 때 지연기를 갖는다. 이들은 지속적으로 탐구하고 연구해야 할 중요한 주제입니다[11].
티로시나아제와 관련 기질 사이의 반응은 주로 기질의 수산기와 티로시나아제 활성 중심 사이의 효과적인 배위 결합의 형성을 통해 이루어집니다. Olivareset al. [12] 포유동물의 에옥시 및 적합한 기질이 마이코페놀레이트 활성 및 디페놀라제 활성을 유발한다고 제안했습니다. 미코페놀레이트 활동 중에 모노페놀(L-Tyrosine)은 산화되어 o-퀴논(o-dopaquinone), 멜라닌의 중요한 전구체 및 Edeoxy를 형성합니다. 디페놀라제 활동 중에 Eoxy와 Emet은 o-diphenol(L-DOPA)을 산화시켜 o-dopaquinone을 생성할 수도 있습니다[13]. 이 메커니즘은 멜라닌 생성의 속도 제한 단계가 모노페놀 주기인 티로시나아제의 동역학 특성을 가장 정확하게 반영할 수 있기 때문에 일반적으로 연구자들에 의해 받아들여지고 있습니다[14].
3.1. 마이코페놀레이트 활동의 메커니즘
멜라닌 합성 동안 효소의 주요 기능은 모노페놀 기질을 Eoxy에 의해 o-퀴논으로 산화시키는 것입니다. 이 과정은 tyrosinase를 catechol oxidase와 같은 다른 oxidoreductase와 구별하는 중요한 특징입니다. 모노페놀 주기 동안(그림 2), 탈양성자화된 페놀의 산소 원자는 산화된 티로시나제 활성 중심의 구리 이온과 배위 결합하여 마이코페놀레이트 에옥시 복합체(EoxyM)를 형성한 다음 페놀이 오르토-전자친화적으로 디페놀라제 Emet으로 치환됩니다. 복잡한 (EmetD). EmetD는 분해 과정을 거쳐 o-퀴논과 에데옥시를 직접 생성합니다. Edeoxy는 산소 분자와 직접 결합하여 Eoxy를 재형성합니다. 이것은 마이코페놀레이트 활동의 순환 과정입니다. 이 과정은 기질 반응이 완료될 때까지 끝나지 않습니다. 모노페놀 사이클의 반응 과정에서 자연 상태의 Emet이 모노페놀 기질과 만나면 매우 느린 산화 반응을 일으키고 모노페놀 반응의 정상적인 진행을 방해합니다. 따라서 Emet 자체가 산소 분자와 결합할 수 없기 때문에 이 기간을 '지체 기간'이라고 합니다[12].

3.2. 디페놀라제 활성의 메커니즘
4. 티로시나아제의 기능
Tyrosinase는 3형 구리 계열의 일부이며 멜라닌 형성 초기 과정에 존재합니다. 주로 다음 두 가지 반응 과정에 참여합니다[17]: (1) L-티로신의 L-DOPA로의 하이드록실화; (2) 도파퀴논을 형성하기 위한 L-DOPA의 산화. 도파퀴논은 결국 일련의 반응을 통해 멜라닌을 형성합니다. 3형 구리 계열의 다른 두 계열 구성원은 카테콜 산화효소와 헤모시아닌입니다. Catechol oxidase는 diphenolase 활성만 나타내며 hemocyanin은 많은 연체동물과 절지동물 산소 운반체의 림프에 있습니다. 3형 구리 계열 단백질의 활성 센터는 전체 구조와 산소 분자를 연결하는 능력 측면에서 보존되지만, 효소 센터에 대한 기질의 부착 가변성 또는 기질은 도달할 수 있습니다.

멜라닌 생성 과정에 참여하는 것 외에도 티로시나아제는 다른 중요한 생리학적 기능도 가지고 있습니다. 해면, 식물 및 일부 무척추 동물에서 tyrosinase는 주로 상처 치유 및 1차 면역 반응 과정에 관여합니다[18]. 절지동물에서 티로시나아제는 털갈이 후 동물의 각질층의 경화 과정을 촉진할 수 있습니다. 박테리아 티로시나아제는 토양에서 분비될 수 있으며 부식질을 형성하기 위해 다양한 방향족 화합물의 무작위 결합 과정에 참여할 수 있습니다. 그리고 티로시나아제가 벤젠 독성 물질에 대한 잠재적인 해독제가 될 수도 있음이 밝혀졌습니다[13,19]. 또한 페놀계 공생균에 대한 기생식물의 사멸, 천연색소의 생성, 린코마이신 등의 아미노산계 항생물질의 합성에 없어서는 안 될 역할을 한다. 이러한 효과의 공통점은 산소 분자와의 산화환원 반응을 사용하는 티로시나아제와 불가분의 관계에 있습니다[11].
5. 티로시나제 관련 질환
티로시나아제의 분포는 식물과 동물의 생리적 기능과 밀접한 관련이 있습니다. 일반적으로 깃털, 머리카락, 눈, 곤충 표피, 씨앗 및 기타 색소의 색상은 티로시나아제의 결과라고 믿어집니다[10]. Tyrosinase는 다른 유기체에서 다양하지만 중요한 기능을 가지고 있습니다. 정상적인 생리 조건 하에서 대부분의 곤충에서 tyrosinase는 zymogen의 형태로 존재하며, 곤충의 특정 부위에는 다양한 종류의 tyrosinase가 존재하여 특정 생리 기능을 완성한다[20]. 멜라닌 생성에 참여하는 것 외에도 곤충 티로시나아제는 각화증에 관여하는 유일한 효소입니다. 곤충 경화 케라틴은 미생물과 이물질의 침입을 차단하고 연약한 무척추 동물의 몸을 보호할 수 있습니다. 절지동물에서 티로시나아제는 두 가지 다른 중요한 생리학적 과정, 즉 방어 반응과 상처 치유에도 참여합니다. 포유류에서 tyrosinase에 의해 생성된 멜라닌은 표피와 모발의 각질세포로 분비되어 체표면을 변색시켜 피부와 눈을 보호하고 자외선에 저항하며 내부조직의 과열을 방지한다[10]. 포유류에서 발견되는 Tyrosinase는 일반적으로 피부, 모낭 및 눈에 존재하여 색소를 생성하는 고도로 특이적인 세포인 멜라닌 세포에서 발견됩니다[4,21]. 티로시나제 기능이 저하되거나 소실되면 멜라닌 대사에 영향을 미치고 간질 및 백색증과 같은 질병을 유발합니다. 동물과 인간의 상염색체 열성 질환도 티로시나아제의 손실이나 활성 감소와 관련이 있습니다[22].
6. 티로시나제 프로브
탐침은 표적을 구체적으로 인식하고 표적의 존재와 활동을 반영하는 감지 가능한 신호를 방출하는 물질입니다. 티로시나제 분석을 위한 전통적인 비색법은 감도가 낮기 때문에 제한적이었습니다[23]. 처음에 Willner 그룹[24e27]은 전기화학 및 금 나노입자를 기반으로 하는 몇 가지 다른 검출 방법을 보고했으며, 이는 검출의 다양성을 증가시킬 뿐만 아니라 감도 측면에서 비색계를 크게 업데이트합니다. 그림 3과 같이 고감도 티로시나아제 탐침을 설계하기 위해 형광 전략도 도입되었습니다. 초기에 개발된 양자점 및 공액 고분자 형광 탐침은 티로시나아제의 활성을 모니터링하는 데 적용될 수 있습니다[28]. 그럼에도 불구하고 저분자 형광 프로브는 감도, 특이성 및 호환성과 같은 특별한 이점 때문에 특히 매력적입니다. 2008년에 Zhu의 팀은 티로시나제에 대한 형광 프로브로서 티로신 탄두(WH)를 포함하는 FL 형광단으로서 새로운 수용성 올리고(페닐렌비닐렌)(Pr1)를 합성했습니다. 지금까지 Pr1은 아가로스 겔에서도 완충 수용액에서도 티로시나제의 활성을 검출하는데 적합하다는 것이 입증되었다[29]. 첫째, 2010년 Ma et al. [30]. 반응 전후의 현저한 색상 변화는 육안으로 감지할 수 있습니다. 그러나 이러한 프로브는 또한 티로시나제 촉매 산화에 의해 생성된 퀴논 모이어티에 의해 발생하는 턴오프 모드를 보여줍니다. 그러나 기능적 사용을 위해 가장 좋은 방법은 생체 시스템에서 티로시나아제의 생체 이미징에 대한 감도와 더 적합성 때문에 켜기 모드에서 생물 검정을 구현하는 것입니다. 2010년 Kim et al. [31]은 살아있는 흑색종 세포에서 내인성 티로시나제 활성을 검출하기 위해 BODIPY 기반 턴온 형광 프로브를 제안했습니다(Pr3, 그림 4). 아민 보호기[32]를 제거하기 위해 적용한 티로시나아제의 이전 연구를 기반으로 Yan et al. [33] 2012년에 페놀 그룹과 나프틸아민 그룹이 우레아 연결을 통해 연결된 티로시나아제 프로브 Pr4 및 Pr5를 준비했습니다. 중요한 것은 Pr4가 티로시나아제의 활성을 감지하도록 설계된 최초의 2광자 턴온 형광 프로브라는 것입니다. 수성 완충액 및 살아있는 세포에서. 2013년에 Wang et al. [34]는 페놀 모이어티(WH)를 포함하는 NBD-NH2- 기반 형광 프로브(Pr6 및 Pr7)를 사용하여 티로시나아제의 활성을 감지하고 "켜짐"으로 잠재적인 티로시나아제 억제제를 스크리닝할 수 있음을 보여주었습니다. 전략. 그러나 이 연구에서 세포 이미징과 관련된 생물학적 실험은 없습니다. 2016년에 Li와 동료들은 FL 형광단으로서 7-amino-4-(trifluoromethyl)-coumarin을 기반으로 하는 새로운 프로브 그룹을 설계하고 FL 사이의 다양한 거리를 갖는 Pr8-11을 합성했습니다. 형광단 및 페놀. Pr9는 살아 있는 흑색종 세포를 이미징하기 위한 매우 민감하고 선택적인 "켜짐" 형광 프로브인 것으로 밝혀졌습니다[35]. 2018년 Wu의 팀은 설치류 마우스 모델에서 초기 흑색종을 진단하기 위해 FL 형광 프로브(Pr12)를 처음으로 사용했습니다(그림 4 및 5A). 프로브는 티로시나제 매개 산화에 의해 활성화된 다음 요소 결합을 가수분해하여 형광 신호를 생성할 수 있습니다. 동시에 살아있는 세포와 제브라피쉬의 내인성 티로시나아제 수준을 민감하고 선택적으로 모니터링할 수도 있습니다(그림 5 B/C)[36].

2016년 Ma의 그룹[37]은 Mela-TYR(Pr13, 그림 4)이라는 새로운 형광 프로브를 개발하여 티로시나아제의 활성을 감지하기 위해 멜라노솜을 표적으로 삼았습니다. Pr13은 프탈이미드와 모르폴린 및 4-아미노페놀 유래 요소를 결합하여 설계되었습니다. 프로브는 산화-절단 반응을 통해 티로시나제에 대해 매우 민감하고 선택적인 턴온 반응을 보입니다. 위에서 설명한 형광 프로브는 인식 부분(WH)으로 4-하이드록시페닐 그룹을 주로 포함하고 여러 활성 산소 종(ROS) 및 티로시나아제에 대해 병렬 형광 반응을 나타내어 ROS에 의해 방해를 받았습니다. Ma의 그룹은 tyrosinase와 ROS에 대한 다양한 반응 메커니즘을 보여주는 새로운 tyrosinase 인식 부분인 3-hydroxy benzyloxy(WH)를 발견했습니다[38]. NIR 형광단(HXPI)에 3- hydroxy benzyloxy를 삽입하여 NIR 형광 탐침(Pr14, Fig. 4)을 개발하였으며, ROS 대신 tyrosinase에 대해 매우 특이적인 off-on 반응을 보여 간섭을 극복하였다. 3- 하이드록시 그룹의 존재는 ROS가 아닌 4- 위치 공석에서 티로시나아제에 의한 하이드록실화를 촉진하고 중간체는 자발적인 1,6-재배열 제거를 거쳐 자유 형광단을 방출합니다. 개발된 프로브의 높은 특이성은 살아있는 세포와 제브라피쉬의 내인성 티로시나제 활성을 이미징 및 검출하여 입증되었으며, 프로브의 높은 특이성은 효소 결합 면역흡착 분석을 통해 추가로 확인되었습니다(그림 4 및 6). 이후 Ma의 그룹은 3-hydroxyphenyl 그룹[39]과 통합된 resorufin을 기반으로 하는 또 다른 턴온 형광 프로브(Pr15, 그림 4)를 개발했습니다. 다양한 살아있는 세포에서 내인성 티로시나제의 활성을 감지하고 이미지화하는 데 사용되었습니다. 위의 설계에서 영감을 받아 Zhang과 동료[40]는 resorufin을 형광단으로 사용하고 m-tolyl boronic acid pinacol ester(WH)를 새로운 티로시나제 인식으로 사용하는 fluorogenic tyrosinase probe(Pr16, 그림 4)를 제안했습니다. 절반. 프로브는 ROS를 포함한 다른 생물학적 물질보다 티로시나제에 대해 높은 선택성을 보였다. 그러나 H2O2에 의해 심하게 방해를 받았습니다. 2019년 Hu et al. [41]는 플루오레세인(Pr17, 그림 4)에 기반한 높은 화학적 선택성을 가진 새로운 형광 프로브를 보고했으며, 이는 시험관 내 및 생체 내에서 티로시나아제를 추적할 수 있고 티로시나아제의 높은 화학선택적 검출을 실현할 수 있습니다. 또한 프로브는 수용액에서 반응하여 티로시나아제 존재 하에서 24배 이상의 형광증강을 나타내었다. 또한 Pr17은 뛰어난 세포막 및 조직 투과성 특성을 보여 별개의 도움을 받은 살아있는 세포 및 제브라피시 모델에서 내인성 티로시나제 활성을 따르는 데 성공했습니다. Ding의 그룹은 생리학적 온도와 pH 내에서 매우 안정하고 유비쿼터스 개체에 의해 방해받지 않고 생물학적 시스템에서 티로시나아제를 정확하게 검출할 수 있는 티로시나아제를 특이적으로 인식할 수 있는 새로운 수용성 NIR 형광 프로브(Pr18, 그림 4)를 구성했습니다. 살아있는 세포, 제브라피쉬, 이종 마우스 모델에서 티로시나아제를 영상화하는 데 사용할 수 있습니다[42].

Sidhuet al. 나프탈이미드를 기반으로 비율 측정 형광 프로브(Pr19, 그림 4)를 고안하고 합성했습니다. Pr19는 tyrosinase에 대한 높은 선택성과 민감도를 가지며 검출 한계(LOD)가 매우 낮습니다[43]. 여기 또는 방출 스펙트럼 이동은 탐침이 반응물과 결합된 후에 발생합니다. 두 개의 서로 다른 파장에서 측정된 형광 강도의 비율을 사용하여 기록할 수 있으며 이를 비율 측정이라고 합니다. 이 원리에 기반한 비율 측정 형광 탐침은 민감도와 선택성을 나타내며 살아있는 시스템에서 효소 기능 연구에 사용될 수 있습니다[44]. Guo의 팀은 내인성 티로시나제 활동의 실시간 감지를 위해 새로운 비율 측정 및 켜기 NIR 형광 프로브(Pr20, 그림 4)를 제안했습니다. 희귀한 세포독성, 우수한 광물리학적 특성 및 세포막 투과성과 결합된 Pr20의 이러한 특수한 특성은 내인성 티로시나아제 활성의 정량적 검출에 이상적입니다[45]. 전형적인 NIR 형광 염료인 시아닌 유도체는 수용액에서 제어 가능하게 응집될 수 있으므로 상당히 다른 많은 스펙트럼 특성을 나타냅니다. 시아닌 골격의 중심에 있는 염소 원자는 다른 관능기로 쉽게 대체됩니다. 이 기능을 기반으로 Zhang et al. [46]는 티로시나제 활성의 비례 형광 검출을 위한 새로운 시아닌 기반 형광 프로브(Pr21, 그림 4)를 개발했습니다(그림 7). 비율 결정은 우수한 신호 대 잡음비를 얻었고 티로시나아제 활성의 LOD 값은 0.02 U/mL였습니다. 또한, Pr21은 B16 세포에서 내인성 티로시나제 활성을 영상화하고 티로시나제가 없는 다른 암/정상 세포와 질적으로 구별하는 데 성공적으로 사용되었습니다(그림 7).
7. 티로시나제 억제제
억제제는 일반적으로 효소와 상호작용하는 억제제가 효소를 영구적으로 불활성화시키는지 여부에 따라 가역적 억제제와 비가역적 억제제로 나뉜다. 티로시나아제의 억제 특성은 가역적 억제입니다. 가역적 억제를 특징으로 하는 억제의 경우, 억제제와 효소의 조합은 가역적 동적 평형 과정입니다[47e49]. 억제제의 농도를 높이면 효소 활성이 감소하지만 억제제는 효소를 영구적으로 비활성화하는 것이 아니라 효소 활성을 억제할 뿐입니다. 억제제 농도가 감소하면 티로시나제 활성이 증가합니다. 한편, 비가역적 억제는 티로시나아제의 영구적인 불활성화일 것이다. 티로시나제 억제제가 효소와 상호 작용하는 부위와 방법에 따라 경쟁형, 비경쟁형, 혼합형 및 느린 결합의 네 가지 형태로 나눌 수 있습니다.


플라보노이드는 세 개의 탄소 사슬로 연결된 두 개의 벤젠 고리로 구성된 화합물 세트입니다. 하이드록실, 메톡시 및 글리코사이드 측쇄 그룹이 벤젠 고리에 있기 때문에 배열은 플라보놀, 칼콘, 디하이드로플라본 및 오렌지색으로 세분될 수 있습니다(그림 8)[56]. 플라보노이드는 식물의 잎, 씨앗, 껍질 및 팔로워에 광범위하게 분포되어 있으며 연구자들은 4000개 이상의 플라보노이드를 확인했습니다. 일부 식물의 경우 플라보노이드와 그 파생물이 자외선, 병원체 및 초식 동물로부터 보호합니다[57]. 감초 뿌리 추출물의 구조를 분석한 결과 네오 글리시리진, 글리시리진, 이소리퀴리티제닌, 글리시리진의 티로시나제 억제 능력이 이들의 친유성과 관련이 있음을 보여줍니다. 그 중 모노페놀의 억제가 디페놀보다 더 효과적이어서 산화 반응의 첫 번째 단계에서 속도 제한 반응임을 나타낸다[58].
{{0}}하이드록시-4-케톤 구조를 포함하는 일부 플라본은 티로시나아제의 활성 부위에서 구리를 킬레이트화하여 효소 활성을 경쟁적으로 억제하여 티로시나아제를 돌이킬 수 없는 불활성화시킬 수 있습니다. 티로시나아제를 킬레이트화한 후 분자는 이론적으로 평면 구조를 잃고 왜곡됩니다. 경쟁적 억제제는 일반적으로 기질과 구조가 평행하므로 분자가 티로시나제 활성 부위에 쉽게 들어가고 L-DOPA의 진입을 방지합니다[59,60]. 정 외. Zanthoxylum piperitum의 잎에서 두 개의 플라보놀을 추출했습니다. 플라보놀은 경쟁적 억제인 버섯의 티로시나제 활성을 억제할 수 있지만 Streptomyces bikiniensis의 멜라닌 생성을 억제할 수는 없습니다. 이후 필리핀 포르모사에서 분리한 플라보노이드 화합물도 티로시나제를 억제할 수 있으며 억제 효과가 코지산보다 우수하다는 사실이 밝혀졌다[62]. Liang et al. 잇꽃 황색 색소는 또한 1.01 mg/mL의 반 최대 억제 농도(IC50) 값으로 버섯 티로시나제 활성을 억제할 수 있음을 발견했습니다. 이 억제 관계는 용량 의존적인 것으로 보입니다 [63]. Shuiliao에서 추출한 (2R,3R)-(þ)-purpurin은 tyrosinase 활성을 70% 억제하며 농도는 0.50mM이다. 억제 능력은 코지산 및 알부틴보다 우수합니다[64].
7,8,40 -trihydroxyflavone은 IC50 값이 10.31 ± 0.41mM이고 Ki가 9.50±0.40mM. 티로시나아제에 대한 이 화합물의 작용 메커니즘은 정적 메커니즘이며 298K에서 결합 상수가 (7.05 ± 1.20) × 104 M-1인 단일 결합 부위를 보여줍니다. 열역학적 매개변수는 결합 과정이 서로 관련되어 있음을 보여줍니다. 수소 결합과 반 데르 발스 힘[51].

Scolopendra 보조금 mutilans에서 분리된 3,8-hydroxyquinoline(In1, 그림 9[65])은 Melan-a 세포에서 멜라닌 생성 및 산화를 억제할 수 있습니다. In1은 농도-발달된 항산화 효과를 나타내며 비경쟁적 억제를 통해 버섯 티로시나제 활성을 현저하게 억제한다. 동시에, In1은 표 1[65]에 나타난 바와 같이 연구에서 세포독성이 없는 것으로 밝혀졌습니다. Nymphaea nuchal 꽃 추출물(NNFE)의 에틸 아세테이트 분획(100 mg/mL)은 멜라닌 생성을 효과적으로 줄이고 버섯 티로시나제 활성을 억제할 수 있습니다. 기본 메커니즘은 멜라닌 합성에서 전사 인자 및 보편적 신호 경로를 방해하는 것과 관련이 있습니다[66]. 고추에서 추출한 캡사이신(In2, 그림 9 [67])과 디하이드로캡사이신(In3, 그림 9)은 티로시나제 활성을 억제할 수 있습니다. 결과는 In2의 IC50 값이 In3보다 1.73배 작다는 것을 보여줍니다. 억제 상수(Ki)는 또한 티로시나아제에 대한 In3(0.39mM, 표 1)의 억제 활성이 In2(0.30mM, 표 1)보다 낮다는 것을 뒷받침합니다[67]. 동백나무 꽃가루에서 추출한 카페인(In4, 그림 9[68])은 표 1과 같이 비경쟁 모델에서 버섯 티로시나제에 대해 강한 억제 활성을 나타내는 것으로 나타났다. In4는 L-티로신과 링의 결합 부위를 변화시킨다 tyrosinase에 결합하여 활성 센터에 인접한 형태. 실험 결과는 In4가 세포 내 티로시나제 활성에 명백한 억제 효과를 가지며 B16F10 흑색종 세포의 멜라닌 생성이 농도와 관련이 있음을 보여줍니다[68]. 포도에서 추출한 caftaric acid(In5, 그림 9)는 tyrosinase를 경쟁적으로 억제할 수 있으며 IC50 값(표 1)은 관계 화합물인 caffeic acid와 chlorogenic acid보다 낮습니다[47]. 플로레틴(In6, 그림 9)은 정적 과정을 통해 티로시나아제에 결합할 수 있으며, 이는 티로시나아제의 구조를 변화시켜 활성을 억제합니다. 동시에 In6는 강력한 항산화 능력과 o-dopaquinone을 LDOPA로 환원시키는 능력을 가지고 있습니다.

연구자들은 두 가지 스피로 아크리딘(AMTAC-01, In7, 그림 9) 및 (AMTAC-02, In8, 그림 9)를 티로시나아제 억제제로 평가했습니다. 결과는 아크리딘 유도체가 버섯 티로시나아제와 강력하게 상호 작용한다는 것을 보여줍니다. In8은 표 1에 나타난 바와 같이 In7보다 효소 활성 억제에 더 효과적이며, 이는 In8의 메톡시기가 억제 활성과 높은 상관관계가 있음을 나타낸다[49]. 여러 21개의 할로겐화 티오세미카르바존(TSC)을 합성하고 조사했습니다. TSC 6, 12 및 21(In9/10/11, 그림 9[69])은 각각 다른 IC50으로 강력한 억제 특성을 나타내는 것으로 나타났습니다(표 1). 이들은 티로시나아제를 억제하는 상호 가역적이고 경쟁적인 메커니즘을 보여줍니다. 연구된 화합물 중에서 thiosemicarbazones의 para-치환된 acetophenone 유도체는 효소에 가장 높은 친화력을 가지고 있습니다[69]. 페니실린 V(In12, 그림 9)는 세균 분해 b-lactam 항생제입니다. 연구에 따르면 In12는 마이코페놀레이트 및 디페놀라제 활성을 억제할 수 있습니다. 형광 소광 및 분자 도킹 연구는 In12가 효소의 촉매 포켓 근처에서 정적 상호작용을 형성할 수 있음을 보여주었고, 따라서 활성 부위로의 기질 수송을 방해하고 촉매 작용을 위한 구리의 가소성을 감소시킵니다[70]. 최근 Raza et al. N-(치환된-페닐)-4-{(4-[(E)-3- 페닐-2-프로페닐]-1-피페라지닐) 부탄아미드( 5a-e) 티로시나제에 대한. 모든 화합물은 생물학적으로 활성이 있는 것으로 나타났으며, 5b(In13, 그림 9)가 가장 높은 억제 가능성을 나타냈습니다[71]. Mahajanet al. 퀴나졸리논 벤 아미드 4a-h(In14e21, 그림 9)를 설계하고 합성했습니다. tyrosinase의 활성에 대한 화합물의 억제 효과에 대한 연구를 통해 표 1과 같이 모든 화합물이 표준 코지산보다 낮은 IC50 값을 나타내는 것으로 나타났습니다[72]. Shenet al. 새로운 티로시나아제 억제제인 펩타이드 ECGYF(EF-5, In22)를 그림 9와 같이 발견했습니다. In22와 티로시나아제 사이의 결합은 주로 수소 결합과 소수성 상호작용에 의존하며 티로시나아제 억제 효과는 알부틴과 글루타티온 [73]. He et al. 도 9에 나타낸 바와 같이 3개의 타마리시놀 1/2/3(In23/24/25) 및 2개의 페놀릭 4 및 5(In26 및 27)를 분리하였다. 실험은 모든 분리주가 버섯 티로시나제에 대한 억제 효과를 갖는 것으로 나타났으며, In23은 가장 효과적인 것(표 1) [74].

자세한 정보: david.deng@wecistanche.com WhatApp:86 13632399501






