아데노 관련 바이러스 벡터 제제의 바이러스 외 DNA는 인간 형질세포양 수지상 세포에서 TLR9 의존 선천 면역 반응을 유도합니다
Oct 11, 2023
인간 유래 HEK 세포 또는 Spodoptera frugiperda(Sf9) 곤충 세포에서 생성된 Adeno 관련 바이러스(AAV) 벡터 현탁액은 AAV 캡시드 단백질에 표시된 종별 번역 후 변형뿐만 아니라 잔류 숙주 세포 구성 요소 측면에서도 다릅니다. . 여기서 우리는 벡터의 면역원성 특성에 대한 이러한 차이의 영향을 분석했습니다. 우리는 다양한 제조업체에서 파생된 다양한 HEK 세포 생산 및 Sf9 세포 생산 AAVCMV-eGFP 벡터를 사용하여 인간 형질세포양 수지상 세포를 자극했습니다. 우리는 AAV8-CMV-eGFP 및 AAV2-CMV-eGFP 벡터가 로트별 염증성 사이토카인 반응을 유도했지만 생산 플랫폼별 또는 제조업체별 염증성 사이토카인 반응을 유도하지 않음을 발견했습니다. 이는 유료 유사 수용체 9 신호 전달을 차단하거나 DNase를 사용하여 벡터 로트에서 DNA를 효소적으로 감소시킴으로써 감소되거나 폐지될 수 있습니다. DNase 처리된 AAV 로트 및 DNA 분석에 의한 성공적인 HEK 세포 형질도입은 DNase가 벡터의 완전성에 영향을 미치지 않지만 바이러스 외 DNA를 분해한다는 것을 입증했습니다. 우리는 HEK 및 Sf{21}} 세포 유래 AAV 제제 모두 로트 특이적 염증성 면역 반응을 유발할 수 있는 면역원성 바이러스 외 DNA 성분을 함유할 수 있다는 결론을 내렸습니다. 이는 바이러스 외부 DNA 불순물을 제거하기 위한 개선된 전략이 AAV 벡터 제제의 면역원성 특성을 감소시키는 데 도움이 될 수 있음을 시사합니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
지난 10년 동안 기초 연구와 임상 적용을 위한 새로운 재조합 아데노 관련 바이러스(AAV) 기반 전략의 개발에 엄청난 관심이 집중되었습니다1-3. 주된 이유는 AAV 벡터가 표적 조직에 치료 유전자를 효율적이고 안전하게 전달할 수 있는 능력을 고려할 때 유전자 치료 분야에서 매우 다재다능한 도구라는 사실에 있습니다4. 그러나 점점 더 많은 수의 연구자들이 전임상 및 임상 연구에서 AAV 전달 후 국소 및 전신 면역 반응을 암시하는 결과를 독립적으로 보고하고 있습니다5-8.
AAV 벡터는 톨 유사 수용체(TLR)2 및 TLR9와 같은 선천적 면역 패턴 인식 수용체를 활성화하여 염증성 사이토카인 및 I형 인터페론(IFN)9,10을 방출하는 것으로 나타났습니다. 이러한 반응을 자극할 수 있는 AAV의 면역원성 구성 요소에는 캡시드 단백질과 벡터 게놈이 포함됩니다9,10. AAV 적용 후 면역 반응은 벡터 현탁액5,11의 불순물에 의해 유발될 수도 있습니다. 이러한 불순물은 원하는 제품 이외의 정제된 AAV 벡터 현탁액에 존재하는 모든 성분으로 정의되었으며12 벡터 생산 과정에서 발생합니다. 임상 재조합 AAV 벡터를 생산하는 두 가지 주요 방법은 플라스미드 DNA를 HEK 세포에 형질감염시키는 것과 바콜루바이러스로 Spodoptera frugiperda(Sf9) 곤충 세포를 감염시키는 것입니다13. 따라서 AAV 벡터 현탁액에 포함된 잠재적인 면역원성 불순물에는 내독소, 세포 배양 배지 성분, AAV 정제에 사용되는 시약, 숙주 세포에서 유래된 단백질 및 DNA, 잔류 바큘로바이러스 DNA 또는 플라스미드 DNA가 포함될 수 있습니다5. AAV 벡터 현탁액의 면역원성에 영향을 미칠 수 있는 추가 요인은 다양한 벡터 생산 플랫폼5에 의해 캡시드에 각인된 번역 후 변형(PTM)입니다. 중요한 것은 HEK 세포 유래 및 Sf9 세포 유래 AAV 벡터는 PTM, 잔류 숙주 세포 단백질 불순물11 및 잠재적으로 DNA 불순물(HEK 세포 DNA 대 Sf9 세포 DNA 및 잔류 플라스미드 DNA) 측면에서 크게 다릅니다. 대 바큘로바이러스 DNA)14. 형질세포양 수지상 세포(pCD)는 바이러스 감염 시 다량의 I형 IFN 및 전염증성 사이토카인을 분비하고9,15 AAV 벡터 감지에 중요한 역할을 하는 특수한 선천 면역 세포 유형입니다9. 따라서 HEK 세포에서 생성된 AAV 벡터와 Sf9-세포에서 생성된 AAV 벡터 간의 차이로 인해 면역원성 특성에 차이가 발생하는지 분석하기 위해 두 생산 시스템에서 얻은 동일한 AAV 벡터의 서로 다른 로트를 사용하여 인간 pDC를 자극했습니다. 그리고 다른 제조업체. 우리는 조사한 벡터 로트 중 절반이 벡터 생산 시스템이나 제조업체와 관련이 없는 로트 특이적 전염증성 면역 반응을 유도한다는 사실을 발견했습니다. 이러한 반응은 TLR9 신호전달에 의해 매개되었으며 DNase를 사용한 벡터 로트 처리에 민감했습니다. 미처리 및 DNase 처리 AAV 벡터 로트와 AAV 제제의 DNA 분석에 의한 성공적인 HEK 세포 형질도입은 DNase가 AAV 입자 무결성에 영향을 미치지 않고 오히려 표적화된 비캡슐화된 추가 바이러스 DNA에 영향을 미친다는 것을 시사했습니다. 종합적으로, 이는 AAV 벡터 제제가 인간 pDC에서 AAV 벡터 제제의 면역원성 특성에 영향을 미칠 수 있는 비캡슐화된 추가 바이러스 DNA를 함유할 수 있음을 시사합니다.

시스탄체 튜불로사의 장점-면역체계 강화
결과
AAV는 인간 pDC에서 로트 특이적 선천성 면역 반응을 유도합니다.
연구에 따르면 HEK 세포 유래 및 Sf9 세포 유래 AAV 벡터는 바이러스 현탁액11에 포함된 PTM 및 불순물 측면에서 다릅니다. 우리는 이러한 요인이 HEK 세포 유래 벡터 로트와 Sf9 세포 유래 벡터 로트 사이의 면역원성 특성에 차이를 초래할 수 있다는 가설을 세웠습니다. 이 가설을 테스트하기 위해 우리는 거대세포바이러스 프로모터(CMV)의 동일한 DNA 서열과 향상된 녹색 형광 단백질(eGFP)(AAV8-)에 대한 동일한 도입유전자를 포함하는 총 8개의 AAV 혈청형 8(AAV8) 벡터 로트를 분석했습니다. CMV-eGFP; HEK- 5개 및 Sf9 세포 유래 로트 3개) 및 AAV{14}}CMV-eGFP 로트 4개(HEK- 2개 및 Sf9 세포 유래 로트 2개)(제조업체 A; 아이오와대학교(미국 아이오와주)의 바이러스 벡터 핵심 시설, 제조사 B; Virovek(미국 캘리포니아주) 및 제조사 C; Vigene Biosciences (MD, 미국)]. 로트 간의 유사성을 최대화하기 위해 제조업체 A와 제조업체 B(표 1)의 7개 AAV8 로트를 동일한 원래 플라스미드를 사용하여 생산했습니다. 추가적으로, AAV 벡터 로트의 벡터 게놈(vg)의 액적 디지털 PCR(ddPCR) 등록은 두 개의 서로 다른 표적을 사용하여 병렬 측정으로 수행되었습니다. 하나는 CMV 서열 내에 있고 다른 하나는 eGFP 서열 내에 있습니다. 벡터. CMV 표적의 정량화를 통해 얻은 결과는 다음 실험에서 AAV 벡터 로트의 적정에 사용되었습니다(표 1). pDC는 AAV 벡터를 포함하여 바이러스 감염 시 I형 IFN을 대량으로 생성하는 특수 바이러스 센서입니다. HEK 세포 생성 AAV 벡터와 Sf9- 세포 생성 AAV 벡터가 면역 능력 세포에서 선천성 면역 반응을 유도하는 능력이 다른지 여부를 조사하기 위해 위에 나열된 AAV 벡터 로트로 인간 pDC를 자극했습니다. 이를 위해, 자기 활성화 세포 분류(MACS)를 사용한 음성 선택에 의해 개별 건강한 인간 공여자의 말초 혈액 단핵 세포(PBMC)로부터 pDC를 정제하였다. 유세포 분석을 통해 분리된 pDC의 순도가 90% 이상임을 확인했습니다(그림 S1). 10개, 개별 공여자의 pDC를 시딩하고 18시간 동안 1:1 x 106vg/세포의 MOI에서 AAV8 및 AAV2 벡터 로트로 자극했습니다. 50ul/웰의 총 12,500개 세포에 적용된 1:106vg/세포의 MOI는 2.5×1011vg/ml의 역가로 해석됩니다. 우리는 이 역가가 인간(예: 1× 1012 vg/ml16 또는 4 × 1011–1.3 × 1012 vg/ml17)과 비인간 영장류(예: 5 × 1012 vg/ml17)의 망막 유전자 치료 연구에 적용되는 범위 내에 있기 때문에 사용했습니다. 1011–5 × 1012vg/ml6 ). 차량을 이용한 자극이 통제 역할을 했습니다. AAV8 및 AAV2 벡터 로트와의 인큐베이션은 pDC에서 검출 가능한 이식유전자 발현을 초래하지 않았습니다. 그러나 8개 AAV8 로트 중 4개(로트 A-HEK-1, A-HEK-2, A-HEK-3, A-Sf9-1)와 2개 4개의 AAV2 로트(로트 B-Sf9-1, B-Sf9-2)는 자극된 pDC에서 반응성 세포 증식을 유도했습니다(그림 1a). 이는 전염증성 사이토카인(IP-10, MIP-1 및 TNF-)과 I형 IFN(IFN-)의 방출을 동반했습니다. 반대로, 세포 증식이나 사이토카인 방출은 나머지 AAV8(로트 A-Sf9-1, B-HEK-1, B-Sf9-1, C-HEK{{92})에 의해 유도되지 않았습니다. }) 및 AAV2 로트(로트 C-HEK-1, C-HEK-2). 이러한 결과는 한 개인 기증자의 세포를 사용하여 각각 수행된 3~4개의 독립적인 실험에서 확인되었습니다(그림 1a-c 및 표 S1). 이러한 독립적인 실험에서 사이토카인 농도의 로트별 차이는 선형 혼합 효과 모델과 사후 Dunnett 검정(Q{101}}.6)을 사용하여 다양한 AAV 벡터 로트의 최소 제곱 평균을 차량 제어(표 S2 및 S3). 이는 "면역원성" AAV 벡터 로트(AAV8 로트 A-HEK-1, A-HEK-2, A-HEK-3, A-Sf{) 사이의 사이토카인 반응에 통계적으로 유의미한 차이가 있음을 입증했습니다. {114}} 또는 AAV2 로트 B-Sf9-1, B-Sf9-2 각각) 및 대조군이지만 "비면역원성" AAV 벡터 로트(AAV8 로트 A-Sf{{ 123}}, B-HEK-1, B-Sf9-1, C-HEK-1 또는 AAV2 로트 C-HEK-1, C-HEK-2 각각) 및 제어(표 S3). 멀티플렉스 분석에 포함된 나머지 측정된 사이토카인의 농도는 분석 범위보다 낮았습니다(즉, IL-1, IL-2, IL-4, IL-5 , IL-6, IL-10, IL-12, IL-13, IL-17, GM-CSF, IFN-) 또는 "면역원성"도 아니고 "비면역원성" 벡터 로트는 방출(즉, IL-7, IL-8, G-CSF, MCP-1)의 상당한 증가를 유도했습니다(그림 S2). AAV 매개 사이토카인 반응의 특이성 정도. 초기 시점에서 사이토카인 반응을 조사하기 위해 pDC를 "면역원성" AAV8 벡터 로트 A-HEK-1로 자극했습니다. 우리는 pDC 자극 후 2시간에 이미 상층액에서 TNF- 농도가 크게 증가하는 것을 관찰했습니다. 이 반응 패턴은 각각 한 개인 기증자의 세포를 사용하여 수행된 세 가지 실험에서 확인할 수 있습니다(그림 S3). 더 높은 용량의 "비면역원성" AAV8 벡터 로트가 면역 반응을 유발할 수 있는지 여부를 조사하기 위해 우리는 기술적으로 최대 적용 가능한 MOI(1:4.61×106 vg)로 pDC를 자극했습니다. 흥미롭게도, 이 증가된 역가에 의한 자극에서는 반응성 세포 증식이나 사이토카인 반응이 검출되지 않았습니다(그림 S4). 우리의 가설과는 달리, 이러한 결과는 pDC의 AAV에 대한 선천적 면역 반응이 로트 특이적이며 특정 생산 시스템이나 제조업체/정제 방법과 관련이 없음을 보여줍니다.

표 1. 본 연구에 사용된 다양한 AAV8 및 AAV2 바이러스 벡터 로트.

그림 1. 인간 pDC에서 AAV 벡터 로트 특이적 면역 반응의 유도. 인간 pDC는 18시간 동안 다양한 로트의 AAV8-CMV-eGFP 및 AAV{4}}CMV-eGFP(MOI: 1:1× 106 vg)로 자극되었습니다. (a) 다음으로 자극된 pDC의 대표적인 명시야 이미지 차량 제어(상단 이미지) 또는 면역원성 AAV 벡터 로트(하단 이미지). 스케일 바는 100μm입니다. (b) AAV8-자극 pDC에 의한 IP-10, MIP-1, TNF- 및 IFN- 2의 사이토카인 방출. (C) AAV2-자극된 pDC에 의한 사이토카인 방출. 3~4개의 독립적인 실험 중 하나의 대표적인 플롯입니다. IFN- 2 측정(b,c) 및 TNF- 측정(c)에서 일부 값이 분석 범위 아래로 떨어지므로 측정된 모든 IFN{20}} 및 TNF- 값에 상수 1을 추가하여 제시했습니다. 반로그 플롯에서. 중앙값과 사분위수 범위가 표시됩니다. 개별 벡터 로트의 라벨에는 세 제조업체가 문자 A, B, C로 표시됩니다. HEK 세포 유래 및 Sf9- 세포 유래 벡터는 "HEK 및 "Sf9"로 표시되며 동일한 제조업체 및 동일한 생산 시스템의 해당 로트는 "1, 2, 3"으로 번호가 지정됩니다. 벡터 로트; 삼각형: Sf9-파생 벡터 로트; 검정색: 제조업체 A의 벡터 로트; 주황색: 제조업체 B의 벡터 로트; 녹색: 제조업체 C의 벡터 로트.
pDC의 AAV 자극에 대한 면역 반응은 캡시드/VG 비율의 차이에 영향을 받지 않습니다.
전임상 연구에 따르면 AAV 벡터 현탁액의 전체 벡터 입자 수와 빈 벡터 입자 수의 차이가 면역 반응에 영향을 미칠 수 있는 것으로 나타났습니다18. 분석된 벡터 로트 간의 면역원성 특성의 차이가 전체 벡터 입자와 빈 벡터 입자 비율의 차이로 인한 것인지 평가하기 위해 AAV 적정 ELISA를 통해 모든 AAV 로트에서 벡터 캡시드의 역가를 결정하고 캡시드/VG를 계산했습니다. 비율. 흥미롭게도 모든 AAV 로트 간에 capsid/vg 비율의 큰 차이가 발견되었습니다(그림 2). AAV8-CMV-eGFP 로트 A-HEK-1, A-HEK-3, A-Sf{{11}에서 vg(2:1)보다 약 2배 더 많은 캡시드가 발견되었습니다. } 및 AAV2-CMV-eGFP B-Sf9-1; AAV8 로트 A-Sf9-1에서는 4배 더 많습니다(4:1). 나머지 로트에서는 1:1 비율이 관찰되었습니다. 그러나 "면역원성" 및 "비면역원성" AAV 벡터 로트의 캡시드/vg 비율 간에는 AAV8(P=0.27)이나 AAV2(P=0.37)에서 발견되지 않았습니다. 벡터 로트(그림 2). 이는 분석된 AAV 벡터 로트의 면역원성 특성의 차이가 전체 벡터 입자와 빈 벡터 입자의 비율 차이와도 관련이 없음을 시사합니다.

cistanche 보충 혜택 - 면역 체계를 강화하는 방법
TLR9에 의한 "면역원성" AAV8 벡터 로트의 인식.
쥐과 인간 pDC에 의한 AAV의 선천적 면역 인식은 TLR99를 감지하는 DNA에 의해 매개되는 것으로 나타났습니다. 따라서 우리는 TLR9가 "면역원성" AAV8 벡터 로트의 인식에도 관여하는지 여부를 평가했습니다. 이를 위해 pDC를 설명된 대로 시딩하고 TLR9 길항제 H154(50μM)로 배양한 후 "면역원성" AAV8 벡터 로트 A-HEK-1, A-HEK-2, A로 자극했습니다. -HEK-3 및 A-Sf9-1(MOI: 1:1× 106 vg). 18시간 후에는 세포 증식의 증거가 관찰되지 않았으며(그림 3a), IP-10, MIP-1, TNF- 및 IFN- 방출이 크게 감소한 것으로 측정되었습니다(그림 3a). 3b). 이는 인간 pDC의 "면역원성" AAV8 벡터 로트에 대한 면역 반응이 TLR9 신호전달에 의해 매개된다는 것을 나타냅니다.

그림 2. 서로 다른 AAV8-CMV-eGFP와 AAV2-CMV-eGFP 벡터 로트 간의 capsid/vg 비율 비교. Te capsid/vg 비율은 (a) 8개의 AAV8 벡터 로트 및 (b) 4개의 AAV2 벡터 로트의 흡광도 측정(ELISA) 및 ddPCR 결과에서 파생됩니다. 점선은 "비면역원성" AAV 벡터 로트와 "면역원성"을 구분합니다. 막대는 반복실험의 평균과 표준 편차를 나타냅니다. 통계적 유의성은 짝을 이루지 않은 Student t-test를 사용하여 결정되었습니다.

그림 3. pDC에 의한 "면역원성" AAV8-CMV-eGFP 벡터 로트의 인식은 TLR9에 따라 다릅니다. 인간 pDC를 TLR9 길항제 H154(5{24}} μM)로 처리한 후 "면역원성" AAV8 벡터 로트(MOI: 1:1× 106 vg)로 18시간 동안 자극했습니다. (a) "면역원성" AAV 벡터 로트(상단 이미지) 또는 "면역원성" AAV 벡터 로트 및 H154(하단 이미지)로 처리된 정제된 pDC의 대표적인 명시야 이미지. 스케일 바는 100μm입니다. (b) 자극된 pDC에 의한 IP-10, MIP-1, TNF- 및 IFN- 2의 사이토카인 방출. IFN- 2 측정에서 일부 값이 분석 범위 아래로 떨어지기 때문에 반대수 플롯으로 표시하기 위해 측정된 모든 IFN- 2 값에 상수 1을 추가했습니다. 평균과 표준 편차가 표시됩니다. 통계적 유의성은 일원 분산 분석(one-way ANOVA)과 Holm-Sidak의 사후 분석을 사용하여 결정되었습니다. P 값: 0.05 이하: *; 0.01 이하: **; 0.001 이하: ***.
DNase 처리는 "면역원성" AAV8 및 AAV2 벡터 로트의 면역 반응을 감소시킵니다.
"면역원성" AAV8 벡터는 pDC에서 TLR9-의존성 면역 반응을 유도했지만, "비면역원성" 로트에서는 그러한 반응이 유도되지 않았습니다. TLR9는 DNA, 특히 메틸화되지 않은 CpG 모티프9를 포함하는 DNA에 반응하여 활성화됩니다. 중요한 것은, 우리의 ddPCR 측정을 통해 동일한 바이러스 DNA 구성 요소가 "면역원성" 및 "비면역원성" 벡터 로트 모두에 존재한다는 것을 확인했다는 것입니다. 종합적으로, 이는 바이러스 내 DNA가 아닌 바이러스 현탁액에 있는 포장되지 않은/유리 DNA가 "면역원성" AAV 벡터 로트에 대해 관찰된 면역 반응의 원인이 될 수 있음을 시사합니다. 따라서 "면역원성" AAV8 벡터 로트의 바이러스 현탁액에 잔여 유리 DNA가 존재하는 경우 선천적 면역 반응은 DNase에 의해 약화되어야 합니다. 이 가설을 테스트하기 위해 "면역원성" AAV8 및 AAV2 벡터 로트를 AAV 자극 전 30분 동안 DNase I(100μg/ml)로 전처리했습니다. pDC 또는 AAV 입자에 대한 DNase 처리의 비특이적 효과를 배제하기 위해 AAV 단독 자극에서 벡터에 pDC 자극 전에 DNasemock 처리를 적용했습니다. DNase가 없는 이러한 모의 처리에서 AAV 입자는 DNase 처리된 AAV와 동일한 기간 동안 동일한 DNase 분해 배지에서 37도에서 배양되었습니다. 10, pDC를 DNase 전처리 또는 모의 처리된 "면역원성" AAV 벡터 로트(MOI: 1:1 x 106 vg)로 시딩하고 자극했습니다. DNase 단독으로 배양되거나 비히클과 함께 가짜 처리된 pDC가 대조군으로 사용되었습니다. 흥미롭게도, "면역원성" AAV8 및 AAV2 벡터 로트의 DNase 처리는 반응성 세포 증식을 감소시켰으며(그림 4a) 완전히 폐지되었습니다(AAV8 로트 A-HEK-2 및 A-Sf9-1; AAV2 로트). B-Sf9-1 및 B-Sf9-2) 또는 대폭 감소(AAV8 로트 A-HEK-1 및 A-HEK-3) IP 출시{{40} }, MIP-1 AAV 자극 후 TNF- 및 IFN-(그림 4b,c). 관찰된 DNase 효과가 실제로 벡터의 완전성에 대한 DNase의 영향이 아니라 바이러스 외부 DNA의 소화에 의해 발생했음을 확인하기 위해 AAV 벡터 로트의 DNase 처리가 AAV의 형질도입 능력에 영향을 미치는지 여부를 조사했습니다. AAV 적용으로 인해 검출 가능한 pDC 형질도입이 발생하지 않았기 때문에 HEK 세포는 AAV 형질도입 시 형질도입 효율을 분석하는 잘 알려진 세포 모델이므로 HEK 세포를 이러한 분석에 사용했습니다. 우리는 DNase 처리 및 가짜 처리된 AAV8 및 AAV2 벡터 로트(MOI: 1:8×104 vg)로 HEK293T 세포를 자극하고 벡터 적용 3일 후 형광 현미경으로 형질도입 효율을 평가했습니다. 기재된 바와 같이, AAV2 벡터는 AAV8 벡터에 비해 더 높은 형질도입 효능을 나타내었다. 더욱이 중요한 것은 DNase를 사용한 전처리가 HEK 유래 또는 Sf{61}} 세포 유래 AAV8 및 AAV2 벡터 로트에서 형질도입 효율을 감소시키지 않았다는 것입니다(그림 S5a,b). 이러한 결과는 벡터 로트의 면역원성 특성에 대한 DNase 효과가 바이러스외 DNA의 분해로 인한 것이라는 추가 증거를 제공합니다. TLR9 길항제 H154가 4개의 면역원성 AAV8 로트 모두에 대해 염증성 사이토카인의 방출을 근본적으로 폐지했지만(그림 3), DNase 전처리는 AAV8 로트 A-HEK에 대한 염증성 사이토카인 반응도 제거할 수 있었습니다{{75} } 및 A-Sf9-1, AAV8 로트 A-HEK-1 및 A-HEK-3에 대해서는 완전히 제거되지 않았습니다(그림 4). 증가된 DNase 처리 시간이 이 사이토카인 반응을 폐지할 수 있는지 여부를 테스트하기 위해 각 로트(A-HEK-1 및 A-HEK{{87})의 DNase 배양 시간을 10배 증가시킨 후 pDC의 시뮬레이션 실험을 반복했습니다. }). 우리는 벡터를 5시간 동안 DNase 처리한 후 AAV 자극 세포의 상등액의 평균 사이토카인 농도가 더 이상 감소하여 비히클 대조군과 더 이상 크게 다르지 않음을 관찰했습니다. 이 반응 패턴은 각각 한 명의 개인 기증자의 세포를 사용하여 수행된 세 가지 실험에서 확인할 수 있습니다(그림 S6). 이는 pDC에서 TLR{91}}의존적 전염증성 면역 반응의 중심 원인이 실제로 바이러스 외부 DNA임을 시사합니다. 바이러스 내 DNA의 방출이 AAV 벡터의 면역자극 활성을 증가시키는지 여부를 테스트하기 위해 의도적으로 "면역원성" AAV8 로트 A-HEK-1의 바이러스 캡시드를 95도에서 10분간 열처리하여 열었습니다. . 그런 다음 열처리된 벡터 로트를 사용하여 pDC를 자극했습니다. 열처리 유무에 관계없이 AAV8 로트 A-HEK{103}} 자극 시 반응성 세포 증식에는 차이가 없었지만 IP-10, MIP-1 방출이 크게 증가했습니다. , TNF- 및 IFN-은 가열 처리 조건에서 캡슐화된 바이러스 DNA가 벡터 현탁액으로 방출되면 면역 반응 유도에 기여할 수 있음을 나타냅니다(그림 5). 함께, 이들 데이터는 AAV 벡터 제제가 pDC에서 로트 특이적 면역 반응을 유발할 수 있는 바이러스외 DNA 오염물질을 포함할 수 있음을 나타냅니다. 이러한 반응은 TLR9 신호전달에 의해 매개되며 벡터 로트를 DNase로 처리하면 감소/폐지될 수 있습니다.

그림 4. DNase 전처리는 "면역원성" AAV8-CMV-eGFP 및 AAV2-CMV-eGFP 벡터 로트에 의해 유도된 면역 반응을 감소시킵니다. 인간 pDC를 DNase 처리된 "면역원성" AAV8 벡터 로트로 18시간 동안 자극했습니다(MOI: 1:1×106 vg). (a) "면역원성" AAV 벡터 로트(상단 이미지) 및 1{{30}}0 ug/ml의 DNase로 전처리된 "면역원성" AAV 벡터 로트로 자극된 정제된 pDC의 대표적인 명장 이미지 나(하단 이미지). 스케일 바는 500μm입니다. (b) AAV8-자극 pDC에 의한 IP-10, MIP-1, TNF- 및 IFN- 2의 사이토카인 방출. (c) AAV2-자극된 pDC에 의한 사이토카인 방출. IFN- 2 측정(b 및 c) 및 TNF- 측정(b)에서 일부 값이 분석 범위 아래로 떨어지므로 측정된 모든 IFN- 2 및 TNF- 값에 상수 1을 추가했습니다. 반로그 플롯으로 표현. 평균과 표준 편차가 표시됩니다. 통계적 유의성은 일원 분산 분석(one-way ANOVA)과 Holm-Sidak의 사후 분석을 사용하여 결정되었습니다. P 값: 0.05 이하: *; 0.01 이하: **; 0.001 이하: ***.
AAV8 벡터 준비에서 바이러스 외 DNA 오염물질에 대한 탐색적 분석.
AAV 벡터 로트에서 바이러스외 DNA 성분의 첫 번째 탐색적 특성 분석을 수행하기 위해 대표적인 "면역원성"(A-HEK-1) 및 "비면역원성"(B-HEK-1) HEK 세포 유래 벡터 로트를 분석했습니다. 이 로트는 위에서 설명한 대로 37도에서 30분 동안 pDC 배지에서 DNase 처리했거나, 모의 처리하고 100 kDa 컷오프 필터링 장치를 사용하여 한외여과했거나, 모의 처리만 했습니다(그림 S7a- g). 정제된 DNA의 연속적인 Bioanalyzer LabChip 분리 및 평가를 통해 각 로트의 처리된 샘플과 모의 처리된 샘플에서 비슷한 양의 벡터 DNA(그림 S7b-g)가 존재하는 것으로 나타났습니다. 이는 한외여과나 DNase 처리가 DNA 함량에 영향을 미치지 않았음을 확인시켜 줍니다. 캡시드 내부. 추가적으로, "면역원성"(그림 S7a-d)만 있고 "비면역원성" 벡터 로트(그림 S7a,e-g)에는 100에서 450bp 크기 범위의 추가 DNA 분자가 포함되어 있음을 보여주었습니다(그림 S7a,e-g). .S7c,d 및 h). 중요한 것은 이러한 추가 DNA 분자가 모의 처리된 샘플과 초여과된 샘플에서 검출될 수 있었지만 DNase 처리된 샘플에서는 사실상 존재하지 않았다는 것입니다(그림 S7a-d). 이는 이들 DNA 분자가 DNase에 의해 분해될 수 있지만 한외여과에 의해 벡터 현탁액에서 제거될 수 없는 바이러스 외 DNA 오염물질을 나타냄을 나타냅니다. 이러한 오염물질이 "면역원성" 벡터 로트에서만 검출될 수 있고 "비면역원성" 벡터 로트에서는 검출되지 않는다는 자금 지원은 이러한 바이러스외 DNA 분자의 발생이 로트 특이적이며 추가로 이러한 분자가 유발하거나 기여한다는 것을 시사할 수 있습니다. 벡터의 면역자극 특성. "면역원성"(A-HEK-1) 및 "비면역원성"(B-HEK-1) 로트에서 HEK의 정량적(q)PCR 분석에서 오염 DNA의 잠재적 소스를 평가하기 위해 세포 DNA, 플라스미드 DNA 및 AAV 벡터 DNA를 수행했습니다. HEK 세포 기원의 Alu 반복, 핵 게놈 다중 복사 NPIP 유전자 및 미토콘드리아 16S rRNA 유전자 서열(mt16S)의 증폭을 위해 DNase 처리, 모의 처리 및 초여과 및 각 로트의 모의 처리 샘플의 주형 DNA를 사용했습니다. , AAV8 역전된 말단 반복 앰플리콘(ITR2; 벡터 및 이식유전자 플라스미드 DNA 기원)의 증폭과 blah(암피실린 저항성) 유전자(Amp; 플라스미드 DNA 기원)에 대한 앰플리콘의 증폭에 대한 것입니다(표 S4). HEK 세포 DNA 특이적 앰플리콘 대 ITR2 앰플리콘(즉, Alu 대 ITR2, NPIP 대 ITR2, mt16S 대 ITR2)과 플라스미드 DNA 특이적 앰플리콘 대 ITR2 앰플리콘의 ΔCt 값 비율 비교(Amp 대 ITR2)는 각각 두 로트에 무시할 수 있는 양의 HEK 세포 핵 및 미토콘드리아 DNA가 포함되어 있음을 나타냅니다. 대조적으로, 분석은 "면역원성" 및 "비면역원성" 벡터 로트 모두에서 상당한 양의 플라스미드 DNA를 나타냈습니다(AAV DNA에 비해 카피수 측면에서 각각 약 1/32 및 1/50). 다른 AAV 벡터에 대해 보고된 값 범위 내에 있는 비율입니다(그림 S7). 그럼에도 불구하고 두 벡터 로트의 DNase 처리 샘플과 모의 처리 샘플 또는 초여과 샘플과 모의 처리 샘플 사이의 플라스미드 및 HEK 세포 DNA에 대한 벡터 DNA의 상대적 비율에는 뚜렷한 차이가 없었습니다(그림 S8). 이는 포장되지 않은 오염 DNA가 포장된 DNA와 표적 서열 구성이 유사하다는 것을 의미할 수 있습니다. 그러나 qPCR 분석의 한계는 불완전한 표적 서열을 가진 상당한 양의 단편을 포함하는 오염 물질 DNA의 크기(100-450bp)입니다.
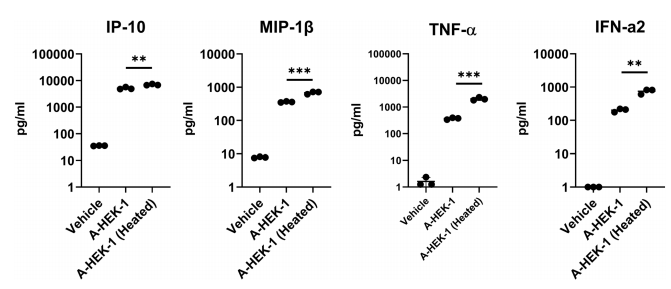
그림 5. 벡터의 열처리에 의한 바이러스 내 DNA의 방출은 pDC에서 전염증성 사이토카인 반응을 향상시킵니다. 열처리된 AAV8 로트 A-HEK-1(MOI: 1:1× 106 vg). 수평선은 평균과 표준 편차를 나타냅니다. 열처리된 벡터와 처리되지 않은 벡터에 의해 유도된 사이토카인 반응 사이의 통계적으로 유의미한 차이는 스튜던트 t-테스트를 사용하여 결정되었습니다. P 값: 0.01 이하: **; 0.001 이하: ***.
논의
AAV 벡터는 유전자 치료에서 가장 유망한 도구 중 하나입니다. 그러나 축적된 증거는 AAV의 면역원성이 무시할 수 있다는 견해에 이의를 제기합니다5. 이에 비추어 AAV에 대한 면역 반응이 발생하는 메커니즘을 더 잘 이해하는 것이 점점 더 중요해지고 있습니다. 이 연구에서 우리는 (1) AAV8과 AAV2가 캡시드/vg 비율이나 생산 플랫폼, 제조업체/정제 방법에 특이적이지 않은 인간 pDC에서 로트 특이적 선천적 면역 반응을 유도하고; (2) pDC의 선천적 면역 반응은 TLR9 신호 전달에 의존하며 DNase를 사용한 전처리로 감소될 수 있습니다. (3) DNase 처리는 HEK293T 세포에서 AAV8 및 AAV2 벡터 로트의 형질도입 속도를 감소시키지 않으므로 벡터 입자의 완전성에 영향을 미치지 않습니다. (4) AAV 벡터 로트는 DNase로 벡터 로트를 처리하여 제거될 수 있는 바이러스외 DNA 분자를 포함할 수 있습니다. 이는 HEK 및 Sf{15}} 세포 유래 AAV 제제 모두 선천적 면역 반응을 자극하는 바이러스 외 DNA 불순물을 포함할 수 있음을 시사합니다. 최근 연구에서는 다양한 숙주 세포 종(HEK 세포 및 Sf9 세포)의 AAV 벡터를 사용하여 비교 분석이 수행되었습니다. 저자는 테스트한 모든 AAV 혈청형과 제조업체에서 HEK 및 Sf{21}} 유래 벡터의 PTM 및 잔류 숙주 세포 단백질 불순물이 다르다는 사실을 발견했습니다. 또한 그들은 AAV 형질도입에 대한 1차 인간 섬유아세포의 사이토카인 반응을 분석하여 HEK 및 Sf{23}} 유래 벡터의 면역원성 특성이 다를 수 있음을 발견했습니다. 우리 연구에서 우리는 또한 서로 다른 제조업체의 동일한 AAV 구성의 서로 다른 로트와 두 개의 서로 다른 혈청형을 사용하여 이 두 가지 주요 생산 시스템을 비교했습니다. 그러나 우리가 인간 pDC 모델에서 관찰한 벡터 유발 면역 반응은 주어진 생산 시스템, 제조업체 또는 혈청형과 특별히 관련이 있는 것이 아니라 로트 특정적이었습니다. 망막 유전자 치료에 대한 이전의 전임상 및 임상 연구에서는 안구 염증이나 면역 세포 침윤과 같은 AAV 벡터에 대한 면역 반응이 캡시드/vg 비율18 또는 용량 차이5의 차이에 의해 영향을 받을 수 있다고 보고했습니다. Timmers 등18은 비인간 영장류를 대상으로 한 전임상 연구에서 바이러스 현탁액에서 빈 AAV 캡시드를 제거하면 염증이 감소하고 바이러스 형질도입이 개선된다는 사실을 보여주었습니다. 그러나 우리의 결과는 "면역원성" 및 "비면역원성" AAV 벡터 로트 모두에서 증가된 캡시드/vg 비율이 존재한다는 것을 보여주었습니다. 이는 바이러스 현탁액에서 더 많은 수의 캡시드(빈 캡시드)가 바이러스 유도에 책임이 없음을 의미합니다. 인간 pDC 모델의 벡터 로트 특이적인 면역 반응. 게다가, 우리는 이전에 AAV8이 비인간 영장류6,8에서 용량 의존적 방식으로 면역 반응을 유도한다는 것을 보여주었습니다. 그러나 본 연구에서 "비면역원성" AAV 벡터의 용량을 증가시키는 것은 인간 pDC에서 면역 반응을 유발하는 데 충분하지 않았습니다. 따라서 벡터의 면역원성 특성 차이의 원인을 이해하기 위해 "면역원성" AAV 로트의 인식과 관련된 메커니즘을 조사했습니다. 시험관 내 면역능력 세포 모델의 사용을 통해 과학자들은 AAV 벡터에 의해 생성된 선천성 면역 반응에서 TLR 경로의 역할을 보다 정확하게 연구할 수 있었습니다9,10. Zhu 등은 먼저 전통적인 DC나 비-pDC가 아닌 pDC가 AAV 자극에 반응하여 다량의 I형 IFN 및 전염증성 사이토카인을 방출하고 AAV8 및 AAV2 인식에 TLR9 경로가 관여함을 입증했다고 설명했습니다. 마우스 pDC를 사용합니다. 저자는 또한 AAV2가 인간 pDC에서 TLR{49}}의존 면역 반응을 유도함을 관찰했습니다. 우리 연구에서 가장 특이적인 TLR9 길항제 중 하나인 H1549,21-24를 사용하여 AAV2뿐만 아니라 AAV8 벡터도 인간 pDC에서 TLR{56}}의존적 선천 면역 반응을 유도한다는 것을 간접적으로 보여주었습니다. 하지만 매우 구체적인 방식으로요. TLR9는 DNA 수용체이기 때문에 이는 "면역원성" AAV 벡터 로트에 대한 면역 반응이 DNA 구성요소에 의해 유도되었음을 시사합니다. 그러나 ddPCR 측정을 통해 동일한 포장 DNA 구성 요소가 "면역원성" 및 "비면역원성" 벡터 로트 모두에 존재한다는 것이 확인되었지만 "비면역원성" 로트는 pDC에서 면역 반응을 유발하지 않았습니다. 추가적으로, DNase 처리는 "면역원성" AAV 벡터 로트의 면역자극 특성을 감소시키거나 폐지했지만 HEK 세포에서 이들 벡터의 형질도입 효능을 감소시키지 않았습니다. 벡터 현탁액은 손상되지 않았지만 손상되지 않은 캡시드 내의 벡터 게놈의 무결성에는 영향을 미치지 않았습니다. 이는 대표적인 DNase 처리 및 모의 처리된 "면역원성" 및 "비면역원성" 벡터 로트의 비교 DNA 분석을 통해 추가로 확인되었습니다.

cistanche tubeulosa - 면역 체계를 향상시킵니다.
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
종합적으로, 이러한 모든 실험은 pDC의 "면역원성" 벡터 로트에 대한 면역 반응이 AAV 입자에 포함된 DNA(즉, 벡터 게놈 또는 AAV 캡시드에 포장된 잠재적인 DNA 불순물)에 의해 조정되지 않고 접근 가능한 외부 바이러스 DNA에 의해 조정되었음을 나타냅니다. 바이러스 현탁액에 포함된 구성 요소(즉, 바이러스 캡시드에 의해 보호되지 않거나 외부에 있는 DNA). 우리는 또한 "면역원성" 벡터 로트의 바이러스 캡시드에 포함된 DNA가 벡터의 열처리에 의해 세포에 노출되었을 때 면역 반응이 증가한다는 것을 관찰했습니다. 캡시드를 연 후 면역자극 활성의 증가가 벡터의 단일 가닥 DNA 때문인지 아니면 잔류 숙주 세포 핵산, 잔류 헬퍼 DNA 서열, 백본 서열과 같은 AAV 캡시드에 포장된 잠재적 불순물 때문인지는 확실하지 않습니다. 카세트와 함께 포장된 단편 또는 ITR의 역프라이밍으로 인해 AAV12,25에 포장된 작은 백본 단편이 생성됩니다. pDC에 의한 바이러스 외부 DNA 흡수의 정확한 메커니즘은 아직 알려져 있지 않습니다. CpG 올리고뉴클레오티드에 대한 pDC의 반응성은 pDC가 유리 DNA에 반응할 수 있음을 보여줍니다. 이는 pDC의 면역 반응이 벡터 현탁액에 포함된 자유 오염 DNA의 흡수에 의해 촉발될 수 있음을 시사합니다. 또한, pDC가 AAV 벡터를 흡수할 수 있는 것으로 나타났으며 이는 AAV 입자를 흡수하는 동안 잠재적인 캡시드 결합 DNA가 세포 내로 운반될 수 있음을 시사합니다. AAV 벡터 준비에 바이러스 외 DNA 오염이 존재하는 것은 벡터의 생산 및 정제 과정에서 발생하는 각 벡터 로트의 고유한 특성일 수도 있고, 부적절한 보관 조건으로 인해 캡슐화된 DNA가 방출되었기 때문일 수도 있습니다. . 이 실험에서 조사된 모든 벡터 로트는 동일한 기간 동안 획득되었습니다(조사된 8개 AAV8 벡터 로트 중 5개, 그 중 2개는 "면역원성"이었습니다(A-HEK-2; A-HEK-3). 세 개는 "비면역원성"이었습니다(A-Sf9-2; B-Sf9-1; B-Sf9-2)는 이 연구를 위해 특별히 동시에 생산되었습니다). 각 제조업체는 동일한 운송 상자에 배송되었으며, 수령 시 모든 로트는 온도 경보로 보호되는 -80도 냉동고의 동일한 서랍에 나란히 보관된 후 모든 로트의 분취량이 동시에 해동되어 pDC에 적용되었습니다. 병행 실험에서. 이는 부적절한 보관보다는 AAV 생산 및 정제 공정이 이들 로트의 바이러스외 DNA 함량 및 면역자극 특성의 차이에 책임이 있음을 강력히 시사합니다. 과거에는 유전자 치료를 위해 생산된 임상 등급 AAV 벡터 로트(alipogenetiparvovec, Glybera)가 잠재적으로 면역원성인 잔류 숙주 세포 DNA를 포함한 다량의 불순물로 인해 더 이상 승인되지 않았습니다. 바이러스 현탁액에서 DNA 불순물을 제거하는 작업은 일반적으로 생산 공정 중에 수행됩니다. 여기서 Benzonase29 또는 DNase30 처리는 최종 바이러스 현탁액에서 잔류 DNA를 제거하기 위해 일상적으로 적용됩니다. 프로토콜에 따라 이 처리는 30분에서 3시간 동안 지속되며 그 후 효소는 염화세슘염과 같은 화학물질에 의해 비활성화됩니다. 우리의 실험에서 아이오와 대학의 바이러스 벡터 코어 시설에서 파생된 5개의 AAV8 로트 중 4개와 Virovek의 AAV2 벡터 로트 모두 pDC에서 면역원성인 것으로 밝혀졌습니다. "재료 및 방법" 섹션에 설명된 대로 두 제조업체의 벡터 로트 정제 과정에는 여러 정제 단계가 포함되며 그 중 일부는 서로 크게 다릅니다. 따라서 아이오와주 핵심 시설의 정제 공정에는 터보뉴클레아제 처리, 이어서 요오딕사놀 구배 초원심분리, 음이온 교환 컬럼 크로마토그래피, 플러터 멸균, 원심분리 필터를 사용한 완충액 교환이 포함됩니다. 이에 비해 Virovek은 벤조나제 처리, CsCl의 초원심분리, 탈염 및 필터 멸균을 적용합니다. 반면에 Vigene의 정제 공정에는 DNase 처리가 포함되지 않지만 Iowa의 Core Facility에서 사용하는 것처럼 요오딕사놀 구배 초원심분리가 포함됩니다. 그러나 놀랍게도 Vigene(AAV8: C-HEK-1; AAV2: C-HEK-1 및 2)에서 파생된 세 가지 벡터 로트 중 어느 것도 pDC에서 면역 반응을 유도하지 않았으며, 이는 "비면역원성"을 시사합니다. "벡터 로트는 DNase 처리를 포함하지 않는 생산 공정으로도 생성될 수 있습니다.

cistanche 보충 혜택 - 면역 체계를 강화하는 방법
전반적으로, 세 제조업체가 사용하는 부분적으로 유사하고 부분적으로 다른 정제 단계로 인해 pDC에서 관찰된 벡터의 면역원성 특성을 제조 공정의 단일 단계에 연결하는 것이 어렵습니다. 임상 시험에서는 엄격한 품질 관리를 받는 우수제조관리기준(GMP) 등급 벡터를 사용합니다. 본 연구에 사용된 세 제조업체의 벡터 중 어느 것도 GLP(Good Laboratory Practice) 등급이 아니므로 임상 등급 벡터보다 순도가 낮을 수 있습니다. 따라서 인간을 대상으로 한 임상 시험에 사용된 GMP 벡터는 본 연구에서 관찰한 차이를 나타낼 수도 있고 나타내지 않을 수도 있으며 유전자 치료법의 임상적 사용에 대한 우리 연구 결과의 관련성이 명확하지 않다는 점을 인식하는 것이 중요합니다. 그러나 우리의 경험에 따르면 GMP 등급 벡터를 사용하더라도 숙주 세포 단백질과 같은 오염 성분의 농도에 있어 로트별 상당한 차이가 발생할 수 있으며 GMP 등급 벡터의 경우에도 어느 정도 수준인지에 대해 일률적으로 합의된 사양이 없습니다. 수용 가능5. 종합적으로, AAV 벡터의 제조 공정을 개선하는 것은 의도하지 않은 면역 반응의 가능성을 최소화하기 위해 바이러스 현탁액에 잔류 불순물의 존재를 피하는 데 중요합니다. 결론적으로, 우리는 바이러스 외 DNA 불순물이 인간 pDC에서 AAV 벡터의 면역원성 특성에 영향을 미칠 수 있음을 입증했습니다. 동물 모델이나 인간 환자에서 AAV 매개 유전자 치료의 안전성에 대한 이러한 발견의 의미를 조사하기 위해서는 추가 연구가 필요합니다.
참고자료
1. Gaj, T., Epstein, BE & Schafer, DV 아데노 관련 바이러스를 사용한 게놈 공학: 기본 및 임상 연구 응용. 몰. 테르. 24, 458–464 (2016).
2. Garita-Hernandez, M. 외. 인간 유도 만능 줄기 세포에서 유래된 3D 망막 오가노이드에 AAV 매개 유전자 전달. 국제 J.Mol. 과학. 21, 994(2020).
3. 러셀, S. 외. RPE65-매개 유전성 망막 이영양증 환자를 대상으로 한 voretigene neparvovec(AAV2-hRPE65v2)의 효능 및 안전성: 무작위 대조, 공개 라벨, 제3상 시험. Lancet 390, 849–860 (2017).
4. He, X., Urip, BA, Zhang, Z., Ngan, CC & Feng, B. 궁극적인 치료법을 향한 AAV 전달 치료법의 진화. J.Mol. 메드. 99, 1–25. https://doi.org/10.1007/s00109-020-02034-2(2021).
5. Bucher, K., Rodríguez-Bocanegra, E., Dauletbekov, D. & Fischer, MD 아데노 관련 바이러스 벡터를 사용한 망막 유전자 치료에 대한 면역 반응 - 치료 성공 및 안전성에 대한 영향. 음식물. 레틴. 눈 해상도. 83, 100915(2020).
6. Reichel, FF 외. AAV8은 영장류 눈에서 선천성 및 적응성 면역 반응을 유도할 수 있습니다. 몰. 테르. 25, 2648-2660(2017).
7. Boyd, RF 외. 개의 후유리체 절제술 후 rAAV의 유리체강내 전달로 망막 형질도입이 감소하고 이식유전자 지향 면역원성이 향상되었습니다. 진 터. 23, 548–556(2016).
8. Rodríguez-Bocanegra, E. 외. 비인간 영장류에서 아데노 관련 바이러스의 망막하 전달 후 망막의 과민성 초점에 대한 종방향 평가. 번역. 비스. 과학. 기술. 10, 15(2021).
9. Zhu, J., Huang, X. & Yang, Y. Te TLR9-MyD88 경로는 생쥐의 아데노 관련 바이러스 유전자 치료 벡터에 대한 적응 면역 반응에 중요합니다. J. 클린. 조사하다. 119, 2388-2398(2009).
10. Hösel, M. 외. 아데노 관련 바이러스 벡터에 대한 인간 비실질 간 세포의 톨 유사 수용체 2-매개 선천적 면역 반응. 간학 55, 287–297 (2012).
11. Rumachik, NG 외. 방법이 중요합니다. 재조합 AAV를 위한 표준 생산 플랫폼은 화학적으로나 기능적으로 별개의 벡터를 생성합니다. 몰. 테르. 방법 임상. 개발. 18, 98–118(2020).
12. Wright, JF 임상 등급 재조합 AAV 벡터의 제품 관련 불순물: 특성화 및 위험 평가. 생물의학 2, 80–97 (2014).
13. Clément, N. & Grieger, JC 임상 시험을 위한 재조합 아데노 관련 바이러스 벡터 제조. 몰. 테르. 방법 임상. 개발. 3, 16002(2016).
14. Penaud-Budloo, M., François, A., Clément, N. & Ayuso, E. 재조합 아데노 관련 바이러스 생산의 약리학. 몰. 테르. 방법 임상. 개발. 8, 166–180(2018).
15. Ye, Y., Gaugler, B., Mohty, M. & Malard, F. Plasmacytoid 수지상 세포 생물학 및 면역 매개 질병에서의 역할. 클린. 번역. 면역. 9, e1139(2020).
16. Fischer, MD 외. 맥락막혈증 환자를 위한 아데노 관련 바이러스 벡터를 이용한 망막 유전자 치료의 유효성 및 안전성: 무작위 임상 시험. JAMA 안과. 137, 1247~1254(2019).
17. Weleber, RG 외. RPE65-결핍 레버 선천성 흑내장증 및 중증 유아기 발병 망막 이영양증에 대한 유전자 치료 2년 후의 결과. 안과학 123, 1606-1620(2016).
18. Timmers, AM 등. 아데노 관련 바이러스 벡터의 유리체 강내 주입에 대한 안구 염증 반응 : 게놈과 캡시드의 상대적 기여. 흠. 진 터. 31, 80–89(2020).
19. Ran, G. et al. 부위 지정 돌연변이 유발은 캡시드 라이브러리 유래 재조합 AAV 벡터의 형질도입 효율을 향상시킵니다. 몰. 테르. 방법 임상. 개발. 17, 545–555(2020).
20. Ellis, BL et al. 9개의 천연 아데노 관련 바이러스(AAV1-9)와 1개의 조작된 아데노 관련 바이러스 혈청형을 사용하여 포유류 일차 세포 및 세포주의 생체외/체외 형질도입 효율을 조사합니다. 비롤. J. 10, 1–10(2013).
21. Yamada, H. et al. CpG에 의한 면역 활성화에 대한 억제 DNA의 효과. J. Immunol. 169, 5590-5594(2002).
22. Zhang, P. et al. Toll 유사 수용체 9 길항제는 실험적 자가면역 중증근육무력증에서 체액성 면역을 억제합니다. 몰. 면역. 94, 200-208(2018).
23. Chan, YK 외. 선천적 면역 및 염증 반응을 회피하기 위해 아데노 관련 바이러스 벡터를 설계합니다. 과학. 번역. 메드. 13, eabd3438(2021).
24. Bayik, D., Gursel, I. & Klinman, DM 면역억제성 올리고뉴클레오티드의 구조, 메커니즘 및 치료적 유용성. Pharmacol. 결의안. 105, 216–225 (2016).
25. Brimble, MA et al. 547. AAV 제제에는 ITR 바로 외부에 있는 생산 플라스미드의 DNA 서열로 인한 오염이 포함되어 있습니다. 몰. 테르. 24, S218~S219(2016).
26. Latz, E. et al. TLR9는 ER에서 리소좀의 CpG DNA로 전위된 후 신호를 보냅니다. Nat. 면역. 5, 190-198(2004).
27. Veron, P. et al. 인간 수지상 세포의 주요 하위 집합은 자가 상보적 아데노 관련 바이러스 벡터 1 및 2에 의해 효율적으로 형질도입됩니다. J. Virol. 81, 5385-5394(2007).
28. 평가 보고서: Glybera. https://www.ema.europa.eu/en/documents/assessment-report/glybera-epar-public-assessment 보고서_en.pdf. 2022년 3월 3일 액세스(2012)
29. Arden, E. & Metzger, J. 천연 및 생체공학 재조합 아데노 관련 바이러스 정제를 위한 저렴하고 혈청형 독립적인 프로토콜. J. Biol. 방법 3, e38(2016).
30. Grieger, JC, Choi, VW & Samulski, RJ 아데노 관련 바이러스 벡터의 생산 및 특성화. Nat. 프로토콜. 1, 1412~1428(2006).
31. 키무라(Kimura), T. 외. 시험관 내 및 생체 내 적용을 위한 아데노 관련 바이러스 벡터의 생산. 과학. 9, 13601(2019).
32. Ayuso, E. et al. 높은 AAV 벡터 순도는 혈청형 및 조직과 무관하게 형질도입 효율을 향상시킵니다. 진 터. 17, 503-510(2010).






