당뇨병성 신장질환에서 포도당 및 비포도당으로 유발된 미토콘드리아 기능 장애 Ⅱ
Jan 17, 2024
3. DKD의 포도당 유발 미토콘드리아 기능 장애
사구체 세포에서 포도당은 다음에 의해 흡수됩니다.포도당 수송체(GLUT) 촉진 확산 수송을 통해. GLUT의 각 구성원의 발현 패턴은 세포마다 다릅니다. 메산지움 세포는 GLUT1과 4를 발현하고, 족세포는 GLUT1, 4, 8을 발현하며, 내피 세포는 GLUT1을 발현합니다.32]. 대조적으로, 세뇨관 세포는 주로 나트륨 의존성 포도당 공동수송체(SGLT)를 통해 사구체 여과액으로부터 포도당을 재흡수합니다. 관형 세포에 의해 재흡수된 포도당은 기저측 원형질막의 GLUT를 통해 소멸되어 간질로 확산됩니다. 근위 세뇨관 세포는 또한 포도당 신생합성을 통해 포도당을 생산할 수 있습니다.제2형 당뇨병 [33]. 고혈당증은 주요 병원성 인자이자 일부 중간 대사산물입니다.포도당 대사에도 기여한 바 있다.DKD의 세포 손상. 2000년 Brownlee와 동료들이 제시한 통합 가설에서는 OXPHOS로의 유입 증가로 인한 mtROS의 과잉 생산이핵 DNA 복구 효소폴리(ADP-리보스) 중합효소(PARP)는 글리세르알데히드의 활성을 감소시킵니다.3-인산염 탈수소효소(GAPDH) 및 그에 따른 독성 중간체의 축적포도당 대사 [11]. 그러나 이후 연구에서는 미토콘드리아가 기능 장애를 일으키고 기질의 단순한 증가 외에 다른 메커니즘이 해당작용의 증가와 그에 따른 독성 대사산물의 축적에 기여한다는 사실이 제시되었습니다.

신장 기능을 위한 25% 에키나코사이드와 9% 액테오사이드가 함유된 천연 유기농 시스탄체 추출물을 얻으려면 여기를 클릭하세요
Wecistanche의 지원 서비스 - 중국 최대의 cistanche 수출업체:
이메일:wallence.suen@wecistanche.com
Whatsapp/전화:+86 15292862950
더 많은 사양을 보려면 쇼핑하세요.
https://www.xjcistanche.com/cistanche-shop (영어)
3.1. 바르부르크 효과
일반적으로 암세포는 강화된 해당작용과 손상된 산화적 인산화를 나타냅니다. 이러한 대사 과정의 단시간 및 가역적 전환을 크랩트리 효과(Crabtree effect)라고 하는 반면, 장기간의 대사 재프로그래밍을 워버그 효과(Warburg effect)라고 합니다.
Warburg 효과는 원래 암에서 OXPHOS에서 호기성 해당작용(젖산염이 포도당의 최종 생성물로 생성됨)으로의 전환을 설명하는 데 사용된 용어입니다[35]. 최근 연구에 따르면 이러한 변화는 당뇨병성 신장에서도 발생하는 것으로 나타났습니다[9,19]. 위에서 설명한 것처럼 당뇨병 조직의 미토콘드리아는 기능 장애가 있습니다. 전사체, 대사체 및 대사산물 플럭스 분석에서는 포도당 대사가 증가하고 포도당 대사가 감소하는 것으로 나타났습니다.미토콘드리아 기능db/db 마우스의 신장 피질에서 [9]. 소변 샘플의 대사체학 분석에서는 건강한 대조군에 비해 DKD 환자에서 13개의 대사산물이 크게 감소한 것으로 나타났으며, 그 중 12개는 미토콘드리아 대사와 관련이 있었습니다[19]. 미토콘드리아 기능 장애가 해당작용으로의 전환을 유발하는지, 아니면 해당작용의 증가가 미토콘드리아 기능 장애를 유발하는지 여부는 아직 확립되지 않았습니다[36].
피루베이트 키나아제는 해당과정의 마지막 비가역적 단계인 포스포에놀피루베이트를 피루브산으로 전환시키는 과정을 촉매하는 효소입니다. 피루베이트 키나아제 M2 활성 감소는 Qi와 동료들에 의해 DKD에서 Warburg 효과의 가능한 메커니즘으로 확인되었습니다[37]. 그들은 먼저 50년 이상 DKD가 발생하지 않은(보호된) 제1형 당뇨병 환자와 조직학적으로 DKD가 확인된(비보호) 환자로부터 분리한 사구체에 대한 단백질체학 분석을 실시했습니다. 포도당 대사 및 항산화에 관여하는 일부 효소는 보호된 사구체에서 증가하는 것으로 나타났으며, 특히 피루베이트 키나제 M2(PKM2) 발현 및 활성이 상향조절되었습니다. 고혈당으로 처리된 족세포와 STZ를 주입한 생쥐를 이용한 기계적 연구에서 DKD 마우스 모델에서 PKM2 활성이 감소하고, PKM 하향조절이 DKD 악화에 기여하며, PKM2의 약리학적 활성화가 독성 포도당 대사산물의 상승을 역전시키는 것으로 확인되었습니다. 그리고 미토콘드리아 기능 장애. 마찬가지로, 피루브산 키나아제 활성화의 감소는 암에서 Warburg 효과를 유발합니다[38].

DKD에서 Warburg 효과를 유발하는 것으로 가정되는 다른 요인으로는 스핑고미엘린과 푸마르산염 축적이 있습니다[39]. 매트릭스 보조 레이저 탈착/이온화 질량 분석 이미징(MALDI-MSI)은 DKD 마우스의 사구체에서 ATP/AMP 비율 및 특정 스핑고미엘린 종(SM(d18:1/16:0))의 상당한 증가를 나타냈습니다. [40]. 시험관 내에서 메산지움 세포에 SM(d18:1/16:0)을 추가하면 해당작용이 활성화됩니다. Fumarate는 DKD에서 Nox{12}}유발 손상을 매개하는 인자로 확인되었습니다[41]. 생체 내에서 Nox4의 족세포 관련 유도는 DKD로 인한 사구체 손상을 재현했으며 대사체 분석에서는 푸마레이트가 증가한 것으로 나타났으며 이는 Nox1/Nox4 억제로 역전되었습니다. 푸마르산염은 해당작용의 활성화와 OXPHOS의 억제를 유발할 수 있는 저산소증 유발 인자(HIF) 안정제 역할을 할 수 있습니다.
3.2. 포도당 대사의 독성 대사산물
해당과정에서 분기되는 네 가지 주요 경로는 독성 중간 대사산물을 생성하는 것으로 알려져 있습니다: 폴리올 경로, 헥소사민 경로,고급 당화 최종산물(AGEs) 경로 및 단백질 키나제 C(PKC) 경로[12](그림 3). 이러한 경로 각각을 억제하면 개선됩니다.고혈당으로 인한 부상전임상 모델에서 [42-45]. 특히, 이러한 경로의 활성화는 정상혈당증의 회복으로 즉시 역전될 수 있습니다.
특히, AGE 경로에서 글리세르알데히드 분해에 의해 생성되는 반응성 카르보닐 종(RCS)의 구성원인 3-데옥시글루코손(3DG) 및 메틸글리옥살(MGO)의 수준은 해당과정의 활성화와 함께 증가합니다. RCS는 반응성이 높은 카르보닐기를 갖고 있으며 단백질과 DNA를 변형시킬 수 있습니다. RCS에 의해 당화된 단백질은 AGE의 형성을 유도합니다. 세포외 AGE는 매트릭스의 가교를 증가시켜 동맥 경화를 유발할 수 있습니다[46]. AGE는 또한 AGE(RAGE) 수용체에 결합하여 ROS 형성, 염증 및 섬유증을 유발하는 핵인자-κB(NF-κB) 활성화를 비롯한 다양한 신호를 세포에 전달할 수 있습니다.
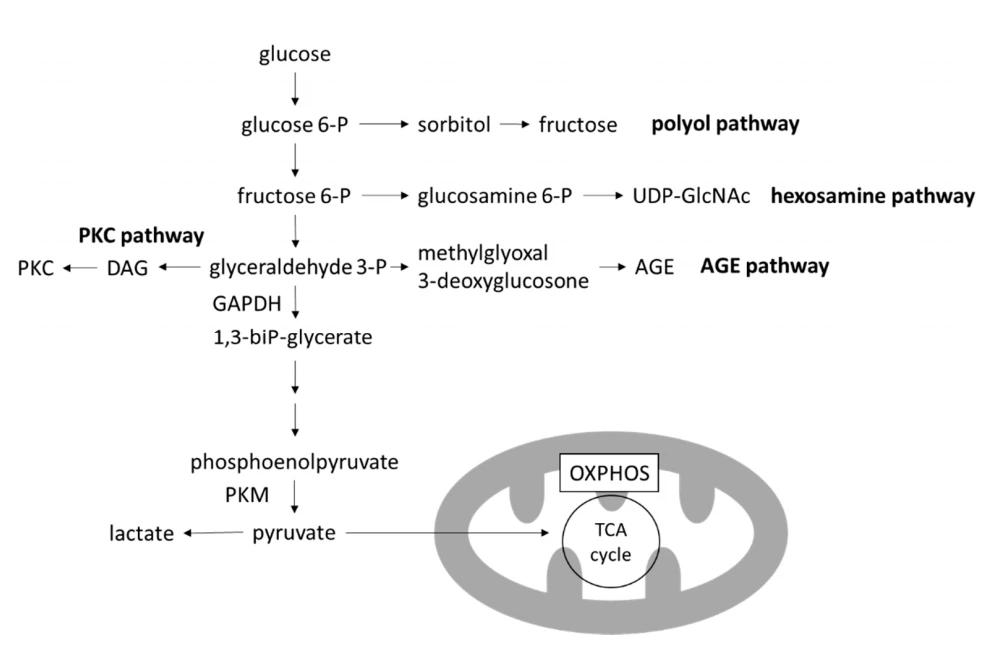
그림 3. 해당과정과 분기 경로. DKD의 고혈당 환경에서는 해당과정이 증가하고 OXPHOS가 감소하여 해당과정의 분기 경로에서 생성된 독성 대사산물이 축적됩니다. AGE, 고급 당화 최종 생성물; DAG, 디아실글리세롤; GAPDH, 글리세르알데히드-3-인산염 탈수소효소; OXPHOS, 산화적 인산화; PKC, 단백질 키나제 C; PKM, 피루베이트 키나제 M; TCA 회로, 트리카르복실산 회로; UDP-GlcNAc, 우리딘 디포스페이트 N-아세틸글루코사민.
4. DKD의 비글루코오스 유발 미토콘드리아 기능 장애
고혈당증은 DKD 발병의 핵심 요소이지만 DKD와 관련된 다른 요인도 미토콘드리아 기능 장애에 기여할 수 있습니다. 이상지질혈증과 지질과다는 DKD의 흔한 합병증이며, 만성신장질환(CKD)의 원인과 관계없이 세뇨관 간질의 저산소증이 발생한다[48]. 엔도텔린-1(Edn1)은 국소 분절 사구체 경화증(FSGS) 모델에서 변환 성장 인자-(TGF-)의 하류 인자로 처음 확인되었으며 사구체 내피 세포에서 mtROS를 통해 알부민뇨를 유발하는 것으로 나타났습니다. 나중에 동일한 신호 전달 경로가 DKD에서도 상향 조절되는 것으로 밝혀졌습니다[49,50]. 이 섹션에서는 미토콘드리아 기능 장애에서 DKD의 발달과 진행에서 이러한 요인의 역할에 대해 논의합니다.

4.1. 지방독성
DKD 환자의 신장 생검에서 건강한 대조군과 비교하여 사구체 내피 세포, 족세포 및 관형 세포에서 전자 현미경으로 광범위한 지질 방울 축적이 관찰되었습니다 [51,52]. 이들 샘플의 유전적 분석에서는 퍼옥시좀 증식자 활성화 수용체(PPAR)-, 카르니틴 팔미토일트랜스퍼라제 1(CPT1), 아실-CoA 산화효소 및 L-FABP를 포함한 지방산 산화(FAO) 관련 유전자의 하향조절이 밝혀졌습니다. 저밀도 지질단백질(LDL) 수용체, 산화된 LDL 수용체 및 아세틸화된 LDL 수용체를 포함하는 콜레스테롤 수용체의 상향조절; ATP 결합 카세트 운반체 A1(ABCA1), ATP 결합 카세트 운반체 G1(ABCG1) 및 아포지단백질(APOE)을 포함한 콜레스테롤 유출 관련 유전자의 하향 조절이 포함됩니다. FAO 관련 유전자의 하향 조절은 지질 축적의 원인으로 미토콘드리아 지질 대사의 감소를 암시하지만, 지질 축적 자체는 미토콘드리아 기능 장애를 유발할 수 있습니다. 우리는 이전에 DKD 환자의 혈청으로 치료된 인간 족세포가 종양 괴사 인자(TNF) 발현이 증가했으며 전신 TNF가 아닌 국소 TNF가 족세포에서 ABCA1의 억제를 통해 유리 콜레스테롤 축적 및 손상을 유발한다는 것을 보여주었습니다[53,54]. 특히 ABCA1 억제는 미토콘드리아에서 카디오리핀 축적과 과산화를 유도하여 족세포를 손상에 민감하게 만듭니다. Elamipretide에 의한 ABCA1 과발현 또는 카디오리핀 과산화의 억제는 실험적 DKD에서 족세포 손상을 구출했습니다.
관형 세포는 용질 재흡수를 위해 많은 양의 ATP를 필요로 하며 지방산이 다른 에너지원보다 그램당 더 많은 ATP를 생성하기 때문에 FAO에 의존합니다[56]. 당뇨병의 초기 단계에서 FA 플럭스 증가로 FAO가 증가하고 ROS 생성은 FAO, 특히 아실-CoA 탈수소효소에서 조효소 Q로 전자를 이동시키는 전자 전달 플라보단백질의 전자 누출에 기인합니다. 그럼에도 불구하고 앞서 설명한 바와 같이 당뇨병이 확립된 경우 FAO는 결국 감소합니다[51,58].
이상지질혈증과 단백뇨가 당뇨병을 동반하는 경우가 많기 때문에 DKD 환자의 관형 세포는 지방산 결합 알부민에 노출될 가능성이 높습니다. 알부민 자체는 재흡수 시 세뇨관 세포 손상을 일으킬 수 있는 반면, FA 결합 알부민은 더 심각한 세뇨관 손상을 유발하는 것으로 나타났습니다[59,60]. FA 또는 당화 알부민으로 인한 세포 독성은 메갈린 복합체를 통한 일반적인 알부민 재흡수와는 달리 인간의 브러시 경계에 있는 분화 36/FA 트랜스로카제 단백질 클러스터(CD36/FAT)를 통한 흡수에 의해 매개되는 것으로 나타났습니다. 큐빌린과 양막이 없다[61]. 재흡수 외에도 FA 합성도 상향 조절됩니다 [62,63]. FA는 장쇄 아실-CoA(LC-CoA) 합성효소(ACSL)에 의해 에스테르화되며, 이는 마우스 db/db 모델과 인간 DKD 신장 샘플 모두에서 상향조절됩니다[64,65]. LC-CoA는 CPT1과 CPT2를 통해 미토콘드리아로 전달되어 FAO를 통해 ATP를 생성하고, 대사되지 않은 LC-CoA는 지질 독성을 방지하기 위해 절단되거나 지질 방울에 저장됩니다. 완충 능력이 포화되면 LC-CoA는 Na+/H+ 교환기 1(NHE1)과 포스파티딜이노시톨 4,5-비스포스페이트[PI(4,5)P2] 결합의 억제제 역할을 하여 근위 세뇨관에서 세포사멸을 유발합니다. 세포 [66].
FAO의 유전적 및 약리학적 강화는 DKD 환자를 위한 새로운 치료 전략을 나타낼 수 있습니다. PCG1 및 페노피브레이트 처리의 형질전환 발현은 CPT 및/또는 아실-CoA 산화효소의 복원을 통해 관형 세포 세포사멸을 개선했습니다[58,67].
4.2. 저산소증
세뇨관간질성 저산소증은 CKD 진행의 최종 공통 경로로 알려져 있습니다[48]. 질병의 원인과 관계없이 혈관 확장 장애로 인한 혈류를 통한 산소 공급 감소, 혈관계 손실, 섬유화, 빈혈, 용질 재흡수 증가로 인한 산소 요구량 증가, 미토콘드리아 분리로 인한 ATP 생성 비효율로 인해 저산소증이 발생할 수 있습니다. 이는 CKD의 공유 메커니즘입니다.
최근 급성 저산소증이 ETC에서 mtROS 생성을 유발하는 메커니즘이 밝혀졌습니다 [68]. 급성 저산소증은 복합체 I의 구조적 변화를 촉진하여 내부 미토콘드리아 막의 Na+/Ca2+ 교환기를 활성화시킵니다. 매트릭스로 유입된 Na+는 인지질과 상호작용하여 막 유동성을 감소시켜 자유 유비퀴논이 복합체 II와 복합체 III 사이를 이동할 수 없도록 만듭니다. 따라서 Complex III은 ROS를 생성합니다.
산소는 ETC에서 전자를 받는 데 없어서는 안 될 요소이기 때문에 저산소증은 오랫동안 OXPHOS의 직접적인 억제 인자로 간주되어 왔습니다. 그러나 OXPHOS를 급격하고 직접적으로 감속하려면 산소 농도가 0.3%만큼 낮아야 합니다[69]. 경미하고 장기간의 저산소증에서 HIF1은 ROS 생성을 방지하기 위해 OXPHOS를 억제하고 해당작용을 증가시키는 매개체 역할을 합니다. HIF1은 ETC 복합체를 변형하고 호기성 OXPHOS에서 혐기성 해당작용으로의 대사 전환을 촉진합니다. 그럼에도 불구하고, 만성 저산소증에서 이러한 변화는 미토콘드리아의 ATP 생산 능력을 제한하고 ATP 결핍을 유발하여 세포 독성을 유발할 수 있습니다.

4.3. 엔도텔린-1(Edn1)/Edn1 수용체 유형 A(Endra) 신호
엔도텔린-1(Edn1)은 TGF- -유도 FSGS에서 족세포에 의해 방출되는 신호 분자로 처음 특성화되었습니다[49]. 놀랍게도 Edn1은 mtROS를 유발하고 예비 호흡 능력을 감소시키며 Edn1 수용체 유형 A(Ednra) 활성화를 통해 내피 세포에서 mtDNA 손상을 유발하지만 이는 족세포에서는 나타나지 않습니다. 이 경로는 내피 표면층에서 글리코사미노글리칸 분해를 유도하여 천공의 손실을 초래합니다[70]. 흥미롭게도, 내피 세포에서의 EDNRA 활성화는 족세포 족돌기 소멸 및 세포사멸에도 필요합니다[49].
내피 세포와 Edn1에서 mtROS와 EDNRA의 유사한 역할은 DKD에도 설명되어 있습니다 [50]. 순환하는 Edn1은 당뇨병이 있는 인간과 생쥐에서 증가했습니다 [50,71]. 특히 Ednra는 건강한 인간 신장이나 DKD 내성 C57BL/6J 마우스의 사구체에서는 검출되지 않았지만 인간 DKD 신장 및 당뇨병 DBA/2J 마우스의 사구체에서는 존재했습니다. Ednra는 고혈당으로 처리된 족세포에서 유도될 수 있었지만, 이 족세포는 Edn1을 발현하지 않았는데, 이는 이 신호 전달 계통에 다른 세포 유형이나 자극이 있음을 의미합니다[50]. 따라서 Edn1/Ednra 신호 전달은 FSGS 및 DKD의 미토콘드리아 기능 장애를 통한 족세포와 내피 세포 간의 상호 누화에 중요합니다.
또 다른 혈관 활성 경로인 레닌-안지오텐신-알도스테론 시스템(RAAS)도 DKD를 포함하여 CKD 진행에 참여하는 것으로 알려져 있습니다. 전신 및 사구체 내 혈압 증가의 해로운 효과 외에도, 안지오텐신 II 치료는 생체 내 및 시험관 내에서 족세포의 mtROS 생성 및 미토콘드리아 단편화를 악화시키는 것으로 밝혀졌으며 이는 미토콘드리아 표적 항산화제인 미토퀴논에 의해 역전될 수 있습니다.
5. 결론
미토콘드리아 기능 장애는 DKD의 발달과 진행에 중심적인 역할을 합니다. 따라서 DKD의 미토콘드리아 기능 장애를 표적으로 삼는 것은 DKD 환자를 위한 새로운 치료 전략이 될 수 있습니다. 그러나 DKD 치료로서 전신 항산화제 투여의 유익한 효과를 조사한 연구에서 알 수 있듯이 미토콘드리아 기능 장애에 대한 개입은 세포 유형 및 상황에 따라 달라야 하는 것 같습니다. 또 다른 흥미로운 관점은 DKD의 미토콘드리아 기능 장애의 연령 및 성별 관련 차이입니다. 나이는 미토콘드리아 기능과 DKD의 발달 및 진행에 영향을 미치는 중요한 요소이지만 정확한 메커니즘에 대해서는 알려진 바가 많지 않습니다. 성별에 있어서는 특정 조직의 미토콘드리아에서 남성과 여성 사이에 많은 차이가 관찰되며, 에스트로겐과 테스토스테론이 신장 미토콘드리아 생체에너지를 중재할 수 있습니다.73]. DKD에서 미토콘드리아 기능 장애를 일으키는 정확한 메커니즘을 밝히고, 연구 결과가 환자에게 임상적으로 적용되어 예후를 바꿀 수 있는 정도까지 추가 조사가 필요합니다.
저자 기여:개념화, MI, MZG 및 AF; 작문 원본 초안 준비, MI; 집필-검토 및 편집, MI, SM, AF 모든 저자는 출판된 원고 버전을 읽고 동의했습니다.
자금:MI는 만페이 스즈키 당뇨병 재단의 지원을 받습니다. AF 및 SM은 국립 보건원 보조금 R01DK117599, R01DK104753 및 R01CA227493의 지원을 받습니다. AF는 U54DK083912, UM1DK100846, U01DK116101 및 UL1TR000460(Miami Clinical Translational Science Institute)에서도 지원됩니다.
기관 검토 위원회 성명서:해당 없음
.I고지된 동의서:해당되지 않습니다.
데이터 가용성 설명:해당되지 않습니다.







