프로바이오틱스의 면역 조절 잠재력: 가축 건강, 면역 및 생산성 향상을 위한 새로운 전략 2부
Jun 27, 2023
5. 가축 동물 모델로 세포주를 이용한 프로바이오틱스의 적용(In Vitro 연구)
생체 내 연구는 프로바이오틱스가 돼지, 소, 염소 및 양과 같은 주요 농장 동물 종의 성장 성능, 영양소 이용, 장내 미생물 및 장 건강을 개선하는 데 성공적으로 사용되었음을 나타냅니다(표 1 및 2). 프로바이오틱스를 포함하는 일부 기능성 사료는 패턴 인식 수용체 및 GIT에서 사이토카인 유도를 통해 면역적격 세포뿐만 아니라 상피 세포의 영감을 통해 장 면역을 개선하는 것으로 생각됩니다[86,87]. 그러나 사료 면역학 분야에서는 농장 동물을 위한 적절한 장 면역분석 시스템을 사용할 수 없기 때문에 소의 장 면역의 기본 메커니즘에 대한 많은 부분이 알려져 있지 않습니다.
상피 세포는 신체의 가장 바깥쪽 세포층으로, 신체의 표면과 통로를 덮고 외부 환경으로부터 격리합니다. 그들은 감염과 부상으로부터 우리를 보호하고 우리 면역 체계의 중요한 부분입니다.
상피세포는 점액, 점액 등의 물질을 분비하여 보호막을 형성하여 외부 병원체의 침입을 막는다. 또한, 상피세포는 병원균을 인식하고 식균작용을 할 수 있으며, 병원균을 직접적으로 제거하는 역할을 한다. 병원체가 이러한 보호 조치를 벗어나 감염을 일으키면 상피 세포는 면역 반응을 유발하는 일련의 사이토카인을 방출합니다. 이 사이토카인은 백혈구를 감염 부위로 유인하고 활성화하여 병원체를 제거하는 작업을 수행합니다.
또한 상피 세포는 인체의 면역 조절 과정에도 참여합니다. 그들은 특정 면역 세포의 활동을 강화하거나 억제하는 것을 포함하여 다양한 사이토카인을 방출하여 면역 세포의 기능을 조절할 수 있습니다. 따라서 상피 세포의 면역 기능은 우리의 신체 건강에 매우 중요합니다. 이러한 관점에서 우리는 면역력을 향상시켜야 합니다. Cistanche는 면역력을 향상시킬 수 있으며 육류의 다당류는 인간 면역 체계의 면역 반응을 조절하고 면역 세포의 스트레스 능력을 향상시키고 면역 세포의 살균 효과를 향상시킬 수 있습니다.

결과적으로 농장 동물 모델에 대한 기능성 식품의 프로바이오틱스 보충을 위한 프로바이오틱스/면역생물학적 평가 시스템 개발이 중요합니다. 이러한 상황에서 우리 그룹은 PIE 세포 단층에서 항염증 반응을 사용하여 프로바이오틱스/면역생물학 및 면역원성을 평가하기 위한 돼지 및 소 장 상피세포(PIE 및 BIE) 세포주를 개발했습니다. Peyer의 패치 배양 모델(그림 2)[12,54,88–90].

우리의 작업은 장 상피세포(PIE, BIE)가 병원체와 돼지/소 장 상피 세포(IEC) 사이의 관계 평가, 프로바이오틱/면역 미생물의 선택 및 IEC의 프로바이오틱 LAB에 의한 기본 면역 조절 메커니즘. 현재, 우리의 연구와 몇 가지 다른 체외 연구는 면역 건강 증진 요인의 효과와 함께 농장 동물에서 프로바이오틱스의 "건강 개선" 활동을 설명하는 데 중점을 두었습니다(표 3).
로타바이러스 감염 전에 L. acidophilus(LA)로 치료하면 PRV 복제와 PRV 감염에 대한 IL-6 반응이 증가하여 LA가 보조 효과가 있음을 나타냅니다. 로타바이러스 감염 후 LGG 요법은 IL-6 반응을 감소시켰고, 이는 IPEC-J2 세포주에서 LGG의 항염증 특성을 나타냅니다[50]. L. casei MEP221106은 TLR3- 매개 면역 반응을 통해 PIE 세포에서 항바이러스 면역 반응을 유의하게 조절하는 것으로 보고되었습니다[90].
Fujie et al. (2011)은 PIE 세포주에서 B. breve MCC-117가 ETEC(Enterotoxigenic E. coli)에 의해 생성된 염증 반응을 효과적으로 제어할 수 있음을 발견했습니다. 그들은 또한 MCC-117가 PIE를 변경하는 균주의 능력과 면역 세포의 상호작용과 관련되어 조절 T 세포의 자극과 ETEC 유발 장 염증을 예방하는 탁월한 면역 조절 활성을 가지고 있음을 발견했습니다[12 ].
한편, 또 다른 연구에서는 L. jensenii TL2937이 ETEC에 의한 전염증성 사이토카인 및 케모카인 발현을 유의하게 감소시켜 염증성 장질환을 예방하는 것으로 나타났다[54]. 그 후, Tomosada et al. (2013)은 B. longum BB536 및 B. breve M-16V 균주가 처리된 PIE 세포에서 인터루킨-8, 인터루킨-6 및 MCP-1의 발현을 감소시키는 것으로 나타났습니다. 열로 죽인 ETEC [10].
유사하게 Takanashi et al. (2013)은 L. casei OLL2768이 전염증성 사이토카인의 생성을 감소시켜 PIE 세포의 염증을 감소시킨다는 것을 보여주었습니다[52]. 또한, Abedi et al. (2013)은 L. delbrueckii가 Caco-2 세포를 사용하여 장에서 E. coli 감염을 억제하는 탁월한 능력을 보였다[51].
또한 L. jensenii TL2937은 TGFin EIC와 같은 면역조절 인자의 생성을 자극하고 IEC를 기능적으로 조절하여 감염 저항성을 개선하고 비보호성 염증을 최소화할 수 있는 것으로 보고되었습니다[11]. 우리의 연구는 B. thermophilum이 보충된 사료가 면역 세포를 자극하여 면역 조절을 발휘함을 시사하며, 이는 이 사료가 AM 사료 재료를 사용하지 않고 자돈의 건강을 향상시키는 데 기여할 가능성이 있음을 나타냅니다[55].
Kang et al. (2015)는 L. ruminis SPM0211, B. Longum SPM1205 및 B. longum 1206이 시험관 내 및 생체 내 로타바이러스 복제를 방지하는 데 능숙하다고 밝혔습니다. 또한 type I IFNs의 조절을 통해 면역 반응을 조절하기 때문에 프로바이오틱스의 항바이러스 효과를 기대할 수 있음이 제시되었다[57]. 또 다른 연구에서는 LAB가 병원성 박테리아 ETEC 및 바이러스(폴리(I:C))로 공격받은 후 PIE 세포의 염증 반응을 유익하게 조절하고 돼지 숙주에서 장 면역을 조절하는 능력을 보고했습니다[29].

또 다른 최근 연구에서는 L. delbruecki TUA4408L이 TLR-2을 통해 PIE에서 ETEC 유도 염증 반응을 약화시켰고 PIE 세포가 TUA4408L로 사전 자극되었을 때 ETEC 유도 염증 사이토카인이 하향 조절되었음을 보여주었습니다[91]. Kobayashi et al.의 최근 연구. (2017)은 B. infantis MCC12 또는 B. breve MCC1274가 BIE 세포에서 RV 역가를 낮추고 선천적 면역 반응을 차별적으로 제어할 수 있음을 입증했습니다.
또한, 박테리아 균주는 RV에 감염된 BIE 세포에서 IFN-와 같은 항바이러스 인자 생산을 강화하는 것으로 나타났다. 또한, 최근 우리는 PIE[15]에서 입증된 바와 같이 L. rhamnosus CRL1505 및 L. plantarum CRL1506이 바이러스성 장 감염에 대한 강화를 강화하는 능력을 가진 면역생물학적 균주라고 보고했습니다.
폴리(I:C)를 이용한 PIE 세포 자극은 IFN- 및 IFN, 케모카인, 부착 분자, 사이토카인 및 프로스타글란딘 생합성 유전자의 생성을 향상시켰다. CRL1505 및 CRL1506은 PIE 세포에서 선천적 항바이러스 면역 반응을 조절하고 생체 내 바이러스 감염 및 염증 손상으로부터 보호합니다[92].
Kanmani et al.의 또 다른 최근 연구. (2018)은 L. delbrueckii OLL1073R-1이 돼지 장 상피 세포에서 선천적 항바이러스 면역 반응을 조절한다는 것을 입증했습니다[59]. Iida 등의 최근 연구. (2019)는 paraimmunobiotic Bifidobacteria(B. longum BB536 및 B. breve M-16V)가 장 감염 저항을 강화하기 위한 대체물 또는 염증 감소를 위한 치료 장치로 사용될 수 있음을 입증했습니다[60].
Mizunoet al. (2020)은 L. plantarum CRL1506이 장내 선천적 항바이러스 면역 반응을 상당히 향상시켰음을 입증했습니다[61]. Sli ´ zewska et al. (2021)은 새로운 ˙ 락토바실러스 균주가 병원성 박테리아의 집락화를 줄임으로써 장 감염을 예방하는 데 도움이 될 수 있음을 입증했습니다[62]. 그 결과 프로바이오틱 락토바실러스 균주를 사용하면 동물 유래 육류 및 식품의 안전성과 품질을 향상시킬 수 있습니다. 따라서, 이전 연구는 면역바이오틱스/프로바이오틱스의 사용이 다양한 건강 장애를 예방하고 개선하기 위한 면역조절에 대한 좋은 잠재력을 가지고 있음을 시사합니다.
In Vitro 및 In Vivo 연구 모델에서 프로바이오틱스 사용에 대한 제한 사항
체외 연구는 고려해야 할 다양한 한계가 있는 것으로 나타났습니다. 예를 들어, 다른 IEC로 얻은 결과는 모든 세포주가 동일한 특성을 갖는 것은 아니기 때문에 주의해서 취해야 합니다. 문화적 상황이 일부 분자 특성이 표현되는 방식에 영향을 미칠 수 있다는 점도 주목할 가치가 있습니다. 생체 내 프로바이오틱스 작용에 대한 분자적 설명은 진정한 프로바이오틱스를 식별하고 질병 예방 및/또는 치료에 가장 적합한 것을 선택하는 데 도움이 될 것입니다. 그럼에도 불구하고 동물 영양에 사용되는 프로바이오틱스가 인간 먹이 사슬에 들어가는지 여부와 인간 건강에 미치는 영향을 결정하기 위해서는 추가 연구가 필요합니다. 2 동물의 자궁은 무균 상태이지만 출생 후 어린 동물은 갑자기 박테리아와 바이러스에 노출됩니다.
병원성 세균과 바이러스 감염을 예방하기 위해 어린 가축은 초유에서 면역글로불린과 사이토카인뿐만 아니라 어미의 질과 젖에서 토착 세균을 획득하여 면역원성 잠재력을 발달시킵니다. 그 중에서 AM제제 없이 동물을 기르는데 유용한 면역생물학적 물질이 발견된다면 사람은 물론 동물에게도 안전할 것이다. 따라서 면역생물학적 형태의 유산균을 찾아 AM 대체물질로의 활용 가능성을 모색하고, 유산균의 전이경로를 대표할 산모에서 태아로의 전이경로를 확립하기 위한 면역생물학적 라이브러리 구축을 시도하기 위해서는 더 많은 연구가 필요할 것이다. 엄마에게서 아이에게 토착 박테리아.
또한 프로바이오틱 LAB 균주의 작용 메커니즘을 밝히기 위해 3 더 많은 연구가 필요합니다. 3D 모델에서와 같이); 4 in vitro 및 in vivo 모델을 이용하여 각종 감염성 질환의 예방 또는 치료에 있어 대체약물로 사용될 수 있는 프로바이오틱스를 탐색한다. 5 면역바이오틱스를 이용한 건강한 성장 시스템 개발을 위해 유전체 편집, AI/IoT 시스템 등 신기술을 발굴한다.
6. 가축 생산에 프로바이오틱스의 적용
최근 수십 년 동안 프로바이오틱스 분야의 새로운 범위를 설명하고 잠재적인 프로바이오틱 미생물을 발견하기 위한 일부 연구가 수행되었습니다. Sun et al.,(2021)에 따르면 L. acidophilus, L. casei, B. thermophilum 및 E. faecium으로 구성된 다종 프로바이오틱스가 장독소 생성 E. coli(ETEC) F18 플러스로 인한 설사를 줄이는 데 성공적으로 사용되었습니다. 갓 젖을 뗀 돼지[93]. 또한 다종 프로바이오틱스는 장 염증, 산화 스트레스 및 형태학적 손상 감소를 통해 성장 성능을 향상시키는 데 도움을 주었습니다. Sobrinoet al. (2021)은 돼지 생산에서 AM 대체물을 연구하려고 시도했습니다. 그들은 암퇘지의 우유에서 추출한 Ligilactobacillus salivarius 균주를 사용하여 임신한 암퇘지와 새끼 돼지에게 먹였습니다.
결과는 치료군에서 명백해진 항생제 내성 락토바실러스의 존재가 현저하게 감소했음을 시사했습니다[94]. 최근 연구에서 Prevotella는 성장 성능과 면역 반응을 향상시켜 돼지 생산에 긍정적인 결과를 가져온다고 제안되었습니다[95-98]. Lactobacillus, Escherichia, Shigella 및 Bacteroides는 소장 미생물군을 지배하는 반면, Prevotella는 신생아 단계에서 대장 미생물군을 지배합니다.
또한 Prevotella는 이유 후 돼지의 소장과 대장을 지배합니다[99]. 또한, 설사를 하지 않는 새끼 돼지는 설사를 하는 새끼 돼지보다 장내 Prevotella가 상당히 더 많은 것으로 보고되었습니다. Prevotellacea UCG-003는 co-correlation network analysis[98]에 따르면 자돈의 비설사성 미생물군에서 핵심 박테리아였습니다. Ngo et al. (2021)은 휘발성 지방산 생성을 줄이고 펠렛 사료의 풍미를 방지하는 고농축 사료 펠렛에 새로운 프로바이오틱스(B. amyloliquefaciens H57)를 사용했습니다. 이는 반추 동물의 더 높은 사료 섭취를 촉진합니다[28]. 혐기성 진균에 대한 최근 연구에서 두 가지 방법, 즉 효소적 및 기계적으로 식물 세포벽을 분해함으로써 반추위 섬유 이용에 본질적으로 기여한다는 것이 입증되었습니다[100,101]. 놀랍게도, 진행 중인 탐사는 완고한 섬유질에 대한 곰팡이 CAZymes의 친화력을 보여주었고, 이는 낮은 품질의 마초를 반추 동물에게 먹였을 때 혐기성 곰팡이의 특정 용도를 명확히 할 수 있습니다.
따라서 이것은 반추 동물 영양에서 잠재적인 프로바이오틱스로도 사용될 수 있습니다[102]. 가축 영양에서 포자 형성 프로바이오틱 박테리아로 B. subtilis를 활용하는 연구는 안전하지 않은 영향을 나타내지 않았으며 주로 AM, 세포 강화 완화 및 효소 전시로 인해 프로바이오틱으로 활용 가능성을 보여주었습니다. 면역 조절 작용 [103]. Cai 등의 연구. (2021)은 S. cerevisiae와 C. butyricum 및 이들의 혼합물이 pH를 확장하고 산화를 줄임으로써 반추위 상태를 개선했으며 보충제의 흡수성을 확장하고 VFA 생산을 더욱 발전시켜 반추위 성숙 능력을 업그레이드했다고 열거했습니다. 그 시점부터 열 스트레스를 받은 염소의 생산 성장이 더욱 향상되는 것이 관찰되었습니다[104].
Debaryomyces hansenii는 또한 육상 동물과 수생 동물 모두를 위한 새로운 잠재적 프로바이오틱스로서 매력을 얻고 있습니다. D. Hansenii의 경구 전달은 면역 자극 효과, 장내 미생물 조절, 세포 증식 증가, 분화 및 소화 기능 개선과 같은 프로바이오틱 기능과 관련이 있습니다. 세포벽 구성 요소와 폴리아민을 포함하여 생체 활성 분자가 확인되고 면역 조절 효과와 연결됩니다[105]. 따라서 가축 생산에서 진화적 역할을 할 수 있는 많은 잠재적 프로바이오틱 미생물이 여전히 발견되어야 합니다.

7. 가축 프로바이오틱스의 작용기전
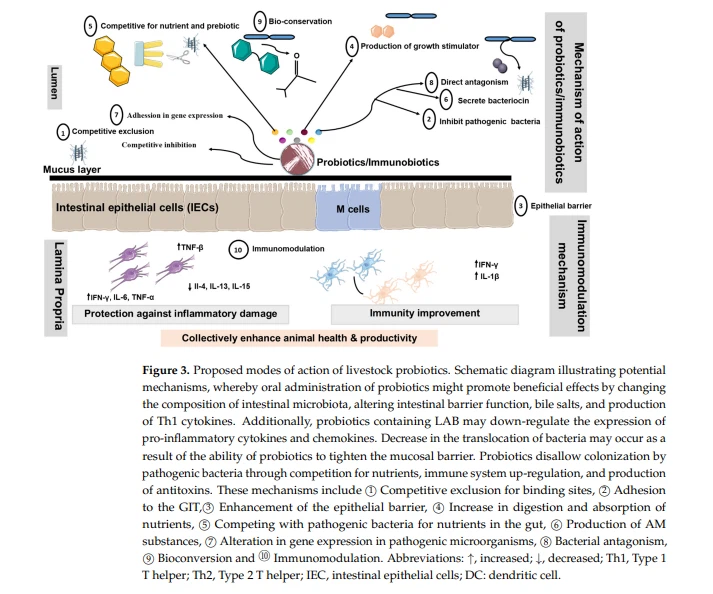
가축 프로바이오틱스에 대해 제안된 수많은 작용 방식이 있습니다[106-114]. 그러나 프로바이오틱스에 대해 제안된 주요 작용 메커니즘은 다음 세그먼트에서 고려됩니다(그림 3에 요약됨).
1 GIT의 미생물 개체 수 수정: Probiotics는 Lactobacillus 및 Bifidobacterium과 같은 유익한 미생물의 개체 수를 증가시킬 수 있으며, 이는 이후에 억제 화학 물질을 생성하고 결합 부위를 놓고 경쟁함으로써 해로운 박테리아의 성장을 제한합니다[115,116]. 2 병원성 미생물에 의한 집락 형성을 방지하기 위해 GIT 벽에 부착: 대부분의 장내 병원균은 장 상피에 집락을 형성하여 결과적으로 질병을 일으킬 수 있습니다[117]. 결과적으로 Lactobacillus는 장 상피에 부착할 수 있고 당접합체와 같은 부착 수용체에 대해 병원균과 경쟁할 수 있습니다[118].
Lactobacillus와 Bifidobacterium은 동물 세포 표면에 부착하여 비특이적으로 박테리아를 돕는 소수성 표면층 단백질을 가지고 있습니다[119]. 3 상피 장벽 강화: 모델 동물을 대상으로 한 실험 연구에서 프로바이오틱스 P. acidilactici가 이유 후 새끼 돼지에서 장독소 생성 대장균의 장간막 림프절로의 장 상피 전위의 투과성을 감소시켜 장 장벽 기능을 개선하는 것으로 나타났습니다. ETEC 챌린지 후 대조군[120]. 우리의 현재 연구 결과는 L. jensenii TL2937이 DSS에 노출된 PIE 세포에서 세포 내 Ca2 플러스 플럭스를 감소시켜 밀착 연접의 견고성을 증가시킨다는 것을 시사합니다[121].
4 영양소의 소화 및 흡수 증가: 이 경우 포자를 형성하는 박테리아는 영양소 소화를 촉진하는 세포외 효소의 생산을 강화합니다[122,123]. 5 장내 영양소에 대한 병원성 박테리아와의 경쟁: 프로바이오틱 박테리아는 에너지원을 빠르게 활용하여 잠재적으로 박테리아 발달의 로그 단계를 단축함으로써 영양분 및 흡수 부위에 대해 병원성 박테리아와 경쟁할 수 있습니다[116]. 6 항균 물질의 생산: 여러 프로바이오틱 박테리아, 특히 젖산과 아세트산을 생산하는 박테리아는 해로운 미생물을 억제할 수 있습니다[124,125]. 7
병원성 미생물의 유전자 발현 변화: 프로바이오틱스는 병원성 박테리아의 정족수 감지에 영향을 미쳐 병원성을 변화시킬 수 있습니다. L. acidophilus La-5의 발효 산물은 인간 장출혈성 대장균 혈청형 O157:H7에 의한 화학적 신호(자가유도인자-2)의 세포외 생산을 상당히 억제하여 독성 유전자(LEE- 장세포 소실의 위치) 시험관내 발현[126]. 8 세균 길항 작용: 프로바이오틱 미생물은 일단 장에 정착하면 살균 또는 정균 특성을 나타낼 수 있는 유기산, 과산화수소, 락토페린 및 박테리오신을 생성할 수 있습니다[127].
9 살균 활성/생물전환: Lactobacillus는 유당을 젖산으로 전환합니다. 낮음. 병원성 박테리아가 생존할 수 없는 지점까지 pH를 가져옵니다. 또한 살아있는 효모는 전분 분해에서 얻은 당을 소화하기 위해 젖산 생성 박테리아와 경쟁하여 반추위 pH를 안정화하고 산증의 위험을 최소화합니다(128-130D Immunomodulation: 우리의 연구는 면역 조절 기능을 가진 프로바이오틱 LAB가 PIE 세포의 기능을 조절하여 장내 면역 반응을 조절합니다[12,54,56].
또한 프로바이오틱 LAB는 대식세포 활동(54l, 국소 항체 수준 증가, 항염증 사이토카인(인터루킨(IL)10, 인터페론(IFN)-y, B, IL-1P, TGF-B), IL-4, IL-6, IL-8, MCP- 감소 및 킬러 세포 활성화[11,32,54 ].
면역 조절 특성은 균주에 따라 달라지는 것으로 보이며, 이는 유사하지 않은 프로바이오틱스가 병렬 작용 메커니즘을 가질 수 있는 반면 단일 균주는 여러 작용 메커니즘을 가질 수 있음을 의미합니다. 예를 들어, 특정 프로바이오틱스의 작용 메커니즘은 대부분 알려져 있지 않지만 상당히 많은 프로바이오틱 균주가 위장관의 미생물 군집에 비슷한 영향을 미칩니다. 프로바이오틱스의 정확한 작용 방식은 성능에 미치는 영향에 대한 대부분의 연구에서 잘 이해되지 않습니다. 따라서 밀접하게 관련된 프로바이오틱스가 다양한 작용 방식을 가지고 있는 것으로 나타나기 때문에 사례별로 메커니즘을 탐색해야 합니다. 프로바이오틱 효과는 숙주와 프로바이오틱 미생물 간의 상호작용의 결과입니다. 결과적으로 숙주-미생물 상호 작용에 대한 더 많은 연구가 프로바이오틱스의 작용 방식을 밝힐 수 있습니다. 미생물 생태학 연구를 위한 분자 기술 및 게놈 시퀀싱의 급속한 개선은 프로바이오틱스 작용 메커니즘에 대한 이해를 실질적으로 도울 것입니다.
8. 결론
본 리뷰에서는 영양, 건강, 생산성 및 프로바이오틱스의 작용 메커니즘 측면에서 NGP를 포함한 프로바이오틱스가 가축에 미치는 영향에 대한 개요를 제공했습니다. IEC의 프로바이오틱 LAB에 의한 면역 조절 메커니즘 연구를 위한 가축 동물 모델의 체외 시스템에 대한 추가 지식도 설명되어 있습니다. 여러 가축 프로바이오틱스가 동물의 체중 증가, 사료 전환율, 영양소의 소화율, IgG, 면역 상태, 장내 미생물 및 장 건강(대장균 수 감소에 따른 유산균 증가), 장 형태, 우유 생산량 및 품질, 육류 개선에 효과적인 것으로 밝혀졌습니다. 돼지 및 반추 동물 축산업에서 생산 및 도체 품질, 병원체 집락화, 스트레스 및 설사의 위험 감소.
프로바이오틱스는 성장 촉진제 및 다양한 전염병의 예방 또는 치료에서 약물 대체제로 사용될 수 있습니다. 마지막으로, 이 리뷰에서 우리는 또한 면역바이오틱스 LAB가 가축의 장 상피 및 면역 세포의 면역 반응을 조절할 수 있음을 제안하며, 건강한 가축 증진에 기여하기 위해 게놈 편집 및 AI/IoT 시스템과 같은 새로운 기술을 통해 많은 잠재적인 프로바이오틱스를 발견할 수 있음을 제안합니다. 궁극적으로 약물에 의존하지 않는 건강하고 생산적인 가축과 식용 동물을 위한 식품 안전 시스템으로 이어질 AM 사료 재료를 사용하지 않습니다.
저자 기여:
AKMHK와 HK가 원고를 작성하고 수정했습니다. 쓰기 - 원본 초안 준비, MSRR 및 HMM; 쓰기 - 검토 및 편집, 감독, JV, AKMHK 및 HK; 프로젝트 관리, 홍콩; 자금 조달, HK 모든 저자는 원고의 게시된 버전을 읽고 이에 동의했습니다.
자금 조달:
이 연구는 일본 과학 진흥회(JSPS)의 과학 연구 보조금(A)(19H00965)과 NARO Biooriented Technology Research Advancement Institution(Research Program on the 혁신 기술 개발, No. 01002A), 일본 경마 협회(JRA) 축산 진흥 프로젝트에 의해 Kitazawa Haruki에게. 이 연구는 또한 Julio Villena에 대한 ANPCyT–FONCyT 보조금 PICT-2016-0410와 JSPS Core-to-Core Program A(Advanced Research Networks)의 "Establishment of International Agriculture Immunology Research-Core for a Quantum Improvement 식품안전에서"
기관 검토 위원회 성명서:
적용되지 않습니다.

정보에 입각한 동의서:
적용되지 않습니다.
데이터 가용성 진술:
적용되지 않습니다.
이해 상충:
모든 저자는 이해 상충이 없습니다.
참조
1. 코마렉, AM; 던스턴, S.; Enahoro, D.; Godfray, HCJ; 헤레로, M.; Mason-D'Croz, D.; 리치, KM; Scarborough, P.; 스프링만, M.; 설서, 결핵; 외. 소득, 소비자 기호 및 가축 유래 식품 수요의 미래. 글로브. 환경. 2021, 70, 102343을 변경합니다. [CrossRef] [PubMed]
2. 하산, MM; 엘 Zowalaty, ME; Lundkvist, Å.; Järhult, JD; 칸 나옘, MR; 탄진, 애리조나; 바드샤, MR; 칸, SA; Ashour, HM 동물 유래 식품의 잔류 항균제. 트렌드 푸드 사이언스 기술. 2021, 111, 141–150. [CrossRef] [펍메드]
3. Schrijver, R.; Stijntjes, M.; Rodríguez-Baño, J.; Tacconelli, E.; 바부 라젠드란, N.; Voss, A. 인간에 초점을 맞춘 EU의 가축 및 육류에 대한 항균제 내성 감시 프로그램 검토. 클린. 미생물. 감염. 2018, 24, 577–590. [CrossRef] [펍메드]
4. Tiseo, K.; 후버, L.; 길버트, M.; 로빈슨, TP; Van Boeckel, TP 2017년부터 2030년까지 식용 동물의 항균 사용에 대한 글로벌 동향. 항생제 2020, 9, 918. [CrossRef] [PubMed]
5. Cuevas-González, PF; Peredo-Lovillo, A.; Castro-López, C.; 바예호-코르도바, B.; González-Córdova, AF; 가르시아, HS; Hernández-Mendoza, A. 적혈구 식이 제노바이오틱스에 대한 잠재적 보호 도구로서의 식품 등급 유산균 및 프로바이오틱스. 트렌드 푸드 사이언스 기술. 2021, 116, 1041–1055. [교차 참조]
6. Barba-Vidal, E.; Martín-Orúe, SM; Castillejos, L. 돼지 생산에서 프로바이오틱스 사용의 실용적인 측면: 리뷰. 라이브스트. 과학. 2019, 223, 84–96. [교차 참조]
7. 깁슨, MK; 크로프트, TS; Dantas, G. Antibiotics 및 발달중인 영아 장내 미생물 및 저항체. 현재 의견. 미생물. 2015, 27, 51–56. [교차 참조]
8. Tavoukjian, V. 소화관 내 항생제 내성 박테리아의 탈집락화를 위한 분변 미생물 이식: 체계적인 검토 및 메타 분석. J. 호스프. 감염. 2019, 102, 174–188. [교차 참조]
9. 안드레몬트, A.; Cervesi, J.; Bandinelli, P.-A.; 비트리, F.; de Gunzburg, J. 항생제로 유발된 세균불균형으로부터 장내 미생물총을 보존하고 복구합니다: 최신 기술. 마약 발견. 오늘 2021, 26, 2159–2163. [교차 참조]
10. Tomosada, Y.; Villena, J.; 무라타, K.; 치바, E.; 시마즈, T.; Aso, H.; 이와부치, N.; 샤오, JZ; 사이토, T.; Kitazawa, H. 유비퀴틴 편집 효소 A20 발현의 조절을 통한 돼지 장 상피 세포에서 비피도박테리아 균주의 면역 조절 효과. PLoS ONE 2013, 8, e59259. [교차 참조]
11. Suda, Y.; Villena, J.; Takahashi, Y.; Hosoya, S.; Tomosada, Y.; Tsukida, K.; 시마즈, T.; Aso, H.; Tohno, M.; 이시다, M.; 외. 젖을 뗀 돼지의 성장 성능과 생산성을 향상시키기 위한 면역 건강 증진 인자로서의 면역생물학적 락토바실러스 젠세니. BMC 면역. 2014, 15, 24. [CrossRef] [PubMed]
12. Fujie, H.; Villena, J.; Tohno, M.; 모리에, K.; 시마즈, T.; Aso, H.; Suda, Y.; Shimosato, T.; 이와부치, N.; 샤오, JZ; 외. Toll-like receptor-2-activating bifidobacteria strains은 돼지 장 상피 세포 배양 시스템에서 염증성 사이토카인을 차등적으로 조절합니다. 새로운 항염증성 면역생물학을 찾아서. FEMS 면역. 중간 미생물. 2011, 63, 129–139. [CrossRef] [펍메드]
13. Villena, J.; 살바, S.; Núñez, M.; 코르조, J.; 톨라바, R.; 파에다, J.; 글꼴, G.; Alvarez, S. 모두를 위한 프로바이오틱스! 새로운 Immunobiotic Lactobacillus rhamnosus CRL1505와 아르헨티나의 사회적 Probiotic 프로그램의 시작. 국제 J.Biotechnol. Wellness Ind. 2012, 189–198. [교차 참조]
14. 쿠마개, N.; Villena, J.; Tomosada, Y.; 고바야시, H.; Kanmani, P.; Aso, H.; 사사키, T.; 요시다, M.; 다나베, H.; 시바타, I.; 외. 돼지 장내 면역 및 상피 세포에서 사료 미생물 물질의 면역 조절 능력 평가. J. Vet을 엽니다. 중간 2014, 4, 14. [교차 참조]
15. 고바야시, H.; Kanmani, P.; 이시즈카, T.; 미야자키, A.; 소마, J.; 알바라신, L.; Suda, Y.; 노치, T.; Aso, H.; 이와부치, N.; 외. 소 장 상피세포의 로타바이러스 감염에 대한 체외 면역생물학적 평가 시스템 개발. 혜택 미생물 2017, 8, 309–321. [교차 참조]
16. Dowarah, R.; 버마, AK; Agarwal, N.; 파텔, BHM; Singh, P. 재배자-비육 교배 돼지의 성능, 설사 점수, 장내 미생물 및 장 건강에 대한 돼지 기반 생균제의 효과. 라이브스트. 과학. 2017, 195, 74–79. [교차 참조]
17. Kwak, M.-J.; 탄, PL; 오, JK; 채석원; 김제이; 김성서; Eun, J.-S.; 치, SW; 강동건; 김성서; 외. 성장기-비육돈의 성장 성능, 간 대사, 장 완전성 및 분변 미생물총에 대한 다종 프로바이오틱 제제의 효과. 애님. 피드 과학. 기술. 2021, 274, 114833. [교차 참조]
18. 멩, QW; Yan, L.; 아오, X.; 저우, 텍사스; 왕, JP; 이정호; Kim, IH 성장기 비육돈의 성장 성능, 영양소 소화율, 육질 및 혈액 특성에 대한 다양한 에너지 및 영양 밀도 사료에서 프로바이오틱스의 영향. J.애님. 과학. 2010, 88, 3320–3326. [교차 참조]
19. Veizaj-Delia, E.; 피우, T.; Lekaj, P.; Tafaj, M. 혼합 프로바이오틱스를 사용하여 광범위한 농장 조건에서 젖을 뗀 새끼 돼지의 성장 성능을 개선합니다. 라이브스트. 과학. 2010, 134, 249–251. [교차 참조]
20. Giang, H.; Viet, T.; 오글, B.; Lindberg, J. 생육기 돼지의 성능, 영양소 소화율 및 분변 미생물에 대한 프로바이오틱스 보충의 효과. 아시아-오스트랄라스. J.애님. 과학. 2011, 24, 655–661. [교차 참조]
21. 수오, C.; Yin, Y.; 왕, X.; 루, X.; 송디; 왕, X.; Gu, Q. lactobacillus plantarum ZJ316이 돼지의 성장과 돼지질에 미치는 영향. BMC 수의사. 해상도 2012, 8, 89. [CrossRef] [PubMed]
22. 허펠, TM; Jacobi, SK; 린, X.; 조니, ZE; Chichlowski, M.; 스탈, CH; Odle, J. Bifidobacterium longum 균주 AH1206의 식이 보충은 맹장 풍부를 증가시키고 신생 새끼 돼지에서 장내 인터루킨-10 발현을 증가시킵니다. 식품화학 독성. 국제 J. Publ. 브. 산업바이오. 해상도 협회 2013, 60, 116–122. [CrossRef] [펍메드]
23. 리우, H.; 장제이; 장, S.; 양에프; 새커, 펜실베니아; 장지.; Qiao, S.; Ma, X. Lactobacillus fermentum I5007의 경구 투여는 장 발달을 촉진하고 분유를 먹인 새끼 돼지의 장내 미생물군을 변화시킵니다. J. Agric. 식품화학 2014, 62, 860–866. [CrossRef] [펍메드]
24. 소니아, T.; 지효; 홍석, M.; Chul-Ju, Y. 장내세균에 감염된 젖을 뗀 새끼돼지에서 유산균 및 바실러스 기반 프로바이오틱스의 항생제 대체제 평가. 아프리카 J. Microbiol. 해상도 2014, 8, 96–104. [교차 참조]
25. 칸타스, D.; Papatsiros, VG; 타시스, PD; Giavasis, I.; Bouki, P.; Tzika, ED Bacillus toyonensis(Toyocerin®)를 함유한 사료 첨가제는 이유 후 자돈의 장내 병원균을 예방합니다. J. Appl. 미생물. 2015, 118, 727–738. [CrossRef] [펍메드]
For more information:1950477648nn@gmail.com
