선천적 및 적응 면역 기억: 병원체에 대한 숙주 반응의 진화적 연속체(1부)
Jun 08, 2022
자세한 내용을 알아보려면 plz에 문의하십시오.david.wan@wecistanche.com
면역 기억기억은 재감염 시 숙주의 생존을 향상시키는 중요한 진화적 특성이며, 기억은 면역계의 선천적 및 적응적 팔 모두에서 인식되는 특성입니다. 선천성 면역 기억과 후천성 면역 기억이 유도되는 메커니즘과 특성은 다르지만 병원체에 대한 숙주 방어를 향상시키기 위해 결탁합니다. 여기에서 우리는 타고난 면역 기억 또는 "훈련된 면역"이 염색질 구조 재배열로 인한 숙주 방어 적응의 원시적 형태이며, 이는 재감염에 대한 증가하지만 비특이적 반응을 제공한다고 제안합니다. 대조적으로, 적응 면역 기억은 후성적 변화를 통해 매개되는 반응의 크기가 증가하고유전자 재조합. 면역 기억의 통합 모델은 숙주 방어에 대한 광범위한 이해와 감염 및 면역 매개 질환이 있는 환자의 이익을 위해 이를 조절하는 가장 효과적인 접근 방식을 식별하는 데 중요합니다.

Cistanche에 대해 자세히 알아보려면 여기를 클릭하세요.
선천성 및 적응성 면역
일반적으로 숙주면역은 선천면역과 후천면역으로 나뉜다. 전자는 병원체에 신속하고 비특이적으로 반응하는 반면, 후자는 오래 지속되는 면역학적 기억의 생성과 함께 느리지만 특정한 방식으로 반응합니다(Farber et al., 2016). 이 이분법은 지난 반세기 동안면역학적 연구, 그리고 수많은 연구에서 숙주 방어의 이 두 가지 주요 구성 요소 각각의 세포 및 분자 기질을 정의했습니다. 선천 면역은 골수 세포, 자연 살해(NK) 세포 및 선천 림프 세포(그러나 특정 상황에서는 비면역 세포도 포함)와 같은 선천 면역 세포 집단과 방어소 및 보체와 같은 고대 체액 시스템에 의해 매개됩니다. . 적응 면역은 턱뼈가 있는 척추동물(Danilova, 2012)의 면역글로불린 계열과 세포와 류신이 풍부한 반복(LRR) 세그먼트로 구성된 가변 림프구 수용체(VLR)를 기반으로 하는 비교적 새로운 진화적 특성입니다. 턱이 없는 척추동물에서(Boehm et al., 2012).
감염 중에 선천성 면역이 가장 먼저 촉발되며(염증 반응) 완전히 활성화되는 데 몇 분에서 몇 시간이 걸리지 않습니다(Netea et al., 2017). 이것은 새로운 감염의 첫 번째 단계에서 숙주 방어에 중요합니다. 선천성 면역은 일반적으로 병원체를 효율적으로 제거할 수 있지만, 감염의 수 또는 독성이 높기 때문에 초기 감염 제거가 실패할 수 있습니다.침입하는 병원체. 이러한 상황에서 림프구와 적응 면역 메커니즘이 활성화되어 병원체를 특이적으로 인식하고 제거할 수 있습니다. 적응 면역의 확립은 1-2주가 필요하며 재자극에 대해 보다 효과적으로 "기억"하고 반응하는 능력으로 인해 감염 후기 및 2차 감염 동안 숙주 방어에 중요합니다(Farber et al., 2016). .
선천성 면역 과정과 적응 면역 과정은 처음에는 상대적으로 시간이 지남에 따라 구분된 반응으로 여겨졌지만 지난 20년 동안의 연구는 그들 사이의 강력한 연결과 효율적인 네트워크를 분명히 보여주었습니다. 림프구에서 적응 면역 반응의 활성화와 고전적 면역 기억의 유도는 선천 면역계, 특히 수지상 세포와 같은 항원 제시 세포에 의존합니다. 림프구 활성화의 다운스트림 효과는 식균 작용과 같은 타고난 면역 반응을 증폭하고 특정 타고난 면역 세포에 의한 병원체의 사멸에 의해 발휘됩니다. 선천 면역과 후천 면역을 구별하는 두 가지 속성은 한편으로는 특이성과 다른 한편으로는 오래 지속되는 면역학적 기억을 구축하는 능력입니다. 선천적 면역 반응은 전통적으로 비특이적이고 적응 능력이 없는 것으로 생각되는 반면, 적응 면역 반응은 면역글로불린 유전자 패밀리의 유전자 재조합 과정을 사용하여 매우 정밀하게 다른 병원체를 인식하고 후속적으로 면역학적 기억을 구축합니다(Danilova, 2012)(그림 1). 선천 면역이 비특이적이라는 개념은 패턴 인식 수용체(PRR)의 발견으로 인해 도전을 받았습니다. 선천 면역계 내의 다양한 세포에서 발현되는 이러한 수용체는 면역 체계의 특정 구성 요소를 인식합니다.미생물, 그리고 면역 세포에 의해 발현되는 PRR의 조합은 마주치는 미생물의 유형에 대한 부분적으로 특이적 인식으로 이어질 수 있습니다. 예를 들어, 선천성 면역 세포는 그람-음성 박테리아와 그람-양성 박테리아의 차이를 인식하지만 두 박테리아 사이의 차이는 인식하지 못합니다. 관련 종 또는 계통(Medzhitov and Janeway, 2000). 이 검토에서는 PRR을 통해 병원체 인식을 이해하는 과정에 대해 논의하지 않을 것입니다. 이는 문헌에서 많은 우수한 최근 개요의 주제이기 때문입니다(예: O'Neill et al., 2013).

그림 1. 선천적 면역 반응 대 적응 면역 반응
감염 초기 몇 시간 및 며칠 동안 병원체의 침입은 대식세포, 단핵구 또는 NK 세포와 같은 선천 면역 세포 또는 보체와 같은 체액 인자의 활성화를 유도합니다. 이러한 경로는 염증 반응을 강력하게 활성화하고 병원체를 제거합니다(선천성 면역). 감염이 제거되지 않은 소수의 경우 항원 제시 세포가 병원체를 섭취하고 처리한 후 항원 제시 및 특정 활성 자극을 유발합니다.T 및 B 림프구. 결과적으로 이는 클론 확장 및 효과기 기전(예: 사이토카인 및 면역글로불린의 방출)(적응 면역)의 활성화로 이어집니다.
여기에서 우리는 선천성 및 적응성 숙주 방어 메커니즘을 구별하는 두 번째 속성인 면역 기억의 유도에 초점을 맞출 것입니다. 초기 문헌과 대조적으로, 선천적 면역 반응이 적응 특성을 나타낸다는 증거가 증가하고 있습니다(Bowdish et al., 2007; Netea et al., 2011). 적응 면역이 없는 식물과 무척추 동물에서 재감염에 대한 지속적인 보호가 보고되었습니다(Kurtz, 2005). 포유동물에 대한 연구에서는 다양한 병원체에 의한 감염에 대한 교차 보호가 있음을 입증했으며(Quintin et al., 2014), 기능적 적응 면역 세포가 없는 마우스에 대한 실험 연구에서는 특정 백신 접종 모델에서 부분적으로 보호하는 것으로 나타났습니다(Bistoni et al., 1986; Wout et al, 1992). 따라서 선천성 면역은 미생물 또는 미생물 제품과의 이전 만남에 의해 조절될 수 있으며 이 특성을 "훈련된 면역"이라고 하며 사실상의 선천성 면역 기억을 나타냅니다.
그러나 두 가지 유형의 면역 기억을 매개하는 뚜렷한 분자 메커니즘이 있습니다. 분자적, 면역학적, 진화론적 논증을 바탕으로 우리는 선천적 면역 기억이 모든 살아있는 유기체에 존재하는 면역 기억의 원시적 형태인 반면, 적응 면역 기억은 척추동물의 진화적 혁신을 나타내는 진보된 형태의 면역 기억이라고 제안합니다. 두 가지 유형의 면역 기억의 상보적 특성과 아래에 설명된 생물학적 논증의 범위에 기초하여 우리는 이 관점에서 선천 면역 기억과 적응 면역 기억의 발달이 진화적 연속체를 나타낸다고 주장합니다. 우리는 또한 이 두 가지 형태가 잠재적으로 병원성 물질로 가득 찬 환경에 대한 효과적인 적응 메커니즘의 개발을 향한 두 가지 진화적 단계라고 제안합니다.미생물.
적응 진화 특성으로서의 면역학적 기억
면역학적 기억이 적응 면역계에 국한된다는 교리는 진화론적 관점에서 볼 때 개념적 어려움에 직면해 있습니다. 면역 기억이 진화론적 관점에서 유리하다는 것은 천연두와 같은 치명적인 고대 질병에 의해 잘 설명됩니다. 역사적으로 최초 감염의 사망률은 20% -60 퍼센트였지만 개인은 그 이후 질병에 완전히 면역되었습니다(Riedel, 2005 ). 따라서 면역 기억은 살아있는 종의 약 1% -2%를 차지하는 척추동물에서만 진화했다고 상상하기 어렵습니다(Gourbal et al., 2018). 대조적으로 시력과 같은 다른 중요한 유리한 특성은 다양한 그룹의 동물이 진화하는 동안 여러 번 독립적으로 진화했습니다(소위 "수렴 진화")(Gehring, 2004). 재미있게,면역 기억척추동물 혈통 내에서 한 번이 아니라 두 번 진화했습니다. 첫째, 턱 없는 물고기(칠성장어와 같은)에서 VLR 기반 기억의 발달, 둘째, LG 기반 기억(B 및 T 림프구 기억 발달의 기초이기도 함)의 발달 다른 모든 턱뼈가 있는 척추동물. 척추동물에서 면역 기억으로 이어지는 두 가지 별개의 사건이 있을 것이라는 사실(Cooper and Alder, 2006)은 다른 모든 후생동물에는 전혀 존재하지 않습니다.
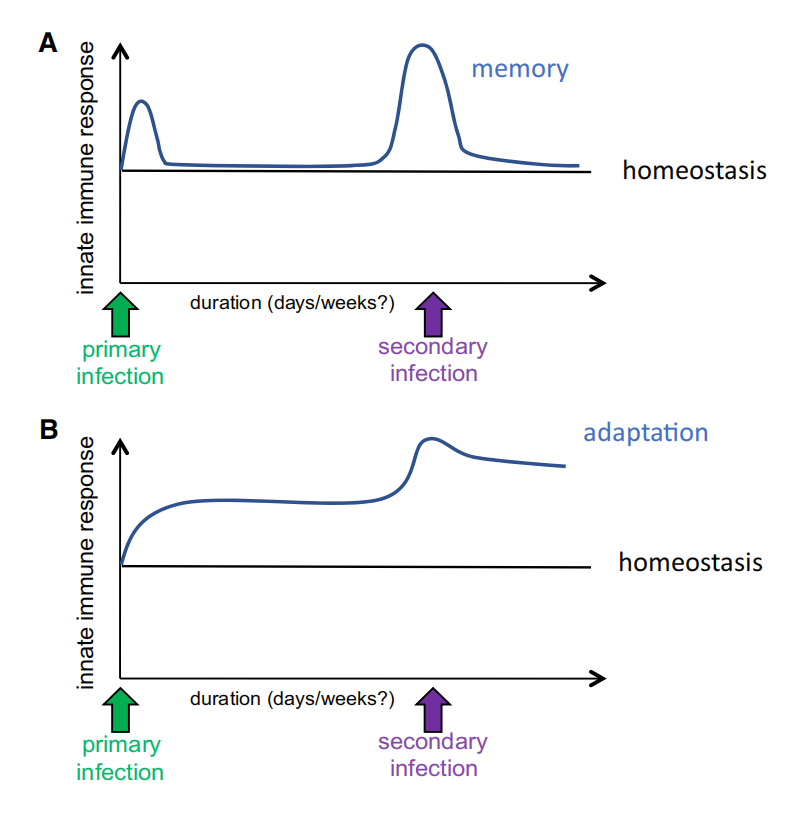
그림 2. 면역 기억 대 면역 적응
면역 기억은 급성 감염(또는 백신 접종) 후 숙주의 면역 체계의 변화된 상태로 정의되며, 이는 재감염에 대한 보다 효과적인 반응으로 이어집니다. 중요한 것은 면역 기억이 유도되는 동안 첫 번째 감염과 재감염 사이에 면역 상태가 기능적으로 낮은 기초 상태로 돌아가는 반면 재자극에 더 강하게 반응하는 능력은 후성적 수준에서 각인된다는 것입니다(A). 대조적으로, 적응은 환경 조건의 지속적인 변화 또는 만성 손상(예: 만성 감염)으로 인해 결정되는 면역 반응의 장기적인 변화로 정의되어 새로운 기능 상태로 이어집니다. 중요한 것은 적응 중 기능적 면역 상태가 모욕 이전의 낮은 기초 상태로 돌아가지 않는다는 것입니다(B).
이에 따라 식물 면역학에 대한 많은 연구에서 식물 숙주 방어가 적응 특성, 즉 전신 후천성 내성(SAR)이라는 반응을 포함한다는 것이 입증되었습니다(Jaskiewicz et al., 2011; Kachroo and Robin, 2013; Reimer-Michalski 및 콘라스, 2016). SAR의 분자 메커니즘과 생화학적 매개체는 널리 알려져 있으며(Kachroo and Robin, 2013), 숙주 방어의 후성 유전 기반 재배선이 중심 역할을 한다고 제안되었습니다(Luna and Ton, 2012). 무척추 동물의 타고난 면역에는 기억 특성이 부족하다는 믿음(Kurtz, 2005). 선천성 면역 반응의 적응 특성은 여러 무척추 동물 계통에서 보고되었습니다. 예를 들어,미생물군Plasmodium(Rodrigues et al, 2010)으로부터 모기를 보호하기 위해 타고난 면역 기억을 유도하는 것으로 나타났으며, 사회적 곤충인 Bombus Terrestris는 세 가지 다른 병원체(Sadd and Schmid-Hempel, 2006) 및 촌충 Schistocephalus에 대해 타고난 면역 기억을 표시하는 것으로 나타났습니다. solidus는 요각류 갑각류에서 기억을 유도하고(Kurtz and Franz, 2003), 타고난 면역 기억은 달팽이의 방어 메커니즘입니다(Pinaud et al, 2016). 이러한 연구는 기능적 적응 면역 반응이 없는 경우에도 실험적 쥐 모델에서 재감염으로부터 부분적인 보호를 유도할 수 있음을 보여주는 척추동물의 데이터로 보완되었습니다(Bistoni et al., 1986; can't Wout et al., 1992). ). 더욱이, 역학 연구는 광범위한 감염에 대한 인간 백신에 의한 이종 보호를 보여주었으며(Benn et al., 2013), 메커니즘은 고전적 적응 면역 반응과 독립적일 가능성이 있습니다. 따라서 면역기억은 척추동물뿐만 아니라 고전적 적응면역체계가 존재하지 않는 식물과 하등동물(Kurtz, 2005; Ne-tea et al., 2011)에서도 발견될 수 있다고 결론짓는 것이 합리적이다.

선천 및 적응 면역 기억: 진화 과정
이러한 데이터가 고등 유기체의 모든 그룹에 면역 기억의 존재를 강력하게 주장한다면 이것을 어떻게 정의할 수 있습니까? 간단한 정의는 면역학적 기억이 병원체에 보다 빠르고 효과적으로 반응하는 면역 체계의 능력을 의미한다는 것입니다. 이 정의는 다양한 유기체 그룹 내에서 관찰되는 작용의 차이를 구별하지는 않지만 식물, 무척추동물 및 척추동물에서 면역 기억으로 기술된 모든 과정을 포함합니다. 최근 검토에서 Pradeu와 Du Pasquier(2018)는 척추동물의 고전적 적응 기억, NK 세포 면역 기억, 골수 세포의 훈련된 면역 등 6가지 종류의 면역 기억을 구별하는 면역 기억의 다차원 모델을 제안합니다. , 무척추 동물의 프라이밍, 식물의 면역 기억(예: SAR), 박테리아와 고세균의 Crispr/Cas 기반 기억(Pradeu and Du Pasquier, 2018). 이러한 형태의 면역학적 기억은 강도, 속도, 소거(기저 상태로의 반전), 지속 기간 및 특이성과 같은 반응의 여러 기본 특성에 따라 특성이 다릅니다. 그러나 이 분류는 모든 살아있는 유기체에서 면역 기억의 편재적 존재를 이해하는 데 유용하지만 우리는 이것이구획화면역 기억의 특성은 다른 유기체의 기억 특성에 대한 일반적인 분자, 생물학적 및 기능적 기질을 반영하지 않습니다.
이 관점에서 우리는 두 가지 개념에 기반한 면역 기억의 통합 모델을 제안합니다.
면역 기억과 면역 분화라는 두 가지 형태의 면역 적응 사이에는 개념적 차이가 있습니다.
진화적 연속체는 타고난 면역 기억과 적응 면역 기억을 연결합니다.
정의해야 할 첫 번째 개념은 면역 기억과 면역 적응의 차이로 표현됩니다. 우리는 면역 기억을 급성 감염(또는 백신 접종) 후 숙주의 면역 체계의 변화된 상태로 정의하여 재감염에 대해 보다 효과적인 반응을 유도합니다. 중요하게도, 면역 기억을 유도하는 동안 첫 번째 감염과 재감염 사이에 면역 상태가 기능적으로 낮은 기초 상태로 돌아가고 재자극에 더 강하게 반응하는 능력은 후성적 수준에서 각인됩니다(그림 2A). 대조적으로, 우리는 면역 분화를 환경 조건의 지속적인 변화에 의해 결정되거나 만성 손상(예: 만성 감염), 새로운 기능 상태로 이어집니다. 중요한 것은 분화 중 기능적 면역 상태가 모욕 이전에 존재하는 낮은 기저 상태로 돌아가지 않는다는 것입니다(그림 2B). 면역 분화를 통한 적응을 특징으로 하는 생물학적 상황이 많이 있습니다. 이러한 상황 중 하나는 예를 들어 국소 면역 반응에 대한 장기적인 영향을 유도하는 것으로 알려진 장내 미생물총의 안정적인 변화에 의해 유도될 수 있습니다. 면역 분화 과정은 다른 많은 훌륭한 리뷰의 주제이며 이 관점의 초점이 아닙니다.
또 다른 중요한 구별은 프라이밍과 메모리입니다. 프라이밍은 2차 자극에 대한 증가된 반응을 설명하는 데 사용되는 용어이기도 하지만, 이는 종종 장기 기억 효과를 포함하지 않는 급성 과정입니다. 예를 들어, 급성 말라리아 감염 중에 심각한 급성 증상을 유발할 수 있는 그람 음성 미생물에 대한 면역 세포의 과민 반응이 잘 알려져 있습니다. 그러나 이것이 몇 달 또는 몇 년 동안 지속되는 기억 반응을 의미하지는 않습니다.
여기에서 우리는 모든 살아있는 유기체를 특징짓는다고 믿는 면역 기억의 개념에 초점을 맞출 것입니다. 우리는 별개의 메커니즘에 의해 매개되는 두 가지 기본 속성을 기반으로 하는 타고난 면역 기억과 적응 면역 기억 사이에 진화적 연속체가 있다고 제안합니다.
● 면역 재활성화의 크기 및 동역학 증가
재감염 시 반응, 후성적 과정에 의해 매개되고 선천 및 후천 면역 기억(모든 유기체에 존재)을 특징짓습니다.
● 유전자에 의해 매개되는 기억 반응의 특이성
재조합, 적응 면역 기억에 특정한 특성(지금까지는 척추동물에서만 설명됨)

타고난 면역 기억
척추동물 면역에서는 선천적 면역 반응이 감염 후에 적응할 수 없다고 오랫동안 가정되어 왔으며 재감염 시 매번 동일한 반응이 도출되지만 식물이나 무척추 면역에서는 이러한 가정을 따르지 않았습니다. 위에서 설명한 식물 및 무척추 동물 숙주 방어에 대한 연구(적응 진화 특성으로서의 면역학적 기억 참조) 외에도 무척추 동물의 선천적 면역 기억 유도를 설명하기 위해 다음과 같은 조절 경로의 상향 조절 또는 "훈련"을 포함한 여러 메커니즘이 제안되었습니다. Toll 또는 Imd(Boutros et al., 2002) 및 면역 세포 집단의 양적 및 표현형 변화(Ro-drigues et al., 2010). 일부 연구자들은 곤충에서 다양성 생성 메커니즘의 존재를 제안하기도 했습니다. 이러한 후보 메커니즘은 게놈 수준에서 높은 비율의 다양화(Zhang et al., 2004) 또는 펩티도글리칸 인식 분자 및 렉틴과 같은 특정 수용체의 발현 상향 조절(Steiner, 2004)을 갖는 피브리노겐 관련 단백질을 포함할 수 있습니다.
척추동물의 타고난 면역에도 적응 특성이 있다는 중요한 단서가 쥐 실험 연구에서 보고되었습니다. 이러한 여러 연구에 따르면 미생물 리간드로 마우스를 프라이밍하거나 훈련시키면 치명적인 감염을 예방할 수 있습니다. 예를 들어, -글루칸(진균에서 유래)에 의해 유도된 훈련된 면역은 황색포도상구균에 의한 박테리아 감염에 대한 보호를 유도합니다(Di Luzio and Williams, 1978; Marakalala et al, 2013). 유사하게, 세균성 펩티도글리칸 성분 muramyl dipeptide는 Toxoplasma에 대한 보호를 유도하고(Krahenbuhl et al, 1981), CpG oligodeoxynucleotide 투여는 패혈증과 대장균 수막염으로부터 보호합니다(Ribes et al, 2014). 또한, 그람 음성 박테리아의 플라젤린은 그람 양성 박테리아 Streptococcus pneumoniae(Munoz et al., 2010) 및 로타바이러스(Zhang et al., 2014a)에 대한 보호를 유도할 수 있습니다. 미생물 리간드 외에도 특정 전염증성 사이토카인이 훈련된 면역을 유도할 수 있다는 증거가 있습니다. Pseudo-monas aeruginosa에 감염되기 3일 전에 재조합 IL{10}} 1회 용량으로 마우스를 감염시키면 마우스가 사망으로부터 보호됩니다(van der Meer et al., 1988). 훈련된 면역 효과의 비특이적 특성은 적응 면역에 의해 매개되는 고전적 기억 효과에 반대하고 비특이적 타고난 면역 메커니즘의 활성화를 제안합니다. 조사해야 할 중요한 측면은 훈련된 면역의 보호 효과 기간입니다. 쥐와 사람을 대상으로 한 연구에서는 3개월에서 심지어 1년 후에도 효과가 나타났지만(Kleinnijenhuis et al, 2014), 백신의 이종 보호 효과를 기반으로 한 역학 데이터에 따르면 백신이 적어도 {{15}5년 동안 기능할 것이라고 제안합니다. 연령.
훈련된 면역은 백신 접종의 보호 효과 중 적어도 일부를 중재할 수 있습니다. 전 세계적으로 가장 일반적으로 사용되는 결핵 백신인 BCG(Bacillus Calmette Guerin) 백신 접종이 동물에서 Candida albicans, Schistosoma mansoni 또는 인플루엔자에 의한 2차 감염에 대해 T 세포 독립적 보호를 유도한다는 연구에서 강력한 증거가 나옵니다(Spencer et al. .,1977, Tribouley et al.1978, Wout et al., 1992). 인간 데이터는 다음 연구를 완료합니다: 인간 지원자의 BCG 백신 접종은 황열 백신 바이러스의 실험적 감염을 예방하는 반면(Arts et al, 2018), 대규모 역학 연구는 BCG 및 홍역 예방 접종에 대한 보호 이종 효과를 보고했습니다(Benn et al, 2013). ; Goodridge et al, 2016). 또한, 헤르페스바이러스 잠복기는 IFNγ의 생산 증가 및 대식세포의 전신 활성화를 통해 달성된 보호와 함께 박테리아 병원체 Listeria monocytogenes 및 Yersinia pestis에 대한 내성을 증가시킵니다(Barton et al., 2007). 유사하게, 기생충 기생충인 Nip-strongyles brasiliensis에 의한 감염은 기생충을 손상시키고 T 및 B 림프구와 독립적으로 재감염으로부터 보호를 유도하는 장기간의 대식세포 표현형을 유도합니다(Chen et al., 2014).
선천성 면역 기억을 담당하는 것으로 보고된 주요 세포 집단은 단핵구, 단핵구 유래 대식세포 및 자연 살해(NK) 세포입니다. 감염으로부터 대식세포 의존적 2차 보호는 비특이적인 반면, NK 세포 매개 면역 기억은 증가된 특이성을 제공할 수 있습니다. NK 세포 기억의 첫 번째 증거는 서로 다른 T 및 B 세포 결핍 마우스(RAG 녹아웃, SCID 및 nu/nu)가 합텐 기반 접촉 증감제에 대한 강력한 회상 반응을 올릴 수 있다는 관찰에서 비롯됩니다(O'Leary et al. 알, 2006). NK 세포는 합텐 특이적 접촉을 매개할 수 있습니다과민증(CHS) 이 동물에서 NK 세포 기억은 NK.1.1 + DX{3}}CXCR6 + CD49a + 표현형의 간 상주 세포로 제한됩니다(OLeary et al,2006; Paust et al,2010; Peng et al., 2013). 마우스 간 상주 NK 세포는 바이러스 유사 입자(VLP)를 비롯한 다양한 합텐 및 기타 항원에 대한 특정 기억을 개발할 수 있습니다. 그러나 항원 인식 메커니즘은 알려져 있지 않습니다(Paust et al., 2010). 항원 특이적 및 오래 지속되는(비장 및 간) NK 기억 세포 반응은 붉은털 원숭이에서도 관찰되었으며, 이는 항원 특이적 기억 NK 세포가 인간에게도 존재할 수 있음을 시사합니다(Reeves et al., 2015).
NK 세포는 거대 세포 바이러스에 의해 활성화될 수 있습니다. 쥐의 거대 세포 바이러스(mCMV) 감염 후(Nabekura et al.,2015; Schlums et al.,2015; Sun et al.,2009; Sunset al.,2012) Ly49H 수용체를 지닌 NK 세포가 증식합니다. , NK 세포 반응의 수축 단계 동안 림프 및 비 림프 기관에서 지속됩니다. 재감염 시 "기억" NK 세포는 2차 확장을 거쳐 빠르게 탈과립화되고 사이토카인을 방출하여 보호 면역 반응을 유도합니다(Sun et al, 2009). IL{7}}/IFNy 축(Sun et al, 2012) 또는 공동 자극 분자 DNAM의 활성화를 포함하여 NK 세포의 기억 속성을 설명하기 위해 여러 가지 가능한 메커니즘이 제시되었습니다.{10 }}(DNAX 보조 분자{11}}, CD226)(Nabekura et al., 2014).

CMV로 유도된 NK 기억은 특이적인 것으로 보입니다. 마우스 연구는 인플루엔자 또는 리스테리아와 같은 다른 감염에 대해 mCMV로 유도된 NK 기억 세포의 반응성이 향상되지 않음을 보여주었습니다(Min-Oo and Lanier, 2014). 유사하게, 인간 연구는 인간 (H)CMV + 개인에서 확장된 NKG2C + CD57 + NK 세포 집단의 반응성을 나타내지 않습니다(Hendricks et al, 2014). 사이토카인 프라이밍된 NK 세포는 또한 기억과 유사한 특성을 발달시키는 것으로 제안되었습니다. IL12, IL15 및 IL18의 조합으로 자극된 마우스 및 인간 NK 세포는 사이토카인 프라이밍 후 몇 주 후에 사이토카인 또는 종양 세포를 사용한 2차 자극에 대한 반응으로 향상된 IFNγ 생성을 나타냈다(Cooper et al., 2009; Keppel et al, 2013). ; Romee et al., 2012).
NK, B 및 T 세포와 공통 림프 전구를 공유하는 선천 림프 세포 그룹 2(ILC2)는 항원 수용체를 보유하지 않지만 사이토카인에 의해 활성화될 수 있습니다. 그들은 또한 활성화 상태를 "기억"하고 2차 자극 시 향상된 반응을 생성할 가능성을 보여줍니다. 폐에서 흡입된 알레르겐은 ILC2를 자극하여 IL-33-의존 방식으로 IL-5 및 IL{4}}을 생성합니다(Halim et al., 2014). 알레르겐 유도 활성화 후, 폐 ILC2는 확장 후 사이토카인을 생성하지 않는 수축 단계를 거칩니다. 알레르겐 경험이 있는 ILC2 집단은 폐와 림프절에 지속됩니다. 관련되지 않은 알레르겐에 대한 2차 도전에서 기억 유사 ILC2는 보다 강력한 면역 반응을 나타냅니다. IL{13}}이 있는 마우스의 감작은 ILC2 기억의 비항원 특이적 특성을 나타내는 알레르겐 2차 자극에 반응하는 기억 ILC2를 생성하기에 충분했습니다(Martinez-Gonzalez et al., 2016).
이러한 관찰은 또한 선천 면역과 적응 면역 사이의 진화적 교차로에서 ILC와 NK 세포의 독특한 위치를 강조할 수 있습니다.
종합하면, 이러한 상호 보완적인 뮤린 및 인간 연구는 타고난 면역 반응이 "훈련"될 수 있는 능력을 갖고 있으며, 이에 따라 재감염 시 새로운 유형의 면역학적 기억을 발휘할 수 있음을 보여줍니다. 이에 대해 훈련된 면역이라는 용어가 제안되었습니다(Netea et al, 2016; Netea et al., 2011). 훈련된 면역 개념의 확장은 최근 상피 세포와 같은 비면역 세포 유형도 포함하도록 제안되었습니다(Cassone, 2018).
