세포 치료에서 신장 미세 순환 이미징
Mar 17, 2022
연락처:ali.ma@wecistanche.com
카테리나 아펠트 외

신장 질환에 대한 Cistanche 줄기, 샘플을 얻으려면 여기를 클릭하십시오
추상적인:
신장미세혈관 희박은 진행성에서 중추적인 역할을 합니다.신장질병. 따라서 신장의 미세 순환을 시각화하는 양식은 질병 메커니즘에 대한 이해를 높이고 결과적으로 세포 기반 치료를 평가하기 위한 새로운 접근 방식을 제공할 수 있습니다. 그러나 현재 임상 실습은 신장 질환으로 고통받는 환자에서 시간 경과에 따른 신장 미세혈관 변화를 모니터링하기 위한 비침습적이고 안전하며 효율적인 영상 기법이 부족합니다. 중요성을 강조하기 위해 우리는 신장 미세순환에 대한 현재 지식을 요약하고 진행성 신장 질환의 관련성에 대해 논의했습니다. 또한, 신장 미세혈관 형태, 기능 및 행동을 밝히는 데 사용 가능한 영상 기술에 대한 개요가 관련 이점 및 제한 사항과 함께 제공됩니다. 궁극적으로 생체 내 판독값을 기반으로 모세혈관 수준까지의 분해능으로 신장 질환을 평가하고 조사할 필요성은 다음 분야의 진단 및 치료에 대한 패러다임 전환을 제공할 수 있습니다.신장학.
키워드: 신장; 미세순환; 미세혈관희박; 세포 요법; 이미징
1. 소개
신장 혈관계는 고유한 생리학적 기능을 반영하는 해부학적으로 복잡한 구조를 가지고 있습니다[1]. 혈역학적 변화에 대한 미세혈관 네트워크의 매우 역동적인 적응에도 불구하고, 혈관 기능 장애는 다음의 결과이거나 심지어 원인일 수 있습니다.신장질병 발달 및 진행 [2,3]. 따라서 미세혈관 기능장애는 섬유성 신장 손상의 초기 특징으로 작용할 수 있으며, 이는 신장 미세혈관 구조 및 기능의 비침습적 평가 및 검증이 신장 섬유증 감소를 목표로 하는 요법의 효능을 평가하는 데 큰 개선이 될 것임을 암시합니다.
임상에서 만성질환의 중증도는신장질병(CKD)은 사구체여과율(GFR)을 기준으로 분류되며, 이는 경증(60-89mL/min/1.73m2), 중등도(30-59mL/min/1.73m2) 또는 중증(15-29mL/)을 반영합니다. 최소/1.73m2 ) 감소신장기능미리 정의된 범주를 기반으로 합니다[4]. 진행성 CKD 및 말기 신장 질환(ESRD)으로의 질병 진행은 GFR이 15mL/min/1.73m2 미만인 사구체 경화증 및 세뇨관 간질 섬유증의 발생으로 정의됩니다. 여러 연구에서 신장 모세혈관 소실 현상, 즉 신장 미세혈관 희박화가 신장 질환의 중증도와 밀접한 관련이 있으며 CKD로의 후속 진행의 생물학에 관여한다는 것을 보여주었습니다[3,5-7]. 신장 섬유증의 형성은 이러한 세뇨관 주위 모세혈관 손실과 그에 따른 신장 상피 손실의 중심 특징으로 강조되었습니다. 신장의 미세혈관 구조가 보호되거나 회복될 수 있다면 신장의 구조적 조직 무결성이 향상되고 질병 진행을 예방할 수 있습니다[2,8]. 또한, 치료 창은 잠재적으로 신장 손상의 정도가 되돌릴 수 없는 정도가 되기 전에 손상의 심각성을 평가하기 위해 정의될 수 있습니다. 특히, 중간엽 기질 세포(MSC)의 유망한 응용과 같은 세포 요법의 활용은 신장 혈관 질환 치료를 위해 평가되고 개선될 수 있습니다. 그러나 신장 미세혈관 희박화에 대한 자세한 이해는 혈관 구조 및 기능의 고해상도 및 비침습적 모니터링을 가능하게 하는 이미징 양식의 부재로 인해 여전히 방해받고 있습니다.

이 검토에서 우리는 미세 순환에 영향을 미칠 수 있는 신장 미세혈관 구조와 병리학적 메커니즘에 대한 현재 지식을 요약합니다. 우리는 혈관주위세포의 중요성에 대해 논의하고 미세혈관 기능 장애 및 희박화를 통해 신장 질환 진행을 유발하는 중심 역할과 혈관 주위 세포의 발달에 대한 통찰력을 제공합니다.신장섬유증. 우리는 이후에 신장 미세 순환의 이러한 변화를 모니터링할 수 있는 이미징 기술의 새로운 개발을 설명합니다.
2. 신장 혈관계
2.1. 신장 혈액 순환
인체의 미세혈관은 세동맥, 모세혈관, 세정맥으로 구성되어 있으며 혈액과 주변 조직 사이에서 산소, 영양소, 대사산물의 교환을 수행합니다[8,9]. 분명히, 미세 순환의 중요한 기능은 기관의 대사 요구에 따라 엄격하게 조절됩니다. 세동맥의 주요 책임은 모세혈관 수준에서 중요한 교환이 실행될 수 있도록 저항을 조정하여 혈류를 조절하는 것입니다[10]. 이와 관련하여 기본 조직의 항상성 요구에 대한 지속적인 적응은 주로 내피 세포의 동적 가소성에 의존합니다. 동시에 미세순환의 내피 건강은 물리적으로 혈관을 안정화시키고 혈관신생을 조절하며 혈류를 조절하는 혈관주위세포와의 긴밀한 세포간 통신에 의존합니다[11,12].
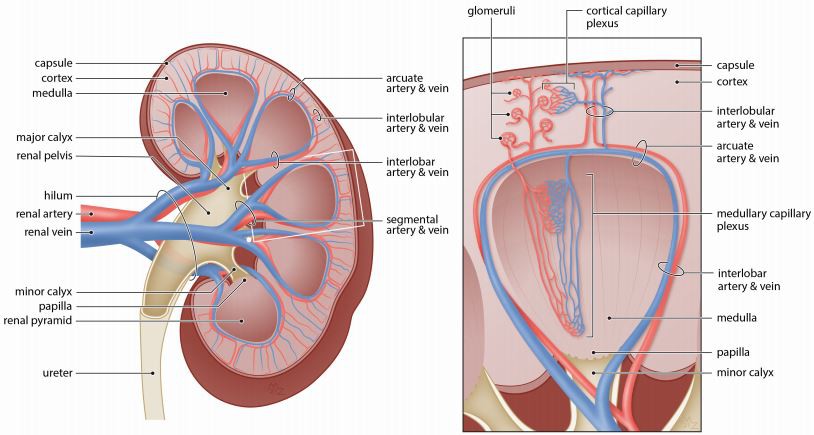
신장은 혈관 네트워크의 현저한 이질성을 반영하는 독특한 형태학적 및 기능적 특성을 나타내는 고도로 혈관화된 기관입니다[1,10]. 혈액은 hilum(그림 1)을 통해 신장 동맥을 통해 신장으로 들어가며, 이 동맥은 신장 골반에서 분절 동맥으로 이분법적으로 나뉘며, 소꽃받침 수준에서 점차적으로 신장 피라미드 사이에 퍼지는 엽간 동맥으로 분기됩니다[1,13 ]. 피질과 수질 사이의 경계에서 엽간 동맥은 아치형 동맥으로 흘러 양쪽 신장 구획 사이에 해부학적 분리를 형성합니다[1]. 피질에서, 피질 방사 동맥 또는 피질 관통 세동맥으로도 알려진 소엽 간 동맥은 아치형 동맥에서 수직으로 발생하고 사구체 나무의 다양한 가지에 공급하기 위해 구심성 세동맥으로 분기됩니다. 사구체의 위치에 따라 여과된 혈액은 Henle 고리 수준에서 근위 및 원위 세뇨관 또는 수질 모세혈관 신경총을 둘러싸는 피질 모세혈관 신경총에 모입니다. 마지막으로 혈액은 소엽간, 아치형, 소엽간, 분절을 통해 신장을 빠져나가는 동맥 네트워크와 평행하게 흐르는 정맥계로 흘러들어가고 결국에는 요관 바로 위의 신장 정맥으로 흘러들어갑니다. 일반적으로 말해서, 이 기본 혈관 패턴은 포유동물에 걸쳐 보존됩니다[14,15].
2.2. 신장의 모세혈관망
신장 미세혈관 구조의 복잡성은 다양한 신장 혈관의 다양한 형태에 의해 반영됩니다(그림 2). 신장 내피와 주변 혈관주위 세포의 구조적 및 기능적 이질성은 모세혈관 네트워크의 유형과 밀접하게 관련되어 있습니다[15-17]. 사실, 다양한 모세혈관층의 존재는 사구체 모세혈관망을 통한 여과와 세뇨관주위 모세혈관망과 수질모세혈관망을 통한 분비 및 재흡수를 보장하는 놀라운 특징입니다[1,13,14]. 대뇌피질의 미세순환은 주로 사구체 여과액의 재흡수를 보장하는 반면 염분과 수분의 배설은 주로 골수 미세혈관 구획에 의해 조절됩니다[14]. 흥미롭게도 수질은 전체 신장 조직 질량의 약 30%를 구성하지만 전체 신장 혈류(RBF)의 10%만이 이 부분을 구성합니다[10]. 해부학적 위치에 따라 신장 미세 순환은 (i) 피질 미세 순환; 및 (ii) 골수 미세 순환 [13,14].
피질 미세순환은 사구체 모세혈관 네트워크에 공급하기 위해 양쪽에서 여러 구심성 세동맥으로 더 분기되는 소엽간 동맥을 발생시키는 아치형 동맥에 의해 물리적으로 분리됩니다[14]. 분지는 피질 내 사구체의 위치에 따라 다른 각도에서 발생합니다. 구심성 세동맥을 통해 6-8개의 모세혈관 고리로 구성된 사구체 모세혈관 네트워크에는 여과된 후 원심성 세동맥을 통해 나가는 혈액이 공급됩니다[10]. 사구체 모세혈관(그림 2a)은 족세포로 덮인 얇고 연속적이며 대부분 평평한 천공 내피로 형성됩니다. 구멍이 뚫린 영역은 전체 세포 표면의 최대 20-50%를 차지할 수 있습니다[16]. 피질 사구체는 신장에 존재하는 모든 사구체의 90%를 구성하므로 대부분의 RBF가 우세하게 통과하는 것은 놀라운 일이 아닙니다[13]. 모든 사구체의 나머지 10%는 피질-수질 경계에 위치하며 크기가 더 큽니다. 사구체의 크기 차이 외에도, 피질 및 골수 인접 사구체를 공급하는 구심성 및 원심성 세동맥의 구조적 차이는 모세관 압력을 보존하는 중요성으로 설명될 수 있습니다.
적절한 혈액 여과를 보장하기 위해 피질 구심성(그림 2b)과 피질 원심성(그림 2c) 세동맥 사이의 직경 차이는 15μm 대 10μm입니다[13]. 혈압은 평활근 세포(SMC)에 의해 싸여 있는 연속적인 내피를 설명하는 저항 변화 수단을 통해 구심성 세동맥 측면에서 조절됩니다[18]. 구심성 세동맥을 자세히 검사하면 일반적으로 마주치는 전체 혈관 길이를 따라 균일한 내피가 아닌 두 개의 혈관 세그먼트가 있음을 알 수 있습니다. 구심성 세동맥의 근위 부분은 혈관 수축에 필요한 단단히 배열된 SMC가 있는 비투과성 내피로 구성됩니다. 사구체에 밀접하게 위치하고 천공의 존재로 인해 투과성 내피로 구성된 말단 부분과 대조됩니다. 흥미롭게도, 이 구멍은 혈관 내압이 높은 혈관에서는 흔하지 않은 특징입니다. 게다가, 입방체 모양의 레닌을 생성하는 혈관주위세포는 구심세동맥의 말단부를 감싸 사구체의 국부혈압 조절을 중재한다[17,19].

여과된 혈액은 원심성 세동맥을 통해 각각의 피질 사구체를 빠져나가 신세뇨관을 둘러싸고 있는 조밀한 피질 모세혈관 신경총으로 모입니다[10]. 사구체 모세혈관 시스템과 별도로 이 두 번째 모세혈관 구획은 세뇨관 주위 모세혈관 시스템으로 알려져 있습니다[16]. 세뇨관 주위 모세혈관(그림 2d)은 약 7μm의 평균 직경으로 천공되고 얇은 벽으로 되어 있습니다[13,15]. 이러한 모세혈관은 신피질에 위치한 세뇨관에 산소와 영양분을 제공하지만 반드시 그것이 기원하는 세뇨관에는 제공되지 않습니다[10,15]. 세뇨관 주위 모세혈관은 직장의 수질 모세혈관에 비해 직경이 더 작을 뿐만 아니라 더 연속적인 내피를 나타냅니다[13,16]. 신질환에서 사구체 손상은 최종적으로 하류에 순차적으로 배열된 세뇨관주위 모세혈관에 영향을 미쳐 신질환의 진행을 가속화시킨다[10,20].
골수 인접 구심성 세동맥(그림 2e)은 대략적인 직경이 20μm인 반면, 골수 인접 원심성 세동맥(그림 2f)은 20-25μm의 더 두꺼운 내부 직경을 가지고 있습니다[13]. juxtamedullary glomerulus를 나가는 efferent arteriole은 여러 SMC로 둘러싸여 있습니다. 혈관 직경의 이러한 눈에 띄는 차이와 증가된 근육화는 허혈에서 이 사구체 유형의 관련에 대한 논쟁을 불러일으키고 있습니다. 신장 혈관 구조는 허혈성 손상으로부터 수질을 보존하기 위해 특정 방식으로 조직화되어 있는 것으로 보입니다. 골수 인접 사구체의 구심성 및 원심성 세동맥이 수질 혈액 펠로우(MBF) 조절을 담당하지 않을 수 있다는 가설이 있지만, 이것은 또한 사구체 여과율을 조절하는 역할과 모순될 수 있습니다[21]. 대신, 외부 수질의 내부 줄무늬에 위치한 혈관 다발의 하강 직결관(DVR)이 이 혈관 구획을 감싸고 있는 많은 수의 혈관주위세포를 설명할 수 있는 MBF를 제어하는 역할을 하는 것으로 보입니다. 따라서 DVR은 동맥압의 장기적 조절에 중요한 역할을 합니다[13]. 외측 수질의 안쪽 줄무늬에 위치한 혈관 다발을 통해 juxtamedullary glomeruli에 연결된 원심성 세동맥이 DVR로 바뀝니다. DVR은 상행 정 맥 (AVR)에 연결된 골수 모세 혈관 네트워크를 생성합니다 [1].
수질 미세 순환은 수질 인접 사구체에서 유래한 원심성 세동맥이 조직 깊숙이 들어가 수질로 알려진 신장 조직의 나머지 30%를 공급할 때 시작됩니다[13,14]. 한 신장 피라미드의 수질은 해부학적으로 두 부분으로 나뉩니다. 피질 바로 아래에 위치한 외부 수질과 유두라고 하는 실질의 정점까지 퍼지는 내부 수질입니다. 일반적으로 수질모세혈관의 수는 신장 피라미드 끝에서 증가합니다. 더 자세히 관찰하면 외부 수질은 외부 스트립과 조밀한 모세관 신경총 및 속속 신경총을 포함하는 고도로 혈관화된 내부 스트립으로 더 세분화될 수 있음을 나타냅니다[15]. 다발간 모세혈관은 천공된 내피를 특징으로 하며 아치형 정맥에 연결되어 있습니다[14,22].
각각의 juxtamedullary efferent arteriole은 혈관 번들로 알려진 여러 번들로 분할되어 피질의 세뇨관 주위 모세 혈관에 비해 더 큰 직경을 갖는 DVR의 가지를 형성합니다(그림 2g). 혈관다발 DVR의 내피에는 여러 개의 혈관주위세포가 붙어 있다[17]. 흥미롭게도 혈관을 감싸는 혈관주위세포의 수는 내부 수질의 DVR(그림 2h)에서 감소합니다[15,17]. 외부 및 내부 수질 구획에서 DVR의 이러한 형태적 배열은 이중 기능을 반영합니다[10]. 더 자세히 설명하면, DVR의 혈관수축은 외측 수질에 위치한 근위부에서 주로 나타납니다[15]. 그러나 원위부, 즉 내수질에서는 주로 전해질 교환이 일어난다. 이러한 해부학적 차이는 형태학적 외양과 기능적 특성 측면에서 혈관주위세포의 뚜렷한 하위집단을 직접적으로 의미합니다[15,17].
내부 수질 깊숙한 곳에서 DVR의 다양한 가지가 훨씬 더 작은 AVR에 연결되기 전에 복잡한 모세관 네트워크로 분할됩니다[10]. DVR의 내피는 연속적으로 형성되어 있으며, AVR의 내피 세포(그림 2i)는 구멍이 많이 뚫려 있습니다. 결국, 모든 혈액은 AVR뿐만 아니라 피질 모세혈관 신경총의 정맥주위 모세혈관에서 정맥계로 수집됩니다. 일반적으로 신정맥은 혈관벽이 극히 얇으며 소엽간, 아치형, 소엽간정맥은 천공되어 있으며 횡격막을 포함하고 있다. 놀랍게도, 소엽 사이 정맥은 일반적으로 얇고 고도로 천공된 상피로 인해 정맥보다 세뇨관 주위 모세혈관과 더 큰 유사성을 보입니다.
다양한 신장 미세혈관 분절과 세포 수준에서의 우아한 형태는 기존의 복잡성이 훨씬 더 복잡한 질병 기전으로 해석된다는 의혹을 불러일으킵니다. 따라서 다음 섹션에서는 신장 미세혈관 기능 장애와 관련된 기본 과정에 중점을 둡니다.

3. 신장 미세혈관 기능 장애
3.1. 내피 기능 장애
신장 내피는 생리학적 조건에서 대부분 정지 상태입니다. 그러나 전단응력, 저산소증, 산화응력, 염증 등의 미세환경 변화에 반응하여 내피세포가 활성화되고 혈관신생 성장인자가 생성된다[24]. 방아쇠에 따라, 내피 세포 활성화는 미세혈전 형성을 위한 면역 세포 접착 및 침윤을 촉진하기 위해 친염증성 및 친혈전성 표현형을 유도할 수 있습니다. 그러나 적절한 광대한 조절 기능과 용질 수송을 위한 투과성을 위한 혈관 장벽을 유지하려면 활성화된 내피 세포뿐만 아니라 정지 상태의 대사 상태를 엄격하게 조절하는 것이 필수적입니다.
조직 무결성과 기관 기능은 주로 미세혈관 네트워크의 적절한 관류에 달려 있습니다[8]. 따라서 내피 세포가 모세관 수, 형태적 모양 및 기능을 조정하여 환경 변화에 대한 동적 적응을 보장하기 위해 높은 가소성을 나타내는 것은 놀라운 일이 아닙니다[1,2,8]. 그러나 장기간의 상승된 혈압은 미세순환에 비가역적인 변화를 일으켜 손상된 적응 특성을 특징으로 하는 손상된 내피 세포를 유발합니다. 이러한 방해된 항상성은 산화질소(NO), 저산소증 유발 인자-1(HIF{6}}) 및 혈관 내피 성장 인자(VEGF)의 감소와 함께 다음과 같은 다른 요인의 증가에 의해 반영됩니다. 지오스타틴, 엔도스타틴 및 트롬보스폰딘 [1]. 특히, 신장의 내피 기능 장애에 대한 감수성은 다양하고 신장 미세 순환의 여러 구획 내에 위치한 내피 세포 유형에 따라 다릅니다[16,24]. 신장 내피 세포의 이질적 표현형과 미세혈관 변화에 대한 상이한 반응을 설명하기 위해 Dumas et al. [25] 최근 단일 세포 RNA 시퀀싱을 사용하여 신장 내피의 고해상도 아틀라스를 제공했습니다.
내피 기능 장애는 종종 급성 및 진행성 신장 기능 저하와 함께 발생합니다[24]. 이 오작동은 혈관 저항을 증가시키고 RBF의 감소를 동반합니다[26]. 장기간의 혈관 수축은 부적절한 조직 관류 및 스트레스 및 성장 인자의 활성화를 유발하여 형태학적 변화를 유발합니다[1]. 심각도와 특히 주어진 손상의 기간에 따라 RBF는 미세 순환의 구조적 변화를 도입하여 비가역적으로 변경될 수 있습니다. 이러한 형태학적 변화는 미세혈관 리모델링으로 알려진 과정에 의해 발생합니다. 미세혈관 리모델링은 미세혈관 구조의 기능적 변화에 대한 반응으로 정의되며, 이는 결과적으로 혈역학적 항상성에 도달하기 위한 마지막 시도에서 구조적 수준에서 미세혈관 구조의 변경을 일으킬 수 있습니다[1,2,8]. 마지막으로, 내피 기능 장애는 관류가 회복되지 않는 'no-reflow'라는 현상을 초래할 수 있으며, 결국 급성 신장 손상(AKI)을 초래하는 관상 상피 세포 손상을 초래합니다[24].
내피 기능 장애가 신장 질환과 관련이 있을 뿐만 아니라 적극적으로 질환 진행을 유도한다는 점을 강조하는 것이 매우 중요합니다[24]. 신장 미세혈관 기능 장애는 세포 손상에 의해 유발된 내피 기능 장애에 의해 반영되며, 이는 혈관주위세포와 내피층의 긴밀한 상호 작용을 방해하고 세포 통신을 방해합니다.
3.2. 신장 기능 부전에 대한 혈관 주위 세포 관련
CKD의 중심적인 특징은 희박화(rarefaction)라고 하는 과정인 세뇨관 주위 모세혈관 네트워크의 점진적인 손실입니다[27]. 세뇨관간질 섬유화증과 손상된 세뇨관 상피는 신장에서 이러한 모세혈관 희박화가 선행되는 반면[27], 이러한 미세혈관 희박화는 섬유화증의 중증도와 직접적인 상관관계가 있습니다[28,29]. 더욱이 희박 정도는 CKD 환자에서 사구체 여과율의 변화뿐만 아니라 간질 손상의 정도를 예측하는 것으로 밝혀졌다[28]. 이러한 발견은 CKD의 발병과 섬유증의 발병기전에서 미세혈관 불안정화/소실이 조기에 속도를 제한하는 역할을 시사합니다[30]. 심혈관 위험 인자에 의한 만성 내피 세포 활성화는 내피 세포와의 상호 작용을 통해 모세 혈관의 안정화 및 증식에 중요한 역할을 하는 혈관주위 세포의 손실을 유발할 수 있습니다[31]. 실제로, 축적된 증거는 혈관주위세포의 중요성과 신장 미세혈관 건강에 대한 관여를 정확히 지적합니다[17].
혈관주위세포는 모세혈관의 기저막 내에 묻혀 있는 내피를 덮는 길쭉한 돌기를 가진 혈관주위벽화세포이다[32]. 그들은 중간엽 기원의 세포이며 Forkhead box D1(FoxD1)과 기질 전구 집단에서 발생하며, 이는 또한 SMC, 상주 섬유아세포, 레닌 세포 및 간간세포를 포함하는 신장 혈관계의 다른 벽화 세포를 생성합니다. 신장 혈관계의 모든 내피 세포는 줄기 세포 백혈병(SCL)과 전구 세포에서 유래합니다[34]. 혈관주위세포는 혈관 기저막에 내장되어 있기 때문에 상주(혈관주위) 섬유아세포와 다르지만, 신장에 대한 대부분의 연구에서는 특정 마커가 없기 때문에 혈관주위세포와 혈관주위 섬유아세포를 구별하지 못합니다[31,35]. 혈관주위세포를 식별하는 데 일반적으로 사용되는 마커에는 혈소판 유래 성장 인자 수용체-(PDGFR), 콘드로이틴 설페이트 프로테오글리칸 NG2, -평활근 액틴(SMA), 분화 클러스터 73(CD73) 및 PDGFR이 포함되지만 이러한 마커는 서로 다른( 중첩) 다른 해부학적 영역에 국한된 혈관주위세포의 하위 집합으로, 이 세포 집단의 이질성과 기능적 이질성을 반영할 가능성이 가장 높습니다. Pericytes는 혈관 발달, 안정화, 성숙 및 리모델링을 엄격하게 조절하고 [11] 혈관 수축에 의해 혈류를 조절합니다. 혈관주위세포는 기능적으로는 안지오텐신 II 및 아데노신 삼인산(ATP)과 같은 혈관수축 인자와 NO 및 프로스타글란딘과 같은 혈관 확장 인자에 의해 조절됩니다[17]. 혈관의 성숙은 혈관구조를 안정화하고 혈압을 조절하기 위해 혈관주위 세포의 동원에 의존한다[12].
신장에서 혈관주위세포는 대뇌피질 사구체의 구심세동맥의 말단부를 감싸고 있으며 주로 세뇨관주위 모세혈관과 직장정맥에 존재한다[13,19]. 또한, 메산지알 세포는 사구체 모세혈관에 대한 구조적 지지를 유지하고 사구체 혈역학을 조절하는 데 중요한 신주위세포의 (특화된) 하위 집합입니다. 또한 세동맥에 위치한 수축성 사구체주위세포는 국소 사구체 혈압을 매개하고 레닌 분비를 통해 전신 혈압에 영향을 미친다[19]. 흥미롭게도, 간질 구획에서 파생된 레닌 전구체 세포는 시공간적으로 혈관 발달과 연결되어 있는 반면, 동맥 분지 형성은 분지 지점에서 레닌 발현 세포의 출현이 선행되는 것으로 나타났습니다[33,36]. 또한, 형질전환 레닌 리포터 제브라피쉬를 사용하여 레닌 발현 세포가 혈관신생 콩나물보다 선행하는 것으로 나타났다[37]. 성체 마우스 신장에서 레닌 기원의 세포가 혈관주위 위치에서 관찰되고 혈관주위세포 마커(PDGFR/NG2)와 함께 염색되어 혈관 유지에서 이 부분집합이 중요한 역할을 할 수 있음을 시사합니다.
3.3. 내피 세포-주위 세포 신호 상호 작용
Pericytes는 안정화 및 혈관 신생 발아에 필요한 신호 전달 경로를 조절하는 다수의 상호 상호 작용을 통해 내피 세포와 상호 작용합니다. 혈관주위세포는 VEGF, PDGF, 변형성장인자(TGF-), 안지오포이에틴-1(Ang{4}})과 같은 분비 인자와 직접적인 내피-주위세포 누화를 통해 내피에 신호를 보냅니다[39 ]. 유사하게, 내피는 안지오포이에틴-2(Ang-2) 및 PDGF와 같은 인자를 사용하여 주변 기질 세포에 신호를 보냅니다. Ang{9}}은 Ang 매개 Tie{11}} 신호 전달을 부정적으로 방해하여 혈관주위세포-내피 세포 상호작용을 방해하고 이에 따른 혈관 불안정화 및 비정상적인 미세혈관 리모델링을 초래합니다[40,41]. 모세혈관 네트워크의 유지에서 혈관주위 간질 세포와 내피 세포 사이의 상호 작용의 결정적인 중요성은 마우스 연구에서도 입증되었으며, 이는 혈관 주위 세포의 투자가 방해를 받으면 모세혈관 네트워크가 불안정해지고 희박화가 발생함을 보여줍니다[42]. 예를 들어, 고혈당은 내피 Ang{15}} 발현을 증가시켜 혈관주위 기질 세포가 모세혈관에서 멀어지게 합니다[43]. 우리 연구실의 최근 연구에 따르면 쥐[44]와 인간 기증자 신장[45] 모두에서 허혈-재관류 손상이 Ang{20}}/Ang{21}} 균형의 급격한 상승을 초래하며, 이는 미세혈관 완전성의 상실과 함께. 또한 당뇨병 환자에서 신장-췌장 동시 이식 후 12개월 이내에 모세혈관 건강의 역전과 Ang{22}}/Ang{23}} 비율 및 가용성 트롬보모듈린(내피 세포 손상 마커)의 감소가 관찰되었습니다[46 ]. 안지오포이에틴/Tie2 경로[47] 다음으로 내피-주위세포 누화는 TGF 수퍼패밀리 신호[48], VEGF[49] 및 스핑고신{31}인산염(S1P) 신호 전달 경로[50]에 의해 조절됩니다.
3.4. 근섬유모세포의 전구체로서의 혈관주위세포
쥐의 유전적 혈통 추적 모델은 신장 섬유증의 마우스 모델에서 혈관주위세포(및 기타 혈관주위 세포)가 -SMA 양성 근섬유아세포의 주요 공급원임을 입증했습니다[51,52]. 사실, 단일 세포 RNA 시퀀싱과 관련된 최근의 우아한 연구는 인간 신장에서 근섬유아세포의 세 가지 주요 출처를 정확히 지적했습니다. (i) NOTCH3 + RGS5 + PDGFR - 혈관주위세포; (ii) MEG3 + PDGFR + 섬유아세포; 및 (iii) COLEC11 + CXCL12 + 섬유아세포 [53]. 세포주위세포에서 근섬유아세포로 분화하는 동안 분화 및 확장과 일치하는 세포 주기 변화가 관찰되었으며 풍부한 경로에는 표준 WNT 및 활성인자 단백질{14}}(AP{15}}) 신호 전달과 전사 활성화가 포함되었습니다. 인자 2(ATF2), PDGFR, 인테그린, 세포외 기질(ECM) 수용체 상호작용 및 TGF-신호전달 경로[53]. PDGFR 플러스 세포 집단의 작은 부분이 혈관주위 Gli1과 혈관주위 MSC 유사 세포 집단을 표시하는 전구세포로 구성되며, 이는 근섬유아세포 생성을 통해 손상 유발 기관 섬유화증의 주요 기여자이기도 하다는 것이 입증되었습니다. [54] . 더욱이, 신경교종 관련 종양유전자 상동체 1(Gli1)과 혈관주위세포 손실은 모세관 희박화 및 근위 세뇨관 손상을 유도하는 것으로 나타났습니다[55]. 참고로, 혈관주위세포는 이전에 연결되어 있고 MSC와 밀접하게 관련되어 있기 때문에[56], 이것은 또한 혈관주위세포의 하위 집합이 MSC일 수 있는지 여부에 대한 질문을 제기하며, 따라서 신장 재생에 기여합니다. 사실, 많은 연구에서 다양한 조직에서 혈관주위세포에 대한 다능 전구 유사 역할을 발견했습니다[35,57,58].
종합하면, 미세혈관 희박화는 섬유증에서 흉터 조직의 주요 구성요소인 ECM 단백질의 과도한 생성을 담당하는 근섬유아세포 풀에 직접적으로 기여합니다. 또한, 혈관주위세포에서 근섬유아세포로의 전이는 혈관벽에서 혈관주위세포의 박리를 유발하여 그 자체로 희박을 유발하는 불안정한 모세혈관을 초래한다[52]. 그럼에도 불구하고, 만성 신부전의 발병기전에 대한 희박의 주요 영향은 수질 허혈을 더욱 악화시키고 TGF 및 결합 조직 성장 인자의 증가된 발현에 의해 매개되는 간질 섬유증의 발병을 유발하는 신관류의 손실에 의해 유발됩니다. (CTGF) [59]. 따라서 미세혈관 희박화는 만성 신부전의 발병기전에서 속도를 제한하는 전섬유화 스위치로 잘 기능할 수 있습니다. 실제로, PDGFR- 또는 VEGF 수용체 신호전달을 목표로 하는 내피 세포-주위세포 상호작용을 표적으로 하는 요법은 근섬유아세포 전이를 방지하고 섬유증의 발달을 제한할 수 있으며 [60-62], 이는 신장 손상에서 모세관 네트워크의 주요 역할을 설명하고 다음과 같이 잠재적인 치료 표적.
위의 내용을 바탕으로 신장의 복잡한 혈관 구조는 각각 고유한 기능과 요구 사항을 가진 여러 개의 혈관주위 구획을 생성한다는 것이 분명합니다. 따라서 위치, 세포 형태 및 기능을 기반으로 하위 개체군을 특성화하여 신주위 세포를 심층적으로 분류하는 데 중점을 둔 향후 연구가 필요합니다. 따라서 작은 크기의 혈관에 비침습적으로 접근하는 것을 목표로 하는 새로운 영상 기법이 이 필수 정보를 제공할 수 있습니다. 신경생물학[12] 분야에서 예시된 바와 같이, 혈관주위세포의 다른 아형에 대한 잘 정의된 분류는 혈관 기능 부전에 대한 표적 치료의 개발을 위한 새로운 길을 제공할 수 있습니다.
4. 혈관 이미징 양식
다른 신장 질환은 미세 구조 변경의 특징적인 패턴을 반영합니다. 생체의학 영상 분야의 기술 발전의 결과로 지난 수십 년 동안 신장 생리학적 및 병태생리학적 메커니즘이 밝혀졌습니다[63]. 조직 구조의 해부학적 및 형태학적 변화에 초점을 맞춤으로써 신장 질환에 대한 지식이 점진적으로 확대되어 진단이 개선되고 혁신적인 치료 기회가 제공되었습니다. 그러나, 혈관의 동적 변경은 시계열 실험에서 혈관 거동을 조사해야 하는 과제로 인해 주로 무시되었습니다. 그 결과, 신장 미세순환의 혈역학을 모니터링하기 위한 비침습적 영상 기술을 개발해야 하는 의학적 요구가 충족되지 않았습니다[16].
혈관 신장학 분야의 (새로운) 바이오마커에 이미징 결과를 연결하는 것도 흥미로울 것입니다. 예를 들어, 우리는 비암호화 RNA가 혈관 손상과 밀접하게 연결되어 있음을 입증했습니다[64,65]. 이러한 측정을 결합하면 새로운(인과 관계) 관계와 진단을 위한 새로운 가능성을 얻을 수 있습니다. 또한, 새로운 영상 기법이 단일 세포 RNA 시퀀싱 및 공간 전사체[53,66,67]와 같은 단일 세포 기반 기술의 최근 개발과 결합될 때 구성 및 역학에 대한 전례 없는 심층 분석을 가능하게 할 수 있습니다. 신장 혈관계의. 다음 섹션에서는 신장 미세혈관의 형태학적 및 기능적 측면을 조사하기 위해 이미 사용 가능한 생체 외 및 생체 내 이미징 양식을 요약합니다.
4.1. 엑스 비보
신장 미세혈관에 대한 우리의 많은 지식은 조직 생검의 포괄적인 생체외 분석에서 파생됩니다. 따라서 세포 기반 치료는 종종 조직 절단 및 염색에 의해 평가됩니다. 신장 혈관계에 대한 MSC의 치료 효과를 조사한 많은 연구가 있지만[68], 3D 구조를 조사하여 MSC 치료를 평가하기 위해 미세 컴퓨터 단층 촬영(micro-CT)과 같은 정교한 영상 기법을 활용한 연구 그룹은 거의 없습니다. 신장 혈관계 [69-74].
4.1.1. 마이크로 컴퓨터 단층 촬영(Micro-CT)
플래너리 등의 마이크로컴퓨터 단층촬영(micro-CT) 도입. [75] 1987년에 높은 공간 해상도로 질병 기전에 대한 지식을 얻기 위해 설치류의 온전한 혈관 구조를 연구하는 새로운 길을 열었습니다. 이 생체 외 양식은 신장 미세혈관 구조의 시각화와 사구체 수, 공간 분포 및 부피의 정량화를 가능하게 했으며, 이는 전체 기관의 병태생리학적 상태에 대한 지표로 사용될 수 있습니다[76]. 10, 243개의 복셀이 있는 하나의 3D 시야에서 해상도는 구심성 및 원심성 세동맥과 설치류 신장의 사구체 모세혈관을 시각화할 수 있습니다. 쥐에서는 21μm의 재구성된 복셀 크기가 사용되었고[77], 돼지에서는 40μm의 복셀 크기와 1.2mm의 스캔 시야로 신장 혈관계가 연구되었습니다[78]. 마이크로 CT 분야의 발전은 2mm의 스캔 시야 내에서 1μm의 복셀 해상도로 쥐의 네프론 혈관을 이미지화할 수 있는 기회를 제공했습니다[79].
Hillman et al.에 의해 개발된 정량화 기술을 기반으로 합니다. [80] 기존 CT를 사용하여 조직학적 조직 섹션을 기반으로 신장 혈관을 평가한 유사한 연구에 따라 서로 다른 신장 조직 구획 내의 혈관 구조 및 혈관 부피가 결정되었습니다[77]. 흥미롭게도 micro-CT와 같은 영상 기법을 적용하여 사구체 모세혈관 네트워크의 역할에 대한 기존의 사고 방식 외에도 세뇨관 주위 모세혈관과 병리학적 상태에 대한 관여를 조사하는 중요성이 높아졌습니다.
미세혈관 구조의 초기 구조적 변화는 미세 CT로 시각화하고 감지할 수 있으므로 신장 질환과 관련된 혈관 수준의 여러 분자 메커니즘이 미세 CT로 확인된 것은 놀라운 일이 아닙니다. 다낭성 신장 질환(PKD)과 같은 다양한 신장 질환 모델에서 17μm 복셀 크기의 해상도로 미세 CT에 의해 결정된 바와 같이 병리와 감소된 미세혈관 구조 사이의 상관관계가 설명되었습니다[81]. 더욱이, 고콜레스테롤혈증에서 증가된 피질 미세혈관 밀도가 진행성 신장 형태학적 손상의 초기 징후로 관찰되었다[78]. 만성 담관 결찰이 있는 랫드에서 미세 CT로 피질 관류 저하가 감지되었으며, 이는 추가 질병 진행과 함께 염분 및 수분 저류 장애를 설명할 수 있습니다[82]. 또한, 협착성 신장에서 증가된 산화 스트레스는 신장 미세혈관 재형성과 관련이 있으며, 만성 항산화 중재를 통한 치료 가능성을 제시하였다[83].
마이크로 CT의 주요 장점은 혈관 시스템의 방사상 기하학뿐만 아니라 축 방향도 정의할 수 있다는 것입니다[84]. 신장 혈관 구조를 3D로 시각화하는 것 외에도 미세혈관의 공간 밀도를 평가할 수 있으며[78,83] 다양한 해부학적 신장 구획에서 최대 80μm의 직경으로 혈관 밀도와 크기를 결정할 수 있습니다[77,78,83,85 ], 그리고 혈관의 비틀림이 관찰될 수 있다[83]. 더욱이, 사구체의 혈관 모세혈관 부피와 세뇨관 주위 모세혈관은 피질 내에서 구별되고 정량화될 수 있었습니다[82].
표준화된 정량화 프로토콜은 혈관 밀도와 직경을 결정하기 위해 구조적 수준에서 잘 정의된 피질 및 수질 구획 내의 미세혈관 변경을 조사하는 데 널리 사용되었습니다[77,82]. Ngoet al. [84]는 micro-CT와 광학현미경의 비교 연구를 수행하고 micro-CT로 획득한 신장 혈관 구조의 정량화가 실현 가능하고 정확한 기술이라고 결론지었습니다. 마이크로 CT와 비교하여 광학 현미경 영상의 유일한 부가 가치는 혈관벽을 시각화할 수 있는 가능성을 통해 동맥과 정맥을 구별할 수 있다는 것입니다. 그러나 마이크로 CT를 적용하여 쥐와 토끼의 직경이 각각 100 및 60 μm인 동맥을 3D로 시각화할 수 있었습니다. 그러나 10 µm보다 작은 크기의 혈관은 마이크로 CT로 제대로 식별할 수 없으므로 가장 작은 신장 모세혈관까지 포착하기 위해서는 면역조직화학으로 되돌아갈 필요가 있다[85].
4.1.2. 라이트 시트 형광 현미경(LSFM)
광시트 형광현미경(LSFM)의 도입으로 오늘날에는 대용량의 고해상도 이미징이 합리적인 시간 내에 달성될 수 있습니다[86,87]. LSFM의 가용성을 통해 관심은 조직을 단면화한 다음 미세혈관을 염색하는 것을 포함하는 일상적으로 적용되는 기존의 조직학적 기술에서 조직 전체를 이미징하는 방향으로 옮겨졌습니다. 체적 분석은 조직의 선택된 부분을 검사할 뿐만 아니라 혈관 구조 및 거동의 동적 특성도 3D 보기에서 보존되기 때문에 유리합니다.
3D 정보를 유지하기 위해 다양한 광학 조직 제거(OTC) 프로토콜을 통해 생물학적 표본을 투명하게 만들어 추가 FL 형광 염색을 위한 광 산란 및 광 흡수를 최소화합니다[87]. 최근 몇 년 동안 OTC 방법은 3D 이미징이 LSFM의 현대적인 발전으로 인해 온전한 장기를 연구할 수 있는 기회를 제공하기 때문에 인기를 얻었습니다. 3D에서 세포 수준의 해상도를 가진 온전한 기관 또는 전체 동물의 구성은 몇 분 이내에 획득할 수 있습니다[88]. 그러나 공초점 FL 형광 현미경과 비슷한 해상도를 가진 LSFM은 신호 대 잡음비가 2배 더 우수하여 FL 형광단 표백 및 광독성을 극적으로 줄여 OTC에 필요한 대규모 이미징 처리를 가능하게 합니다[89]. 추가적인 장점은 기록된 프레임 수와 기록 속도가 더 빠른 반면 전체 이미징 기간은 훨씬 짧다는 것입니다.
LSFM이 도입된 이후로 여러 종에서 파생된 다양한 조직 표본 및 기관에 대해 여러 OTC 프로토콜이 개선되고 개선되었습니다. 지난 몇 년 동안 에틸 신나메이트(ECi)에 의한 무독성 솔벤트 기반 청소가 쥐의 신장을 청소하는 데 널리 적용되었습니다[88,90,91]. 이 프로토콜은 예를 들어 선구적인 프로토콜인 CLARITY(투명한 지질 교환 아크릴아마이드 하이브리드 경질 이미징), CUBIC(투명하고 방해받지 않는 뇌/신체 이미징 칵테일 및 컴퓨터 분석) 및/또는 DISCO(3차원 이미징 용제 제거된 기관), 그러나 낮은 양의 자가형광이 남아 있는 비교적 합리적인 신장 청소를 제공합니다. SHANEL(작은 미셀 매개 인간 장기의 효율적인 제거 및 라벨링)이라는 새로운 조직 투과화 접근법으로 전체 인간 신장을 성공적으로 제거한 Ertürk와 동료들이 놀라운 작업을 수행했습니다. 피질 구역은 직경 221 ± 37 mm의 사구체 모세혈관을 포함하는 약 2742 ± 665 mm(평균 ± SD)의 치수를 갖는 것으로 결정되었고, 구심성 세동맥의 직경은 71 ± 28 mm였습니다. 또한 VesSAP(vessel segmentation & analysis pipeline)라고 하는 OTC 이후의 신경 혈관계를 정량화하기 위한 고도로 정교한 딥 러닝 기반 프레임워크가 신경 과학 분야에서 개발되었습니다[93].
최근 몇 년 동안 OTC 분야에서 많은 발전이 이루어졌음에도 불구하고 내인성 FL 형광단의 발현이 대부분 만족스럽게 보존되지 않아 형질전환 동물의 사용을 제한하는 몇 가지 단점이 남아 있습니다. 그러나 주요 관심사는 조직의 형태학적 크기와 결과적으로 혈관 구조가 OTC에 필요한 가혹한 용매에 의해 변경된다는 것입니다. 또한 LSFM이 생성하는 엄청난 양의 데이터는 적절한 데이터 저장 및 처리뿐만 아니라 정량적 분석에도 여전히 과제로 남아 있습니다[87].
간단히 말해서, 마이크로 CT 또는 SFM과 같은 기술을 적용하는 한 가지 중요한 이점은 공간 혈관 분포를 캡처할 수 있고 혈관 네트워크의 구조적 희박화가 거의 모든 신장 모세혈관 구조를 이미지화하기에 적합한 해상도로 식별된다는 것입니다. 그러나 두 기술 모두 고정이 필요하므로 생체 외에서만 수행할 수 있습니다. 신장 미세혈관의 형태학적 및 기능적 변경을 모니터링하려면 생체 내 시간 이미징 전략이 필요합니다.
4.2. 생체 내
생체 내 영상화 방식의 적용은 실시간으로 세포 기반 치료를 평가하고 혈관 수준에 대한 가능한 치료 효과를 검증할 수 있는 기회를 제공할 것입니다. 결과적으로, 생체내 생체의학 이미징 분야의 발전은 신장 혈관계에 대한 MSC 기반 효과 연구를 위해 시급합니다. 다광자현미경(MPM)[94], CT[95,96], 자기공명영상(MRI)[95-97]을 활용하여 MSC 작용을 조사하기 위해 생체 내 이미징을 적용한 연구는 매우 많습니다.
4.2.1. 다광자 현미경(MPM)
다광자 현미경(MPM)은 1995년에 사용 가능하게 된 초점 평면 내에서만 둘 이상의 광자의 동시 흡수에 의존합니다[98]. 동적 과정은 세포 수준에서 생체 내에서 시각화될 수 있으며, 신장 혈관 혈류를 연구하는 것 외에도[63], MPM은 다양한 신장 미세혈관 세그먼트를 실시간으로 모니터링할 수 있는 기회를 제공합니다. 고해상도로 구심성 및 원심성 세동맥과 사구체 모세혈관을 시각화할 수 있습니다. 기술적으로 골수 미세순환에 접근하는 것이 가능하지만 침투 깊이로 인해 여전히 문제로 남아 있습니다[98]. 그러나 대략적인 직경이 100 μm인 전체 사구체를 시각화하고 세포 수준에서 동적 프로세스에 액세스하는 것이 가능합니다.
중요하게도, 생체 내 미세혈관 누출은 MPM에 의한 섬유성 신장의 Evans blue extravasation을 통해 시각화되고 정량화될 수 있습니다[99]. 관류된 모세관의 수를 정량화했으며 직경은 10μm보다 훨씬 아래로 결정되었습니다. 최근 우리 연구 그룹은 MPM을 적용하여 인간 만능 줄기 세포(hPSC) 유래 신장 오르가노이드가 신장 피막 이식 후 마우스의 기존 신장 혈관계와 기능적 연결을 형성한다는 생체 내 증거를 제공했습니다[100,101].
MPM의 장점은 초점이 맞지 않는 FL 형광이 없고 초점 영역 내에서 제한된 광표백이 없다는 것입니다[98]. 그러나 단점 중 하나는 생체 내에서 신장 혈관계에 접근하기 위해 복부 영상 창을 적용해야 하는 제한된 영상 깊이이다[102,103]. 이 복부 창은 최대 한 달 동안 몇 주 동안 생체 내 이미징을 허용합니다. 그러나 이러한 이미징 창을 삽입하려면 침습적 수술이 필요하며 염증의 가능성이 있습니다. 더욱이, 이미징 윈도우가 때때로 손실되고 조직 괴사가 발생할 수 있다[102]. 분명히, 이 영상 양식은 임상 실습으로 번역할 수 없습니다.
임상 실습에 휴대용 생체 현미경(HVM)이 도입된 이후로 침상에서 비침습적으로 모세혈관 혈류를 모니터링하는 흥미로운 대안이 달성될 수 있습니다[104]. 이 이미징 방식이 사이드스트림 및 입사 암시야 비디오 현미경과 같이 완전히 다른 기술을 기반으로 하지만 표면에 위치한 모세관에 대한 실시간 평가를 제공합니다. MicroTools 소프트웨어 패키지로 알려진 새로운 임상 구현 알고리즘은 혈관 신생, 혈관 확장/수축, 체액 균형에 접근하기 위한 총 및 관류 혈관 밀도의 자동화된 미세혈관 영상 분석을 가능하게 할 뿐만 아니라 모세관 헤마토크릿 및 적혈구 속도를 기반으로 하는 산소 전달 능력을 가능하게 합니다[105 ]. 그러나 신장 미세혈관 구조를 연구하기 위해 이러한 방식은 제한된 침투 깊이로 인해 적합하지 않습니다.
4.2.2. 컴퓨터 단층촬영(CT)
CKD로의 질병 진행에서 미세혈관의 역할을 결정하기 위해 신장 미세혈관의 형태학적 및 기능적 변경을 모니터링하고 정량화할 수 있는 비침습적 영상 기법이 매우 요구됩니다. 모세혈관 희박과 신섬유증의 진행 사이의 인과관계는 수년 동안 인식되어 왔음에도 불구하고 Ehling et al. [3]은 CKD 진행 중 해부학적 및 기능적 혈관 변화에 대한 비침습적 정성적 및 정량적 분석을 최초로 수행했습니다. 신장 혈액량의 점진적인 감소는 진행성 신장 섬유증, 즉, 허혈-재관류 손상(IRI), 일측성 요관 폐쇄 및 Alport 마우스가 있는 3개의 뮤린 모델에서 생체내 대조 강화 마이크로 CT에 의해 관찰되었습니다. 미세혈관의 기능적 변화 외에도 세뇨관 주위 혈관 손실은 세 가지 CKD 마우스 모델 모두에서 섬유성 조직 형성과 관련이 있습니다. 그러나 분기점, 혈관 직경 및 비틀림에 대한 정보를 얻으려면 생체 외 미세 CT가 필요했으며, 이는 세포 해상도에 가까운 생체 내 미세 혈관에 대한 액세스를 제공하는 새로운 생물 의학 이미징 기술의 필요성을 나타냅니다.
CT의 주요 장점은 신장 혈관 구조의 시각화가 합리적인 해상도로 몇 분 이내에 획득되어 혈관 조직에 대한 3D 정보를 제공한다는 것입니다. 요오드 기반 조영제를 사용하면 대비가 향상되고 미세혈관 구조가 훨씬 더 자세히 묘사됩니다. 최근에는 생리학적 및 병리학적 조건에서 쥐의 신장을 미세 CT로 측정하여 정성적 및 정량적 평가가 혈관 내 조영제를 향상시키기 위해 PTA(phosphotungstic acid)를 관류하여 개선되었습니다[106]. 동맥과 정맥을 명확하게 구분할 수 없다는 한계점에도 불구하고 in vivo에서 40μm의 voxel 크기와 ex vivo에서 12.5μm의 voxel 크기로 조직을 아치형 혈관 수준까지 포착했습니다.
그러나 CT를 사용하여 신장 질환을 모니터링하는 것의 또 다른 주요 단점은 요오드화된 방사선 조영제를 사용해야 한다는 것입니다. 이러한 조영제는 신독성을 유발하는 것으로 알려져 있으며, 이는 기존의 신장애 환자에게 임상적용이 금지된다[107-109]. 투여된 조영제로 인한 신장의 급성 손상은 신장 혈역학을 변경하고 신장 미세혈관 희박화를 조사할 때 특히 바람직하지 않은 골수성 저산소증을 유발합니다. 유사하게 MRI에서 널리 사용되는 가돌리늄계 조영제는 신장에서 제거되어 신장애를 일으키는 것으로 보인다[110].
4.2.3. 자기공명영상(MRI)
MRI는 1980년대에 임상 실습에 도입되었으며 즉시 가장 많이 사용되는 영상 기술 중 하나가 되었습니다[111]. MRI는 강한 자기장을 가하는 비침습적 비이온화 영상기법으로 T1, T2 조영제의 변형을 이용하여 혈액의 이완성을 감지할 수 있다. 또한 자기공명혈관조영술(MRA)은 가돌리늄 기반 조영제를 활용하여 작은 동물의 혈관 구조를 시각화합니다. 그러나 MRA의 가장 큰 단점은 필요한 조영제의 사용이 어렵다는 것입니다. 다행히도 신관류는 이점과 한계를 모두 제공하는 조영제의 필요 여부와 관계없이 결정할 수 있습니다[112].
조영제를 사용하지 않고 스핀 라벨링은 내인성 물을 확산성 추적자로 활용하여 수질 통과 시간이 캡처하기에는 너무 길기 때문에 신장 피질 내에서 관류를 정량화할 수 있습니다. 또한, 신장 혈류를 결정하기 위해 한 방향을 따라 스핀의 위상 이동이 측정되는데, 이는 정확한 측정을 달성하기 위해 관심 동맥을 향한 수직 영상 평면이 필요함을 의미합니다[112]. 따라서 이 기술이 작은 피질 모세혈관은 말할 것도 없고 신장 동맥을 시각화할 때 큰 도전을 제공한다는 것은 놀라운 일이 아닙니다.
혈관 기능은 MR-관류로 RBF를 정량화하고 혈액 산소 수준 의존적 조영제(BOLD) 영상으로 산소 상태를 모니터링하여 결정할 수 있습니다[112,113]. 그러나 기능적 MRI의 주요 한계는 간이나 장에 비해 움직임 인공물에 덜 민감하지만 신장을 비롯한 호흡 운동의 영향을 받는 기관에서 신뢰할 수 있고 재현 가능한 결과를 얻는 것입니다[112]. 1.5 Tesla 기능 MRI 수행 타당성 연구가 복셀 단위 정량화를 수행할 때 큰 가능성을 제공했음에도 불구하고[114], 관류 이상은 경미한 혈관 변화가 충분히 감지될 수 있는지에 대한 의문을 제기하는 병리학적 영역에서만 감지될 수 있었습니다. 자기장 강도가 3인 MRI 스캐너가 도입되면서{13}} Tesla에서 신호 대 잡음비가 크게 향상되었지만[115,116], 획득한 해상도는 여전히 문제로 남아 있습니다.
MRI가 제공하는 해상도는 주로 자기장 강도에 따라 달라지며 펄스 시퀀스를 조정하여 주어진 자기장에 최적화할 수 있습니다[111]. 공간 분해능은 주로 빠른 획득 시간을 요구하고 일반적으로 픽셀 크기에서 3 × 4mm의 분해능을 달성하는 신호 대 잡음비에 의해 제한됩니다[117]. 7 Tesla의 높은 자기장이 가해지면 BOLD로 얻을 수 있는 최상의 해상도는 약 500 µm입니다. 만족스럽지 못한 해상도와 대부분의 동적 프로세스를 시각화하는 데 한계가 있는 것 외에도 MRI는 높은 비용과 연결되고 특수 시설 및 유지 관리가 필요하다는 또 다른 주요 단점이 있습니다.
4.2.4. 초음파
초음파의 발전은 구조적 및 기능적 신장 미세혈관 변화의 비침습적 모니터링을 위한 패러다임 전환을 도입했으며 비교적 저렴한 비용으로 휴대용 시스템으로 작은 혈관을 탐색할 수 있는 새로운 길을 열었습니다. 1시간 동안 심한 관류저하로 인한 급성 허혈 쥐 모델에서 색과 펄스파(PW) 도플러 초음파를 이용하여 실시간으로 신장 혈류를 평가하였다[118]. 컬러 도플러 영상은 또한 궁형 동맥의 상대적으로 작은 크기와 혈류를 계산하고 도플러 각도 보정을 적용하는 데 필요한 동맥 흐름을 포착하기 위한 수직 프로브 위치로 인해 궁형 동맥을 시각화하는 데 어려움이 있음을 보여주었습니다. 그러나 혈류 속도는 신장내 동맥, 즉 분절, 엽간 및 궁상 동맥에서만 계산할 수 있습니다. 따라서 기존의 초음파가 제공하는 해상도의 한계로 인해 미세순환에 대한 정보를 얻을 수 없었습니다.
초고속 도플러 초음파 기술의 도입으로 라인당 주사선을 스캔하는 것보다 하나의 전체 시야에서 동시에 높은 프레임 속도로 여러 개의 동기파를 보내는 초점 없는 파동 전송으로 더 큰 해상도를 얻을 수 있습니다. 집중된 빔 전송 [119]. 이 평면파 전송은 초고속 도플러 초음파 영상의 기본 개념이며 직경이 1mm 미만인 이식된 인간 신장의 피질 혈관을 감지할 수 있게 해줍니다[120]. 또한, 초고속 도플러 초음파는 전임상 연구에서 신장 미세혈관 희박화를 모니터링하는 매우 유리한 생체 내 기술을 제공합니다(그림 3A). 초고속 도플러 초음파의 발전에도 불구하고 모세혈관 수준에 대한 접근은 여전히 조영제를 사용하는 데 의존합니다[121]. 그럼에도 불구하고, 특히 종종 신독성을 나타내는 CT 및 MRI 조영제와 비교하여 Doppler 초음파에 조영증강제를 사용할 때 언급할 만한 안전 문제는 없습니다[122]. 그러나 쥐의 신장 혈관계의 놀라운 해상도는 생체 내에서 달성할 수 있습니다(그림 3B).
ULM(Ultrasound localization microscopy)은 한편으로는 초고속 도플러 초음파 이미징을 적용하고 다른 한편으로는 가스가 채워진 미세 기포 형태의 초음파 조영제를 사용하여 공간 해상도와 침투 깊이 간의 균형을 해결했습니다. [121,123,124]. 그 중에서도 Errico et al. [123]은 두께가 약 10mm인 쥐 뇌의 전체 깊이에 걸쳐 직경 10μm의 두개골 미세혈관을 이미지화하기 위해 ULM을 제안했습니다. 최근 간행물에서 Demené et al. [125]는 정맥 주사된 미세 기포를 개별적으로 추적하여 초고해상도 영상을 개선하고 최대 25μm의 혈관 해상도를 가능하게 함으로써 인간 두뇌 깊숙이 있는 미시적 수준에서 뇌혈관 혈류 역학을 포착할 수 있었습니다. 이 놀라운 성과를 파악하려면 다른 어떤 비침습적 이미징 방식도 생체 내 미세혈관 구조를 밀리미터 단위 이하로 시각화할 수 없다는 점을 언급하는 것이 중요합니다. 생체 내에서 이 놀라운 공간 해상도에 도달하기 위해 극복해야 할 두 가지 주요 과제가 있었습니다: 두개골 수차와 모션 인공물. 신장과 같은 복부 장기에 대한 ULM의 적용은 뼈 구조의 이상에 의해 방해받지 않지만 운동 인공물은 큰 어려움을 나타냅니다. 그러나 최근의 생체 내 연구는 ULM으로 신장 혈관계를 영상화하려는 첫 번째 시도를 성공적으로 제공했습니다[5,126,127].

쥐의 신장 내 다른 혈관 구획을 구별할 수 있었고, 미세 기포를 적용하여 해상도를 증가시켜 서로 400μm의 거리로 분리된 직장 정관의 얇은 혈관 다발을 시각화했습니다[5]. 또한, 신장 미세혈관의 흐름과 관련된 축 방향 혈액 속도, 즉 2mm/s 미만은 20μm보다 작은 혈관 직경에 도달할 수 있는 직경 1μm의 주입된 미세 기포를 추적하여 추정되었습니다. Song et al. [127] 토끼의 신피질 미세혈관을 이미지화했으며 직경 76μm의 생체 내에서 혈관을 명확하게 분리할 수 있었습니다. 호흡 운동은 교정될 수 있지만 평면 외 운동 인공물은 여전히 도전적이고 이미징 정보를 완전히 획득할 수 없기 때문에 교정이 불가능합니다[5].
최근 AKI에서 CKD로의 진행은 편측 IRI의 마우스 모델에서 조영제 강화 초고속 도플러 초음파에 의해 연구되었습니다[6]. 미세 기포를 주입하여 32μm의 작은 신장 혈관을 확인하고 신장의 혈관 변화, 즉 신장 혈액량, 혈관 밀도 및 비틀림을 정량화했습니다. 생체 내 이미징 동안 초음파로 획득한 피질 및 피질수질 접합부의 혈관 밀도는 혈관 생물학에서 황금 표준으로 인식되는 CD31 면역염색 후 얻은 정량화와 일치했습니다. 이것은 Cao et al.에 의해 수행된 또 다른 연구와 일치합니다. AKI 중증도는 미세 기포 주입을 통한 조영증강 초음파에 의해 결정될 수 있음을 설명했습니다. 생체내 신장 관류 측정은 조직학적 수준에서 결정된 신장 손상과 밀접한 상관관계가 있습니다.
이러한 초음파 연구에 따르면 Hueper et al. [7] 이전에 신장 관류가 MRI에 의해 결정된 AKI에서 CKD로의 진행을 예측할 수 있다고 제안했습니다.
신장 혈관계의 미세 기포 강화 초음파 영상은 이미 인간에서 신장 미세 혈관 관류를 결정하는 데 성공적으로 수행되었으며 진단에 대한 훌륭한 전망을 보여주었습니다 [129-133]. 흥미롭게도, 이 영상 양식은 급성 거부 반응을 예측하기 위한 적절한 비침습적 판독값을 제공할 수 있는 신장 동종이식편의 관류 상태를 결정하기 위해 신장 이식에 적용되었습니다[134]. 초음파 활용 시 제약이 될 수 있는 시술자 의존성 외에도 두 독자 사이에 관찰자 간 합의의 강도가 매우 높아 임상 현장에 적용할 때 실현 가능성이 높다[132]. 휴대성, 시간 절약형 및 간단한 맞춤형 응용 프로그램으로 인해 조영제 강화 미세 기포가 있는 초음파는 임상 실습, 특히 ICU 환자에서 신장 미세혈관을 평가하는 데 훌륭한 관점을 제공합니다[135]. 따라서 이 기술은 고정밀로 강력한 미세 기포 추적을 위한 복부 운동 인공물의 교정을 성공적으로 마스터한 후 임상 실습으로의 번역에 대한 큰 가능성을 제공합니다.
5. 결론 및 전망
신장 혈관 구조의 현저한 이질성은 복잡한 기능적 다양성과 구획화를 반영하며, 논리적인 결과로 미세혈관 변경 및 희박화를 연구하려면 정교한 이미징 양식이 필요합니다. 신장 혈관 질환을 연구하기 위한 생체 내 이미징 방식의 개발, 적용 및 개선은 혈관 수준에서 MSC와 같은 세포 요법의 작용에 대한 더 큰 이해를 제공하고 질병 진행 중에 모니터링할 수 있는 특정 바이오마커를 해명할 수 있습니다.

참고문헌
1. Chade, AR 신장 혈관 구조 및 희박화. 비교 생리. 2013, 3, 817–831. [교차 참조] [PubMed]
2. Chade, AR 소형 혈관, 큰 역할: 신장 미세순환 및 신장 손상의 진행. 고혈압 2017, 69, 551–563. [교차 참조] [PubMed]
3. Ehling, J.; Bábícková, J.; 그렘세, F.; 클링해머, 비엠; Baetke, S.; Knochel, R.; 키슬링, F.; Floege, J.; Lammers, T.; Boor, P. 진행성 신장 질환에서 혈관 기능 장애의 정량적 마이크로 컴퓨터 단층 촬영 영상. 제이엠 사회 네프롤. 2016, 27, 520–532. [교차 참조] [PubMed]
4. 첸, TK; 다행스럽게도, DH; 그램, ME 만성 신장 질환 진단 및 관리: 검토. 생리. 행동 2019, 322, 1294–1304. [교차 참조] [PubMed]
5. 푸아레, J.; Zhang, H.; Ilovitsh, T.; Mahakian, L.; 탐, 에스.; Ferrara, KW 초음파 국소화 현미경으로 쥐 신장의 미세혈관을 이미지화하고 평가합니다. 과학. 대표 2017, 7, 13662. [CrossRef] [PubMed]
6. 첸, 큐. 유, J.; 러쉬, 비엠; 스토커, SD; 탄, RJ; Kim, K. Kidney Int. 2020, 98, 355–365. [교차 참조] [PubMed]
7. Hueper, K.; Gutberlet, M.; Rong, S.; Hartung, D.; Mengel, M.; 루, X.; 할러, H.; Wacker, F.; 마이어, M.; Gueler, F. 급성 신장 손상: 마우스의 신장 관류 손상을 모니터링하기 위한 동맥 회전 라벨링 - 조직병리학적 결과 및 신장 기능과의 비교. 방사선과 2014, 270, 117–24. [교차 참조]
8. 레비, BI; Schiffrin, EL; 무라드, JJ; Agostini, D.; Vicaut, E.; 사파르, ME; Struijker-Boudier, HA 고혈압, 비만 및 당뇨병에 흔한 병리학적 손상 조직 관류. 발행부수 2008, 118, 968–976. [교차 참조]
9. Carmeliet, P.; Jain, RK 혈관 신생의 분자 메커니즘 및 임상 적용. 네이처 2011, 473, 298–307. [교차 참조]
10. 몰레마, 지. Aird, WC 신장의 혈관 이질성. 세미. 네프롤. 2012, 32, 145–155. [교차 참조]
11. Armulik, A.; Abramson, A.; Betsholtz, C. 내피/주위 세포 상호 작용. 순환 해상도 2005, 97, 512–523. 03.16652.d7. [교차 참조]
12. Attwell, D.; Mishra, A.; 홀, CN; O'Farrell, FM; Dalkara, T. pericyte는 무엇입니까? J. 세렙. 혈류 대사. 2016, 36, 451–5. [교차 참조]
13. 에반스, RG; 조지아주 에펠; 앤더슨, WP; Denton, KM 신장 수질과 피질에서 혈류의 차등 제어의 기초가 되는 메커니즘. J. Hypertens. 2004, 22, 1439-1451. [교차 참조]
14. 팔로네, TL; 실도르프, EP; Turner, MR 신내 혈류: 미세혈관 해부학 및 수질 관류 조절. 클린. 특급 파마콜. 생리. 1998, 25, 383–392. doi:10.1111/j.1440-1681.1998.tb02220.x. [교차 참조]
15. 팔론, TL; 에드워즈, A.; Mattson, DL 신장 수질 순환. 비교 생리. 2012, 2, 97–140. [교차 참조] [PubMed]
16. Guerci, P.; Ergin, B.; Ice, C. 신장의 거대 및 미세 순환. 베스트 프랙티스. 해상도 클린. 마취. 2017, 31, 315–329. [교차 참조]
17. Shaw, I.; 라이더, S.; 멀린스, J.; 휴즈, J.; Péault, B. 신장 혈관계의 Pericytes: 건강과 질병의 역할. Nat. 네프롤 목사. 2018, 14, 521–534. [교차 참조]
18. 로시발, 엘.; Peti-Peterdi, JJ 구심성 세동맥의 이질성 - 형태와 기능 간의 상관관계. 네프롤. 다이얼. 이식. 2006, 21, 2703–2707. [교차 참조]
19. Stefanska, A.; 케년, 시.; 크리스티안, HC; 버클리, 시.; 쇼, 나.; 멀린스, JJ; Péault, B. 인간의 신장 혈관주위세포는 레닌을 생성합니다. 신장 국제 2016, 90, 1251–1261. [교차 참조]
20. Schlondorff, DO 진행성 신장 질환의 병태생리에 기여하는 요인의 개요. 신장 국제 2008, 74, 860–866. [교차 참조]
21. 팔론, TL; Zhang, Z.; Rhinehart, K. 신장 수질 미세 순환의 생리학. 이다. J. Physiol. 렌. 생리. 2003, 284, F253–66. [교차 참조] [PubMed]
22. Palone, TL 복잡한 혈관 다발, 두꺼운 오름차순 사지 및 아쿠아포린: 외부 수질을 짜내십시오. 이다. J. Physiol. 렌. 생리. 2014, 306, 505–506. [교차 참조] [PubMed]
23. 짐머하클, BL; 로버트슨, CR; Jamison, RL 수질 미세 순환. 신장 국제 1987, 31, 641–647. [교차 참조] [PubMed]
24. Dumas, SJ; 메타, 이.; Borri, M.; 루오, Y.; 리, X.; Rabelink, TJ; Carmeliet, P. 표현형 다양성 및 대사. Nat. 네프롤 목사. 2021, 1–24. [교차 참조]
25. Dumas, SJ; 가르시아-카바예로, M.; Carmeliet, P. 뚜렷한 내피 표현형의 대사 서명. 동향 내분비. 메타브. 2020, 31, 580–595. [교차 참조]
26. Jourde-Chiche, N.; Fakhouri, F.; Dou, L.; Bellini, J.; 벌리, 에스.; 형식, M.; 자롯, PA; 카플란스키, G.; 르 퀸트렉, 엠.; Pernin, V.; et al. 신장 건강과 질병에서 내피 구조와 기능. Nat. 네프롤 목사. 2019, 15, 87–108. [교차 참조]
27. Long, DA; 노먼, JT; 파인, LG 만성신장질환을 치료하기 위해 신장 미세혈관을 복원합니다. Nat. 네프롤 목사. 2012, 8, 244–250. [교차 참조]
28. 최용재; 차크라보르티, 에스.; Nguyen, V.; Nguyen, C.; 김, BK; 심씨; 수키, WN; Truong, LD 세뇨관 주위 모세혈관 손실은 인간 신장의 만성 세뇨관 간질 손상과 관련이 있습니다. 혈관 내피 성장 인자의 발현 변경. 흠. 패톨. 2000, 31, 1491-1497. [교차 참조]
29. Ishii, Y.; 사와다, T.; Kubota, K.; 후치노우에, S.; 테라오카, 에스.; Shimizu, A. 만성 동종이식 신병증의 발달로 인한 세뇨관 주위 모세혈관의 손상 및 진행성 상실. 신장 국제 2005, 67, 321–332. [교차 참조]
30. Seron, D.; Alexopoulos, E.; 래프터리, MJ; Hartley, B.; Cameron, JS 단클론 항체에 의해 평가된 간질 모세관 단면의 수: 간질 손상과의 관계. 네프롤. 다이얼. 이식. 1990, 5, 889–893. [교차 참조]
