그룹 A 연쇄상 구균 감염의 병인, 역학 및 통제
Oct 09, 2023
화농성 연쇄구균(그룹 A연쇄상 구균; GAS)는 인간 숙주에 절묘하게 적응하여 무증상 감염, 인두염, 농피증, 성홍열 또는 침습성 질병을 유발하고 감염 후 면역 후유증을 유발할 가능성이 있습니다. GAS는 감염에 대한 선천적 면역 반응과 적응성 면역 반응을 모두 방해하여 숙주 내에서 식민지화, 전파 및 전파를 허용하는 다양한 독성 결정 요인을 배포합니다. 전 세계적으로 변동하는 GAS 역학은 새로운 GAS 클론의 출현을 특징으로 하며, 종종 감염 틈새 시장에 더 잘 적응하거나 숙주 면역을 회피하는 새로운 병독성 또는 항균 결정 요인의 획득과 관련이 있습니다. 최근의 아이디어페니실린 민감도가 감소하고 마크로라이드 내성이 증가하는 임상 GAS 분리균의 확인은 최전선 항생제 치료와 페니실린 보조 항생제 치료 모두를 위협합니다. 세계보건기구(WHO)는 GAS 연구 및 기술 로드맵을 개발하고 선호하는 백신 특성을 설명하여 안전하고 효과적인 GAS 백신 개발에 대한 새로운 관심을 불러일으켰습니다.

한약재 시스탄체 식물-항종양
소개
화농성 연쇄상구균(Group A Streptococcus; GAS)은 인두염, 농가진과 같은 양성 인간 감염을 비롯하여 패혈증, 연쇄상 구균 독성 쇼크 유사 증후군(STSS) 및 괴사 성 근막염. 반복적인 GAS 감염은 류마티스성 심장 질환(RHD)으로 이어질 수 있는 류마티스열을 포함한 자가면역 후유증을 유발할 수 있습니다1. 역학적으로 GAS는 220mm 이상의 유형으로 분류될 수 있으며2(표면에 노출된 M 단백질의 아미노 말단의 유전자 서열을 기준으로) 지역적 및 전체적 분포 패턴이 서로 다릅니다3. 최근 역학 조사를 통해 아시아와 영국4-7에서 성홍열의 다클론성 발병이 발견되었으며4-7 영국의 발병은 침습성 감염의 급증과 병행되었습니다4. 숙주에 적응된 인간 병원체로서 GAS의 생존에는 끊임없는 전파 주기, 일차 감염 부위(피부 또는 목)에 대한 부착, 집락화 및 증식, 선천성 및 적응성 면역 체계에 대한 방어, 그리고 후속적으로 새로운 숙주로의 전파가 필요합니다. 숙주 방어 메커니즘을 조작하기 위해 GAS가 사용하는 새로운 독성 전략이 발견되고 있습니다. 예를 들어, GAS 프로테아제 연쇄상 구균 발열성 외독소 B(SpeB)에 의한 가스더민 A(GSDMA)의 절단은 숙주 세포 발열증을 유발하는 것으로 밝혀진 반면8,9 점막 관련 불변 T 세포(MAIT 세포)는 최근에 매우 높은 것으로 확인되었습니다 STSS 환자에서 활성화되며 이 질병과 관련된 사이토카인 폭풍의 주요 원인으로 작용합니다. 상업용 GAS 백신이 없는 경우, GAS에 대한 의학적 개입은 감염을 치료하거나 예방하기 위해 항생제를 사용하는 것입니다. 그러나 GAS 항생제 내성이 증가하고 있으며 페니실린 감수성을 감소시키는 첫 번째 돌연변이가 보고되었습니다11-15; 그럼에도 불구하고 GAS는 여전히 α-락탐 항생제에 취약합니다. GAS 백신 개발을 촉진하기 위해 세계보건기구(WHO)는 GAS 연구 및 기술 로드맵을 개발하고 선호하는 제품 특성을 설명했습니다16. 글로벌 GAS 인구 구조를 정의하고 백신 항원 적용 범위를 예측하기 위해 대규모 유전체학이 적용되었습니다17. M 단백질 및 비 M 단백질 항원에 대한 새로운 GAS 백신 제제가 개발 중입니다18. GAS 인두염의 비인간 영장류 모델은 최근 GAS 백신 효능을 평가하는 데 사용되었으며19 GAS 인두염의 통제된 인간 감염 모델(CHIM)의 개발은20 인간 숙주에서 백신 효능을 평가할 수 있는 향후 기회를 제공합니다. 지난 10년 동안 GAS 연구 분야는 큰 발전을 이루었지만, 새로운 실험적 감염 모델 및 치료 전략의 지속적인 개발, 백신 개발 노력의 활성화, 적극적인 감시 노력에도 불구하고 GAS 질병에 대한 전 세계적 부담은 여전히 충족되지 않은 대중으로 남아 있습니다. 건강 도전. 다제내성 균주와 새로운 독성 GAS 클론의 출현과 보급은 인간 GAS 감염을 예방하거나 치료하기 위한 공중 보건 전략을 개선해야 할 긴급한 필요성을 강조합니다. GAS 감염의 역학적, 임상적, 분자적 측면을 모두 다루는 것은 이 리뷰의 범위를 벗어나므로 여기서는 가장 최근의 연구 개발 및 발전에 중점을 둡니다.
GAS로 인한 질병
정교하게 인간에 적응된 병원체인 GAS는 광범위한 질병 발현을 일으킬 수 있습니다. 표 1은 GAS와 관련된 가장 흔한 질병을 설명하지만 다른 관련 질병으로는 중이염, 부비동염, 수막염, 심내막염, 폐렴, 복막염 및 골수염이 있습니다1. GAS로 인해 매년 50만 명이 사망하고 RHD와 침습성 감염이 대부분의 사망 원인인 것으로 추산됩니다21. 최근 추정치는 GAS 감염으로 인한 상당한 건강 부담을 강조하여 RHD가 10백만 이상의 장애 조정 수명에 책임이 있으며 0.1%는 어린이의 GAS 인두염에 기인한다고 제안합니다22. 이러한 추정치는 다른 GAS 질병에 대해서는 결정되지 않았으며, 특히 저소득 및 중간 소득 국가의 역학 데이터는 여전히 부족합니다. 호주와 뉴질랜드의 연구에 따르면 봉와직염은 RHD 이상에서도 이러한 환경에서 모든 GAS 질병 중 가장 높은 건강 및 경제적 부담을 초래하는 것으로 나타났습니다23. 종합적으로, 모든 GAS 관련 질병의 건강 및 경제적 부담에 대한 전 세계적 추정치는 여전히 잘 이해되지 않고 있으며, 전 세계적으로 이 병원체의 영향을 이해하기 위해서는 질병 데이터의 더 나은 부담이 시급히 필요하다는 점을 강조합니다. 지난 10년 동안 WHO의 중요한 옹호 운동은 RHD와 RHD가 전세계적인 질병 부담에 미치는 영향, 이미 취약한 인구 집단의 사회적 불평등 심화에 대한 인식을 높였습니다24,25. 또한, 미국과 이스라엘의 연구에서는 RHD가 고소득 국가에서도 여전히 중요한 공중 보건 문제임을 강조했습니다26. 그럼에도 불구하고, 이 질병에 대한 우리의 지식에는 여전히 중요한 격차가 있습니다. 동시 피부 감염과 면역 후유증 발생 사이의 연관성에 대한 가설을 뒷받침하는 강력한 증거를 생성하기 위한 과학적 노력이 진행 중입니다27,28. 20세기 말까지 사실상 사라졌던 성홍열은 최근 중국, 홍콩, 한국, 싱가포르, 영국에서 발병이 보고되면서 다시 등장했습니다4,5,29-31. 현재까지, 발병 균주는 주로 다중클론이며, 특히 아시아에서 외독소를 함유하고 테트라사이클린 및 마크로라이드에 대한 다약제 내성을 부여하는 이동성 유전 요소의 운반과 같은 뚜렷한 역학적 지표와 연결되어 있습니다6. 성홍열과 유사한 전염병 클론은 다른 여러 지역에서도 발견되었습니다32,33. 경미한 질병을 앓고 있는 환자와 취약한 밀접 접촉자가 침습성 감염의 위험이 더 크다는 연구 결과가 나온 점을 고려하면, GAS 질병을 추적하기 위한 더 나은 지역 및 글로벌 감시 시스템에 접근하는 것이 여전히 중요합니다34. 또한 침습성 GAS 질병 발생률의 상당한 증가가 여러 국가, 특히 소외되고 취약한 인구에서 기록되었으며4,35-37, 이는 GAS 역학을 면밀히 모니터링하는 것의 중요성을 다시 한 번 강조합니다. 개선된 중앙 집중식 의료 보고 시스템도 증가세 감지에 기여했을 수 있다는 점에 유의해야 합니다.

cistanche 보충 혜택 - 면역 체계를 강화하는 방법
GAS 감염, 독성 요인 및 메커니즘
GAS에 의한 인간 감염 과정은 감염 발병에 기여하는 숙주 및 박테리아 요인을 모두 포함하는 복잡하고 다인자적입니다. GAS는 조직, 세포 및 면역 반응의 구성 요소에 다양한 영향을 미치는 수많은 세포벽 관련 및 분비 독성 인자를 생성하며(그림 1), 이는 다른 곳에서 광범위하게 검토되었습니다1. 여기에서는 상피 조직의 집락화와 침습성 질환의 진행에 중요한 주요 독성 요인에 중점을 두고 이 분야의 최신 발전을 강조합니다.
표면 결합 독성 인자
M 단백질. GAS는 M 단백질을 코딩하는 유전자의 5' 말단 서열(mm)에 따라 분류됩니다. 220mm 이상의 유전자형이 확인되었습니다2. M 단백질은 박테리아 세포벽 38에서 연장되는 이량체 코일형 원섬유형 단백질입니다. M 단백질을 세포벽에 공유 부착시키는 보존된 카르복시 말단과 다음을 함유하는 초가변 표면 노출 N 말단으로 구성됩니다. M 유형 정의 50개 아미노산은 상당한 항원 다양성을 나타냅니다39. GAS 독성에 대한 M 단백질의 기여는 주로 면역 조절 효과에 기인합니다. 그들은 플라스민(ogen)과 피브리노겐을 포함한 수많은 숙주 성분을 연쇄상 구균 표면에 직접 결합하고 모집하여 선천성 및 적응성 면역 반응에 대한 저항성을 부여할 수 있습니다1. M 단백질은 또한 NLRP3 인플라마솜 기계를 유도하여 대식세포에서 프로그램된 세포 사멸을 유발하여 전염증성 사이토카인 인터루킨-1(IL-1) 및 IL-18( 참고문헌 40,41) 비록 M 유형에 특정한 방식이기는 하지만. 수많은 연구에서 M 단백질이 막 보조 인자 단백질(MCP; CD46으로도 알려져 있음)42 및 세포 표면 글리칸43,44과 같은 상피 세포 수용체와의 접착 상호작용을 통해 숙주 군집화에 기여한다는 증거를 제시했습니다. 이러한 상호작용이 보고되었습니다45.
표 1|GAS 감염으로 인한 질병

히알루론산 캡슐.
GAS의 히알루론산 캡슐은 글루쿠론산과 N-아세틸글루 코카인의 반복되는 이당류 단위로 구성되며 특징적인 젖은 점액 콜로니 형태를 부여합니다. GAS 캡슐은 결합 및 상피 조직을 포함한 많은 신체 조직에서 발견되는 세포외 기질의 주요 구성 요소인 인간 히알루론산과 구조적으로 동일합니다. 따라서 GAS 캡슐은 숙주 면역 체계로부터 병원균을 위장하는 역할을 합니다. 인간 히알루론산의 주요 수용체인 인간 세포 표면 당단백질 CD44에 직접 결합함으로써 GAS 캡슐은 인두와 피부의 상피 세포에 대한 부착을 중재합니다. CD44- 의존적 결합은 상피 장벽 무결성을 방해하는 세포 신호 전달 경로의 활성화를 유도하여 GAS가 더 깊은 기본 조직에 침투할 수 있게 합니다47. GAS 캡슐화는 또한 보체 매개 식세포 살해에 대한 독성과 저항성을 증가시키는 것으로 나타났습니다. 그러나 전체 hasABC 캡슐 유전자 오페론(emm4, emm22 및 emm89)49,50이 부족하거나 hasAB 유전자 내에 불활성화 돌연변이가 있는 여러 다른 유형의 침습성 및 비침습성 균주 모두에서 캡슐 생산의 손실이 보고되었습니다. emm28 및 emm87)51,52. 이러한 유전적 배경에서 캡슐 손실이 전달하는 선택적 이점은 완전히 이해되지 않았습니다.

그림 1|GAS 독성 인자와 세포 부착, 침입 및 면역 회피에서의 역할. ㅏ,
S 단백질.
GAS는 면역 제거를 피하기 위해 많은 독창적인 전략을 발전시켰습니다. 고도로 보존된 표면 결합 단백질(S 단백질)이 선택적으로 적혈구 세포막에 결합하는 것으로 밝혀진 새로운 형태의 분자 모방이 최근 기술되었습니다. GAS 세포 표면의 S 단백질 의존성 막 코팅은 식세포 살해를 방지하여 이 병원체의 특징적인 용혈 활성과 혈액 생존 및 전파를 촉진하는 데 도움이 될 수 있는 면역 위장 전략 사이의 중요한 연결을 제공합니다.
분비된 독성 인자
케모카인 분해. 프로테아제는 선천성 면역체계의 주요 신호 분자를 특이적으로 절단하고 중화하기 위해 병원성 박테리아에 의해 활용됩니다54. GAS는 케모카인 IL-8(C–X–C 모티프 케모카인 리간드 8(CXCL8)이라고도 함)을 절단하는 S. pyogenes 세포 외피 단백질 분해효소(SpyCEP)와 C5a 펩티다제(ScpA)로 알려진 두 가지 프로테아제를 분비합니다. 보체 성분 5a(C5a), 각각55,56. 이러한 강력한 화학유인물질의 절단은 선천성 면역의 주요 방어 메커니즘인 호중구 침투 및 활성화를 손상시킵니다.

cistanche 보충 혜택 - 면역력 증가
디옥시리보뉴클레아제.
다양한 병원성 연쇄구균은 숙주의 면역 방어와 싸우기 위해 세포외 데옥시리보뉴클레아제(DNase)를 생산합니다57. 서열이 분석된 모든 GAS 균주에는 적어도 하나의 세포외 DNase58이 포함되어 있습니다. 전체적으로 6개의 프로파지 인코딩(sda1, sda2, spd1, spd3, spd4 및 sdn)과 2개의 염색체 인코딩(spnA 및 spdB) DNase 유전자가 GAS57에서 확인되었습니다. 이들 중 SpnA는 필수 분류 효소 기질 LPXTG 모티프를 포함하는 유일한 세포벽 고정 DNase입니다. 연쇄상 구균 DNase의 주요 기능은 호중구 세포외 트랩(NET)의 DNA 프레임워크를 분해하여 포획된 박테리아의 방출을 촉진하고60-62 박테리아 DNA를 자가 분해하여 면역 세포에 의한 TLR{14}}의존 인식을 억제하는 것으로 보입니다63 . 여러 감염 모델의 결과는 GAS 질병의 발병에서 DNase가 중요한 역할을 한다는 것을 시사합니다60-62.
스트렙토키나제.
스트렙토키나제(SK)는 강력한 인간 특이적 플라스미노겐 활성화 단백질입니다. 다른 플라스미노겐 활성화제와 달리 SK에는 고유한 효소 활성이 없습니다. SK-플라스미노겐 복합체는 플라스민 유사 활성을 가지며 침습성 GAS 질병의 발병에 중요하며, 숙주 방어 단백질의 단백질 분해를 통한 박테리아 전파를 돕습니다 64-67.
면역글로불린 분해 효소.
적응 면역을 회피하기 위해 GAS는 IdeS/Mac-1, Mac-2 및 EndoS로 알려진 세 가지 면역글로불린 분해 효소를 분비하며, 이는 특히 옵소닌화 IgG 항체를 표적으로 합니다. IdeS는 IgG68의 중쇄를 절단하는 시스테인 프로테아제입니다. Mac-2은 유사한 IgG 엔도펩티다제 활성을 갖는 IdeS의 대립유전자 변종입니다. 두 단백질 모두 IgG 엔도펩티다제로 기능합니다. 그러나 그들은 또한 식세포의 Fc 수용체와 상호작용하여 Fc 매개 숙주 방어 메커니즘을 방해합니다. 이와 대조적으로 EndoS는 엔도글리코시다제 활성을 가지며 인간 IgG 항체의 코어 글리칸을 특이적으로 가수분해하여 감염 중에 항체 이펙터 기능을 중화합니다70.
SpeB. SpeB의 광범위한 기질 특이성은 상피 접합부의 세포간 장벽 단백질71, 숙주 세포외 기질 단백질72, 보체 인자73, 카텔리시딘 유래 항균 펩타이드 LL-37(참조. 74), 자가포식 성분75 및 케모카인76. SpeB는 또한 IL-1(참조 77) 및 상피 IL-36(참조 78)의 전구체를 직접 절단하고 활성화함으로써 전염증성 특성을 나타냅니다. 이는 두 가지 강력한 염증성 사이토카인입니다. 감염과 부상에 대한 숙주 방어 반응. 최근에 발견된 또 다른 전염증 메커니즘은 염증 세포 사멸의 용해 형태인 파이롭토시스를 유발하는 피부 상피 세포에서 기공 형성 GSDMA의 절단 및 활성화와 관련이 있습니다8,9. SpeB에 의한 GSDMA의 카스파제 독립적 절단은 매우 선택적이며 SpeB가 감염된 세포의 세포질로 들어가야 합니다. 흥미롭게도 감염 과정의 초기 단계에는 SpeB가 필요하지만 SpeB 음성 변종은 M1T1 GAS79-81의 심각한 침습성 감염 중 면역 선택에서 자주 발생하며 비 M1 GAS82에서는 그 정도가 적습니다. covR/S 조절 시스템의 돌연변이로 인해 SpeB 발현이 상실되면 표면 결합 플라스민 활성이 축적되어 생체 내에서 GAS의 전신 전파가 촉발됩니다83.
스트렙톨리신 및 NAD 글리코하이드롤라제. GAS의 거의 모든 임상 분리물은 진핵 세포막에 기공 형성을 일으키는 두 가지 강력한 세포 용해 독소인 스트렙톨리신 S(SLS)와 스트렙톨리신 O(SLO)를 분비합니다. 두 세포용해소는 모두 상피 세포와 면역 세포를 포함한 광범위한 숙주 세포에 대해 세포독성을 나타냅니다. SLS와 SLO에는 연조직 손상, 조직 침범, 선천적 면역 회피에서 염증 반응 활성화에 이르기까지 다양한 기능이 할당되어 있습니다. 말초신경계는 SLS의 또 다른 특정 표적으로, 감각 뉴런을 활성화하여 통증을 생성하고 면역 세포의 동원을 억제하여 감염 중 박테리아 생존을 촉진합니다89. GAS에서 콜레스테롤 의존성 세포용해소 SLO의 활성은 동시에 발현되는 독소 NAD 글리코하이드롤라제(NADase, SPN 또는 NGA라고도 함)90와 기능적으로 상호의존적이며, 이는 세포 에너지 저장의 숙주 세포를 고갈시킵니다91. SLO와 NADase는 분비 후 물리적으로 상호작용하고 공동 안정화됩니다92. NADase 의존성 막 결합은 SLO93에 의한 기공 형성을 촉진하며, 이는 반대로 NADase가 숙주 세포로 이동하는 것을 촉진합니다94. SLO와 보조 독소인 NADase는 결합하여 대식세포와 상피 세포에서 GAS 세포내 생존과 세포 독성을 촉진하고95,96 골지 단편화를 통해 이러한 세포 유형의 숙주 방어를 손상시키며97 생체 내 발병에 기여합니다98. 연쇄상 구균 균주의 출현 및 유행은 NADase-SLO 유전자좌에서 고활성 프로모터 재조합 사건과 관련되어 있으며 이는 NADase 및 SLO 독소의 발현을 증가시킵니다50,52,99,100. 이러한 재조합 관련 게놈 리모델링은 무낭성 분리주에서 종종 관찰되며, 이는 높은 독소 발현 균주50,52,100에서는 캡슐 생산이 필요하지 않을 수 있음을 시사하지만, 이 관계에 대한 기계적 기초는 아직 결정되지 않았습니다.

남성의 면역체계 강화를 위한 시스탄체의 효능
초항원. 일반적으로 Spes라고도 불리는 초항원은 T 세포 수용체 사슬의 가변 영역(TCR V )을 항원 제시 세포(APC)의 MHC 클래스 II 분자와 비항원 특이적 방식으로 교차 연결하여 결과를 초래하는 강력한 외독소입니다. T 세포의 광범위한 활성화 및 통제되지 않은 사이토카인 반응101. 연쇄구균 초항원은 다양한 인간 질병, 특히 독성 쇼크 증후군과 성홍열과 관련이 있습니다101. 현재까지 GAS에서는 13개의 별개의 초항원이 확인되었습니다(염색체 인코딩: speG, speJ, speQ, speR 및 smeZ; 프로파지 인코딩: speA, speC, speH, speI, speK–M 및 ssa)102. 이들 중, 세 가지 초항원(SpeA, SpeC 및 SSA)은 성홍열 및 침습성 질병을 유발하는 현대 GAS 계통의 체력 증가 및 독성과 관련이 있습니다4,61,103. 초항원 민감성 감염 모델로서 인간 백혈구 항원(HLA) MHC 클래스 II 분자를 발현하는 형질전환 마우스를 사용하여 초항원 생물학 분야에서 상당한 진전이 이루어졌으며, 이는 GAS에 의한 급성 비인두 감염에서 SpeA 및 SpeC의 중요한 역할을 확립하는 데 도움이 되었습니다61 ,103,104.
GAS 감염에 대한 호스트 반응
인간 제한 병원체로서 GAS 질병의 동물 모델은 인간 질병과 제한된 충실도를 공유하며 이는 기계적 면역학 연구에 장애가 됩니다. GAS 인두염에 대한 CHIM이 최근 개발되었으며, 이는 표면 GAS 감염에 대한 초기 인간 면역 반응을 유도하는 세포 및 체액 요인을 조사할 수 있는 탁월한 기회를 제공합니다20,105. CHIM 지원자로부터 수집한 혈청을 분석한 결과 초기 전신 반응은 IFN, IL{3}}, CXCL10 및 IL{5}}Ra가 기준선 105 이상으로 상승하는 것이 특징인 것으로 나타났습니다. 이는 인두염이 발생한 환자의 타액에서 IL-1Ra, IL-6, IFN 및 IP-10가 기준치보다 높았으며, 무증상인 환자에서는 덜 두드러졌습니다. 전염증성 사이토카인의 증가는 단핵구 및 수지상 세포의 수 증가와 기존 CD{11}} T 세포(T 여포성 보조 세포, T 보조 17 세포(TH17 세포), TH1 세포)의 감소와 관련이 있었습니다. 및 혈액 내 B 세포뿐만 아니라 δT 세포에 의한 활성화 마커의 발현이 증가합니다. T 여포 보조 세포와 B 세포가 CHIM의 감염 부위로 빠르게 유입되는 것은 재발성 편도선염이 T 여포 보조 세포 및 B 세포 기능 결함과 관련된 면역 감수성 질환이라는 발견과 일치합니다. 비판적으로, MAIT 세포는 GAS에 노출된 후 활성화되었으며, MAIT 세포를 활성화하는 IL-18는 피험자의 타액에서 증가했는데, 이는 비인두 감염의 마우스 모델을 사용한 연구에서는 보고된 바가 없습니다.
MAIT 세포
GAS 감염의 마우스 모델에서 얻은 기계적 통찰력에 대한 신중한 해석의 필요성을 강조하면서 MAIT 세포는 GAS 질병의 맥락에서 초점이 되지 않았습니다. 또한, 쥐 MAIT 세포는 처음에 GAS107에 의해 활성화되지 않는 것으로 보고된 반면, 인간 MAIT 세포는 두 가지 별개의 메커니즘을 통해 GAS에 의해 활성화됩니다. MAIT 세포는 최근 STSS 환자에서 고도로 활성화되는 것으로 나타났으며 이 질병과의 사이토카인 폭풍 연관성에 대한 주요 기여자로 확인되었습니다. 말초 혈액 T 세포 집단의 1~10%만을 나타냄에도 불구하고, GAS가 있는 STSS 환자의 말초 혈액 단핵 세포의 생체 외 자극 동안 MAIT 세포는 각각 IFN 생성 T 세포의 41%와 TNF 생성 T 세포의 15%를 나타냈습니다. . 일부 환자의 경우 MAIT 세포는 IFN 생성 T 세포의 거의 60%를 차지했으며10, GAS로 자극하기 전에 말초 혈액 단핵 세포에서 MAIT 세포가 고갈되면 IFN , IL-1 , IL{{15 }} 및 STSS 사이토카인 폭풍 동안 면역병리학을 유발하는 TNF입니다110. 마찬가지로 MAIT 세포는 활동성 급성 류마티스열(ARF) 환자와 ARF로 인해 최근 퇴원한 환자의 혈액에서 건강한 개인에 비해 높게 상승합니다111. 또한 ARF 환자의 MAIT 세포는 건강한 개인에서 얻은 것보다 더 높은 구성적 IFN 및 TNF 생산을 나타내며, 이는 면역병리학에 기여할 가능성이 높습니다. 이러한 관찰은 MAIT 세포가 제1형 당뇨병114, 강직성 척추염115 및 염증성 장질환116을 포함한 다른 자가면역 질환에서 중심적인 병리학적 역할을 차지한다는 것을 시사하는 새로운 패러다임과 일치합니다. 종합하면, 이러한 발견은 인두염, 침습성 GAS 및 ARF의 발병에 MAIT 세포가 관련되어 있음을 의미하며(그림 2), 여전히 가설에 불과하지만 MAIT 세포 활동을 선택적으로 손상시키는 치료법이 치료법으로 폭넓게 적용될 수 있다고 추측하고 싶습니다. GAS 질환, 특히 사망률이 용납할 수 없을 정도로 높은 STSS의 경우. MAIT 세포 지향 면역요법은 아직 시장에 출시되지 않았지만, 다른 염증성 질환에 대한 치료제로서 MAIT 세포에 대한 개입이 개발 중입니다118. 그러나 MAIT 세포 생물학에 대한 우리의 이해는 아직 미성숙하며 개별 MAIT 세포 하위 유형이 GAS 질병에 미치는 정확한 기여를 정확하게 밝혀야 합니다.
ARF 및 RHD의 발병 기전에 대한 면역학적 통찰
ARF 및 RHD의 동물 모델은 질병 병태생리학의 많은 주요 특징을 요약하지 못하여 이러한 질병의 면역병인을 조사하는 데 유용성이 제한됩니다. 그러나 최근 연구에서는 이러한 질병의 발병을 촉진하는 면역학적 과정, 즉 TH1 세포가 승모판으로 선택적 이동하는 것을 설명할 수 있는 IL{0}} –GM–CSF 축의 존재에 대한 기계적 통찰력을 제공했습니다. 마음119. 이 세포는 인간의 CD{3}} T 세포 중 GM-CSF의 주요 공급원이며120 심근염 발병에 독립적으로 관여합니다121,122. 또한, CXCR3에 대한 리간드는 RHD123으로의 ARF 진행과 관련된 판막 조직 병변에 대한 T 세포 모집을 촉진합니다. ARF 또는 RHD 환자의 말초 혈액 단핵 세포에서 IL-1 방출이 지속된다는 것은 조절되지 않은 피드백 억제 메커니즘이 괴사성 근막염과 같은 다른 GAS 질병 외에도 두 질병의 발병에 대한 위험 요소일 수 있음을 시사합니다. 과도한 IL{11}} 생산에 대한 병리학적 역할은 잘 알려져 있습니다124.

그림 2|GAS 감염 중 MAIT 세포 활성화의 병원성 메커니즘 개요
GAS 역학 및 진화
GAS의 주요 역학적 표지는 지난 세기 동안 GAS 계통을 정의하는 데 중심이 되어온 면역우세 M 단백질을 기반으로 합니다. 원래 혈청학적 방법으로 개발된 M-형 분류 계획은 emm 유전자의 초가변 N-말단 영역이 M 단백질 혈청 특이성을 전달한다는 것을 분자적 방법으로 확인한 후 199{25}}에 유전자 기반이 되었습니다126,127. emm 유형을 기반으로 한 GAS의 전 세계 역학은 2009년에 지배적인 GAS emm 유형의 우세가 고소득 환경에서 보고되었을 때 요약되었습니다. 이는 저소득 환경(예: 아프리카 및 태평양 내)과 대조적입니다. 이러한 GAS 유형은 드물게 관찰되며 순환에서 지배적인 GAS emm 유형이 일반적으로 부족합니다3. 최근에는 전체 유전자 함량과 관련 서열 변이 모두의 변이를 기반으로 GAS 집단 간의 관계를 정의하기 위해 전체 게놈 기반 접근법이 사용되었습니다. emm 유형과 전체 게놈 서열 클러스터와 같은 역학적 마커 간의 상관관계는 글로벌 맥락에서 다르지만 mm 유형 지정과 같은 유전자 기반 방법은 지역적이고 짧은 시간 프레임 조사에 효과적인 것으로 입증되었습니다. 최근 리뷰 기사는 유전체학과 GAS 역학의 교차점에 대한 포괄적인 배경을 제공하며129-131 여기서는 GAS 집단 생물학의 최신 발전에 중점을 둡니다. 이러한 분야의 지속적인 지식 발전은 발병기전의 새로운 패러다임, 병원체 추적을 위한 더 나은 프레임워크, 전염 역학 및 백신 발전을 제공하고 있으며, 이는 결국 GAS 감염에 대한 임상 및 공중 보건 통제를 개선하는 데 사용될 것입니다. 인구 게놈 연구에 따르면 GAS 게놈의 전체 크기는 1.7~2.0Mbp로 상대적으로 안정적이며 1,500~2개000 유전자를 인코딩하는 것으로 나타났습니다. 약 1,300개의 '핵심' 유전자가 모든 GAS 유형에서 보존되며, 축적된 '부속품' 또는 가변 유전자 함량은 핵심 게놈보다 약 5배 더 큽니다17,129. 전 세계 GAS 개체군 유전체학의 중심 서술은 수백 개의 공동 진화하는 게놈 '클러스터' 또는 '계통'을 갖는 유전적으로 다양한 병원체라는 점을 중심으로 진행되며 이러한 클러스터의 상대적 풍부함과 변동은 지리와 시간에 따라 실질적으로 다릅니다. 이러한 계통은 유전적으로 구별되지만, 이들의 진화 궤적은 글로벌 GAS 계통의 진화적 성공에 중요한 역할을 하는 상동 및 비상동 재조합 사건에 의해 크게 영향을 받습니다. 다양한 지리적 설정 사이에서 대조되는 GAS의 인구 구조가 그림 3에 예시되어 있습니다. 여기서 교대로 회색 상자는 이전에 정의된 ~300개의 진화적으로 구별되는 GAS 계통을 나타내고 해당 계통이 보고된 지리적 영역은 색상으로 구분되어 있습니다. 이 두 가지 측면(지리 및 게놈 계통)을 연결하는 선은 많은 계통이 전 세계적으로 분산되어 있지만 태평양 및 아프리카 지역에는 다른 위치에서는 거의 관찰되지 않는 GAS 계통이 포함되어 있음을 나타냅니다. 다양한 지리적 환경 사이에서 대조되는 GAS 인구 구조는 감비아132, 케냐133 및 원격 호주17,134의 예비 조사 결과에 예시되어 있으며, 순환하는 GAS 계통은 고소득 환경에서 유래한 계통과 진화론적으로 구별됩니다. 이러한 데이터에 대한 한 가지 해석은 GAS 계통의 빈도가 전 세계적으로 다르며 질병 부담이 가장 높은 지역에서 더 많은 수의 GAS 유전자형이 유지된다는 것입니다. 인구 구조의 이러한 시간적 공간적 차이를 유지하는 원동력은 아직 불분명하지만 이러한 역학은 다양한 전염 경로, 사회 경제적 요인 및 병원체/숙주 유전자 선택 이벤트의 복잡한 상호 작용일 가능성이 높습니다. 게놈 역학은 공중 보건 감시 노드 내에서 GAS 균주를 식별하고 추적하는 데 중추적 역할을 해 왔으며, 특히 선택된 신고 대상 병원체에 대한 게놈 서열 분석이 중앙 집중화되고 자원이 제공되는 고소득 관할 구역에서 더욱 그렇습니다. 이러한 설정 내에서 코어(~1.7Mbp) 게놈에 걸쳐 27개의 단일 뉴클레오티드 다형성이 존재한다는 점에서 조상 M1 집단과 다른 최근에 등장한 GAS emm1 클론(M1UK라고 함)이 확인되었습니다4. 이 우려 변종의 '빠른' 확산은 다른 고소득 감시 노드135-137에서 관찰되었으며, 이는 이 클론의 전염병 특성을 강조합니다. GAS 클론의 선택적 대체를 이끄는 분자적 사건에는 항균 저항성 마커와 연쇄상 구균 초항원을 운반하는 이동 유전 요소의 획득, 주요 독성 유전자좌(특히 NADase-slo 유전자좌)와 관련된 상동 재조합 사건, 규제 네트워크의 변형도 포함됩니다50,52,129. GAS 집단의 진화 궤적에 영향을 미치는 기본 요인이 여전히 해결되고 있지만, 분명한 것은 진화가 역동적이고 지속적인 과정이며 시간적, 공간적 요인의 영향을 크게 받는다는 점입니다. 이는 글로벌 GAS 감시 및 설계에 대한 과제를 나타냅니다. 치료 개입의. 이러한 장애물에도 불구하고 인구 게놈 프레임워크는 최근 높은 글로벌 서열 범위를 나타내는 제안된 GAS 백신 항원의 식별을 통해 글로벌 GAS 백신 개발을 지원하는 데 사용되었습니다. 최근 통찰력은 전체 게놈 시퀀싱을 통해 제공되는 해결 방법이 전통적인 역학 도구를 사용하여 쉽게 관찰할 수 없는 전염 경로에 대한 새로운 시각을 제공할 수 있음을 보여줍니다. 미국의 여러 감시 노드에 걸쳐 침입성 질병 발생 클러스터를 조사한 연구에서는 주로 사회적으로 불리한 집단 내에서 전송 클러스터 간의 연관성을 발견했습니다138. 이 연구의 중요한 확장은 인두염과 침습성 질환 게놈 클러스터가 동일한 전송 네트워크를 공유할 가능성이 있다는 관찰이었습니다. 환경 및 매개물 전파의 기여도는 잘 알려져 있지 않지만, 최근 아급성 의료 환경에서 발생한 침습성 GAS 발생140,141과 학교 기반 감시 환경에서 성홍열 발생142은 매개물 매개, 에어로졸 및 가정 매개 전파가 다음과 같은 확산에 기여함을 시사합니다. 질병으로 인해 일부 환경에서는 지속되고 지배적이 될 수 있는 GAS 클론이 발생합니다141. 이러한 발견은 GAS 질병 발병이 일반적으로 단일 지점에서 발생하지 않는다는 것을 나타내며, 건강 교육을 늘리기 위한 원시 예방 계획 외에도 주요 감염 부위(인후 및 피부)에서 GAS 부담을 줄이는 것을 목표로 하는 개입 전략의 필요성을 강조합니다. , 특히 사회적으로 불리한 환경 내에서 위생 관행을 개선하고 주거 환경을 개선합니다143.
항생제 내성 증가
항생제 치료는 비침습적 및 침습적 GAS 감염 치료에 있어 필수적인 치료 시점으로 남아 있습니다144. GAS는 일반적으로 α-락탐 항생제에 민감하지만, 1차 보조제 및 페니실린 대체 치료 요법(즉, 마크로라이드 및 린코사미드 항생제)에 대한 내성을 부여하는 메커니즘으로 인해 종종 재발성 감염, 치료 실패 및 불량한 환자 결과가 발생합니다145-147 (그림 4). 또한, GAS에서 무증상 α-락탐 저항성의 출현은 여전히 지속적인 우려 사항입니다11-13.
Macrolide 및 Lincosamide 저항성
Ribosomal target site modification in GAS (that is, methylation of a single adenine in 23S ribosomal RNA (rRNA)), mediated by erythromycin resistance methylase (Erm) proteins, confers resistance to macrolides, lincosamides, and streptogramin B, subsequently giving rise to the MLSB phenotype. The MLSB phenotype is frequently attributed to the constitutive or inducible expression of ermB, ermTR (an ermA gene subclass), or ermT methylase encoding genes148. The ermB gene is widely carried on transposons Tn6002 and Tn6003, both derived from the insertion of ermB in Tn916-family mobile genetic elements149. The integrative and mobilizable element IMESp2907 is a primary carrier of ermTR150. Further, the plasmid-borne ermT gene — initially discovered in GAS in 2008 (ref. 151) — has become a significant source of macrolide and clindamycin resistance in GAS152. During invasive GAS disease, inducible erm expression has been associated with high rates of clindamycin-treatment failure13,153,154. The mefA (macrolide efflux pump A) gene in GAS, which is frequently associated with prophage phage φ1207.3 (formerly Tn1207.3), confers resistance to 14 and 15 carbon-ring macrolides (that is, erythromycin and azithromycin)155. Globally, rates of erythromycin and clindamycin resistance vary greatly. Between 2011 and 2019, the US Centers for Disease Control and Prevention (CDC) Active Bacterial Core surveillance program reported an increase from 11.9% to 24.7% and from 8.9% to 23.8% of invasive GAS isolates that were non-susceptible to erythromycin and clindamycin, respectively156, which was largely driven by the expansion of types emm77, emm58, emm11, emm83 and emm92 (ref. 157). Notably, in the United States, both erythromycin and clindamycin resistance have been identified as most frequent among persons experiencing homelessness, incarceration, drug use, and long-term admission to care facilities. In China, GAS surveillance spanning the past three decades suggests that the incidence of both clindamycin and erythromycin non-susceptible ermB expressing GAS has been high since the 1990s (>특정 지역에서는 95%), 클린다마이신의 임상적 유용성을 감소시킵니다154. 통합적이고 결합적인 요소인 ICEemm12는 이 지역에서 분리된 emm12 성홍열 발병 분리에서 마크로라이드 저항성의 주요 동인으로 확인되었습니다6. 최근의 다기관 북유럽 연구에서는 GAS 괴사성 연조직 감염을 나타내는 환자에서 에리스로마이신과 클린다마이신 내성이 모두 1~2% 범위인 것으로 확인되었습니다158. 에리스로마이신과 클린다마이신 내성률의 세계적, 국가적 차이는 종종 더 높은 수준의 클린다마이신 내성을 부여하는 erm 발현 분리주에 비해 mefA 발현 분리주의 지리적 비율 차이에 기인할 수 있습니다154. 특정 지역에서 순환하는 emm 유형 전체 및 내부에서 mefA로 인코딩된 표현형과 erm으로 인코딩된 표현형의 시간적 변화뿐만 아니라 선별된 내성 균주의 클론 및 서브클론 확장은 모두 GAS6에서 마크로라이드 및 린코사미드 내성의 빈도를 높이는 요인입니다. ,152,159,160.
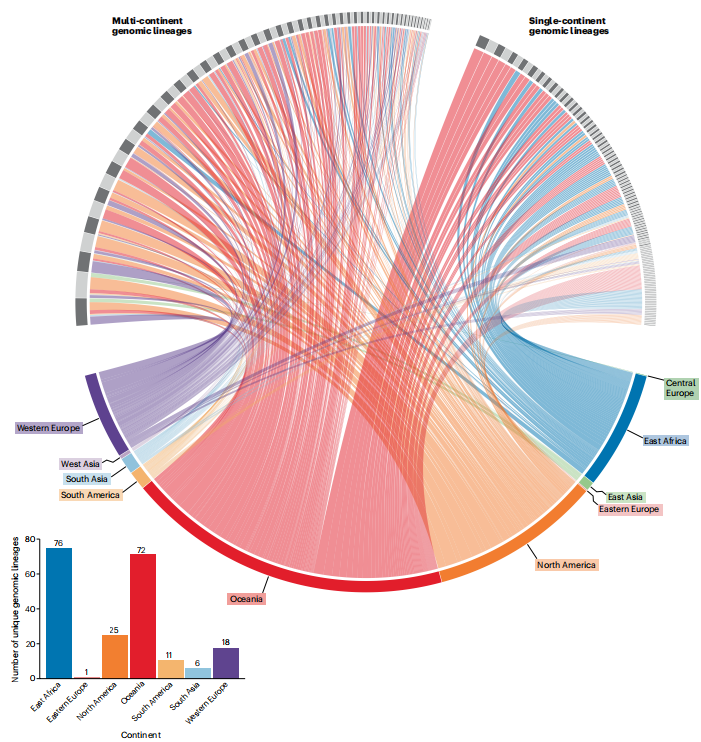
그림 3|GAS의 글로벌 유전적 다양성.

그림 4|GAS 항생제 내성 메커니즘. ㅏ,
테트라사이클린 내성
GAS에서 테트라사이클린 저항성은 리보솜 보호 유전자 tetM 및 tetO와 유출 펌프 시스템 유전자 tetK 또는 tetL161에 의해 부여됩니다. 수평적 유전자 전달을 통해 획득된 tet 유전자는 일반적으로 광범위한 이동 유전 요소에 표시되며 종종 erm 및 mef 유전자와 함께 위치합니다6. 2000년부터 2019년까지 대만에서 수행된 후향적 연구에서 마크로라이드 내성 GAS의 12.3%, 99.2%, 13.1%가 각각 tetO, tetM 및 tetK 유전자를 갖고 있는 것으로 밝혀졌습니다162. GAS 클론 확장과 함께 테트라사이클린 계열 항생제의 사용이 마크로라이드 내성을 유발하는 것으로 제안되었으며 그 반대의 경우도 마찬가지입니다1. 따라서 테트라사이클린 내성 결정 요인의 획득은 진행 중인 역학적 GAS 감시 연구에서 특별한 주의를 기울여야 합니다.
플루오로퀴놀론 내성
플루오로퀴놀론(FQ)은 GAS 감염 관리를 위한 직접적인 치료법으로 간주되지 않지만, GAS에서 낮은 수준 및 높은 수준의 FQ 저항성 표현형은 다양한 빈도로 발생합니다163. GAS FQ 저항의 전 세계 비율에 대한 대규모 최신 정보는 여전히 부족합니다. 최근 두 개의 독립적인 연구에 따르면 일본의 FQ 비감수성 비율은 11.1%(2011~2013년)에서 14.3%(2012~2018년) 범위였으며 주로 emm6 및 emm11 GAS164,165의 확산에 기인한 것으로 나타났습니다. 2011년부터 2016년 사이에 중국 상하이에서 GAS FQ 비감수성 빈도는 1.3%로 보고되었으며, FQ 비감수성 분리균의 80%는 ermB 및 tetM 저항 결정인자를 모두 보유하고 있습니다. 중국 상하이에서는 FQ 비감수성이 emm1, emm6, emm11 및 emm12 GAS166의 확산으로 인해 발생했습니다. 흥미롭게도, 낮은 수준의 FQ 저항성을 부여하는 토포이소머라제 IV ParC-S79A 돌연변이는 emm6 GAS 복합체와 자주 연관됩니다. FQ 소비율이 전 세계적으로 매우 높은 것으로 나타났습니다. GAS에서 FQ 저항성의 동인이 될 수 있는 FQ 항생제 소비와 FQ 다약제 내성 클론의 출현은 FQ 관리 관행의 세계적인 개선 필요성을 강조합니다.
설파메톡사졸 내성
설파메톡사졸과 트리메토프림(공동 트리목사졸 형성)의 조합은 최근 풍토병 환경에서 GAS 피부 감염 치료에 사용되었습니다168. GAS 엽산 주기를 표적으로 삼아 co-trimoxazole은 새로운 엽산 합성과 엽산 주기를 모두 억제합니다. 설파메톡사졸과 트리메토프림에 대한 GAS 저항성은 각각 표적 효소인 FolP와 Dyr의 돌연변이 또는 트리메토프림 저항성 Dyr 변종(DfrF 및 DrfG)의 획득에 기인합니다169,170. 또한 최근 연구에서는 에너지 결합 인자 수송체 S 구성 요소 유전자(thfT)가 GAS가 설파메톡사졸에 의한 엽산 생합성 억제를 우회하여 숙주로부터 직접 세포외 환원된 엽산 구성 요소를 획득할 수 있게 한다는 사실이 확인되었습니다171. ThtF는 활동을 위해 숙주 대사산물이 필요합니다. 따라서 표준 최소 억제 농도(MIC) 테스트는 ThtF 매개 설파메톡사졸 내성을 탐지하는 데 적합하지 않습니다. 현재 전 세계적으로 분리된 GAS 균주 중에서는 드물지만, 적절한 환자 치료를 안내하기 위해 thfT 양성 GAS의 출현과 전파를 모니터링하는 것이 이제 필수적입니다.
-락탐 감수성
β-락탐 항생제의 표적 부위인 페니실린 결합 단백질(PBP)의 돌연변이에 의해 발생합니다. GAS에서 임상 역치를 초과하는 페니실린 저항성은 아직 문서화되지 않았지만, 시애틀(미국 워싱턴)에서 지역사회 GAS 발생으로 인해 암피실린과 아목시실린 모두에 대한 감수성이 8배 감소된 두 가지 관련 임상 emm43.4 GAS 분리균이 확인되었습니다. α-락탐 저항성 발달의 첫 번째 단계와 일치하여, PBP2x에서 미스센스 돌연변이(T553K 치환)가 확인되었습니다(참조 14). 이후 3개의 독립적인 연구에서 저자는 각각 7,025개, 9,667개, 13,727개의 GAS 분리주의 게놈 서열을 조사했습니다. 첫 번째 연구에서는 7,025개의 GAS 균주 중 137개가 pbp2x의 36개 코돈에 비동의적 돌연변이를 포함하는 것으로 확인되었습니다(참조 11). 두 번째 연구에서는 9,667개 균주 중 84개가 무증상 페니실린 MIC에 대한 내성과 관련된 PBP2x 아미노산 변이를 가지고 있었습니다12. 2015년부터 2021년까지 미국에서 침습성 GAS 분리주를 조사한 세 번째 연구에서 388개의 PBP2x 변종은 α-락탐 MIC가 증가한 것으로 나타났으며 emm4/PBP2x-M593T/ermT가 우세한 계통입니다. 이전에 설명한 emm43.3/PBP2x-T553K 변이체는 두 개의 분리주에 존재했으며 가장 높은 무증상 암피실린 MIC15를 보여주었습니다. 초기 연구 결과에 따르면 후자의 연구에서만 emm43.4 GAS의 PBP2x에 T553K 치환이 존재함을 확인했으며 이는 최근 항균제 선택 이벤트가 발생했음을 시사합니다. emm43.3/PBP2x-T553K 변종에서 α-락탐 항생제에 대한 무증상 내성 증가는 이 매우 희귀한 표현형에 존재하는 여러 비PBP 돌연변이에 기인합니다15. 낮은 친화도 PBP를 유발하는 돌연변이는 한때 GAS172에서 적합성 비용을 발생시키는 것으로 생각되었지만 GAS를 발현하는 PBP2x의 T553K 치환은 시험관 내 박테리아 성장에 영향을 미치지 않았습니다. 또한, 감소된 α-락탐 감수성을 부여하는 PBP2x 돌연변이(P601L)를 갖는 동종 돌연변이 GAS 분리물은 생체 내 병독성에는 변화가 없지만 시험관 내 성장은 강화된 것으로 나타났습니다173. 이러한 관련 보고서는 GAS에서 락탐 저항성 표현형을 모니터링할 때 필요한 경계를 뒷받침합니다.
GAS 백신 개발
안전하고 전 세계적으로 효과적인 GAS 백신 개발의 복잡성은 잘 알려져 있습니다18. 100년이 넘는 연구에도 불구하고 GAS 백신은 상업적으로 사용되지 않았습니다. GAS 백신 설계 및 개발은 광범위한 유전적 다양성, 잠재적인 자가면역 에피토프 문제, 그리고 다양한 질병 발현의 원인이 되는 인간에게만 적응된 병원체에 대한 보호 효능을 평가하기 위해 동물 모델을 사용하는 문제를 우회해야 합니다18. 이러한 과학적 장애물은 GAS 백신 개발에 대한 역사적 규제 및 상업적 장벽으로 인해 더욱 복잡해졌습니다. 의심할 여지없이 이러한 장벽 중 가장 중요한 것은 GAS 항원의 자가면역 가능성을 둘러싼 우려에 대응하여 발표된 GAS 및 그 제품의 인간 투여에 대한 미국 연방의약국(FDA)의 25-년 금지 조치였습니다174. 2005년에 판결이 취소되었지만, 이후 초기 단계 인체 실험에까지 진출한 백신 후보는 단 4명뿐이다(표 2).

cistanche tubeulosa - 면역 체계를 향상시킵니다.
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
M-단백질 백신 후보
To date, all vaccine candidates in the clinical pipeline target the GAS M protein. M protein vaccines are specifically designed to exclude auto-epitopes and contain either a mixture of hypervariable N-terminal fragments from various clinically relevant M serotypes or conserved epitopes derived from the protein's C-repeat region. The most advanced multivalent N-terminal peptide-based candidate (StreptAnova) was well tolerated and immunogenic among participants in a 2019 phase I clinical trial175. StreptAnova was formulated based on the 30 M serotypes responsible for >90% of pharyngitis and invasive disease cases in North America and Europe176, but vaccine antisera from rabbits cross-opsonize numerous structurally similar non-vaccine serotypes that dominate diverse geographic regions176,177. Although cross-opsonization of non-vaccine serotypes is predicted to increase coverage of the 30-valent vaccine among populations in both Mali (from 37% to 84%)178 and South Africa (from 63% to >90%)179, 최근 분석에 따르면 RHD가 풍토병인 북부 호주 인구에서는 보장 범위가 여전히 불충분할 것으로 나타났습니다180. 따라서 M 단백질의 C-반복 영역 내에서 고도로 보존된 에피토프를 표적으로 삼는 것은 현재 또는 미래의 역학 경향에 관계없이 전체적인 보호를 제공한다는 중요한 이점을 갖습니다. C-반복 영역 B 세포 에피토프 J8을 포함하는 MJ8VAX 백신의 I상 임상 시험에서는 백신을 접종한 지원자에게서 단일 근육 주사 후 J8-특이적 항체 역가가 증가한 것으로 나타났습니다181. MJ8VAX는 이후 GAS 피부 감염 마우스 모델에서 고병원성 covR/S 돌연변이에 대한 보호를 제공하는 SpyCEP의 추가 변형 에피토프를 사용하여 MJ8CombiVax로 재구성되었습니다182. 역시 C-반복 영역을 기반으로 하는 StreptInCor 및 P*17 백신은 마우스 GAS 챌린지 모델에서 보호 반응을 자극합니다183,184. MJ8CombiVax 및 StreptInCor에 대한 광범위한 안전성 프로파일링이 1상 시험을 준비하기 위해 쥐 모델과 미니피그 모델에서 각각 수행되었습니다. 두 후보 모두에서 백신 관련 자가면역이나 독성의 증거는 관찰되지 않았습니다.
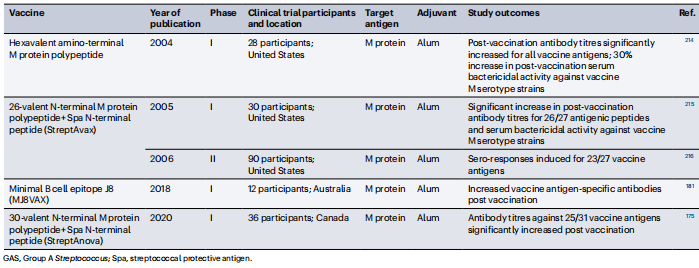
표 2|GAS 백신 후보 임상시험(2004년 이후)
비M 단백질 백신 후보
Numerous studies have identified non-M protein antigens that are protective against GAS challenge in animal models. Multicomponent formulations of selected antigens with high gene carriage and low sequence variation within the global GAS population can theoretically offer high vaccine coverage17, and several experimental vaccines employing this strategy are efficacious in animal models. Leading candidates include the GlaxoSmithKline three-component vaccine (SLO, S. pyogenes adhesion and division protein (SpyAD) and SpyCEP)187, Vaxcyte's VAX-A1 (ScpA, SLO, and SpyAD conjugated to GAS cell wall carbohydrate containing only poly rhamnose (SpyAD-GACPR) 188, Combo#5 (arginine deiminase (ADI), trigger factor (TF), SpyCEP, ScpA, and SLO)189,190, 5CP (Sortase A (SrtA), ScpA, SpyAD, SpyCEP, and SLO)191 and Spy7 (ScpA, SpyAD, oligopeptide-binding protein (OppA), pullulanase A (PulA), Spy1228, Spy1037 and Spy0843)192, which when formulated with alum (or CpG oligodeoxynucleotides in the case of the 5CP vaccine) all stimulate protective immune responses in mouse models of GAS infection. Combo#5/alum vaccination also significantly reduces symptoms of pharyngitis and tonsillitis in non-human primates19. Another candidate, TeeVax, targets multiple T antigens of GAS pili using a multivalent approach analogous to the strategy employed for the StreptAnova vaccine. TeeVax/alum induces modest protection in an invasive GAS mouse model and antiserum from vaccinated rabbits reacts to all 21 T antigens included within the vaccine (representing >모든 알려진 티 혈청형의 95%) 및 세 가지 비백신 아형193.
GAS 백신 연구개발 전망
최근 몇 년 동안 주요 이해관계자들이 GAS 백신 연구를 조정하고 안내하려는 노력이 활성화되었습니다. GAS 백신 연구 및 개발은 ARF 및 RHD194에 대한 WHO 2018 글로벌 결의안의 우선 순위로 선언되었으며 WHO는 침습성 GAS 감염 및 항생제 남용의 증가 추세에 대한 주요 개입으로 명시했습니다16. WHO는 현재 과학적 격차를 해소하고 임상 평가를 지원하며 정책 의사결정을 안내하기 위해 선호하는 제품 특성과 우선순위 연구 활동을 자세히 설명하는 GAS 백신 개발 기술 로드맵을 발표했습니다16. GAS 백신 연구 및 개발은 과거 재정적 투자 부족으로 어려움을 겪었지만, 최근 보건 경제 분석에 따르면 WHO가 선호하는 제품 특성을 충족하는 백신은 매년 최대 10억 달러의 GAS 관련 비용을 절감할 수 있을 것으로 추정됩니다. 미국195. 백신 제제화 및 전달의 발전으로 GAS 예방접종 전략이 개선될 것으로 예상됩니다. 현재까지 임상 시험에서 테스트된 모든 GAS 백신 후보는 명반으로 제형화되었으므로 TH2 세포 유형(항체) 반응을 선호하지만, 실험 보조제 CAF® 01 및 사포닌 QS21을 함유한 에멀젼을 사용한 최근 전임상 연구에서는 TH2 세포 유형(항체) 반응을 유도하는 것이 중요하다는 점을 지적했습니다. GAS 면역에서 세포(TH1 세포)와 항체 반응 모두184,190. 마이크로어레이 패치 백신 전달은 근육 내 백신 접종에 비해 향상된 면역원성, 더 긴 유효 기간 및 사용 용이성으로 잠재적인 용량 절약이라는 이점을 제공합니다. J8-DT 백신 후보는 최근 고밀도 마이크로어레이 패치 전달을 사용하여 효능이 평가되었으며, TH1 세포/TH2 세포 유도 및 생쥐의 GAS 피부 감염에 대한 근육 내 백신 접종에 비해 탁월한 보호를 보여주었습니다196. 인간 GAS 질병을 완벽하게 나타내지는 않지만 침습성 GAS 감염 평가를 위한 인간화 마우스 모델197, 마우스 피부 감염 모델198 및 GAS 인두염의 비인간 영장류 모델19을 포함하여 GAS 백신 후보를 연구하기 위한 귀중한 동물 모델이 확립되고 표준화되었습니다. . 또한 최근 호주 연구자들이 확립한 인간 GAS 챌린지 모델은 면역 보호의 상관관계를 밝히고 현재 및 미래 백신의 임상 평가를 가속화할 것으로 예상됩니다20.
결론 및 향후 전망
GAS 발생은 전 세계적으로 계속해서 발생하여 심각한 질병 발생을 일으키고 병원성 GAS 개체군의 진화 궤적을 정의하는 데 핵심인 연구 및 공중 보건 실험실을 통합하는 지속적인 노력으로 경계심 깊은 모니터링이 필요합니다. GAS 감염의 역학은 변화하는 사회 경제적 요인에 따라 지난 세기 동안 일부 선진국에서 실질적으로 변화했지만, GAS 전송 체인을 정의하고 프레임워크를 제공하려면 저자원 환경에서 용량 및 감시 노드를 구축하기 위한 조정된 노력이 필수적입니다. 향후 예방 조치의 영향을 평가합니다. GAS 병독성 기전을 설명하는 상당한 연구가 존재하지만, GAS 시스테인 프로테아제 SpeB에 의한 GSDMA 전염증 기전의 절단, 파이롭토시스 유발과 같은 새로운 숙주-병원체 상호작용이 문서화되고 있습니다. GAS에 감염된 인간에 대한 직접적인 연구는 STSS 환자에서 MAIT 세포의 역할과 같은 새로운 관점을 제공했습니다. 인간 환자 재료를 사용한 추가 작업은 분명히 보장되며 향후 치료법 및 예방학 개발에 귀중한 통찰력을 제공할 것입니다. 다른 연쇄구균 종에서 페니실린 감수성을 초래한 GAS의 첫 번째 단계 PBP2x 돌연변이를 확인하는 것은 상당한 우려 사항입니다. GAS 질병 부담을 줄이기 위한 안전하고 효과적인 GAS 백신의 개발은 이제 WHO, 백신 개발자 및 기타 주요 이해관계자들에 의해 우선순위로 명확하게 인식되고 있습니다. 이러한 백신의 상업화, 배포 및 광범위한 활용은 GAS 질병 부담을 줄이는 데 많은 도움이 될 것이며, 그 중 전체적으로는 전 세계적으로 전염병 사망의 주요 원인입니다.
참고자료
1. 워커, MJ 외. 그룹 A 연쇄상 구균의 질병 발현 및 병원성 메커니즘. 클린. 미생물. 개정판 27, 264–301(2014).
2. McMillan, DJ 외. 포괄적인 전 세계 연구를 기반으로 한 그룹 A 연쇄상구균 M 단백질의 업데이트된 모델입니다. 클린. 미생물. 감염. 19, E222–E229(2013).
3. Steer, AC, Law, I., Matatolu, L., Beall, BW & Carapetis, JR 그룹 A 연쇄상 구균의 글로벌 emm 유형 분포: 체계적 검토 및 백신 개발에 대한 의미. 랜싯 감염. 디스. 9, 611–616(2009).
4. Lynskey, NN 외. 영국에서 성홍열 활동이 증가하는 동안 지배적인 독성 M1T1 Streptococcus pyogenes 클론의 출현: 인구 기반 분자 역학 연구. 랜싯 감염. 디스. 19, 1209~1218(2019). 이 논문은 영국에서 성홍열과 침습성 감염의 급증에 기여할 수 있는 SpeA 생산 증가를 특징으로 하는 지배적인 새로운 emm1 GAS 계통(M1UK)을 보고합니다.
5. Tse, H. et al. 2011년 홍콩 성홍열 발병의 분자적 특성. J. 감염. 디스. 206, 341–351 (2012).
6. 데이비스, MR 외. 홍콩에서 성홍열 Streptococcus pyogenes emm12 클론의 출현은 독소 획득 및 다제 내성과 관련이 있습니다. Nat. 그 가죽. 47, 84–87 (2015).
7. 터너, CE 외. 영국의 성홍열 급증 및 런던 북서부의 분자 유전 분석, 2014. Emerg. 감염. 디스. 22, 1075-1078(2016).
8. Deng, W. 외. 연쇄구균 발열성 외독소 B는 GSDMA를 절단하고 발열증을 유발합니다. 자연 602, 496–502(2022). 이 논문 보고서는 SpeB가 GSDMA를 절단하여 각질세포 발열증을 유발하여 상피 세포층에서 염증 반응 자극을 위한 메커니즘을 제공한다는 것을 보여줍니다.
9. LaRock, DL 외. 그룹 A 연쇄구균은 각질형성세포에서 GSDMA 의존성 파이롭토시스를 유도합니다. 자연 605, 527–531 (2022). 이 논문은 피부 세포에서 GSDMA의 카스파제 1-독립적 활성화에서 SpeB의 역할을 보여줍니다.
10. Emgård, J. 외. MAIT 세포는 그룹 A 연쇄상 구균 독성 쇼크 증후군의 사이토카인 반응에 주요 기여자입니다. 진행 Natl Acad. 과학. 미국 116, 25923-25931(2019).
11. 머서(Musser), JM 외. pbp2x 유전자의 돌연변이와 관련된 β-락탐 항생제에 대한 화농연쇄상구균의 시험관 내 감수성 감소는 지리적으로 널리 퍼져 있습니다. J. 클린. 미생물. 58, 전자01993-19(2020).
12. Hayes, A., Lacey, JA, Morris, JM, Davies, MR & Tong, SYC Streptococcus pyogenes 페니실린 결합 단백질의 제한된 서열 변이. mSphere 5, e00090-20(2020). 13. Chochua, S. et al. 2015년 미국에서 발견된 침입성 그룹 A 연쇄상구균의 인구 및 전체 게놈 서열 기반 특성 분석. mBio 8, e01422-17 (2017). 이 연구는 미국에서 침입성 GAS 분리균의 상세한 대규모 인구 기반 게놈 특성 분석을 제시합니다.
14. Vannice, KS 외. Streptococcus pyogenes pbp2x 돌연변이는 α-락탐 항생제에 대한 감수성을 감소시킵니다. 클린. 감염. 디스. 71, 201–204(2020).
15. Chochua, S. et al. 미국에서 β-락탐 항생제에 대한 감수성 감소와 관련된 침습성 그룹 A 연쇄상구균 페니실린 결합 단백질 2x 변이체, 2015~2021년. 항균제. 요원 Chemother. 66, e0080222(2022).
16. Vekemans, GR & Kim 그룹 A 연쇄상구균 백신의 경로: WHO 연구 개발 기술 로드맵 및 선호하는 제품 특성. 클린. 감염. 디스. 69, 877–883(2019).
17. Davies, MR 외. 대규모 비교 유전체학을 사용하여 편집된 그룹 A 연쇄상 구균 백신 후보의 지도서입니다. Nat. 그 가죽. 51, 1035–1043(2019). 본 연구에서는 글로벌 GAS 게놈 데이터 세트를 사용하여 플랫폼을 개발합니다.
18. 유전체학을 기반으로 한 백신 설계. Dale, JB & Walker, MJ 그룹 A 연쇄상 구균 백신 개발에 대한 업데이트. 현재 의견. 감염. 디스. 33, 244–250(2020).
19. Rivera-Hernandez, T. 외. 인간이 아닌 영장류 모델에서 인두염과 편도선염을 감소시키는 실험적인 그룹 A 연쇄상 구균 백신. mBio 10, e00693-19(2019).
20. Osowicki, J. et al. 화농성 연쇄구균 인두염의 통제된 인간 감염 모델(CHIVAS-M75): 관찰, 용량 결정 연구. Lancet Microbe 2, e291–e299 (2021). 이 획기적인 논문은 인두염의 최초의 통제된 GAS 인간 감염 모델을 보고합니다.
21. 손, RM, Snelling, TL & Carapetis, JR 그룹 A 연쇄상 구균. Hunter's Tropical Medicine 및 신흥 전염병(eds Ryan, ET, Hill, DR, Solomon, T., Aronson, NE & Endy, TP) 429–438(Elsevier, 2020).
22. 밀러, KM 외. 인후통과 그룹 A 연쇄상 구균 인두염의 전 세계적 부담: 체계적인 검토 및 메타 분석. EClinicalMedicine 48, 101458(2022).
23. Cannon, JW 외. 뉴질랜드에서 그룹 A 연쇄상구균으로 인한 질병으로 인한 경제적, 건강적 부담. 국제 J. 감염. 디스. 103, 176–181(2021).
24. Ordunez, P. et al. 1990~2017년 미주 지역의 류마티스 심장병 부담, 추세 및 불평등: 인구 기반 연구. 란셋 글로브. 건강 7, e1388–e1397(2019).
25. Lv, M. 외. 류마티스성 심장 질환의 세계적 부담과 사회 경제적 발전 상태와의 연관성, 1990-2019. 유로. J. 이전 카디올. 29, 1425~1434(2022).
26. de Loizaga, SR 외. 미국의 류마티스 심장병: 잊혀졌지만 사라지지 않은: 10-년간의 다기관 검토 결과. J.Am. 심장협회 10, e020992(2021).
27. 올리버, J. 외. 이전 그룹 A 연쇄상구균 피부 및 인후 감염은 개별적으로 급성 류마티스열과 연관되어 있습니다: 뉴질랜드의 증거. BMJ글로브. 헬스 6, e007038(2021).
28. Barth, DD et al. 누락된 부분 연구 프로토콜: 원격 서호주에서 그룹 A 연쇄상 구균 인두염 및 농가진의 역학을 결정하기 위한 전향적 감시. BMJ 오픈 12, e057296(2022).
29. Park, DWet al. 성홍열의 발생률과 특성, 한국, 2008~2015. 신흥. 감염. 디스. 23, 658–661 (2017).
30. Yung, CF & Thoon, KC 12-년 동안 싱가포르에서 성홍열이 발생했습니다. 랜싯 감염. 디스. 18, 942(2018).
31. Lamagni, T. et al. 2014~2016년 영국 성홍열 재발: 인구 기반 감시 연구. 랜싯 감염. 디스. 18, 180–187(2018).
32. Cubria, MB, Delgado, J., Shah, BJ, Sanson, MA & Flores, AR 미국 텍사스주 휴스턴의 소아 집단에서 유행성 성홍열 그룹 A 연쇄상구균 계통의 확인. 입장. 미생물. 3, 000274(2021).
33. 워커, MJ 외. 호주에서 유행성 성홍열 그룹 A 연쇄상구균의 검출. 클린. 감염. 디스. 69, 1232~1234(2019).
34. Watts, V. et al. 성홍열 환자의 가족 접촉자에 대한 침습성 그룹 A 연쇄상구균 질환의 위험 증가, 영국, 2011-2016. 신흥. 감염. 디스. 25, 529–537(2019).
35. Ron, M. 외. 침습적 다약제 내성 emm93.0 새로운 게놈 섬을 보유하고 있는 Streptococcus pyogenes 균주, 이스라엘, 2017-2019. 신흥. 감염. 디스. 28, 118–126(2022).
36. Tyrrell, GJ, Bell, C., Bill, L. & Fathima, S. 제1국 인구에서 침습성 그룹 A 연쇄상구균 질병의 발병률 증가, 캐나다 앨버타, 2003~2017년. 신흥. 감염. 디스. 27, 443–451(2021).
37. 발렌시아노, SJ 외. 미국에서 약물을 주사하는 사람과 노숙자를 경험하는 사람 사이의 침습성 그룹 A 연쇄구균 감염, 2010~2017년. 클린. 감염. 디스. 73, e3718–e3726(2021).
38. Phillips, GN Jr, Flicker, PF, Cohen, C., Manjula, BN & Fischetti, VA 연쇄구균 M 단백질: - 세포 표면의 나선형 코일 코일 구조 및 배열. 진행 Natl Acad. 과학. USA 78, 4689-4693(1981).
39. Li, Z. et al. 1064개의 최근 침입성 그룹 A 연쇄상구균 분리주에서 M 단백질 유전자 하위 유형의 배열이 활성 박테리아 핵심 감시에서 회수되었습니다. J. 감염. 디스. 188, 1587-1592(2003).
40. Valderrama, JA et al. 그룹 A 연쇄구균 M 단백질은 NLRP3 염증복합체를 활성화합니다. Nat. 미생물. 2, 1425~1434(2017). 이 포괄적인 보고서는 M1 단백질이 카스파제 1-의존적 NLRP3 인플라마좀 활성화를 유발하여 발열성 대식세포 세포 사멸을 초래한다는 것을 보여줍니다.
41. Richter, J. 외. 스트렙톨리신은 Streptococcus pyogenes 감염 동안 대식세포의 주요 염증복합체 활성화제입니다. 면역. 셀바이올. 99, 1040–1052(2021).
42. Okada, N., Liszewski, MK, Atkinson, JP & Caparon, M. 막 보조 인자 단백질(CD46)은 그룹 A 연쇄상구균의 M 단백질에 대한 각질세포 수용체입니다. 진행 Natl Acad. 과학. USA 92, 2489-2493(1995).
