큐티박테리움 여드름 발효에 의해 생성된 프로피온산은 멜라닌 합성을 개선합니다
Mar 29, 2022
연락처: Audrey Hu Whatsapp/hp: 0086 13880143964 이메일:audrey.hu@wecistanche.com
Hsin-Jou Kao1, Yan-HanWang2, Sunita Keshari3, John JacksonYang3, Shinta Simbolon1, Chun-Chuan Chen1 및 Chun-Ming Huang1*
자외선 조사는 멜라닌 축적을 유도하는데, 이는 화학적 미백 제품을 사용하여 감소시킬 수 있습니다. 그러나 이러한 제품과 관련된 안전 문제로 인해 자연스럽고 무해한 대안을 모색하게 되었습니다. 이 연구는 피부 색소 침착을 감소시키는 천연 산성 제제를 식별하는 것을 목표로 하였다. 대사산물인 프로피온산(CH3CH2COOH, PA)은 큐티박테리움 아크네스(C. 아크네스)의 플루로닉 F68(PF68) 발효 여액에서 가장 풍부한 지방산이었고 유리 지방산 수용체 2(FFAR2). 또한, 4mM PA 처리는 멜라닌 세포 증식을 변경하지 않았으며, 이는 이것이 세포 손상을 일으키지 않는 과색소침착에 효과적인 솔루션임을 나타냅니다. 감소된 DOPA-양성 멜라닌 세포와 티로시나아제 활성은 C. 아크네스와 PF68의 혼합물을 주사한 마우스 귀 피부 조직에서도 관찰되었으며, 이는 멜라닌 생성 억제가 탄소원. 또한 PA는 부모 박테리아인 C. 아크네스의 성장에 영향을 미치지 않았으므로 피부 미생물군집의 균형을 방해하지 않는 강력한 발효 대사 산물입니다.
피부는 인체와 외부 환경 사이의 인터페이스 역할을 하여 병원체, 물리적 및 자외선 손상에 대한 방어를 제공합니다1. 인간의 피부가 많은 세포 유형의 기능과 생존에 영향을 미치는 자외선(UVR)에 과도하게 노출되면 피부 염증을 유발하여 암으로 이어질 수 있습니다2,3. UV 유도 DNA 손상은 세포 복구 신호를 활성화하여 멜라닌 세포에서 멜라닌을 생성하여 피부 색소 침착을 유발합니다. 건강한 인간의 피부 표면은 다양한 미생물 환경에 의해 군집화되어 있으며, 이들 중 다수는 공생 또는 기회 병원체로서 무해합니다6,7. Probiotics는 노화 피부의 징후를 늦추고 UV로 인한 피부 염증의 영향을 완화함으로써 광보호 가능성이 있는 세균 요법의 일반적인 예입니다3,8,9. 예를 들어, 프로바이오틱 유산균은 UV로 인한 염증, 알레르기 반응 및 피부의 면역 억제를 현저하게 예방합니다10. 더욱이, UVR에 반응하여 포르피린을 생성하는 피부 미생물군집의 우세한 박테리아인 Cutibacterium 아크네스(C. 아크네스)의 능력은 불균형을 보호하고 예방하는 역할 때문에 주요 바이오마커가 됩니다2,11,12 실질적인 관심13. 연구에 따르면 발효 여액(GFF)이 인간 흑색종 세포의 멜라닌을 감소시켜 피부 색소 침착을 감소시키는 것으로 나타났습니다14. 유리 지방산(FFA)은 배양된 B16F10 쥐 흑색종 세포에서 멜라닌 생성에 놀라운 조절 효과와 억제된 티로시나제 활성을 가지고 있습니다. 과색소침착에 대한 대부분의 치료 옵션은 멜라닌 생합성에 필요한 주요 조절 효소인 티로시나제 억제제로 작용하는 티로신의 멜라닌으로의 전환을 차단합니다. 최근 화장품 제형에 페놀 및 수은 화합물과 같은 피부 미백제의 광범위한 사용으로 인해 심각한 안전성 문제가 제기되었습니다17. 또한 FFAR2(GPR43이라고도 함)는 골수, 비장 및 정상 피부18와 같은 다양한 조직에 존재하며 비만, 대장염 및 일부 염증 반응19에 대한 유망한 약물 표적입니다. FFAR2는 FFAR220,21에 대한 가장 강력한 효능제인 아세테이트, 부티레이트 및 프로피오네이트와 같은 6개 탄소 미만의 사슬 길이를 갖는 단쇄 지방산(SCFA)에 대한 수용체입니다. 이전에 우리는 마우스 피부에서 FFAR2의 생체 내 녹다운이 UV 자극의 부티르산 매개를 차단한다는 것을 입증했습니다.
C. acnes is abundant on the human skin surface accounting for>박테리아의 60%2. 더욱이, C. 아크네스의 발효 대사산물인 프로피온산(PA)과 그 에스테르화 유도체는 황색포도상구균11,22에 대한 잠재적인 항균제로 작용하고 폴리(에틸렌 옥사이드) 코팅은 감염을 피할 수 있는 유망한 방법입니다. 피부 공생 probiotic 박테리아는 선택적 발효 개시제로서 poly(ethylene glycol) dime-methacrylate의 발효를 통해 USA300의 성장을 억제할 수 있습니다. PEG 기반 폴리머인 PF68은 항균제에 대한 안정적인 젤 캐리어로 약물의 표면 용해도를 증가시키며 일반적으로 식별 가능한 부작용 없이 감염된 상처의 치료에 사용됩니다. 이 연구에서 우리는 고분자 유래 화합물인 PF68이 잠재적으로 안전하고 효과적인 제제이며 피부 공생 C. 아크네스에 의한 PF68의 발효 대사산물을 적용하면 UV로 인한 피부의 과색소침착 또는 멜라닌 생성을 억제할 수 있음을 확인했습니다.

cistanche tubolosa 혜택: 피부의 멜라닌 생성을 억제합니다.
행동 양식
윤리 성명서.
이 연구는 대만 국립중앙대학교(NCU)(NCU{0}})에서 승인된 기관 동물 관리 및 사용 위원회(IACUC) 프로토콜과 도착 가이드라인(https://arriveguidelines)에 따라 엄격하게 수행되었습니다. .org/). ICR(Institute Cancer Research) 생쥐(8-9주령 암컷, 국립 실험 동물 센터, 대만 타이페이)는 닫힌 상자에서 CO2를 사용하여 희생되었습니다. 모든 방법은 관련 지침 및 규정에 따라 수행되었습니다.
세균 배양.
C. 아크네스(ATCC 6919)를 Gas-Pak(BD, Sparks, MD, USA)을 사용하여 혐기성 조건에서 Reinforced Clostridium Medium(RCM, Oxford, Hampshire, England)에서 배양하였다. 박테리아는 대수 성장 단계까지 37도에서 배양되었다. 박테리아 펠렛을 5,{4}} xg에서 10분 동안 원심분리하여 수확하고, 인산완충식염수(PBS)로 세척한 다음, 추가 실험을 위해 PBS 또는 RCM에 현탁했습니다.
박테리아 발효.
C. 아크네스(105 콜로니 형성 단위(CFU)/mL)를 Gas-Pak을 사용하여 혐기성 조건에서 2% PF68(BASF, NY, USA)의 존재 또는 부재 하에 10mL TSB에서 배양했습니다. 37도에서 . TSB의 PF68 단독은 대조군으로 포함되었습니다. TSB의 Te 0.002%(w/v) 페놀 레드(Sigma)는 발효 지표 역할을 했습니다. 적색-주황색에서 황색으로의 색상 변화는 560 nm(OD560)에서 광학 밀도로 검출된 박테리아 발효의 발생을 나타냅니다.
가스 크로마토그래피-질량 분석(GC–MS) 분석.
C. 아크네스(105 CFU/mL)를 2% PF68의 존재 하에 TSB(10 mL)에서 인큐베이션하였다. 1-일 후 발효 배지를 5000g에서 10분 동안 원심분리하고 상층액을 이전에 발표된 프로토콜을 사용하여 SCFA 검출에 사용했습니다. 발효 배지에서 아세트산(AA), PA, 부티르산(BA) 및 이소-부티르산(I-BA)의 Te 수준은 FFA 테스트 표준( Restek Corporation, Bellefonte, PA, USA) 500-, 1,{13}}, 2,{15}}, 5,{17}} 및 10,{19}} 겹.
B16F10 흑색종 세포 배양.
B16F10 흑색종 세포주는 미국 샌디에이고 캘리포니아 대학의 Richard Gallo 박사와 대만의 Chang Gung University of Science and Technology의 Cheng Ching-Yi 박사가 친절하게 제공한 것입니다. 세포는 37도 및 5%에서 10% 소태아혈청(FBS, Life Technologies) 및 1% 페니실린-스트렙토마이신(Life Technologies)이 보충된 Dulbecco's Modified Eagle's Medium(DMEM, Life Technologies, Carlsbad, CA, USA)에서 배양되었습니다. 이산화탄소. 세포는 70-80% 합류가 될 때까지 성장한 다음 Trypsin-Ethylenediaminetetraacetic acid(EDTA, Life Technologies)로 계대 배양했습니다.
역전사-정량적 중합효소 연쇄 반응(RT‑qPCR).
RT-qPCR을 사용하여 48시간 동안 4mM PA로 처리한 B16F10 흑색종 세포에서 티로시나제 유전자 발현을 연구했습니다. Quick-RNA MiniPrep Kit(Zymo Research, CA, USA)를 사용하여 total cellular RNA를 추출한 후 iScript cDNA 합성 키트(Bio-Rad, Hercules, CA, USA)를 사용하여 cDNA로 역전사하고 RT-qPCR로 증폭했습니다. ABI 7300 시스템(Applied Biosystems, Waltham, MA, USA). 비교 주기 역치(ΔΔCT)를 사용하여 유전자 발현의 정량화를 결정했습니다. 글리세르알데히드 3-포스페이트 탈수소효소(GAPDH)의 유전자 수준은 티로신 키나제 유전자의 정상화에 사용되었습니다. 티로시나제 및 GAPDH용 프라이머는 5'-TGACAAAGCCAAAACCCCCA{13}}'(앞으로)입니다. 5'-TTGTTCAAAAATACTTCCAGTGTGT{16}}'(역방향) 및 5'-TGTGTCCGTCGRGGATCTGA{19}}'(앞으로); 5'-GATGCCTGCTTCACCACCTT3'(역방향).
FFAR2 유전자 녹다운 후 세포 티로시나제 활성.
B16F10 흑색종 세포를 {{4}웰 플레이트에 5×104개 세포/웰의 밀도로 시딩했습니다. 또한, 세포를 FFAR2 선택적 길항제 GLPG0974(0.1μM, GLPG) 및 PA(4mM)로 처리하고 24시간 동안 5% CO2에서 37도에서 배양하였다. 세포를 트립신 처리하고 RIPA 완충액(Thermo Fisher Scientific, NJ, USA)으로 용해시켰다. 용해된 세포를 -80도에서 동결하고 두 번 해동한 다음 12,{16}} rpm에서 10분 동안 원심분리했습니다. 상층액을 96-웰 플레이트에서 1 ug/mL의 Levodopa(L-DOPA, Sigma)와 2:1 비율로 혼합하고 실온(RT)에서 1시간 동안 배양하고 475 nm에서 OD를 인큐베이션했습니다. 감지27.

cistanche의 용도: 티로시나아제의 활성 감소
BrdU 라벨링.
B16F10 흑색종 세포는 1{16}}% FBS, 페니실린 및 스트렙토마이신이 포함된 DMEM의 8-웰 챔버 슬라이드(Thermo Fisher Scientific)에서 70% 합류가 달성될 때까지 성장했습니다. Bromodeoxyuridine(10μM, BrdU, ACROS, New Jersey, USA)을 4mM PA와 함께 배양 배지에 첨가하였다. 배양 배지에 PBS가 첨가된 BrdU를 대조군으로 포함시켰다. 24시간 후, 세포를 4% 퍼플루오로 록시(PFA, Sigma)로 고정한 다음 0.2% Triton X{11}}(Sigma)로 10분 동안 투과화했습니다. 다음으로, 세포를 37도에서 25분 동안 2N HCl로 처리하고, 0.1M 붕산염 완충액(pH 8.5)으로 10분 동안 염산으로 중화하고, 항-BrdU 항체(Abcam, MA, USA)를 배양하기 전에 차단 완충액으로 차단하였다. 하룻밤 및 당나귀 항염소 Alexa Fluor 568 IgG(H + L)(Life Technologies)를 4도에서 1시간 동안 두 번째 항체로 사용합니다. 핵은 4,{27}}디아미디노{28}}페닐인돌(DAPI, Sigma)로 대조염색되었습니다. 이미지는 Olympus BX63 현미경에 연결된 cellSens 소프트웨어로 획득했습니다.
마우스 모델은 UV 광 노출에 의해 생성되었습니다.
마우스 모델은 UVR28의 다양한 역할에 대한 이해를 높이는 데 중요한 역할을 했습니다. UVR은 피부, 특히 노출 부위에서 DOPA 양성 멜라닌 세포를 증가시킵니다. 마우스 귀에 C. 아크네스 주사를 치료하기 위한 프로토콜은 이전 연구3에서 설명되었습니다(이 참조는 C. 아크네스 주사에 대해 이야기하지 않음). ICR 마우스의 귀에 2% PF68이 있거나 없는 C. 아크네스(107 CFU)를 피내 주사한 후 UV 램프(모델 EB{ {10}}C, Spectronics Corp., Westbury, NY, USA) 3일 동안 매일 2분. PBS 또는 PF68이 주입된 마우스 귀에 UVB 노출이 대조군으로 포함되었습니다. 실험 쥐의 다른 그룹에서 귀에 4mM PA를 적용한 후 PBS를 대조군으로 사용하여 UV 노출을 적용했습니다.
FFAR2의 siRNA-매개 유전자 침묵.
FFAR2 유전자를 침묵시키기 위해 GenePharma Co.에서 구입한 FFAR2 수용체(FFAR2 siRNA), siRNA 음성 대조군(NC siRNA), 주사하지 않은 대조군(C)을 표적으로 하는 화학적으로 변형된 siRNA를 사용했습니다. (중국 상하이). 그들의 올리고뉴클레오티드 서열은 siFFAR2: 센스 가닥, 5'-CCGGUGCAGUACAAGUUAUTT-3'; 안티센스 가닥, 5'-AUAACUUGUACUGCACCGGTT{11}}'. 대조군: 센스 가닥, 5'-UUCUCCGAACGUGUUCACGUTT-3'; 안티센스 가닥, 5'-ACGUGACACGUUCGGAGAATT{18}}'. 이러한 화학적으로 변형된 siRNA는 미세바늘(2 mg/kg의 마우스 체중)을 사용하여 마우스의 귀에 피내 주사하여 3일 동안 매일 전달되었습니다. 2일차부터 PA 2%, UV노출 3일동안 발라줍니다. 참고 문헌 30에 설명된 대로 마우스에 siRNA를 주입하기 위한 전처리. 10, 생쥐의 귀를 절제하고 4일째에 염색하였다.
웨스턴 블로팅.
마우스 귀에 화학적으로 변형된 FFAR2 및 대조군 siRNA를 주입한 후 3일 동안 2% PA 및 UVB 노출을 적용했습니다. 3일째에 마우스의 귀를 절단하고 균질화한 다음 RIPA 완충액(Thermo Fisher Scientific)으로 용해시켰다. 세포 용해물(30μg)에 10% SDS-PAGE 겔을 적용한 다음, 이를 폴리(비닐리덴 플루오라이드)(PVDF) 멤브레인(Sigma)으로 옮기고 5%(w/v) 무지방 우유로 차단한 다음 4도에서 FFAR2 Rabbit PolyAb(Proteintech, Rosemont, IL, USA) 또는 -액틴(1:1,{14}}; Cusabio Technology, Houston, TX, USA)에 대한 1차 항체. 이어서 양고추냉이 퍼옥시다제-접합 염소 항토끼 2차 항체(1:5000)(Thermo Fisher Scientific)로 1시간 동안 처리하였다. 단백질 밴드는 화학발광 검출 시약(Thermo Fisher Scientific) 및 Omega Lum C Imaging System(Gel Co., San Francisco, CA, USA)으로 검출되었습니다. ImageJ 소프트웨어를 사용하여 단백질 밴드를 수행했습니다.
멜라닌 세포 계산.
마우스에서 연골을 수동으로 제거하고 피부 조직을 37도에서 20분 동안 티오시안산암모늄(Sigma) 용액에 담그었다. 나머지 피부 조직에서 표피층과 기저층을 박리하고 0.14% L-DOPA를 함유한 0.1M PBS(pH 7.2)에 실온에서 3시간 동안 담가 멜라닌 세포를 염색하고 멜라닌 세포 수를 측정했습니다. 피부 조직에서 이전에 발표된 프로토콜29에 따라 현미경으로 측정되었습니다.
통계 분석.
데이터 분석은 Prism 소프트웨어 Te를 사용하여 unpaired t-test에 의해 수행되었습니다. 통계적 유의성의 Te 수준은 다음과 같이 표시되었습니다. *P<0.05,><0.01,><0.001, and="" ns="non-significant." the="" mean±standard="" deviation="" (sd)="" for="" at="" least="" three="" independent="" experiments="" except="" for="" two="" independent="" western="" blotting="" analyses="" for="" fig.="" 4c="" was="" displayed.="" animal="" experiments="" were="" performed="" with="" at="" least="" three="" animals="" per="" treatment="">

시스탄체 투볼로사
결과
C. 아크네스는 PF68의 발효를 유도한다.
이전 연구는 탄소원으로 화합물의 존재 하에 SCFA 생산 유도를 위한 피부 프로바이오틱스의 발효를 입증했습니다. C. 아크네스가 PF68을 발효시킬 수 있는지 조사하기 위해, 박테리아 발효를 모니터링하기 위한 지표로서 페놀 레드와 함께 C. 아크네스를 TSB 배지에서 PF68과 함께 1일 동안 인큐베이션하였다. 박테리아 단독으로 배양한 TSB 배지에서는 박테리아 복제로 인해 페놀 레드가 빨간색에서 주황색으로 변한 반면, 박테리아와 PF68이 포함된 TSB 배지에서는 페놀 레드 색상이 옅은 노란색으로 변하여 pH가 감소하여 PF68을 사용했음을 나타냅니다. 발효를 위한 탄소원(그림 1A). 또한, 페놀 레드의 OD560은 박테리아 또는 PF68 단독에 비해 박테리아 및 PF68(도 1B)을 함유하는 TSB 배지에서 pH 값의 유의한 감소를 나타내었다. PF68로 배양된 C. 아크네스 발효물에 함유된 Te SCFA는 GC-MS 분석(그림 1C)에 의해 확인되었으며 AA, PA, BA 및 I-BA 산인 것으로 나타났으며 PA11이 가장 높은 농도를 나타냈습니다(그림 1D). ).

그림 1. 고분자를 이용한 박테리아 발효는 세포내 pH의 감소를 동반하였다.
PA‑FFAR2를 통한 멜라닌 생성에 대한 PA의 시험관 내 효과.
Fatty acids modulate the degradation of tyrosinase, a crucial enzyme involved in melanin biosynthesis in melanocytes and melanoma cells31. Therefore, to detect the in vitro effect of PA on melanin synthesis, B16F10 melanoma cells were treated with 4 mM PA for 48 h, with the decreased expression of the tyrosinase in PA treated melanoma cells compared to the control (Fig. 2A). The immunostaining of PA-treated melanoma cells after BrdU labeling showed that PA did not alter the proliferation of melanoma cells (Fig. 2B). Furthermore, the effect of PA and AA, two highly expressed SCFAs in the fermentation filtrate (Fig. 1D)32, on melanin production was assessed in melanoma cells, with PA causing a>AA에 비해 멜라닌 생성이 2배 감소합니다(그림 2C). PA 및 AA와 같은 SCFA는 FFAR2 및 FFAR3과의 상호작용을 통해 기능을 조절하며, PA는 이 두 수용체에 대해 가장 강력한 SCFA 중 하나입니다. FFAR2와의 상호 작용을 통한 PA 조절을 고려할 때 선택적 억제제를 사용하여 이 수용체의 신호 전달을 차단하는 것은 멜라닌 생성 조절에서 PA의 역할을 평가하는 데 유용한 접근 방식이 될 수 있습니다. Te 세포성 티로시나아제 활성은 PA로 처리하기 전에 FFAR2 선택적 길항제 GLPG를 사용하여 FFAR2를 차단함으로써 변하지 않았고 대조군과 대조적으로 GLPG 없이 감소하였다(도 2D). 이러한 결과는 세포 증식이 변경되지 않은 흑색종 세포에서 티로시나제 키나제 활성을 억제함으로써 멜라닌 함량의 감쇠에서 PA-FFAR2의 효과적인 역할을 입증했습니다.
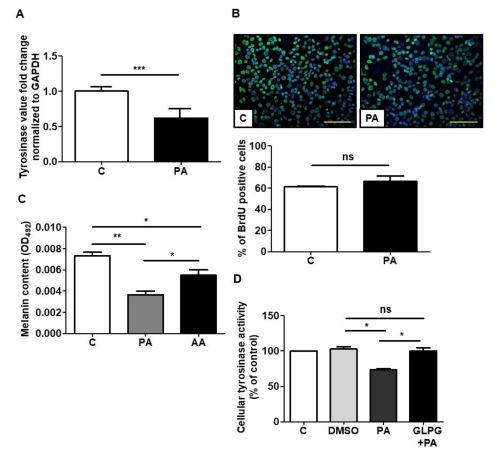
그림 2. PA 처리 후 흑색종 세포에서 티로시나제 유전자 발현 및 세포 증식의 효과.
C. 아크네스와 PF68의 혼합물은 마우스 귀에서 UVB로 유발된 기능 멜라닌 세포를 억제했습니다.
발효 추출물 또는 지방산의 국소 적용은 티로시나제 분해를 조절하여 UV로 인한 피부 과색소침착을 감소시키는 것으로 나타났습니다34,35. 이전 연구에서는 UV 노출 후 멜라닌 생성이 표피 또는 진피에서 기능하는 멜라닌 세포의 활성화로 인한 것임을 입증했습니다. PF68의 C. 아크네스 발효의 주요 SCFA인 PA가 시험관 내에서 멜라닌 생성을 효과적으로 감소시킬 수 있다는 것을 확인한 후, 우리는 C. 아크네스와 PF68이 생체 내에서 이에 미치는 영향을 조사했습니다. ICR 마우스의 귀를 C. 아크네스 및 PF68의 주사와 동시에 3일 동안 격일로 UVB에 노출시켰다. PBS 또는 C. 아크네스 또는 PF68 단독 주사를 대조군으로 포함시켰다. 마우스 귀의 피부 조직에서 표피층과 기저층을 박리하고 멜라닌 세포를 L-DOPA로 염색했습니다. UVB 노출 후 멜라닌 세포 수가 크게 증가했으며 C. 아크네스 또는 PF68 단독 주입 후에도 변화가 없었습니다. 그러나 C. 아크네스와 PF68의 혼합물로 처리한 후 UVB 노출 그룹에서 DOPA 양성 멜라닌 세포 수의 상당한 감소가 감지되었습니다(그림 3A).

그림 3. UVB에 의한 멜라닌 세포의 유도 및 다양한 처리에 의한 억제.
C. 아크네스 발효 대사산물인 PA에 의한 마우스 귀의 UVB 유발 기능 멜라닌 세포 개선.
UV 유도 멜라닌 생성에 대한 PA의 직접 적용 효과를 평가했습니다. 대조군의 마우스 귀 피부에서 UV-유도된 과색소침착 및 티로시나제 발현은 PA를 3일 동안 국소 도포한 후 유의하게 감소되었습니다(그림 3B). Tus, PA, C. 아크네스의 PF68 발효 대사산물은 UVB 유도에 의한 멜라닌 합성과 함께 기능하는 멜라닌 세포 생성을 억제합니다. 티로시나아제 발현은 대조군에 비해 PA 처리 세포에서 현저하게 감소하였다(도 3C).
PA는 생체 내에서 FFAR2를 통해 UVB 유도 기능 멜라닌 세포를 억제합니다.
PA와 동족 수용체의 상호작용을 통해 외인성 멜라닌 생성의 감소가 발생했는지 확인하기 위해 FFAR2가 마우스 귀의 피부 멜라닌 세포에서 녹다운된 후 UVB 노출 및 PA 처리가 뒤따랐습니다. UVB-유도된 멜라닌 세포의 증식 증가와 티로시나아제 활성은 PA 적용 후 NC siRNA를 주사한 마우스 귀 표피에서 유의하게 감소하였다(도 4A, B). 그러나, 멜라닌 세포의 수와 티로시나제 활성은 UVB 조사된 마우스 귀 표피에 PA를 적용한 후에도 FFAR2로 녹다운된 후에도 변하지 않은 채로 남아 있습니다. 웨스턴 블롯 분석을 통해 FFAR2의 단백질 발현 수준을 측정하여 FFAR2 유전자 녹다운을 확인하였다(도 4C). Tus, PA는 PA-FFAR2가 멜라닌 생성에 잠재적인 역할을 하는 티로시나제의 활성을 억제하여 멜라닌 생성을 방해합니다.

시스탄체 튜볼로사 추출물
논의
UV 조사에 대한 피부 방어의 중요한 요소인 멜라닌은 멜라닌 세포의 멜라노솜에서 합성되어 수지상 팁을 통해 인접한 각질 세포로 전달되고 결국 피부 표피 전체에 분포됩니다. 박테리아 발효 대사 산물은 UV 유발 피부 염증 및 감염 장애에 대한 유익한 효과로 인해 피부 치료에 점점 더 많이 사용됩니다3. 이 연구에서 우리는 C. 아크네스의 PF68 발효의 주요 대사산물인 PA가 FFAR2를 통해 시험관 내 및 생체 내에서 티로시나제 활성을 억제함으로써 UVB 유도 기능 멜라닌 세포 수준을 감소시킴을 입증했습니다.
이전 연구에서는 프로바이오틱 LA 및 락토바실러스 박테리아의 발효 대사산물에 의한 티로시나제 억제를 통한 멜라닌 생성 억제가 입증되었습니다24,38,39. 또한 고분자량 PEG 기반 폴리머(~20,{5}})는 아세테이트와 프로피오네이트40를 생성하는 그람 음성 박테리아에 의한 발효를 통해 완전히 분해되었습니다. 이 연구에서 PA(~4mM)는 C. 아크네스의 PF68 발효 여액에서 가장 풍부한 SCFA였으며 AA보다 더 효과적으로 멜라닌 세포의 멜라닌 함량을 감소시켰습니다. 또한, 4mM PA 처리는 멜라닌 세포에서 세포성 티로시나아제 활성을 유의하게 억제하여 PA에 의한 멜라닌 생성 억제가 티로시나아제 유전자 발현의 감소를 통해 발생했음을 입증했습니다. 사람들은 동일한 수의 멜라닌 세포를 가지고 있기 때문에 피부 색소 침착에 영향을 미치는 것이 아니라 UV 조사에 의해 기능하는 멜라닌 세포의 활성화에 영향을 미칩니다36,41. 여기에서 4mM PA 처리는 멜라닌 세포 증식을 변경하지 않았으며 이는 세포 손상을 일으키지 않는 효과적인 치료 옵션임을 나타냅니다. 감소된 멜라닌 세포 수와 티로시나제 활성은 C. 아크네스와 PF68의 혼합물을 주사한 마우스 귀 피부 조직에서도 관찰되었으며, 이는 멜라닌 생성 억제가 PF68을 탄소로 사용하는 C. 아크네스 발효의 발효 대사산물을 통해 매개될 가능성이 있음을 보여줍니다. 원천. 또한, 우리의 연구는 PA가 부모 박테리아인 C. 아크네스의 성장에 변화가 없는 우수한 항균제로 입증되었으며, PA는 피부 미생물군유전체의 균형을 방해하지 않는 강력한 대사 산물임을 보여줍니다.
멜라닌 생성은 여러 신호 시스템에 의해 시작되고 조절되며, 티로시나아제는 티로신을 DOPA로, 그리고 도파퀴논으로 전환하여 멜라닌 세포 색소의 형성을 촉진합니다. 대부분의 경우 피부 미백 시약은 FFAR2를 통해 다양한 수준의 멜라닌 생성에 작용하여 티로시나제 활성에 영향을 미치거나 티로시나제를 직접 표적으로 삼아 피부의 멜라닌 생성을 억제합니다. PA 및 AA와 같은 SCFA는 FFAR2 또는 FFAR3과 같은 선택적 동족 수용체에 결합하여 효과를 발휘하며, PA는 두 수용체에 대해 가장 강력한 SCFA 중 하나입니다. 선택적 FFAR2 길항제인 GLPG 및 FFAR2의 siRNA 매개 유전자 침묵은 FFAR23,48의 차단을 지원합니다. 현재 연구에서 마우스의 귀 피부 조직에서 증가된 멜라닌 세포 수와 티로시나제 유전자 발현은 마우스에서 FFAR2 녹다운에 PA를 적용한 후에도 UVB 방사선에 대한 반응으로 변하지 않았습니다(그림 4A). 또한 시험관 내 PA 처리 후 티로시나제 유전자 발현이 감소했지만 선택적 FFAR2 길항제인 GLPG로 FFAR2 유전자를 차단하면 티로시나제 유전자 발현을 약화시키는 PA의 효과가 개선되었습니다. FFAR2를 차단한 후 FFAR2의 손실은 PA 처리 후 티로시나제 활성의 발현을 증가시킵니다. C. 아크네스의 발효 대사산물인 PA와 AA 모두 FFAR2 결합에 대해 유사한 친화력을 가지고 있지만20, 멜라닌 세포에서 티로시나제 활성을 약화시키는 데 있어 AA의 상대적으로 낮은 효능은 멜라닌 생성에 대한 포스트바이오틱으로서 PA의 치료 가능성을 입증합니다.
UVR이 피부에 미치는 광손상 효과가 주목받고 있다. 자외선 차단제 및 색소 침착 방지 제품이 널리 사용되지만 안전성, 피부 침투성 및 치료 효능에 대해서는 여전히 의문의 여지가 있습니다49. 아보벤존은 자외선에 대한 높은 효능으로 인해 자외선 차단제의 일반적인 구성 요소이지만 광 불안정성으로 인해 안전하지 않으며 만성 적용 후 혈액에서 검출되었습니다50,51. 탄소원으로 probiotic 박테리아 또는 고분자의 발효 대사 산물에 의한 tyrosinase 발현 차단을 통한 효과적인 피부 미백 개발은 멜라닌 생성을 억제하는 효과적이고 자연스러운 방법입니다38,39. 화장품에 생 프로바이오틱스의 사용이 엄격하게 규제됨에 따라 생 프로바이오틱스 유산균의 발효 대사 산물을 통한 유익한 효과의 촉진이 실현 가능한 응용이 되었습니다. 게다가, 프리바이오틱인 PF68은 C. 아크네스 발효로부터 SCFA의 생산을 증가시킬 수 있으며 생물학적 안정성을 향상시키고 인체와의 상호작용에서 6-머캅토퓨린이 로딩된 미소구체와 같은 다양한 치료제를 보조하는 데 사용되었습니다52. 또한 PF68은 세포막에 통합되어 세포로 이동할 수 있으며 항균제의 안정적인 젤 캐리어로 사용되어 피부 치료에서 약물의 표면 용해도를 증가시킵니다. 따라서 PF68은 의약품 및 화장품 개발을 위한 안전하고 효과적인 옵션으로 간주되었습니다. C. 아크네스의 발효 활성을 증가시키는 발효 개시제로서의 PF68의 기능에 더하여, 그것은 또한 약제 시약의 유효량을 감소시키고 난수용성 약물의 용해도를 향상시키는 보조제가 될 가능성이 있습니다.
전반적으로, 이러한 결과는 PA-FFAR2 상호작용이 UVR로 인한 과다색소침착에 대한 프로바이오틱스 또는 포스트바이오틱스의 효과에서 중심 메커니즘일 수 있음을 입증합니다. PA 치료는 멜라닌 세포 증식에 영향을 미치지 않았습니다. 화학 요법과 비교할 때 프로바이오틱스의 대사 산물은 더 부드럽고 자연적입니다53. C. 아크네스의 PF68 발효 대사산물이 멜라닌 생성을 억제하는 정확한 기전은 불분명하지만, 본 연구의 증거는 SCFAs-FFAR2-티로시나제 경로의 관련을 시사합니다. 이러한 결과는 향후 색소침착질환의 임상적 치료 및 미백 제품의 적용범위를 확대하는 화장품 개발에 도움이 될 것이다. 마지막으로, 프로바이오틱스의 다양성은 과색소침착에 대한 맞춤형 치료법과 더 높은 성능을 지닌 전용 제품 개발을 제공합니다.

