암면역주기에 기초한 나노물질과 면역치료의 교향곡
Sep 13, 2023
추상적인
면역 체계는 암의 시작과 진행에 관여합니다. 암과 면역에 대한 연구는 임상적으로 성공적인 여러 면역요법의 개발에 기여했습니다. 이러한 면역요법은 종종 암 면역 주기의 단일 단계에 작용합니다. 최근 몇 년 동안 새로운 나노물질의 발견으로 나노물질의 기능과 응용 가능성이 획기적으로 확대되었습니다. 약물 전달 플랫폼으로 작용하는 것 외에도 일부 나노물질은 암세포의 면역원성 세포 사멸(ICD)을 유도하거나 면역조절제로서 면역 반응의 프로필과 강도를 조절할 수 있습니다. 다재다능함을 바탕으로 나노물질은 항암 면역 반응의 결과를 향상시키기 위해 암 면역 주기의 여러 단계를 동시에 목표로 하는 여러 약물 또는 치료 전략을 위한 통합 플랫폼 역할을 할 수 있습니다. 암 면역주기에 기초한 암 면역치료에서 나노물질의 중요한 역할을 설명하기 위해, 이 검토에서는 면역 체계와 암 사이의 혼선과 약물 전달체, ICD 유도제 및 면역 조절제를 포함한 나노물질의 현재 응용을 포괄적으로 설명할 것입니다. 또한, 본 리뷰에서는 암 면역주기를 기반으로 한 복합 암 면역치료법 개발에 관한 지식에 대한 자세한 논의를 제공하여 나노물질을 활용한 치료의 효율성을 극대화할 수 있기를 기대합니다.

cistanche 보충 혜택 - 면역력 증가
1. 소개
가장 치명적인 질병 중 하나인 암은 현재 전 세계적으로 약 2천만 명의 생명을 위협하고 있습니다1. 전통적으로 암 환자의 치료요법은 수술, 화학요법, 방사선요법이 주요 치료요법이었다. 그러나 전신 독성, 암 재발 및 전이는 환자의 예후에 영향을 미칩니다2. 종양학과 면역학의 상호작용에 대한 이해가 높아짐에 따라 암을 방어하기 위해 환자의 면역체계를 활용하는 것이 가능해졌습니다. 면역학적 기억을 유도할 수 있는 암 면역요법은 암 성장, 재발 및 전이에 대한 지속적인 억제 효과를 입증했습니다3. 면역관문차단(ICB)4e7 및 키메라 항원 수용체 T(CAR-T)8e10 세포 요법과 같은 암 면역요법은 일부 환자, 특히 혈액암 환자의 전체 생존율을 향상시켰습니다. 그러나 이러한 치료법은 고형 종양11에서 제한된 반응을 유도하고 전신 염증12과 관련이 있습니다. ICB와 CAR-T 치료의 임상적 성공 이후 수많은 면역치료제와 조합 전략이 개발되었습니다. 면역요법은 암 치료요법을 재정의하며 현장 암이나 기존 암의 치료에만 국한되지 않습니다. 그러나 불완전한 면역학적 지식과 기술적 한계로 인해 여전히 보다 효율적인 암 면역요법의 개발이 제한되고 있습니다. 새로운 면역학적 표적, 약물 전달 방법 및 시너지 치료법은 암 면역 치료법의 획기적인 발전을 가져올 가능성이 높습니다.
최근 암면역학의 발견으로 암면역치료의 지평이 넓어졌습니다. 암세포의 급속한 증식 과정에서 발생하는 돌연변이로부터 유래된 신생항원은 종양 항원의 면역원성을 크게 증가시킵니다13. 신생항원 백신은 세포독성 T(CD8+ T) 세포를 활성화시키는 것으로 나타났습니다14. 또한, 높은 암 돌연변이 부담은 암 면역요법의 중요한 예후 지표입니다15,16. ICB 치료 중 종양 침윤 CD8+ T 세포의 양은 치료 효과와 직접적으로 연관됩니다17. 종양 항원에 대해 침윤하는 CD8+ T 세포의 수가 더 많은 "뜨거운 종양"은 ICB 치료에 더 큰 반응을 나타냅니다. 암세포에 대한 면역반응을 활성화하는 것 외에도 종양의 면역억제 미세환경을 조절하는 것도 필요합니다. 다양한 사이토카인과 면역세포가 종양 면역억제 미세환경의 발달과 유지에 관여합니다. 여기에는 인터루킨(IL)-10, 변환 성장 인자(TGF)-b, 암세포 표면에 과발현되는 면역 체크포인트, 조절 T(Treg) 세포, M2-형 종양 관련 대식세포가 포함됩니다. (TAM)19. 최근에는 암조직과 면역체계의 상호작용을 설명하는 암면역주기(cancerimmunitycycle)가 등장하고 있으며, 이 개념은 지속적으로 업데이트되고 개선되고 있습니다. 암 면역주기는 손상된 암세포에서 방출된 종양 항원이 APC 세포에 포획되어 CD8+ T 세포에 프라이밍되는 과정과 CD8+ T 세포가 암 조직에 침투하여 암세포를 죽이는 과정을 설명합니다. 암 면역치료에서는 암 면역주기의 모든 단계를 잘 고려해야 합니다. 더욱이, 면역 반응의 시간적, 공간적 활성화를 최적화하는 것은 안전하고 오래 지속되는 항암 효과를 달성하기 위한 기초입니다20.
암 면역요법은 일반적으로 모든 잠재적인 종양에 도달할 수 있도록 전신적으로 투여됩니다. 그러나 이는 대장염, 설사, 내분비병증과 같은 심각한 면역 관련 부작용을 동반할 수 있습니다23,24. 따라서 암 관련 면역세포를 표적화하고 특이적으로 활성화하는 것이 중요합니다.
임상의, 생물학자, 화학자 및 재료 과학자의 공동 노력으로 인해 나노물질은 이제 암 면역요법에서 중요하고 다양한 역할을 수행합니다25e28. 나노물질은 유리 소분자 약물에 비해 암 조직에서 강화될 수 있으며, 이를 향상된 투과성 및 유지(EPR) 효과라고 합니다. EPR 효과는 원래 과투과성 종양 혈관계 및 림프 배수 장애로 인해 발생한다고 믿어졌습니다. 최근 보고서에 따르면 대부분의 나노물질은 활성 경내피 경로를 통해 종양 조직에 들어가는 것으로 나타났습니다31,32. EPR 메커니즘에 대한 보다 자세한 연구를 통해 나노물질을 암 조직 내에서 보다 효율적으로 강화하도록 최적화할 수 있습니다. 이상적인 플랫폼인 나노물질은 조합 또는 시너지 치료 전략을 위해 여러 약물을 통합할 수 있으며, 그 중 일부는 광열, 광역학 및 자기 반응 기능을 포함한 기능을 보유합니다. 또한 일부 나노물질은 부분적으로 APC에 의한 항원 흡수 및 제시를 유도하여 면역체계를 자극할 수 있습니다. 나노물질의 이러한 특성은 공간적, 시간적 정확성으로 암 면역주기의 여러 단계를 동시에 활성화할 수 있게 하여 면역 관련 부작용을 제어하는 데 도움이 되고, 면역 과정의 여러 단계를 시너지적으로 활성화하여 항암 면역 반응을 효과적으로 증폭시킵니다. 암 면역요법에서 나노물질의 현재 적용에는 약물 전달체(세포사멸 유도제, 면역자극제, 광열 또는 광역학 분자, ICB 항체의 전달), 기능성 물질(광열 또는 광역학 과정 유도) 및 면역조절제로서의 사용이 포함됩니다. 본 리뷰에서는 암 면역주기에 대한 면역 메커니즘과 지식을 요약하고, 암 면역주기를 기반으로 암 면역치료를 촉진하기 위한 나노물질의 응용에 대해 자세히 논의했다. 마지막으로, 우리는 암 면역치료에서 나노물질의 결합과 적용을 더욱 촉진할 수 있는 돌파구를 찾기를 희망합니다.
2. 암과 면역의 게임
암 면역요법은 암 발달의 다양한 단계에서 종양과 면역 체계 사이의 상호 작용과 누화를 포함하는 복잡한 학제간 분야입니다. 처음에는 면역 과정과 암 발병 사이에 명확한 연관성이 없다고 믿어졌습니다. 지난 수십 년 동안 암에 면역 과정이 관여한다는 사실을 뒷받침하는 증거가 점점 더 많이 발표되었습니다39,40. 또한, 암은 면역 과정에 영향을 미치고 면역 탈출 또는 면역 억제로 이어지는 것으로 나타났습니다41. 이러한 발견을 바탕으로 수많은 연구가 환자의 면역 체계를 활성화하거나 강력한 면역 세포를 채택하여 암 성장을 모니터링, 억제 및 역전시키는 데 중점을 두었습니다. 그러나 면역 과정의 단일 구성 요소에 대한 암 면역요법의 효과는 암으로 인해 유발된 면역 과정의 다른 부분을 차단함으로써 손상될 수 있습니다. 따라서 암의 발생 및 치료와 관련된 면역반응에 대한 자세한 이해를 해명하는 것이 시급하다.
2.1. 암-면역주기
암-면역 주기는 2013년 Chen et al.20에 의해 처음 요약되었습니다. 이는 암 조직에 대한 세포 면역 과정을 설명합니다. 여기에는 여러 단계가 포함됩니다. 1단계, 종양 항원은 손상된 암세포에서 방출되어 처리를 위해 수지상 세포(DC)에 포획됩니다. 2단계, DC는 T 세포의 MHCI 및 MHCII 분자에 종양 항원을 제시합니다. 3단계, 효과기 T 세포 반응을 프라이밍하고 활성화하는 단계; 4단계, 효과기 T 세포가 종양으로 순환합니다. 5단계, 효과기 T 세포가 종양 조직에 침투합니다. 6단계, 효과기 T 세포는 TCR과 MHC I 복합체에 의해 암세포를 인식합니다. 7단계, 효과기 T 세포가 암세포를 죽입니다. 암세포를 죽이는 마지막 단계는 종양 항원의 방출에 기여하여 암 면역주기의 새로운 라운드를 시작합니다. 따라서 암 면역주기는 시작 시 자체적으로 유지될 수 있습니다. 원래의 암 면역주기는 암 치료에서 세포 면역의 중요한 기능을 강조합니다. 그러나 체액성 면역과 선천성 면역이 암 발생을 억제하는 데 중요한 역할을 한다는 증거가 많이 있습니다43. 그림 1에서 설명한 것처럼 암세포의 종양 항원은 APC에 의해 포착됩니다. 외인성 항원으로서 종양 항원은 엔도솜으로만 세포내이입되므로 일부 시스템은 일반적으로 엔도솜에 풍부한 MHC II 분자와 결합하여 CD4+ T 세포의 프라이밍 및 활성화를 추가로 유도합니다. 이 경로는 항체-항원 공침 또는 NK 세포에 의해 매개되는 항체 의존성 세포 매개 세포독성(ADCC)에 의해 암세포를 죽이는 고전적인 체액성 면역입니다. 그러나 CD8a+ DC와 같은 특정 DC 또는 종양 항원의 엔도솜 누출과 같은 특수한 상황은 종양 항원의 교차 제시를 유도합니다. 교차 제시 상황에서 세포질에 존재하는 종양 항원은 항원성 펩티드 운반체(TAP)에 의해 소포체(ER)로 운반되고 새로 조립된 MHC I 분자와 결합됩니다. MHC I/항원 복합체의 제시는 결국 CD8+ T 세포의 활성화로 이어집니다. 따라서 본 고찰에서는 암 면역주기의 내용을 재구성하고 증폭시켰다(그림 2). 우리는 암 면역주기를 다음 단계로 설명했습니다. (1) 손상되거나 죽어가는 암세포로부터 종양 항원의 방출; (2) APC에 의한 종양 항원의 흡수 및 제시; (3) 항암 체액성 및 세포성 면역을 유발하기 위한 CD4+ 및 CD8+ T 세포의 프라이밍 및 활성화; (4) NK 세포, 종양 항원 특이적 항체, CD8+ T 세포의 밀매; (5) NK 세포, 종양 항원 특이적 항체, CD8+ T 세포의 암 조직으로의 침투 및 농축; (6) CD8+ T 세포의 세포독성과 NK 세포에 의한 ADCC 효과를 통한 암세포 인식 및 박멸.

그림 1 암 치료의 적응 면역. 체액성 면역: APC는 MHC II 분자에 의해 항원을 흡수하고 제시하여 CD 4+ T 세포를 활성화합니다. CD4+ T 세포는 B 세포에 항원을 제시하여 항원 특이적 항체를 분비합니다. 항체는 항원과 결합하여 대식세포에 의한 소화를 위해 공동침전되거나 NK 세포에 의해 매개되는 ADCC 효과를 유도합니다. 세포 면역: 암세포는 APC에 의해 삼켜집니다. APC는 MHC I 분자에 의해 순수 CD8+ T 세포에 항원을 교차 제시하며, 이는 프라이밍된 CD8+ T 세포에서 CTLA{7}} 발현을 동반합니다. 프라이밍된 CD8+ T 세포는 MHC I/항원 복합체를 통해 암세포를 인식하고 퍼포린, 그랜자임 및 Fas/FasL 경로를 통해 세포를 죽입니다. 그러나 CTLA{10}} 또는 PD{11}}와 해당 리간드의 결합은 프라이밍된 CD8+ T 세포의 기능 장애를 유도할 수 있습니다.
2.2. 암 조직의 면역 탈출 및 면역 억제
암과 면역의 관계는 매우 복잡합니다. 최근 연구에 따르면 만성 염증이 암의 시작과 성장에 기여하는 것으로 나타났습니다. 종양 형성 과정에서 암세포에서 유전자 돌연변이 또는 대사산물 변이가 발생합니다. CD8+ T 세포는 암세포에 있는 MHC I 분자에 의해 나타나는 비정상 항원을 모니터링하여 암세포를 인식하고 파괴하는데, 이는 매일 약 107개의 e109 인간 세포에서 돌연변이가 발생한다는 점을 고려하면 암 발생 빈도를 낮추는 것입니다. 일반적으로 암세포에 대한 CD8+ T 세포의 살해 과정은 암 면역주기를 시작하고 암 발생을 효율적으로 억제할 수 있습니다. 그러나 CD8+ T 세포는 때때로 돌연변이 세포의 하위 집합을 인식하지 못하는 경우가 있는데, 이를 암세포의 면역 탈출이라고 합니다. 더욱이, 종양 면역억제 거대환경은 암 면역주기의 작동을 방해하기도 합니다. 면역탈출과 면역억제의 주요 원인을 정리하면 다음과 같다(Fig. 3).
(1) 면역 선택을 통해 상대적으로 면역원성이 약한 종양이 면역 감시를 피해 선택적으로 증식할 수 있습니다47. 발암성 바이러스 및 화학적 발암물질에 의해 유발된 암은 면역원성이 높고 면역체계에 의해 쉽게 제거되는 반면, 동물의 자연발생 암은 면역원성이 약하고 유지되는 경향이 있습니다48. (2) 암세포 표면에 항원을 차단하거나 묻어두는 것은 면역세포의 인식과 공격에 영향을 준다49. 일부 암세포는 시알산51 또는 당단백질52과 같은 점액다당류50를 과발현하여 CD8+ T 세포가 MHC I에 의해 제시된 항원을 인식하는 것을 방지합니다. 시알산을 제거하면 항암 면역 반응이 향상되는 것으로 밝혀졌습니다53,54. (3) 암세포 표면의 MHC I 분자 발현 감소는 프라이밍된 CD8+ T 세포 인식을 제한할 수 있습니다. 그러나 MHC I 분자는 NK 세포의 킬러 세포 억제 수용체(KIR)에 결합하여 NK 세포도 억제합니다. MHC I 분자가 부족하면 NK 세포가 활성화되어 암세포의 용해 또는 세포사멸을 중재합니다57. 따라서 암세포는 비고전적인 MHC I 분자(HLA-E 및 HLA-G)를 발현하여 KIR과 결합하고 NK 세포의 활성을 억제합니다. (4) 암세포 표면의 Fas 발현 장애는 CD8+ T 세포가 Fas/FasL 경로를 통해 암세포 사멸을 유도하는 능력을 제한합니다59. 더욱이 일부 암에서는 FasL을 과발현 및 분비하여 Fas 분자를 T 세포에 결합시켜 T 세포의 사멸을 유도합니다. (5) 암세포는 IL{24}} 및 TGF-b와 같은 억제 인자를 분비하여 숙주 면역 반응을 억제합니다61,62. 이러한 억제 분자는 암 조직에 축적되어 강력한 면역 억제 미세 환경을 형성하여 침투하는 면역 세포를 비활성화하고 죽입니다63. 또한, 암 조직에서는 간질세포가 인돌아민-2,3- 디옥시게나제(IDO)를 분비하여 T 세포의 증식을 억제합니다64. IDO는 트립토판 대사를 위한 속도 제한 효소이며 미세환경에서 트립토판을 소모하여 이펙터 T 세포 증식을 억제합니다65. 일반적인 암 관련 사이토카인은 표 1 66e77에 나열되어 있습니다. (6) 암 관련 섬유아세포(CAF), 조절 T(Treg) 세포, 골수 유래 억제 세포(MDSC) 및 M2-형 종양 관련 대식세포(TAM)를 포함한 억제 면역 세포가 종양 조직에 존재합니다. ). 치유되지 않는 상처로 간주될 수 있는 암은 섬유아세포의 지속적인 활성화를 포함하여 부상과 유사한 반응을 유발할 수 있습니다. 암이 진행되는 동안 암세포는 혈관 내피 성장 인자(VEGF)를 분비하고 fifi-섬유아세포, 내피 세포 및 염증 세포를 모집합니다.

그림 2. 암-면역 주기. (1) 손상되거나 죽어가는 암세포로부터 종양 항원의 방출; (2) APC에 의한 종양 항원의 흡수 및 제시; (3) 항암 체액성 및 세포성 면역을 유발하기 위한 CD4+ 및 CD8+ T 세포의 프라이밍 및 활성화; (4) NK 세포, 종양 항원 특이적 항체, CD8+ T 세포의 밀매; (5) NK 세포, 종양 항원 특이적 항체, CD8+ T 세포의 암 조직으로의 침투 및 농축; (6) CD8+ T 세포의 세포 독성과 NK 세포에 의해 매개되는 항체 의존성 세포 매개 세포 독성(ADCC)을 통해 암세포를 인식하고 근절합니다. 그림 2의 디자인은 Ref.의 그림 1에서 영감을 받았습니다. 20 저작권 허가를 받았습니다. Copyright ª 2013 Elsevier Inc. 섬유아세포와 염증 세포는 암 조직에서 자가분비 회로를 형성하는 숙주 유래 VEGF의 주요 자원입니다78. 그러나 상처 치유 후 관찰된 감소된 섬유아세포 및 염증 내 세포 활성은 암에서는 발생하지 않습니다. (7) 면역 체크포인트
T 세포 활성화에는 항원 결합 MHC I 분자와 TCR의 결합이 필요하며 보조 자극 또는 억제 신호 또는 면역 체크포인트에 의해 조절됩니다(표 2). 면역 체크포인트 쌍은 자가 관용을 달성하고 항병원체 면역 동안 면역 체계가 주변 정상 조직을 손상시키는 것을 방지하는 중요한 전략입니다. 면역 체크포인트는 "자기" 및 "나를 먹지 마세요" 신호를 T 세포에 전송합니다. 암세포는 면역 체크포인트 신호를 상향 조절하여 면역 감시를 피합니다. ICB 전략은 항암 면역을 촉진하는 강력한 치료법을 제공합니다. CTLA-4는 프라이밍된 CD8+ T 세포에서 우세하게 발현되며 CD28과 B7 리간드를 공유합니다. 항원 제시와 함께 B7과 CD28의 결합은 순수 T 세포를 활성화시킵니다. 반대로, B7이 CTLA에 결합하면 T 세포 활성화가 방지됩니다. 프라이밍된 CD8+ T 세포에서 CTLA-4의 상향 조절은 세포 면역의 과잉 작용을 방지합니다79. CTLA-4는 주로 프라이밍된 CD8+ T 세포에서 발현되지만 Th 및 Treg 세포에서도 발견됩니다80. Th 세포에 CTLA{20}}가 관여하면 Th 활성이 감소하는 반면, Treg 세포에 CTLA{21}}가 발현되면 면역 억제 효과가 향상됩니다81. PD-1의 주요 기능은 항병원체 염증 반응에서 말초 조직의 T 세포 활동을 제한하는 것입니다. 그럼에도 불구하고 암이 진행되는 동안 면역억제 기능을 가지고 있습니다. PD-1는 CD8+ T, Treg, B 및 NK 세포를 포함한 많은 종양 침윤 림프구(TIL)에서 발현됩니다82. PD-1의 일반적인 리간드는 PD-L1과 PD-L2이며, 이는 일반적으로 암세포에서 과다 발현됩니다83. PD-1와 그 리간드 사이의 연관성은 CD8+ T 및 NK 세포의 기능 장애를 유도할 수 있습니다. 그러나 PD-1는 리간드 84가 존재할 때 Treg 세포의 증식을 향상시킵니다. 고형암에서 PD-L1은 PD-1의 주요 리간드입니다. 그러나 PD-L1 발현 수준은 다양한 암에서 이질적이며 이는 PD{44}} 및 PD-L1에 대한 치료 전략의 타당성을 고려할 때 중요할 수 있습니다. CTLA-4 또는 PD-1 차단의 항암 효과는 CD8+ T 및 NK 세포 활성화와 Treg 세포 억제의 시너지 효과에서 발생합니다.

그림 3. 암 조직의 면역억제.
풀 사이즈 테이블

2.3. 암 면역주기를 회복시키는 면역항암치료
암의 시작, 발생 및 전이 과정에서 면역 체계의 역할이 점점 더 주목을 받고 있습니다. 암과 관련된 암 면역주기의 확인은 환자의 면역요법 사용을 뒷받침해 왔습니다. 면역치료제가 더욱 표적화되면서 항암면역치료를 받는 환자의 임상 결과가 점차 개선되고 있는 한편, 안전성 프로필도 개선되고 있습니다. 일반적으로 암 면역주기를 직접적으로 재개하거나 암 면역주기에 대한 면역억제 효과를 완화시키는 면역항암치료제는 암을 퇴치할 수 있는 가능성이 크다. 암 면역주기는 스스로 유지될 수 있기 때문에 암 면역주기의 모든 단계를 촉진하는 모든 면역요법은 자가 증폭된 항암 효과를 달성할 수 있습니다. 현재 사용되고 있는 암 면역주기를 회복시키는 암 면역치료제는 비특이적 면역치료, 단일클론항체치료, 입양세포치료(ACT), 항종양백신치료 등이 있다.
2.3.1. 비특이적 면역요법(사이토카인 및 면역자극제)
주로 사이토카인과 면역자극제를 포함한 비특이적 면역요법은 일반적으로 암세포에 대한 면역반응을 체계적으로 활성화합니다. 비특이적 면역요법은 일반적으로 APC의 종양 항원 흡수 유도, CD8+ T 세포의 활성화 촉진, 사이토카인 자극을 통한 종양 면역억제 환경 완화 등 암 면역주기를 촉진하는 다양한 메커니즘을 가지고 있습니다. Coley85는 19세기 말 암 환자에게 보조제로 박테리아 추출물(콜리 독소)을 처음 투여했습니다. Coley의 독소는 사이토카인 수준을 변경하고 일부 환자의 종양 제거로 이어졌습니다. 그 후, IL-2, IFN-g 및 GM-CSF86를 포함한 수많은 사이토카인이 항암 효과를 갖는 것으로 입증되었습니다. IL-2 및 IFN-g는 유망한 항암 잠재력을 입증했습니다. 그러나 IL-2 및 IFN-g의 임상 적용은 전신 투여 후 심각한 독성으로 인해 방해를 받습니다87. 사이토카인과 표적 단백질을 융합하면 종양 내 축적을 증가시키고 후속 결과를 개선하는 동시에 전신 독성을 줄이는 것으로 나타났습니다88. 그럼에도 불구하고 융합 전략은 다양한 사이토카인에 뚜렷한 영향을 미칩니다. 이식유전자 기술과 사이토카인의 결합은 새로운 치료 전략을 제공합니다. 사이토카인 유전자로 변형된 암세포는 야생형 암세포에 대한 후속 공격에 대한 보호 효과를 기반으로 평가되었습니다89,90. 자극성 사이토카인을 제외하고 TLR 작용제 또는 STING 단백질과 같은 면역염색 돌연변이가 APC91e93의 기능을 활성화하는 데 널리 활용됩니다.

시스탄체 보충제 혜택
2.3.2. 단일클론항체(mAbs)
암 면역요법에서 단일클론 항체(mAb)는 미국 식품의약청(FDA) 승인 약물의 상당 부분을 구성합니다. mAbs는 높은 친화력으로 표적과 연결되어 이러한 에이전트의 정확성과 효율성을 보장합니다. 더욱이, mAb는 NK 세포의 ADCC를 매개할 수 있으며, 이는 mAb의 항암 효과를 더욱 뒷받침합니다. 암 면역주기를 표적으로 하는 mAb는 크게 암 면역주기의 면역억제를 완화시키는 면역관문억제제와 암세포의 사멸과 항원 방출을 유도하는 항체-약물접합체(ADC)로 나뉜다. 암세포에 면역 체크포인트가 존재하면 암 면역요법의 효과가 크게 제한됩니다. 프라이밍된 CD8+ T 세포의 기능을 회복하기 위해 CTLA-4 또는 PD-1와 각 리간드의 결합을 억제하는 항체가 널리 연구되었습니다. 임상 데이터는 CTLA-4(ipilimumab), PD-(nivolumab, pembrolizumab) 및 PD-L1(ate zolizumab)94에 대한 mAb의 사회화를 촉진합니다. CTLA-4 및 PD-1 mAb와 비교하여 PD-L1 mAb는 독성이 더 낮은 것으로 나타났습니다. 최근 ADC가 주목받고 있으며, 2019년부터 3종의 ADC가 상용화됐다. 기존의 화학약물은 선택성이 없고 치료 효과를 얻기 위해서는 상대적으로 높은 투여량이 필요하다. 고친화성 항체는 표적과 정확하게 연관될 수 있습니다. 항체 "탄두", 절단 가능한 링커, 세포독성 약물로 구성된 ADC는 항체와 화학 약물의 장점을 결합합니다. 현재 승인된 ADC는 HER-2, CD30, CD33 및 CD2295와 같이 암세포에서 과발현되는 바이오마커를 표적으로 합니다. ADC 기술의 발전으로 이러한 치료법의 적응증이 백혈병에서 고형 악성종양까지 확대되었습니다. 최신 ADC인 Enhertu는 HER{21}} 양성 유방암, 위암, 비소세포폐암 환자에게 사용되었으며 객관적 반응률(ORR)은 약 60%96입니다. FDA 승인 ADC는 표 3에 요약되어 있습니다.
2.3.3. 행동
ACT는 시험관 내에서 자가 면역 세포의 활성화 및 확장을 수반하며, 이를 환자에게 다시 도입하여 면역 체계의 항암 능력을 강화합니다. ACT는 암세포의 식별과 사멸을 직접 수행하고, 다량의 종양 항원을 공급하여 암 면역주기를 다시 시작합니다. ACT의 효과기 세포는 주로 림포카인 활성화 킬러(LAK) 세포97, 사이토카인 유도 킬러(CIK) 세포98 종양 침윤 림프구(TIL), DC, NK, TCR-T 및 CAR-T99입니다. 비특이적 ACT 요법에서 LAK, CIK, DC 및 NK를 포함한 효과기 면역 세포는 특정 종양 항원을 인식하지 않으며 MHC I 제한이 없습니다. 비특이적 ACT 치료법은 MHC I 분자가 결여된 암세포에 대해 탁월한 항암 활성을 입증했지만 정상 조직에 대한 잠재적인 독성은 무시할 수 없습니다. TIL 및 TCR-T를 포함한 특정 ACT 치료법의 효과기 면역 세포는 종양 항원을 인식할 수 있습니다. 암세포의 인식과 그에 따른 치명적인 효과는 MHC I 분자에 따라 달라집니다. MHC I 제한으로 인해 TIL 및 TCR-T 기반 특정 ACT 치료법은 MHC I이 결핍된 암세포에 대해 효과적이지 않습니다. 그럼에도 불구하고 CAR-T는 항체-항원 인식 모델을 활용하여 TCR-CD3와 MHC I의 결합을 대체합니다. /antigen 복합체, MHC I 제한을 피합니다. 그러나 CAR-T는 표면 항원이 있는 암세포만 표적으로 삼을 수 있고 내부 항원이 있는 암세포는 표적으로 삼을 수 없습니다. 킴리아(Kymriah), 예스카타(Yescarta) 등 FDA가 승인한 CAR-T 치료제는 주로 림프종을 표적으로 삼는다. 고형 종양에 CAR-T를 적용하는 것은 여전히 어려운 일입니다. 더 나은 암 바이오마커를 식별하고 CAR의 합리적인 설계가 CAR-T 치료 성공의 주요 결정 요인입니다. 또한 유사한 기술이 CAR-NK 세포에도 활용되어 많은 전임상 연구에서 활용되었습니다. 암을 앓고 있는 환자는 자가 림프구의 수와 활동에 제한이 있어 면역 체계가 약한 경우가 많습니다. 따라서 다른 소스에서 림프구를 개발하는 것은 획기적인 것으로 간주됩니다. 최근에는 유도만능줄기세포(iPSC) 기술로 일차 림프구의 공급원과 투여량이 확대되었습니다. 아마도 후성유전적 기억으로 인해 체세포에 비해 제대혈이나 말초혈 림프구의 iPSC는 CD4+ CD8+ 림프구 생산 효율을 증가시킵니다101. iPSC를 기반으로 한 CAR-T 또는 CAR-NK 치료법은 B세포 악성종양 및 난소암 환자에서 상당한 치료 효과를 입증했습니다102. 또한, 범용 CAR-T는 세포 공급원과 관련된 한계를 극복하여 HLA 매칭 없이 널리 적용 가능한 ACT를 제공합니다. 따라서 성숙한 유전자 편집을 통해 이식 거부 또는 이식편 대 숙주 반응을 피하기 위해 MHC I, MHC II 및 TCR 분자가 제거됩니다. 또한 환자의 NK 세포에 의한 면역 공격을 피하기 위해 HLA-E 또는 HLA-G i가 도입되었습니다103. iPSC 유래 ACT 또는 보편적인 CAR 치료법을 조사하는 임상 시험이 현재 진행 중입니다.
2.3.4. 항암백신
종양의 시작과 진행에는 일반적으로 정상적인 자가 세포의 항원과 다른 독특한 항원을 생성하는 유전적 돌연변이가 동반됩니다. 종양 항원의 방출은 암 면역주기를 시작하는 것으로 추정됩니다. 그러나 종양 미세환경에서 APC의 무능력 또는 종양 항원의 낮은 면역원성은 종양 항원의 포획 및 제시를 방해합니다. 종양항원과 보조제로 구성된 암백신은 종양의 면역억제 환경을 극복하고, 종양항원의 면역원성을 강화하며, 자가 세포 및 체액 면역을 활성화시켜 암을 조절하거나 제거하는 것을 목표로 한다104. 전통적으로 암 백신에는 전세포(암세포 백신 및 DC 백신), 펩타이드, 핵산 백신이 포함되어 있습니다. 최근 유전자 서열 분석 및 생물정보학의 발전으로 개인화된 종양 신생항원을 신속하게 식별할 수 있습니다105. 종양 관련 항원과 비교하여 신생항원은 암세포 돌연변이에서 유래하므로 완전히 새로운 항원입니다. 이러한 종양성 신생항원은 일반적으로 HLA와 특정 결합 능력을 보유하는 폴리펩티드 단편입니다. 그러나 이들의 면역원성은 불확실하며 생체 내 실험에서 결정되어야 합니다. 신생항원을 기반으로 한 펩타이드 백신과 mRNA 백신은 항암 체액성 및 세포성 면역을 유도할 수 있습니다14,106. 암세포 사멸에 대한 심층 연구에 따르면 일부 암세포는 사망 후 면역 반응을 일으킬 수 있으며, 이를 면역원성 세포 사멸(ICD)이라고 합니다. 암세포가 정상적으로 죽을 때, 암세포의 항원과 면역자극 성분은 세포사멸 경로를 통해 분해됩니다. ICD 동안 암세포는 항원을 노출하고 ATP, 고이동성 그룹 단백질 1(HMGB1) 및 칼레티쿨린107을 포함한 손상 관련 분자 패턴(DAMP)을 방출합니다. 이러한 DMAP는 APC 세포에 의한 종양 항원의 흡수 및 제시를 유도하여 항암 효과를 나타냅니다. ICD 과정을 기반으로 한 현장 암 백신은 독소루비신(DOX)109과 같은 전통적인 화학요법 약물의 새로운 항암 메커니즘을 밝혀냈습니다. 또한 광열 요법, 광 역학 요법 및 방사선 요법과 같은 여러 외부 암 치료법이 암세포에서 ICD를 유도하는 것으로 나타났습니다. 그러나 현장 백신 전략의 효과는 보장되지 않으며 종양 항원의 면역원성에 직접적으로 의존합니다. 돌연변이 부담이 더 큰 암은 현장 백신에 더 큰 반응을 보입니다. 더욱이 세포면역을 효율적으로 활성화시키는 암백신은 좋은 항암 효과를 보인다. 외인성 종양 항원에 대한 APC의 교차 제시는 세포 면역 활성화에 중요합니다. 림프절의 CD8a+ DC를 표적으로 삼거나 엔도에서 종양 항원을 방출하여 일부 시스템을 세포질로 방출할 수 있는 암 백신은 APC의 교차 제시와 더 나은 항암 세포 면역을 유발합니다.
표 3 암 치료를 위한 FDA 승인 ADC.

3. 암을 유발하는 나노물질-면역주기
나노물질은 크기 조절, 높은 생체적합성, 우수한 부하 용량 등 다양한 장점을 갖고 있습니다. 암 면역학의 기저가 점차 밝혀지면서 나노물질은 암 면역주기를 기반으로 암 면역치료의 여러 측면을 최적화할 수 있는 잠재력을 가질 것으로 기대된다. 나노물질의 표적화 능력은 암 면역 주기의 다양한 단계가 시간적 및 공간적 정확성으로 활성화되도록 보장하여 항종양 면역 반응을 보장하는 동시에 부작용을 최소화합니다. EPR 효과의 확인은 나노물질(20e200 nm)을 암 표적 약물 전달에 적합한 파트너로 만듭니다110. 나노물질을 담체로 적용하면 암 조직의 면역 조절 화합물을 풍부하게 하여 면역 반응을 강화하고 전신 독성을 줄일 수 있습니다. 또한, 약 25nm 크기의 나노물질은 림프절을 표적으로 삼을 가능성이 더 높으며, 이로 인해 암 백신에 의해 유도되는 강력한 면역 활성화가 발생합니다111,112. 약물 운반체로서 암 면역요법에 참여하는 것 외에도, 암세포에서 ICD를 유도하여 현장 항암 백신을 형성하고 암 면역주기를 다시 시작하는 광열 및 광역학 요법을 포함한 외부 항암 치료를 중재하는 데 점점 더 많은 나노물질이 사용됩니다. 또한, 부분 나노물질은 신체를 자극하여 더 강한 면역 반응을 일으키고 암 면역주기의 억제를 완화할 수 있는 독특한 보조 효과를 입증했습니다. 다음에서는 약물 전달체, ICD 유도제, 면역 보조제로서의 나노물질이 암-면역을 기반으로 암 면역치료를 어떻게 강화하는지 자세히 소개합니다. 나노물질의 다양한 기능은 암 면역 주기의 여러 단계를 동시에 표적으로 삼아 보다 강력한 항암 결과를 달성할 수 있는 조합 암 면역요법을 개발할 가능성을 높입니다(그림 4).

cistanche 보충 혜택 - 면역 체계를 강화하는 방법
3.1. 약물 전달 플랫폼
암 면역요법에서 나노물질은 암 조직이나 면역 조직(예: 림프절)에서 면역 자극 화합물이나 암 백신을 표적으로 삼고 강화하는 데 널리 사용됩니다. 강화된 약물은 농도가 증가하여 면역 체계 활성화를 강화하고 전신 면역 반응으로 인한 정상 조직의 손상을 제한합니다. 암 조직과 림프절을 표적으로 삼는 나노물질은 사용되는 메커니즘에 따라 수동형 표적제와 능동형 표적제로 구분된다. 수동적 표적화는 암 조직이나 림프절에 의한 특정 크기의 나노물질의 흡수에 의존하는 반면, 능동적 표적화는 주로 수용체 분자의 과발현에 의존합니다. 예를 들어, av-인테그린 또는 엽산 수용체는 일부 암 조직에서 과발현되며, av-인테그린 리간드(iRGD) 또는 엽산은 나노물질 표면에서 변형되어 활성 표적화를 달성할 수 있습니다. 만노스 수용체는 림프절의 APC 표면에서 과발현됩니다. 따라서 만노스는 나노물질에서 변형되어 APC를 적극적으로 표적으로 삼을 수 있습니다. 암 표적 나노물질에는 일반적으로 사이토카인, 면역 자극제, ICB 항체 등 면역 억제 미세 환경을 극복할 수 있는 면역 활성화제가 탑재되어 있습니다. 림프절을 표적으로 하는 나노물질에는 일반적으로 종양 항원이 탑재되어 DC에 의한 항원의 처리 및 교차 제시를 촉진하고 림프절에서 암 특이적 CD8+ T 세포를 활성화합니다. ICD 유도물질의 식별과 개발로 인해 이러한 물질을 암 조직으로 운반하기 위해 나노물질을 사용할 수 있게 되었습니다. 또한, 나노물질에 다양한 면역조절제를 합리적으로 조합하면 암 면역치료의 효율성이 더욱 향상될 것입니다.
3.1.1. 사이토카인 및 면역자극제
유리 사이토카인과 면역자극제를 체계적으로 투여하면 통제할 수 없는 면역 폭풍이 발생합니다. 암 표적 나노물질은 암 조직 내부에서 일어나는 면역 활성화를 제한할 수 있다. 저분자량 폴리에틸렌이민(600 Da)의 조립, b-사이클로덱스트린 및 IL{4}} 유전자와의 결합, 엽산과의 결합에 따라 직경 약 100nm의 고분자 나노입자가 다음과 같은 활성화를 유도하는 것으로 나타났습니다. CD4+ T 세포, CD 8+ T 세포 및 NK 세포로 인해 B16eF1 흑색종 이식편이 퇴화됩니다113. IL-2 유전자, IL-12 유전자, 엔도솜 절단 가능 지질 및 엔도솜 절단 가능 RGD 펩타이드의 조합은 크기가 약 100 nm인 나노입자를 생성하여 백혈구 침윤 및 괴사성 암 부위를 증가시켰습니다114. 또한, IL-2-융합된 Fc 단백질과 작용성 CD137 항체를 리포솜에 로딩하면 IL-2과 작용성 CD137 항체의 강력한 항암 효과를 유지하면서 순환 백혈구로 인한 전신 독성을 크게 줄일 수 있습니다115(그림 .5). 사이토카인을 제외하고 면역자극제와 결합된 나노물질은 종양 침윤 백혈구의 국소 활성화를 보장합니다. 순환형 디GMP가 탑재된 양이온성 지질의 정맥 투여는 인터페론(IFN)의 생성과 NK 세포의 활성화를 효율적으로 유발하는 것으로 나타났으며, 이는 B{24}}F10 이종이식 마우스 모델에서 폐 전이를 억제했습니다116. 또한, 면역조절제가 탑재된 나노물질은 암 관련 백혈구를 표적으로 삼을 가능성이 있습니다. 예를 들어, TLR7/8 작용제가 탑재된 나노입자는 크기 효과로 인한 수동적 표적화를 통해 암 조직 및 배액 림프절의 DC를 특이적으로 표적으로 삼았습니다. 항PD{33}} 항체(aPD1) 또는 CD8 항체와 관련된 PLGA-PEG 고분자 나노물질은 PD{36}} 양성 CD8+ T 세포에 특이적으로 결합하는 것으로 나타났습니다. 이러한 PLGA-PEG 고분자 나노물질은 TGF-b 억제제를 전달하여 CD8+ T 세포에 대한 TGFb의 억제 효과를 역전시키는 것으로 나타났습니다118. aPD1로 장식된 유사한 나노입자를 사용하여 NF-kB 억제제를 PD{44}} 양성 TIL에 전달하여 IL-10 및 TGF-b의 생성을 감소시켜 면역억제 상태를 완화시켰습니다119.
3.1.2. mAb
암 면역치료에 사용되는 가장 성공적인 mAb 치료법인 ICB는 TIL과 순환 백혈구 모두에 작용하여 자가면역 염증과 함께 항암 효과를 유도합니다. 나노물질은 ICB 항체를 암 조직으로 운반하고 독성을 개선할 수 있습니다. aPD1을 캡슐화하는 자가 분해성 미세바늘은 aPD1을 흑색종 조직에 방출하고 암 진행을 유의하게 억제하는 것으로 나타났습니다. 제어된 방출 외에도 나노물질은 ICB 항체에 다가 효과를 부여하여 항체와 표적 간의 상호 작용을 강화합니다. aPD-L1을 과분지형 폴리-(아미도아민) 덴드리머와 접합시켜 다가 항-PD-L1 항체(aPD-L1)를 구축하면 유리 aPD-L1121에 비해 PD-L1과의 결합력이 6배 향상되었습니다. 더욱이, aPD1의 재조합 scFv와 iTEP(면역 관용성 엘라스틴 유사 폴리펩티드)의 융합은 aPD1 나노입자의 자가 조립을 가져왔고, 이는 시험관 내 및 생체 내에서 PD{21}} 면역 체크포인트를 차단했습니다122. 또한, aPD1 및 항-OX40 항체(aOX40)와 같은 서로 다른 mAb가 함께 로드된 나노입자는 두 개의 유리 항체에 비해 시너지 효과가 있고 향상된 항암 결과를 보여주었습니다123(그림 6).
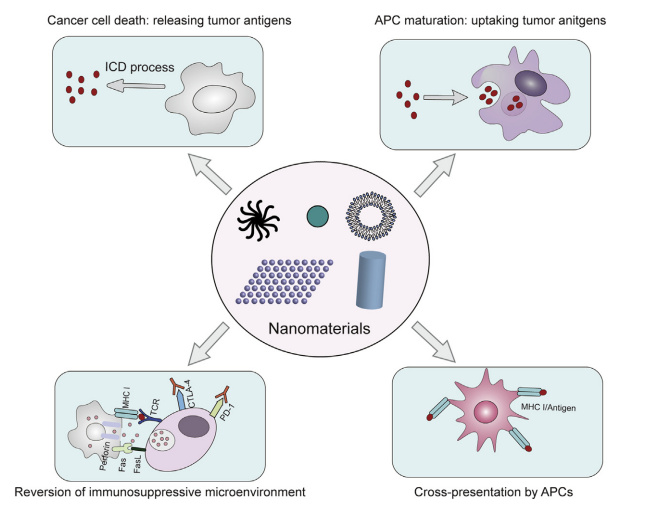
그림 4 나노물질은 암 면역 주기의 여러 단계를 개별적으로 또는 동시에 표적으로 삼습니다. 현재 사용되는 나노물질은 주로 암세포의 ICD를 유도하고, APC의 항원 흡수 및 성숙을 촉진하고, APC의 교차 제시를 강화하며, 암 조직의 면역억제 미세환경을 조절합니다.
3.1.3. 암 백신
암 백신에는 종양 항원과 보조제가 필요합니다. 면역자극제와 같은 보조 성분은 암 백신의 면역원성을 더욱 향상시킬 수 있습니다. 나노물질은 다음과 같이 암 백신 제조에 다양한 이점을 제공하는 다기능 플랫폼입니다124,125: (1) 특정 면역 반응을 강화하기 위해 동일한 APC에 다양한 백신 구성 요소를 동시에 전달하는 능력; (2) 수동적 또는 능동적 표적화를 통해 림프절 또는 암 조직의 APC에 대한 암 백신을 풍부하게 하고; (3) 강력한 면역 반응을 유발하기 위해 암 백신의 크기 및 다가 효과를 중재합니다. (4) 면역 체계의 장기적인 활성화를 보장하는 종양 항원의 제어되고 지속 가능한 방출; (5) 순수 CD8+ T 세포를 효율적으로 프라이밍하기 위해 APC의 교차 제시를 촉진하기 위한 종양 항원의 세포질 전달. 종양 관련 항원(TAA)과 모델 항원은 종양 특이적 항원을 식별하는 것이 상대적으로 어렵기 때문에 암 백신의 일차 식별 및 개발에 널리 활용되어 왔습니다. TAA 및 모델 항원(오발부민, OVA 등)을 기반으로 수많은 나노입자가 암 나노백신을 개발하는 데 사용되었습니다. 예를 들어, 생분해성 PLGA126, (LCP) 나노입자127, 글루타티온 고갈 메조다공성 유기실리카 나노입자128 및 단백질 나노입자129는 TAA 및 모델 항원을 성공적으로 탑재했으며 종양 항원 특이적 면역을 매개하는 것으로 나타났습니다. DC가 암 백신의 흡수 및 취급에 중요한 역할을 한다는 사실이 발견된 이후, DC를 표적으로 하는 암 나노 백신의 수가 점점 늘어나고 있습니다130. 예를 들어, 약 14 nm 크기의 황금 나노입자를 사용하여 모델 항원으로 적색 형광 단백질(RFP)을 로딩하고 보조제로 CPG-ODN을 로딩했습니다. 이 제제는 배액 림프절에서 나노입자의 농축, 항RFP 항체의 높은 역가 및 RFP 발현 B{23}}F10 종양의 퇴행을 가져왔습니다131. 또한, 만노스 또는 CD40 항체와 같은 DC 표적화 분자는 일반적으로 나노입자에서 변형되어 암 나노 백신을 DC에 전달합니다. 예를 들어, Pam3CSK4, Poly(I:C) 및 OVA를 포함하는 PLGA 나노입자는 항-CD40 항체와 연관되어 있어 DC에 대한 효율적인 백신 전달과 CD8+ T 세포의 강력한 활성화를 가져왔습니다. 정상적인 상황에서 DC는 외인성 항원을 삼킨 후 체액성 면역을 유도하기 위해 CD4+ T 세포에 항원을 제시합니다. 그러나 MHC I 분자의 도움으로 DC의 교차 제시에 의해 촉진된 세포 면역은 보다 효율적인 항암 면역 반응을 나타냅니다. 종양 항원을 세포질에 전달할 수 있는 능력을 가진 나노물질은 교차 제시의 가능성과 효율성을 크게 향상시킵니다. 폴리에틸렌이민(PEI) 및 키토산/인산칼슘 나노시트와 같은 양전하를 띤 나노물질은 양성자 스폰지 효과를 통해 화물의 엔도솜 탈출을 유발하는 것으로 나타났습니다. 기공 형성 펩타이드와 같은 엔도솜 교란 물질이 탑재된 나노물질은 함께 전달된 화물의 탈출을 중재할 수 있습니다. 예를 들어 Kong과 Liu 등134은 PLGA에 OVA 및 HCQ(하이드록시클로로퀸)를 탑재하여 나노 백신을 만들었습니다. HCQ는 엔도솜의 막 투과성을 유도하고 OVA의 방출을 촉진했습니다. PLGA/OVA 나노입자와 비교하여 나노 백신은 MHC-I 및 BMDC의 보조자극 분자 CD86의 발현을 향상시키고 IFN-g+ CD8+ T 세포, IFN-g+ CD4+ T 세포 및 중앙 기억의 빈도를 증가시켰습니다. T 세포는 종양의 상당한 퇴행을 촉진했습니다. 2019년에 Xu 등135은 구아니디노 벤조산(DGBA)으로 변형된 폴리아미드 도파민 덴드리머에 OVA와 CpG-ODN을 로딩하여 교차 제시를 촉진하는 또 다른 나노 백신을 구축했습니다. 이 나노 백신은 강력한 항원 특이적 세포 면역을 유도하고 B{56}}OVA 흑색종의 재감염을 예방했습니다. 또한, 이 나노 백신은 aPD-1의 ICB 전략과 결합 시 B16-OVA 흑색종에 대한 강력한 항암 효능을 입증했습니다. 신생항원 식별 기술이 성숙됨에 따라, 암 신생항원은 이제 암 나노백신 제조에 활용되고 있습니다. 신생항원과 CPG-ODN으로 코팅된 나노디스크는 림프 기관이 풍부하고 수용성 백신보다 최대 47-배 더 많은 신생항원 특이적 CTL을 유도하는 것으로 나타났습니다136. 또한 신생항원 발현을 위한 나노캐리어로 T7 박테리오파지를 사용하면 다양한 신생항원을 함유한 나노백신을 얻을 수 있다. 이러한 나노 백신은 높은 역가의 항신생항원 항체와 B 세포 반응을 유도했습니다.

그림 5 IL-2-융합 Fc와 작용성 CD137 항체를 고정하는 리포솜은 전신 독성 없이 항암 면역을 나타냈습니다. (A) IL-2-Fc-리포솜의 Cryo-TEM 이미지(항-CD137 리포솜은 유사함). (B) CD8+ T 세포 수는 수용성 또는 리포솜 IL{11}}Fc(단백질 10ng/mL)로 C57Bl/6 마우스의 다클론성 T 세포를 처리한 후 결정되었습니다. (C) 분비된 IFN-g를 분석한 후 활성화된 T 세포를 가용성 항-CD137 또는 Lipo-aCD137(최종 aCD137 농도: 10mg/mL)과 함께 배양했습니다. (D) Alexa-568-표지 aCD137 및 IL-2-Fc 및 Lipo-aCD137 + Lipo-IL2-Fc를 주사한 후 종양의 동결 절편. (E) aCD137 + IL-2-Fc, Lipo-aCD137 + Lipo-IL-2-Fc 또는 Lipo-IgG로 처리한 후 C57Bl/6 마우스의 종양 크기. (F) Lipo-aCD137 + Lipo-IL-2-Fc 또는 Lipo-IgG로 처리한 후 루시퍼라제 발현 B16F10 종양을 보유하는 C57BL/6 마우스의 생물발광 이미지. Ref.의 허가를 받아 재인쇄되었습니다. 115. 저작권 ª 2019 Nature Publishing Group.

그림 6 PD-1 및 OX40을 표적으로 하는 이중 면역요법 나노입자는 항암 면역력을 향상시켰습니다. (A) 조합 면역요법의 DINP 촉진 강화의 개략도. (B) 항체 접합 전후의 나노입자 이미지(스케일 바: 100 nm). (C) 다양한 약물로 치료한 후 B16F10 종양이 있는 C57BL/6 마우스의 종양 크기 및 생존 곡선. (D) 다른 약물로 치료한 후 종양의 면역형광 이미지. Ref.의 허가를 받아 재인쇄되었습니다. 123. 저작권 ª 2018 WILEY-VCH 출판 그룹.
3.2. ICD 유도제로서의 기능성 소재
나노물질의 종류와 기능은 다양하다. 이들은 약물 전달체(예: 리포솜, 메조다공성 실리콘 및 폴리머)로 사용될 수 있으며 광열 효과, 광역학 효과, 화학적 운동 효과, 자기열 효과 및 방사선 강화 효과와 같은 다양한 기타 기능도 가지고 있습니다. 이러한 기능을 가진 나노물질의 일부는 암세포에서 ICD를 유도하여 종양 항원과 DMAP를 방출하는 것으로 나타났습니다151. 이러한 나노물질을 면역자극제 및 면역관문치료와 같은 전통적인 면역치료와 결합하면 암 면역주기의 여러 단계를 효율적으로 촉진하고 궁극적으로 더 나은 항암 효과를 얻을 수 있는 잠재력이 있습니다. 이 리뷰의 다음 부분에서는 광열, 광역학, 방사선치료, 혈역학 및 기타 기능성 나노물질을 소개하고 암 면역주기를 기반으로 암 면역치료에 대한 응용에 대해 논의할 것입니다.

남성의 면역체계 강화를 위한 시스탄체의 효능
3.2.1. 광열나노소재
광열제(PTA)는 빛 에너지를 열 에너지로 변환합니다. PTA 나노물질은 일반적으로 금속 기반 무기 물질, 탄소 기반 무기 물질, 포스포린 기반 물질, 고분자 물질 및 기타 새로운 PTA152e154로 구분됩니다. 금속 기반 무기 PTA에는 기존 귀금속 소재(Au, Ag, Pd, Pt 포함)와 반도체 소재(CuS, MoS2, WS2 포함)가 포함됩니다. 금속 기반 무기 PTA는 크기와 모양을 조절할 수 있어 쉽게 합성되지만 대사 속도가 느리고 장기간 독성 프로필이 불분명한 등의 단점이 있습니다. 탄소 기반 무기 PTA는 주로 그래핀, 탄소나노튜브, 풀러렌으로 구성된다. 탄소 기반 무기 PTA는 광열 변환 효율과 안정성이 높지만 폐렴을 유발할 가능성이 있어 대규모 생산이 어렵다. 새로 개발된 나노소재인 포스포렌 기반 PTA에는 2차원 흑색 포스포린과 흑색 인 양자점이 포함되어 있습니다. 포스포렌 기반 PTA는 높은 광열 변환 효율과 우수한 생분해 특성을 가지고 있습니다. 그럼에도 불구하고 안정성, 대규모 생산, 저장 용량 등의 문제는 여전히 해결해야 할 과제로 남아 있습니다. 더욱이, 포스포린 기반 PTA와 관련된 급성 독성 및 면역 효과는 아직 명확하지 않습니다. 폴리피롤(PPy)과 폴리도파민(PDA)을 포함한 고분자 PTA는 조정 가능한 분자량으로 쉽게 합성됩니다. 다른 새로운 PTA와 관련하여 일반 공식 Mn+1Xn을 갖는 C3N4 및 MXene과 같이 높은 광열 변환 효율을 갖는 여러 2차원 물질이 생성되었습니다. Mn+1Xn에서 M은 전이금속(Ti, V, Ta, Nb, Mo 및 Zr)을 나타내고 X는 C 또는 N을 나타냅니다. 암 면역치료에서 PTT에 적합한 PTA는 다음 요구 사항을 충족해야 합니다. (1) 상대적으로 높은 광열 전환율 정상 조직에 대한 레이저 손상을 방지하는 효율성; (2) 전신 독성을 방지하기 위한 우수한 생체적합성 및 생분해성; (3) NIR 영역의 광 흡수. 이는 두 번째 NIR(NIR-II) 창(1000e1350 nm)에서 최적입니다. 현재까지 광열 요법은 고온 PTT와 저온 PTT의 두 가지 모델로 기능합니다. 고온 PTT의 경우 암 조직은 50°C155를 초과하는 온도에서 절제됩니다. 높은 온도와 열 전달은 인접한 정상 조직을 손상시킬 수 있습니다156. 일반적으로 포유류 세포는 HSP70 및 HSP90과 같은 열 충격 단백질(HSP)을 과발현하여 열 충격에 반응합니다. 따라서 HSP의 발현과 활성을 억제하여 저온 PTT에 대해 암세포를 감작시키는 연구에 중점을 두고 있습니다157. 최근 연구에서는 PTT가 암세포에서 ICD를 유도할 수 있음이 확인되었습니다144. 조사에 의해 유도된 더 높은 온도는 더 효율적인 세포 사멸을 초래했습니다. 그러나 ICD 바이오마커는 온도 상승에 따라 증가하지 않았습니다. ATP 방출, HMGB1 방출 및 칼레티쿨린 발현과 같은 ICD 마커는 더 높은(83.0e83.5C) 및 더 낮은(50.7e52.7C) 온도보다 63.3e66.4C에서 더 자주 나타났습니다. 더욱이, 다른 PTT로 처리된 신경모세포종에 대한 후속 백신접종으로 시험관 내 결과가 확인되었습니다. 최적의 온도 창 내에서 신경아세포 토마 세포로 면역화된 마우스에 도전하면 더 높거나 낮은 온도 그룹에 비해 장기 생존이 향상되었습니다. 그러나 PTT에 의해 유도된 ICD에 의한 항원 면역원성에만 의존하여 강력한 항암 면역반응을 유도하기는 어렵습니다. 따라서 PTA 나노물질은 암 면역치료의 결과를 향상시키기 위해 다른 전통적인 면역 전략과 자주 결합됩니다. 항-CTLA-4 항체의 전신 투여와 결합된 탄소 나노튜브를 PTA로 활용하면 방사선 조사 시 원격 암과 암 전이를 효과적으로 억제했습니다159. 키토산과 CpG-ODN으로 코팅된 속이 빈 CuS 나노입자는 암 조직에서 NK 세포와 수지상 세포를 활성화하고 림프절을 배출하여 국소적이고 먼 암을 억제하는 것으로 나타났습니다160. 최근에는 포유류 세포가 PTA, Au 나노입자(AuNP)의 현장 생성에 활용되었습니다. HAuCl4로 B16F10 세포를 처리하면 AuNP의 세포 내 생성이 유도되었습니다. 세포외유출 후 AuNP는 다양한 종양 항원을 포함하는 B16F10 막에 캡슐화되었습니다. 그런 다음 AuNP@B16F10 세포를 DC2.4 세포와 함께 배양하여 DC 막을 추가로 장식하고 AuNP@DCB16F10을 형성했습니다. B16F10- 함유 마우스에 AuNP@DCB16F10을 투여하면 방사선 조사 후 암 발생이 크게 억제되고 DC 및 CD8+ T 세포가 활성화되었습니다161(그림 8). 나노물질 매개 PTT는 비침습적 특성으로 인해 기초 연구에서 널리 사용되었지만 아직 성공적인 임상 적용은 없습니다. 임상적 전환에서 나노물질 매개 PTT의 장애물은 6가지 범주로 요약될 수 있습니다. (1) 대부분의 나노물질의 물질적 특징에서 파생되는 한계에는 낮은 혈액 안정성 및 분산, 제한된 장기 순환 용량, 간 강화 및 염증, 불분명한 약동학적 과정 등이 있습니다. (2) 나노물질 기반 PTA의 한계는 특히 금 기반 PTA의 경우 낮은 광열 효율과 열악한 광 안정성을 포함합니다. (3) 빛의 독성, 표면 조직 침투 등 빛의 조사 과정에서 파생되는 장애물. (4) ICD 공정에 유리한 온도는 무엇입니까? 모든 나노물질 기반 PTA에 대한 일반 원칙이 있는가? (5) 나노물질 기반 PTT에 의해 유도된 ICD 과정에 대한 지식의 한계, 예를 들어 모든 나노물질 기반 PTT가 암세포의 ICD를 유발하는지 여부 및 평가 및 예측 방법 ICD 공정을 유도하는 나노물질 기반 PTA의 능력. (6) 나노물질을 이용한 PTT에 의해 유도된 ICD 과정의 강도는 암 면역주기를 잠재적으로 재개하기에 충분하지 않으며, 나노물질을 이용한 PTT와 다른 암 면역요법의 결합이 필요하므로 치료 시스템의 복잡성이 증가합니다.

그림 7 면역보조제 나노입자를 이용한 광열요법으로 항암 면역 유도. (A) ICG 및 R837이 탑재된 PLGA로 구성된 면역 보조제 나노입자의 도식과 면역 체계에 미치는 영향. (B) 원발 종양의 지시된 치료 후 4T1 및 CT26 원거리 종양의 종양 부피. (C) 원발 종양의 지시된 치료 후 원거리 종양의 CD4+ 및 CD8+ T 세포 수. Ref.의 허가를 받아 재인쇄되었습니다. 145. 저작권 ª 2016 Nature Publishing Group.
3.2.2. 광역학적 나노물질
PDT에서 감광제(PS)는 광자를 흡수하여 바닥 상태에서 여기 상태로 변환할 수 있습니다. 여기 상태에서 PS는 일반적으로 불안정하며 고에너지 전자 장치를 다른 기판으로 쉽게 전달합니다. 유형 I 반응에서, 들뜬 상태의 PS는 세포막이나 다른 생체분자와 반응하여 라디칼을 형성하고, 이 라디칼은 O2와 추가로 반응하여 산소화된 생성물을 생성합니다. 유형 II 반응에서 들뜬 상태의 PS는 O2와 직접 반응하여 활성이 높은 ROS162인 단일항 산소를 형성합니다(그림 9). 따라서 PDT 출력은 O2 농도와 밀접한 관련이 있습니다. 저산소 종양 환경에서는 PDT로 높은 효율성을 입증하기가 어렵습니다. PDT는 197년대에 등장하여 표재성 암 치료에 성공적으로 사용되었지만, PDT 매개 면역 활성화는 2세기 후반에 확인되었으며 치료법은 아직 개발 중입니다163e165. 보다 최근의 연구에서 PDT는 암세포에서 ICD를 유도하는 효과적인 방법인 것으로 나타났습니다166,167. 특히, 항산화제가 존재하면 공정의 면역원성이 크게 억제되기 때문에 ICD에는 ROS가 필요한 것으로 보입니다. PDT의 PS에는 유기염료와 나노물질이 포함되어 있다. 유기 염료는 소수성, 낮은 침투 깊이, 암세포에 대한 낮은 특이성을 포함하여 몇 가지 본질적인 단점을 가지고 있습니다. 나노물질을 유기 PS의 담체로 활용하면 몇 가지 단점을 극복할 수 있으며 관련 내용은 3.1.3절에 소개되어 있습니다. 여기에서는 광역학 과정을 유도하는 고유한 능력을 가진 나노물질과 암 면역치료에의 응용을 소개합니다. 일반적인 PDT 나노물질에는 귀금속 나노물질, 탄소 기반 나노물질, 블랙 포스포린, 나노크기 금속-유기 골격(MOF)168이 포함됩니다. 간단히 말하면, 귀금속 나노물질은 금과 은 나노입자로 대표됩니다. 예를 들어, 금 나노막대는 915 nm의 NIR 광 하에서 일중항 산소를 생성하는 것으로 보고되었으며, 이는 마우스 모델에서 B16F0 흑색종 종양을 파괴했습니다. 또한, 이러한 금 나노 막대는 780 nm의 근적외선을 조사한 후 암 조직 주변의 온도 증가를 유도했습니다. 여기광의 스위치는 PTT와 PDT 사이의 치료 모델을 변환할 수 있습니다. 탄소 기반 PS 나노물질에는 탄소나노튜브, 풀러렌, 그래핀 양자점이 포함되어 있습니다. 천연 탄소 기반 PS는 NIR 조사 하에서 제한된 단일항 산소를 생성합니다. 그러나 도핑과 표면 개질은 NIR 조사 하에서 탄소 기반 PS에 우수한 양자 변환 효율을 부여할 수 있습니다170e172. 조정 가능한 밴드 갭, 우수한 생체 적합성 및 생분해성을 갖는 블랙 포스포린은 2015년 PS로 처음 적용되었습니다. 블랙 포스포린은 660nm 조사 시 약 0.91의 단일항 산소 양자 수율을 보여 상당한 세포 사멸 및 종양 억제를 유발했습니다173. 유기 PS를 리간드로, 금속 이온(Hf, Fe, Zn, Zr 이온)을 금속 중심으로 조립한 MOF는 PS 나노물질로 기능하는 것으로 나타났습니다174,175. 예를 들어, 새로운 포르피린 유도체인 5,15- 디(p-벤조아토) 포르피린(H2DBP)은 용매열 반응을 통해 HfCl4와 반응하여 DBP-UiO MOF 구조를 생성했습니다. DBP-UiO-O MOF는 향상된 PDT 효능을 보여주었으며, 단일 투여 및 640 nm 방사선 조사에 한 번 노출된 후 생쥐의 약 절반에서 암이 제거되었습니다176. 후속 연구에서는 H2DBP를 5,15-디(p-벤조에이트)-염소(H2DBC)로 대체하여 염소 기반 MOF를 개발하여 DBCUiO를 얻었습니다. DBCUiO는 적색편이 여기와 기존 MOF에 비해 11-배 더 큰 흡광 계수를 가졌습니다. DBP-UiO177. PTA에 비해 현재 PS 나노물질의 종류와 응용 가능성은 제한적이다. 대부분의 PS 나노물질은 가시광선이나 NIR-I 영역에서 여기되어 조직 침투 깊이가 제한됩니다. 2광자 여기 PDT 나노물질은 NIR-II 조사를 위한 솔루션을 제공합니다178. PS의 기존 1광자 여기는 단일 광자를 흡수하여 PS를 트리거합니다. 그러나 2광자 여기 PS는 두 개의 저에너지 광자를 동시에 흡수하여 두 광자 에너지의 합으로 PS의 밴드갭 에너지를 달성할 수 있습니다. 2광자 여기는 더 깊은 조직 침투를 허용하고 PS의 광표백을 감소시킵니다. 예를 들어, CdSe QD는 1100 nm 레이저에서 여기되어 635 nm 파장의 광자를 방출할 수 있는 2광자 여기 나노물질로 사용되었습니다. CdSe QD에 접합된 실리콘 프탈로시아닌 4(Pc 4)는 635 nm 광자를 흡수할 수 있었고 QD와 Pc 4179 사이의 FL 형광 공명 에너지 전달(FRET) 과정을 통해 PS로 기능했습니다. 현재 PS 나노물질은 국소 암을 강력하게 억제할 수 있지만 , 원격 및 전이성 암의 예방은 다른 암 면역요법과의 병용에 달려 있습니다. 예를 들어, Fe-TBP MOF는 [Fe3O(OAc)6(H2O)3] OAc와 5,10,15,20-테트라(p-벤조에이트) 포르피린(TBP) 리간드로 구성되었습니다. Fe3+는 암 조직에 풍부한 H2O2와 상호 작용하여 O2를 생성하고 암 조직의 저산소증을 완화시켜 PDT 효율을 향상시킬 수 있습니다. aPD- 1와 결합된 Fe-TBP는 전신 효과를 통해 국소 원발암과 원격 암을 모두 억제했습니다180. 최근에는 폴리(g-글루타민산)@글루코스 산화효소 @탄소 도트 나노입자가 구성되어 aPD-1와 결합되었습니다. 이 나노물질은 Mn2+ 촉매작용과 중재된 탄소점 기반 PDT 하에서 H2O2로부터 O2를 생성했으며, 이는 치료된 종양과 치료되지 않은 종양에 대해 항암 면역 반응을 더욱 유도했습니다181. 기존의 유기 PS에 비해 기능성 나노물질을 이용한 PDT는 상대적으로 드물다. 우수한 생체적합성 및 생분해성을 갖는 NIR-II 유도 PDT 나노물질의 개발은 PDT에 새로운 기회를 제공할 수 있습니다. 나노물질의 일반적인 한계를 제외하고, 나노물질을 이용한 PDT는 독특한 장애물을 안고 있습니다. 첫째, 광조사 치료에서 흔히 발생하는 문제인 광독성과 조직 침투 깊이가 좋지 않습니다. 둘째, PDT에서 생성된 ROS는 활성이고 나노미터 범위에서만 효과적이기 때문에 PDT 나노물질의 더 나은 세포 내 흡수가 필요합니다. 셋째, 많은 나노물질이 광자를 열과 고에너지 자유 라디칼로 동시에 변환하는 능력을 가지고 있기 때문에 나노물질에 의해 유도된 PTT와 PDT 공정 사이의 균형을 달성해야 합니다. 넷째, O2는 PDT에 필요하며 암 조직의 저산소증은 PDT의 효율성을 방해합니다. 그러나 나노물질 기반 PS를 이용한 O2 전달은 약물 시스템을 복잡하게 만들고 지속 가능하지 않습니다.
3.2.3. 방사선치료 나노소재
방사선요법은 암에 대한 성숙한 치료법이다. 일부 나노물질은 방사선 치료의 효과를 향상시키는 것으로 알려져 있습니다. 나노물질 기반 방사선치료는 암 표적화 능력과 결합하여 주변 정상 조직의 손상을 줄일 수 있습니다182. 방사선치료로 강화된 나노물질은 일반적으로 높은 Z 원소로 구성됩니다. 가장 널리 사용되는 방사선 감작제는 금 기반 나노입자입니다184. 연구된 다른 방사선 감응제는 란타나이드 기반 NP185,186, Bi2Se3 나노입자187 및 Hf 기반 MOF 나노물질188,189을 포함합니다. 이러한 방사선 민감성 나노입자는 광전 효과와 콤프턴 효과를 향상시켜 방사선 치료의 효율성을 향상시키는 것으로 나타났으며, 이는 2차 전자 방출과 ROS 생성을 더욱 증가시킵니다. 방사선 치료 중에 DNA 라디칼은 O2와 반응하여 DNA 이중 가닥 절단을 유도해야 합니다. 따라서 암 조직의 저산소 환경은 방사선 치료의 항암 효과를 약화시킵니다. 저산소 미세환경을 회피하기 위해 방사선감작제는 일반적으로 MnO2 나노입자 또는 과불화탄소와 같은 O2 전달 분자를 동반합니다. 예를 들어, 코어-쉘 Au@MnO2-PEG는 방사선 감작제의 높은 Z 원자와 O2 생성기를 결합하도록 구성되었습니다. 잘 알려진 방사선 민감제인 Au 코어는 DNA 라디칼의 생성을 향상시킬 수 있습니다. MnO2는 방사선 치료에 대한 저산소증 매개 저항성을 극복하기 위해 H2O2를 O2로 분해하는 능력을 가지고 있습니다190. 또한, 퍼플루오로카본으로 코팅된 중공 Bi2Se3 나노입자는 세 가지 메커니즘을 통해 방사선 치료의 효능을 향상시키는 것으로 나타났습니다. 높은 Z 원자 Bi를 갖는 방사선 증감제인 Bi2Se3 나노입자는 RT의 광전 효과를 효율적으로 향상시켰습니다. Bi2Se3는 근적외선(NIR) 빛을 흡수하고 광열 효과를 발생시켜 종양간 혈액량을 증가시켜 종양 조직의 O2 농도를 증가시킵니다191. 1953년에 처음 제안된 전신 효과는 방사선 치료 하에서 면역 체계의 진화를 암시합니다192. 후속 연구에서는 방사선요법이 MHC I 분자와 TAA의 발현을 상향조절하여 DC의 항원 제시와 CD8+ T 세포의 활성화 및 이동을 유도할 수 있다는 사실이 밝혀졌습니다193. 추가 연구에서는 방사선 요법이 ICD194를 통한 면역 반응을 향상시키는 것으로 나타났습니다. 방사선 치료와 다른 면역치료 전략을 결합하면 면역 반응이 강화되고 시너지 효과가 있는 항암 효과가 유도됩니다. 예를 들어 방사선 감작 효과가 있는 Hf 기반 nMOF는 강력한 CRT 노출과 면역 효과 세포(DC, CD4+ T, CD8+ T 및 NK 세포 포함)의 활성화를 유도하여 원발성 종양과 원거리 종양의 성장을 더욱 억제했습니다. 더욱이, Hf 기반 nMOF를 aPD-L1과 결합하면 면역 반응이 확실히 개선되고 원발성 종양과 전신 종양이 거의 근절되었습니다188. 방사선요법은 광조사보다 더 깊은 조직 침투를 달성합니다. 방사선 요법에 의해 매개되는 면역 유도는 사진 조사와 비교하여 비교적 잘 문서화되어 있습니다. 그러나 종양의 저산소 미세환경은 방사선 치료가 충분한 ROS를 생성하는 데 장애가 됩니다. 더욱이, 상향 조절되는 DNA 복구 효소와 같은 암세포의 방사선요법 저항 메커니즘은 방사선요법의 항암 결과를 감소시킵니다. 아울러, 면역반응 강화에 따른 항암효과와 나노소재의 가격에 대해서도 신중하게 평가할 필요가 있다. 더욱이, 방사선치료에서는 나노물질의 일반적인 한계를 무시할 수 없습니다.

그림 8 PPT와 면역요법의 조합을 위해 B16F10 및 DC에서 생성된 현장 금 나노입자. (A) AUNP@DCB16F10의 구성 및 면역학적 기능에 대한 도식. (B) AUNP@DCB16F10의 TEM 이미지. (C) AuNP, AuNP@DCL929 및 AuNP@DCB16F10의 온도 변화(DT). (D) AuNP@DCB16F10 또는/및 레이저로 처리한 후 살아있는/죽은 세포를 나타내는 이미지. (E) 표시된 치료 후 원발성 종양 부피. (F) 표시된 치료 후 먼 종양의 무게. (G) 표시된 치료 후 DC 성숙. (H) 표시된 치료 후 CD4+ T 세포 수. Ref.의 허가를 받아 재인쇄되었습니다. 161. 저작권 ª 2019 ACS 출판 그룹.

그림 9 광역학 치료의 ROS 생성.
3.2.4. 기타 기능성 나노소재
나노물질은 PTT, PDT, 방사선 치료의 효율성을 향상시키는 것 외에도 화학역학적 효과, 페롭토시스 유도, 자기온열요법(MHT) 효과 등의 다른 기능도 제공합니다. 화학역학적 효과는 주로 Fenton 반응에서 파생되는데, 이는 주로 Fe2+와 H2O2의 반응을 통해 Fe3+ 및 산화 능력이 높은 수산기 라디칼($OH)을 생성하는 것을 설명합니다. 고농도의 $OH는 암세포에 치명적입니다. 철 이온을 제외하고 Cu2+, Mn2+, V2+, Cr4+와 같은 다른 양이온은 Fenton 유사 반응을 촉매할 수 있습니다195. 펜톤 반응을 촉매하기 위해 표면의 Fe2+만을 활용하는 안정적인 Fe3O4 나노입자와 비교하여, 산성 종양 미세환경에서 보다 효율적으로 이온화되고 활성 Fe2+를 방출하는 무정형 Fe 나노입자(AFeNP)는 암 발생 억제를 강화했습니다. H2O2는 정상 세포에 비해 암세포에서 훨씬 더 높은 수준으로 존재하지만, 내인성 H2O2는 시험관 내에서 암세포에 대한 치명적인 화학역학적 효과를 중재하기에는 충분하지 않은 것 같습니다. 많은 CDT 치료법의 경우 암세포 사멸과 종양 퇴행을 유도하려면 추가 H2O2 공급이 필요합니다197. 따라서 CDT는 일반적으로 다른 암 치료법과 결합됩니다. 예를 들어, 우리 그룹은 FeS2 코어와 Fe2O3 쉘을 갖춘 Z 구조 이종접합을 개발했습니다. 새로운 2D 열산화 황철석 나노시트(TOPY NS)는 글루타티온 소비, 펜톤 반응, 이종접합 매개 PDT 및 PTT를 통해 암세포를 죽일 수 있었습니다. 더욱이 TOPY NS는 650 및 808 nm의 조사 하에서 HepG2 이종 이식 종양을 거의 근절했습니다. CDT는 PDT처럼 ROS를 생성하므로 암세포에서도 ICD를 유도할 수 있습니다. 그러나 CDT와 면역 체계 사이의 상호 작용에 대해서는 추가 연구가 필요합니다. Ferroptosis는 새로운 유형의 프로그램된 세포 사멸입니다. 2가 철 또는 에스테르 산소화효소의 작용으로 세포막의 불포화 지방산의 높은 발현을 촉매하여 지질 과산화를 유발하여 세포 사멸을 유도합니다. Ferroptosis의 ROS 생성과 Ferroptosis의 비세포사멸적 특성은 면역 체계를 조절하는 능력을 의미합니다. 새로 확인된 천연물인 Ferroptocide는 항산화 시스템의 중요한 구성 요소인 티오레독신에 대한 공유 결합을 통해 페롭토시스를 유도하는 것으로 입증되었습니다. Ferroptosis는 BALB/c를 보유한 4T1- 마우스에서 40%의 종양 지연을 유발했지만 4T{35}}를 보유한 누드 마우스에서는 거의 억제되지 않았는데, 이는 생체 내 종양 억제를 통해 Ferroptosis에 T 세포와 B 세포가 참여함을 암시합니다198 . 화학역학적 효과를 유도하는 나노물질은 Fenton 반응이 리포솜 과산화를 개시할 수 있기 때문에 페롭토시스 과정을 시작할 수 있습니다199. 그러나 2가 철을 함유하지 않은 몇몇 나노물질은 페롭토시스를 유발할 가능성이 있음을 보여줍니다. PEG화된 초소형 실리카 나노입자(약 6 nm)는 영양이 부족한 암세포에서 페로프토시스(ferroptosis)를 유도하는 것으로 입증되었습니다. 실리카 나노입자에 의해 유도된 세포 사멸은 지질 ROS 제거제(liproxstatin{40}}) 처리 또는 글루타티온 또는 N-아세틸시스테인(NAC) 첨가를 통한 글루타티온 보충에 의해 억제되었습니다. 더욱이, 실리카 입자(용량당 12 nmol)의 정맥 주사는 누드 마우스에서 786-O 및 HT{44}} 이종이식 종양의 성장을 유의하게 억제했습니다. 그리고 복강 내 투여량의 liproxstatin-1은 입자 유발 종양 억제를 크게 감소시켰습니다200. 최근 아르기닌이 풍부한 망간 규산염 나노버블(AMSN)은 글루타티온(GSH)의 고효율 고갈을 통해 페롭토시스를 유도하여 글루타티온 의존성 퍼옥시다제 4(GPX4)의 불활성화를 유도하는 것으로 입증되었습니다. AMSN의 망간은 GSH의 고갈을 매개했으며 아르기닌 변형은 종양 표적화 능력을 제공합니다. AMSN은 시험관 내 및 생체 내에서 페롭토시스(ferroptosis) 메커니즘을 통해 종양 억제를 유도했습니다201. 최근에는 아스코르브산(AA)을 코어로, PLGA를 산화철 나노큐브(IONC)로 장식된 쉘로 활용하여 하이브리드 코어-쉘 소포(HCSV)가 구축되었습니다. HCSV는 자기장 처리 후 Fenton 반응과 ferroptosis와 같은 세포 사멸을 통해 calreticulin의 노출을 유도했습니다. 더욱이, HCSV의 종양내 주사는 비장세포의 상당한 증식, 서혜부 LN의 DC 활성화, 종양 및 LN202의 T 세포 활성화를 촉진시켰습니다. MHT는 주로 자기 타겟팅을 달성하고 교류 자기장 하에서 전자기 에너지를 열 에너지로 변환할 수 있는 초상자성 재료에 의존합니다. PDT 및 PTT에 비해 MHT는 침투력이 더 깊고 주변 조직에 대한 독성이 낮습니다203. Fe3O4 나노입자는 가장 널리 적용되는 초상자성 나노물질로, 종양을 43C 이상으로 가열하고 CD4+ 및 CD8+ T 세포의 활성화 및 증식을 유발할 수 있습니다. Fe3O4 나노입자에 의한 원위 및 이차 종양의 억제는 면역체계의 관여를 시사합니다. Fe 나노입자(FeNP)를 MHT 제제로 활용하고 PLGA-R837의 국소 투여와 aCTLA{66}} 체크포인트 차단제의 전신 투여가 암 전이를 효과적으로 예방하는 것으로 밝혀졌습니다205. 결론적으로, 광열, 광역학, 방사선감작, 화학역학, 페롭토틱, 자기온열 효과를 유도하는 기능성 나노물질은 죽어가는 암세포가 종양항원을 방출하고 면역자극 신호를 제시하여 APC를 활성화할 수 있는 암세포의 ICD 과정을 유도할 수 있는 큰 잠재력을 보여줍니다. . 잠재적인 ICD 나노 유발 물질은 표 4에 요약되어 있습니다. 많은 기능성 나노 물질의 경우 암세포의 ICD를 유도하는지 여부와 ICD 강도가 암 면역 주기를 다시 시작하기에 충분한지 여부는 아직 연구 대상으로 남아 있습니다. 또한, ICD를 유발하는 기능성 나노물질에 관한 소수의 보고는 설명하기 어렵고, 동일한 유형의 모든 기능성 나노물질은 ICD를 유발할 수 있다. 그러나 나노물질에 의해 매개되는 ICD 공정에 대한 표준화된 특성화 및 연구가 부족하여 ICD 나노유도제의 합리적인 최적화를 방해합니다.
표 4 잠재적인 ICD 나노유도물질

3.3. 면역조절 보조제
보조제는 병원체나 악성 종양에 대한 면역 반응을 강화 및/또는 형성하는 현대 백신의 필수 구성 요소입니다. 암 백신 분야에서는 종양 항원에 대한 강력한 세포 면역을 유발하는 것이 중요합니다. 다양한 크기, 모양 및 표면 변형을 가진 나노물질은 다음과 같은 메커니즘을 통해 보조제 역할을 할 수 있습니다206: 항원의 전달 및 일관된 방출, 수동적 또는 능동적 방식으로 APC 표적화, APC의 교차 제시를 향상시키기 위한 항원의 세포질 전달 면역 반응을 조절합니다. 종양 항원을 면역 기관과 DC의 세포질로 운반하기 위한 전달 플랫폼으로 나노물질을 사용하는 방법은 섹션 3.1.3에 설명되어 있습니다. 본 논문에서는 나노물질의 면역조절 효과와 이를 암면역치료에 적용하는 방법에 대해 논의한다. 나노물질의 면역조절 효과에는 주로 염증복합체 활성화, 보체 시스템 활성화 및 면역 세포 모집이 포함됩니다207. 임상적으로 널리 사용되는 명반 보조제는 NLPR3 인플라마솜 활성화를 유도하는 것으로 나타났습니다. 병원체, DAMP 또는 PAMP와 같은 위험에 노출되면 NLPR3 및 기타 관련 단백질은 자체 상호작용하여 카스파제의 자가절단을 유도하는 고분자량 복합체를 형성합니다-1. 이는 IL-b 및 IL-18208의 분비를 추가로 조절합니다. 명반 외에도 카본 블랙 나노입자209, SiO{16}},211 및 TiO2 나노입자212를 포함하여 수많은 나노물질이 NLRP3 인플라마솜 활성화를 유도하는 것으로 나타났습니다. 인플라마솜은 리소좀 불안정화 및 ROS 생성과 같은 나노입자가 제공하는 위험 신호에 반응하여 활성화됩니다. 보체 단백질은 인간과 척추동물의 혈청과 조직액에 존재합니다. 보체는 항원-항체 복합체 또는 미생물에 의해 활성화되어 병원성 미생물의 용해 또는 식세포작용을 일으킬 수 있습니다. 최근 연구에 따르면 보체의 일종인 옵소닌이 나노입자에 흡착되어 식세포에 의한 입자의 인식 및 세포내이입을 중재할 수 있음이 입증되었습니다. 나노물질은 식세포가 섭취한 후 식세포가 전염증성 사이토카인과 케모카인을 합성하고 분비하여 대식세포, DC 및 T 세포와 같은 면역 세포를 모집할 수 있습니다. 예를 들어, 2010년 Yang et al.213은 사이토카인 생성(IL{25}}p70 포함), 보조자극 분자 발현 및 MHC 분자 발현을 유도하는 [Gd@C82(OH)22]n 나노입자를 보고했습니다. DC에서. 또한, OVA 및 [Gd@C82(OH)22]n으로 면역화된 마우스는 강력한 Th1 면역 반응을 나타냈습니다. 2017년에 Luo et al.214은 림프절 표적화를 위해 초pH에 민감하고 직경이 20~50nm인 새로운 고분자 PC7A 나노입자를 만들었습니다. 종양 항원을 림프절에 전달하기 위해 다른 면역자극제 없이 PC7A를 운반체로 사용하면 흑색종과 결장암의 성장을 강력하게 억제했습니다. 이러한 PC7A 나노입자는 STING 경로를 통한 DC 성숙 촉진을 포함하여 면역 반응을 조절하는 것으로 나타났습니다. 나노물질의 면역조절 기능은 약물 전달을 위한 나노물질의 적용에서 일반적으로 무시됩니다. 최근에는 많은 나노물질이 면역체계에 영향을 미친다는 공감대가 형성됐다. 나노물질이 면역반응에 미치는 영향은 다양하다. 나노물질의 면역자극 효과를 주로 소개했지만, 염증이나 면역억제를 유발하는 다른 나노물질도 보고됐다. 나노물질에 대한 면역평가가 많이 축적되어야 한다. 나노물질의 구조와 면역조절 기능 사이의 관계는 아직 밝혀지지 않았습니다.

그림 10 NIR은 면역 체크포인트 차단과 함께 PDT 조합 치료를 촉발했습니다. (A) UCNP-Ce6-R837의 항암 기능을 보여주는 도식. (B) 표시된 치료 후 원발성 및 원거리 CT26 종양의 종양 부피; 표시된 치료 후 원거리 종양의 CD8+ CTL 세포(C), Treg 세포(D), CD8+ CTL/Treg 비율(E) 및 마우스의 혈청 내 IFN-g 사이토카인 수준(F). Ref.의 허가를 받아 재인쇄되었습니다. 215. 저작권 ª 2017 ACS 출판 그룹.
3.4. 나노물질을 이용한 복합암 면역치료
위에 자세히 설명된 다양한 구성 요소 또는 암 면역 주기의 다양한 단계에 동시에 작용하는 복합 면역요법은 강력한 항원 특이적 세포 면역을 유발할 가능성이 높습니다. 운반체, ICD 유도제 및 면역조절제 역할을 하는 나노물질은 다양한 항암 기능을 단일 플랫폼에 통합하고 상대적으로 효율적인 항암 결과를 달성할 수 있는 잠재력을 가지고 있습니다. 처음에는 나노물질을 사용하여 면역요법과 결합된 강력한 항암 백신 개발을 위해 종양 항원과 면역자극제를 공동 전달했습니다. 예를 들어, Xu et al.127은 2013년에 만노스로 변형된 지질-칼슘-인산(LCP) 나노입자를 표적 DC에 구축했으며, 이는 흑색종 항원으로 티로시나제 관련 단백질 2(Trp 2) 펩타이드와 CPG ODN이 함께 탑재되어 있습니다. 보조제. 최근에는 ICD 유도제와 면역자극제를 갖춘 나노물질이 ICB 치료법과 함께 사용되어 왔습니다. 예를 들어, 2017년에 Chen et al.145은 ICG와 R837이 탑재된 PLGA로 구성된 나노시스템을 준비했습니다. ICG는 종양 항원의 방출을 매개하는 강력한 광열 효과를 생성했습니다. 강력한 TLR-7 작용제인 R837은 잠재적으로 활성화된 DC입니다. ICG와 R837을 공동 전달하기 위한 PLGA의 활용은 808 nm 조사 하에서 DC 성숙 및 TNF-α 생산에 가장 강력한 효과를 유도하는 것으로 나타났습니다. aCTLA-4와의 병용 치료 후 레이저 조사를 통한 PLGA-ICG-R837은 4T1 및 CT26 원위 이종 이식 종양을 거의 근절하고 종양의 전이 및 재발을 효과적으로 억제했습니다. 암 성장, 전이 및 재발 억제는 CD4+ 및 CD8+ T 세포의 활성화 및 증식과 Treg 세포의 감소에 의해 강화되었습니다. 그 후 Xu 등은 UCNP(upconversion nanoparticles), Ce6, R837 및 aCTLA-4를 결합한 다기능 나노시스템을 구축했습니다. UCNP는 Ce6 및 R837을 로드하기 위해 양친매성 폴리머로 변형되었습니다. UCNP는 980nm의 빛을 흡수하고 550nm의 빛을 방출하여 Ce6를 활성화하고 ROS를 생성할 수 있었습니다. UCNP-Ce6-R837은 908 nm 조사 하에서 DC 성숙 및 전염증성 사이토카인 분비를 강력하게 유도하는 것으로 나타났습니다. 또한 aCTLA-4의 전신 투여와 결합된 UCNP-Ce6-R837은 원발성, 원거리 및 전이성 종양의 성장을 강력하게 억제했습니다(그림 10).

그림 11 RT + BNP 조합으로 유도된 현장 백신. Ref.의 허가를 받아 재인쇄되었습니다. 217. 저작권 ª 2019 John Wiley and Sons Group.

그림 12 OSPS 매개 조합 암 치료법의 계획. Ref.의 허가를 받아 재인쇄되었습니다. 218. 저작권 ª 2019 John Wiley and Sons Group.

그림 13 OSPS에 의해 유도된 항암 면역 반응. (A) OSPS 매개 종양 억제 및 폐 전이. (B) 4T1 종양 보유 마우스의 원발 종양의 성장 곡선. (C) 4T1 종양 보유 마우스에서 원거리 종양의 성장 곡선. (D) 4T1 종양 보유 마우스에서 폐 전이의 H&E 염색. (E) 4T1 종양 보유 마우스의 전이성 결절 수 (F) 4T1 종양 보유 마우스의 원발 종양의 Kyn/Trp 비율. (G) 원거리 종양의 CD3+CD8+ T 세포 집단. (H) 먼 종양에서 IFN-g를 생산하는 T 세포. (I) 먼 종양의 Treg 세포. *P < 0.05, **P < 0.01, ***P < 0.001, n Z 5. CSPN, NLG919가 없는 나노입자. Ref.의 허가를 받아 재인쇄되었습니다. 218. 저작권 ª 2019 John Wiley and Sons Group.

cistanche 보충 혜택 - 면역력 증가
Cistanche Enhance Immunity 제품을 보려면 여기를 클릭하십시오.
【추가 요청】 이메일:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
4. 결론
암과 면역체계의 상호작용은 복잡합니다. 종양 형성에는 일반적으로 장기적인 면역 검사와 면역 관용 미세 환경이 필요합니다. 따라서 개인의 면역 체계만으로는 암세포를 제거하기에 충분하지 않을 수 있습니다. 한 단계 또는 여러 단계에서 암 면역 주기를 다시 시작하는 외부 제제를 사용하는 것이 암 면역요법의 기초입니다. 암 면역 주기를 복원하는 데에는 APC에 종양 항원을 제공하고, APC의 성숙을 유도하고, APC의 교차 제시를 촉진하고, 면역억제성 미세환경을 개선하는 주요 단계가 포함됩니다. 여러 핵심 지점을 동시에 목표로 삼는 것은 보상 메커니즘을 극복하고 강력한 항암 면역을 촉진하는 효과적인 수단입니다. 나노물질은 크기, 모양, 표면 특성을 제어할 수 있기 때문에 진단 및 약물 전달 분야에서 널리 사용됩니다. 나노물질에 대한 개발 및 심층 연구에 따르면 나노물질은 약물 전달에 사용될 수 있을 뿐만 아니라 광열 효과, 광역학 효과, 방사선 치료 강화 능력, 자기 온열 효과 및 면역 조절 효과와 같은 다양한 특성을 가지고 있습니다. 이러한 특성을 통해 나노물질은 암면역 주기의 여러 단계에 초점을 맞춘 다양한 약물이나 전략을 통합하는 포괄적인 플랫폼으로 사용될 수 있으며, 이는 추가적이거나 시너지 효과가 있는 항암 결과를 촉진합니다. 탁월한 약물 전달 플랫폼인 나노물질은 암 조직이나 림프절에 여러 면역조절제를 동시에 탑재하고 지속적으로 방출하여 종양 항원 공급, APC 활성화 및 억제와 같은 암 면역 주기의 다양한 과정을 강력하게 활성화할 수 있는 능력을 갖추고 있습니다. 면역 체크포인트 또는 면역억제 조절 면역 세포. 기능성 나노물질로서 나노물질은 암세포의 ICD 과정을 촉발하여 APC에 의한 면역원성 종양 항원의 흡수와 APC의 활성화를 유도할 수 있습니다. 면역조절제의 경우, 나노물질은 보조제 역할을 할 수 있으며 염증복합체의 활성화와 자극성 사이토카인의 생성을 직접적으로 유도하여 면역체계 활성화 및 면역억제를 용이하게 할 수 있습니다. 나노물질의 세 가지 면은 암면역 주기를 수동으로 조절하는 데 탁월한 후보가 됩니다. 더욱이, 나노물질은 동시에 여러 역할을 가질 수 있습니다. 예를 들어 기능성 나노물질은 소분자 면역조절제를 전달할 수 있습니다.
