정상 및 낭포성 신장에서 네프론의 3차원 구조
Mar 17, 2022
자세한 정보:ali.ma@wecistanche.com
토마스 블랑1,2,7, 니콜라스 구댕3,7, 모하마드 자이단1,4,7, 메리엠 가르파 트라오레3, 프랭크 비에나미1,5,리사 투린스키1, 세르주 가베이1, 클레망 응우옌1, 마틴 버틴1, 게라르드 프리들랜더1,6, 파비올라 테르지1,8마르코 폰톨리오1,8
1Institut National de la Santé et de la Recherche Médicale U1151, Center National de la Recherche Scientifique UMR8253, Université deParis, Institut Necker Enfants Malades, Département « Croissance et Signalisation », 파리, 프랑스;2Service de Chirurgie Viscérale etUrologie Pédiatrique, AP-HP, Hôpital Necker Enfants Malades, 파리, 프랑스;3구조 Fédérative de Recherche Necker, 미국{0}}UMS3633, 파리, 프랑스; 4Service de Néphrologie-Transplantation, AP-HP, Hôpital Bicêtre, Le Kremlin-Bicêtre, 프랑스;5Service d'ExplorationsFonctionneles, AP-HP, Hôpital Necker Enfants Malades, 파리, 프랑스; 그리고6Service d'Explorations Fonctionneles, AP-HP, HôpitalEuropeen Georges Pompidou, 파리, 프랑스
키워드: 낭포성신장질병;신장; 네프론; 신장염; 조직 청소
번역문
제거 방법은 형태학적 변화가 병적 결과로 이어지는 방식을 이해하기 위한 고유한 도구를 제공합니다.신장물, 대사 산물, 전해질 처리를 통해 신체 항상성을 유지하는 중요한 기관으로, 이는 인체의 복잡한 3-차원 구조에 결정적으로 의존합니다.네프론.이 구조적 조직이 변경되면 신장 병태생리가 발생합니다. 현재 연구에서 우리는 광학 클리어링, 다광자 현미경 및 디지털 추적에 기반한 강력한 방법을 개발하여신장생리학적 및 병리학적 조건에서 단일 네프론 수준에서. 특히, 우리는 단일 규모의 다낭신(polycystickidney)의 첫 번째 3-차원 재구성을 제공합니다.네프론. 이 방법은 여러 병리학적 상황에 적용할 수 있어 신장 기능 저하의 복잡한 과정을 더 잘 이해하고 결과적으로 보다 표적화된 치료 전략을 개발할 수 있습니다.
신장은 복합체를 통해 신체 항상성을 유지합니다.3-차원(3D) 네프론 구조. 이 구조적 조직이 변경되면 신장의 병태생리가 발생합니다. 만성병 환자신장질병은 신장 병변의 발달이 특징입니다. 흥미롭게도, 병리학자들은 만성 신장 질환 동안 병변 분포의 광범위한 이질성을 보고했습니다.1,2 이것이 특정 네프론 분절이 다르게 손상될 수 있다는 사실을 반영하는지 아니면 대안적으로 일부 네프론이 전체적으로 손상될 수 있는 다른 감수성을 가지고 있다는 사실을 반영하는지 여부는 알 수 없습니다. 이 문제를 해결하려면 3D(입체) 모양의네프론병리학 적 맥락에서.
저희의 지식으로는,네프론직렬 2D 섹션을 사용하여 완전히 재구성되었습니다.3–5 표준 조직학적 섹션이 고해상도를 제공하지만 3D 재구성은 힘들고 얻기 어렵습니다. 이것은 주로 슬라이싱 절차의 불가피한 영향인 기계적 왜곡으로 인한 것입니다. 또한 3D(2D 이미지에서 재구성하면 전체 장착 조직에서 3D 구조를 직접 이미징할 수 없습니다.
다광자 현미경은 두꺼운 부분에서 형태학적 변화를 감지하는 능력을 향상시켰습니다. 그러나 빛의 산란으로 인해 접근 가능한 깊이가 얕아 중요한 한계가 있습니다. 굴절률 차이를 최소화함으로써 투명제는 깊이를 이미지화하는 능력을 극적으로 향상시켰습니다.6,7 최초의 투명제가 100년 전에 도입되었다는 사실에도 불구하고,8 대부분 뇌를 위한 몇몇 투명화 프로토콜이 개발된 것은 최근에 와서야 이루어집니다.9 –17최근 연구에서는 간, 췌장 또는신장.18–26
다낭성신장여러 모양체 유전자의 돌연변이를 포함하는 유전적으로 이질적인 질환은 가장 흔한 유전성 신장 질환입니다.27,28 다낭성신장질병은 신장의 완전한 파괴로 이어지는 낭종의 발달을 특징으로 합니다.28 미세 해부 연구에 따르면 낭종은 상염색체 우성 다낭성 신장 질환에서와 같이 네프론 분절의 "밀어내기"로 발전할 수 있습니다. 상염색체 열성 다낭성에서와 같이 집합관(CD)의 황홀한 확장으로신장질병; 또는 신증(NPHP)에서와 같이 수질 세뇨관에서만 발생합니다.27,29 그러나 낭종이 3D로 발생하는 방식(입체) 서로 조직화하고 정상적인 이웃 세뇨관은 아직 알려지지 않았습니다.
여기에서 광학 클리어링과 다광자현미경을 결합하여 방법에 대한 새로운 통찰력을 제공했습니다.네프론생리적 조건에서 형성되고 조직되며 방광 형성과 같은 질병 동안 변형됩니다. 우리의 결과는 3가지 유형이 있음을 보여줍니다.네프론그리고 그 혈관은 네프론 공간 구성에 영향을 미칠 수 있습니다. 흥미롭게도 우리는 네프론이 특정 평면에 있는 경향이 있음을 관찰했습니다. 예기치 않게 이 기술을 jckmice에 적용했을 때 우리는 낭종이 정상 세뇨관과 섞인 방추형 낭종이 있는 특정 네프론 분절에서만 발생하는 것을 관찰했습니다.

결과
실험 설정
전체의 형태를 연구하기 위해네프론환경과 관련하여 우리는 opticalclearing 및 multiphoton microscopy에 기반한 기술을 채택했습니다(SupplementaryFigure S1A). 다양한 광학 제거 프로토콜을 비교하여신장, 벤질 알코올 / 벤질 벤조에이트 (BABB)가 효능 측면에서 가장 적절했습니다 (보충 그림 S1B 및 C 및 보충 표 S1).
3D (입체) 재구성 및 디지털 추적에는 고해상도와 높은 신호 대 배경 비율의 고품질 이미지가 필요합니다. 우리는 천연형광에 의해 제공되는 광학 신호가 신장 섹션에 걸쳐 균일하지 않다는 것을 관찰했습니다. 특히, 수질의 이미지는 낮은 신호 대 배경 비율로 잘 대조되지 않았습니다(보충 그림 S2). 신호 대 배경 비율을 개선하기 위해 과요오드산-쉬프를 사용한 웨스테인 섹션(보충 그림 S1D)은 이 염색이 2-광자형광 동안 얇은 섹션에서 고대비를 발생시킨다는 것을 경험적으로 언급했기 때문입니다. 그러나 두꺼운 과요오드산-Schiff-염색 전체에서 신호가 균일하지 않았습니다.신장섹션(보충 그림 S1E). 따라서 우리는 형광색소 결합 렉틴으로 신장절편을 염색했습니다: 사구체와 세뇨관을 염색하는 땅콩 응집소와 밀 배아 응집소, 혈관을 표시하는 Griffonia simple I folia 응집소.30 놀랍게도, selectin의 조합으로 신호 대 배경 비율이 XY 평면과 z 축 모두에서 상당한 개선과 함께 전체 신장 섹션에서 극적으로 증가했습니다(보충 그림 S1E 및 보충 영화 S1).
3D 네프론 세그먼트 시각화
전체의 형태를 시각화하기 위해네프론, 우리는 사구체의 요로 극에서 시작하여 CD 접합부에서 끝나는 경로를 추적했습니다(보충 영화 S2). 전 세계적으로 사용되는 렉틴이 모든 네프론 세그먼트에 결합한다는 사실에도 불구하고, 우리는 주의 깊게 검사했을 때 셀렉틴이 다른 네프론 세그먼트에서 기저막 또는 내강 막을 염색하는 방식에서 특정 패턴을 특징으로 한다는 것을 발견했습니다. 즉, 우리는 다른 네프론 세그먼트를 식별하기 위해 렉틴 염색의 고정 관념 패턴을 이용했습니다. 이러한 방식으로 우리는 6개의 엔티티를 쉽게 식별할 수 있었습니다: 근위 세뇨관(PT), Henleloop의 가는 다리(TL), HL의 두꺼운 상행 다리(TAL), 원위 세뇨관(DCT), 연결 세뇨관(CNT), 그리고 CD. PT와 TL 사이의 전환은 일반적인 PT 브러시 경계 신호의 갑작스러운 손실과 TL에서는 거의 없는 루멘 너비의 감소로 특징지어집니다(그림 1a). 반대로, TL과 TAL 사이의 전환은 외부 관 직경의 상당한 증가와 상대적으로 일정한 내강 너비를 특징으로 합니다(그림 1b). 모든 네프론에서 TAL에서 DCT로의 전환은 사구체의 혈관 극에서 체계적으로 발견되었습니다. 이 전환은 주로 내강 직경의 상당한 증가로 인한 외부 세뇨관 직경의 갑작스러운 확대를 특징으로 합니다(그림 1c). DCT와 CNT 사이의 전환은 관 직경과 내강 모두의 감소를 특징으로 합니다(그림 1d). 마지막으로, CNT와 피질 CD 사이의 연결은 관 직경과 내강 모두의 급격한 증가를 특징으로 합니다(그림 1e). 이러한 형태학적 전환의 정량화는 통계적으로 유의미했으며(그림 1f), 특정 관형 마커로 염색하여 관련성을 확인했습니다(보충 그림 S3–S5 및 보충 영화 S3–S5).
깊이에 따라 모양과 크기가 다른 PT
두꺼운 염색신장섹션을 통해 전체 PT 세그먼트의 공간적 진화 좌표를 추적할 수 있었습니다. 흥미롭게도 우리는 그 모양이 매우 다양하고 피질에서 사구체의 위치에 따라 결정된다는 것을 발견했습니다. 전 세계적으로 3가지 패턴을 식별했습니다. 첫 번째는 가장 피상적인 것에 해당합니다.네프론(SNs)(그림 2a, 보충 영화 S6), 피질의 가장 외부 부분(신장 캡슐에 가까운 가장 외부 30%)을 차지했습니다. 그들의 복잡한 부분은 매우 작고 빽빽하게 채워진 공간을 차지하면서 자신의 사구체 주위에 단지 6-7개의 회선으로 조밀한 구조를 형성했습니다. 이 SN의 회선은 수질로 내려가는 길고 곧은 직근으로 끝났습니다. 이 스펙트럼의 반대쪽 끝에서 우리는 수질 옆에 있는 피질의 가장 깊은 부분(40% 더 많은 내부 깊이)에 위치한 두 번째 네프론 패턴을 관찰했습니다. S6). 그들의 PT는 유두쪽으로 체계적으로 하강한 다음 U가 신낭을 향해 상승하는 초기 shortloop를 특징으로 합니다. SN과 대조적으로, JN 근위 복잡한 세뇨관은 자신의 사구체 주위에서 진화한 큰 코일과 juxtamedullarycortex에서 크고 느슨하게 채워진 영역을 점유하는 특징이 있습니다. JN의 PT의 복잡한 부분은 10~15개의 회선을 가지고 있어 큰 도메인을 형성합니다. 마지막으로, 세 번째 패턴에는 피질(중간 네프론[MN])의 중간 부분에 위치한 네프론이 포함되었습니다(그림 2a, 보충 영화 S6). 흥미롭게도, 이 세관은 SN과 JN 사이의 전환을 나타내는 모양과 공간적 방향을 가지고 있습니다. 사실, 그들은 SN보다 크지만 JN보다 작은 코일을 가진 8-9개의 회선을 포함했습니다. 또한 MN은 JN보다 더 긴 pars recta를 가졌습니다. 흥미롭게도 PT의 모양을 전체적으로 비교하면 SN과 MN은 균질한 패턴을 갖는 반면 JN은 매우 이질적인 것으로 나타났습니다(보충 그림 S6). 또한, 여러 공간의 재구성네프론 PT는 결코 섞이지 않는다는 것을 밝혀냈으며(SupplementaryMovie S6), 이는 각 네프론이 피질에서 자체의 개별 공간을 차지함을 나타냅니다.
형태 측정 분석은 MN에 대한 중간 측면과 함께 SN과 JN의 크기와 모양에서 큰 차이를 확인했습니다. JN의 PT는 SN의 PT보다 2-배 더 길었습니다(그림 2b). 그러나 직진성은 JN보다 SN에서 더 컸으며(그림 2c), JN 세관이 훨씬 더 구불구불하다는 관찰과 일치합니다(그림 2a, 보충 그림 S6).
그림 1|네프론 분절을 식별하는 데 사용되는 형태학적 기준. (a-e) nephron incontrol 쥐의 다른 부분의 형태.네프론사구체의 요극에서 집합관까지 추적되었습니다(근위 세뇨관[PT]: 청록색, Henle 루프의 가는 다리[TL]: 밝은 회색, Henle 루프의 두꺼운 오름차순[TAL]: 어두운 회색, 원위 복잡한 세뇨관 [DCT]: 분홍색, 연결세관 [CNT]: 노란색, 피질 집합관 [CCD]: 주황색). 화살표는 다른 네프론 세그먼트의 직경을 나타냅니다. (계속되는)
그림 1|(계속) (f) 다른 네프론 세그먼트의 외부 관 직경의 정량화. 데이터는 평균으로 표현됩니다.±SEM. Tukey-Kramer 테스트에 따른 분산 분석: **P < 0.01, ***P < 0.001.

그림 2 |입체(3D) 근위 세뇨관 재건은 3가지 다른 모양과 조직을 나타냅니다. (a) 전체 신장 피질을 통한 근위 세뇨관의 대표적인 3D 재건 이미지는 근위 세뇨관(PT)의 모양에 따라 표면(파란색), 중간(초록색), 골수 옆(빨간색) 피질의 3가지 수준(흰색 선)으로 나뉩니다. 피질의 바깥쪽 30%, 중간 30%, 안쪽 40%에 해당합니다. 3가지 종류의 다양한 모양을 참고하세요.네프론특히 골수 인접 세뇨관의 길이와 비틀림. 바{0}} mm. (b,c) 3가지 유형의 근위 세뇨관의 (b) 길이 및 (c) 직진도의 정량화. (d) 각 피질 영역에서 사구체 부피의 정량화. 데이터는 평균 SEM으로 표시됩니다. Tukey-Kramer 테스트가 뒤따르는 분산 분석: 골수 옆 PT 대 표면 PT: ###P < 0.001;="" 골수="" 인접="" pt="" 대="" 중간="" pt:="" ***p="">< 0.001;="" 표면="" pt="" 대="" 중간="" pt:="" $$$p=""><>

그림 3 |입체(3D) 네프론 재구성은 3가지 유형의 네프론을 나타냅니다. (a) 대조군 마우스에서 사구체에서 표면 피질(파란색), 중간 피질(녹색) 및 수질병합 영역(빨간색)의 수집 덕트까지 전체 네프론(왼쪽 패널)의 대표적인 3D 이미지. 3가지 다른 유형의 네프론에 대한 네프론 분할(오른쪽 패널). 바=150 mm. (b) 3가지 유형의 네프론에 대한 헨레 루프의 2개 팔다리 사이의 내부 거리 정량화. (c) (계속)에 대한 네프론 길이의 정량화
그림 3|(계속) 3가지 유형네프론. (d) 네프론의 유형에 따른 네프론의 다른 부분의 길이 정량화. 데이터는 평균으로 표현됩니다.±SEM. Tukey-Kramer 테스트가 뒤따르는 분산 분석: juxtamedullary nephron(JN) 대 표면 nephron(SN): ###P < 0.001;="" jn="" 대="" 중간="" 네프론(mn):="" *p="">< 0.05,="" **p="">< 0.01,="" ***p="">< 0.001.="" cnt,="" 연결="" 세관;="" dct,="" distalconvoluted="" tubule;="" pt,="" 근위="" 세뇨관;="" tal,="" henle="" 루프의="" 두꺼운="" 오름차순="" 사지;="" tl,="" henle="" 루프의="" 얇은="">

사구체 크기는 깊이에 따라 다릅니다.
그런 다음 3개 영역에서 각각 무작위로 선택된 사구체의 깊이와 직경을 분석했습니다. 형태측정학적 분석은 사구체가 JN 및 SN에서 각각 신장 캡슐로부터 평균 783 및 355 mm에 위치하는 것으로 밝혀졌다. 이전에 보고된 바와 같이 우리는 사구체의 크기가 깊이에 따라 변하는 것을 관찰했습니다. 특히 JN의 사구체 부피는 SN 및 MN의 사구체 부피보다 3배 더 컸습니다(그림 2d).
3D 네프론 재건
그런 다음 전체의 공간적 진화를 추적했습니다.네프론PT에서 CNT로. 그들의 3D에 대한 글로벌 뷰(입체) 재구성은 네프론 모양이 SN, MN 및 JN 간에 다르다는 것을 확인했습니다(그림 3a, 보충 영화 S7). 이러한 차이는 주로 PT의 구조에 기인한다. 또한 HL이 다른 3D 공간 구성을 가지고 있음을 관찰했습니다. 특히, TL과 TAL은 SN과 MN에서보다 JN에서 더 멀리 분리되었습니다(그림 3b). 형태학적 분석에 따르면 JN이 전체적으로 SN보다 2-배 더 길었습니다(그림 3c). 증가된 길이는 모든 네프론 유형에서 유사한 절대 길이를 갖는 경향이 있는 TAL 및 DCT를 제외하고 모든 세그먼트에서 비례적으로 분포되었습니다(그림 3d). 이것은 네프론 신장이 놀랍게도 균일하게 패턴화된 과정임을 시사했습니다.
아치형 혈관은 juxtamedullary PT convolution에 영향을 미칩니다.
보다 포괄적인 관점을 얻기 위해신장구조에서 우리는 아치형 혈관과 그 가지를 피질 방사 혈관으로 추적할 수 있는 Griffonia simplicifoliaagglutinin 염색을 이용했습니다(그림 4a, 보충 영화 S8). 흥미롭게도 수반되는 3D(입체) 네프론과 혈관의 재구성은 아치형 혈관이 근처의 세뇨관과 함께 놀라운 평행 공간 조직에 있는 경향이 있음을 보여주었습니다. 특히, 우리는 특정 JN(제약된 JN)이 따르는 경로가 인근 선박의 경로를 따르는 경향이 있음을 관찰했습니다(그림 4b; 보충 영화 S9). 놀랍게도, 이 편향(JN의 하위 집합에서만 관찰됨)네프론) PT 모양의 큰 이질성을 설명했습니다(보충 그림 S6). 형태학적 분석은 "구속된" PT가 "비구속된" PT보다 상당히 더 길고 더 구불구불한(직진도 감소) 것으로 나타났습니다(그림 4c 및 d). SN과 MN 모두의 복잡한 부분이 아치형 혈관 위에 위치하고 구속되지 않았다는 점은 주목할 가치가 있습니다.

Cistanche-만성 신장 질환
세관은 평면에 있는 경향이 있습니다.
흥미롭게도 3D 검사(입체)의 모양네프론그들은 평면에 누워있는 경향이 있음을 나타냅니다(그림 5a; 보충 영화 S10). 이 매개변수를 정량화하고 이 형태의 가능한 통계적 편향을 평가하기 위해 우리는 세뇨관이 루프에 의해 정의된 평면 밖으로 구부러지는 일반적인 경향을 측정했습니다. 우리의 측정은 연속적인 측정 각도와 연속 점 사이의 길이(그림 5b)의 동일한 세트로 생성된 무작위 보행의 시뮬레이션된 모델과 비교하여 세관이 평면에서 더 작은 편차로 진화하는 경향이 있음을 보여주었습니다(그림 5c). 이것은 tubulestended가 평면을 따라 경로를 제한한다는 것을 나타냅니다. 관찰된 차이는 통계적으로 매우 유의했습니다(P <>
3D 네프론 재건은 낭종 발달에 대한 특정 패턴을 나타냅니다
우리의 프로토콜이 무질서한 병리학적 조직에서 네프론을 추적할 수 있는지 여부를 결정하기 위해 우리는 NPHP 및 낭성 질환의 널리 사용되는 모델인 잭 마우스에서 낭종의 모양과 공간적 분포를 특성화했습니다.31–{1}}D 이미지는 두드러진 낭종의 출현, 일반적인 3D(입체) 네프론의 과정은 대조군 쥐의 과정과 크게 다르지 않았습니다(Supplementary Movie S11). 유사하게, 형태학적 분석은네프론, 사구체 부피 및 각 네프론 분절의 길이는 대조군 마우스와 비슷했습니다(보충 그림 S7). 참고로, 낭종 발달로 인해 HL에서 TL과 TAL을 구별할 수 없었습니다. 모든 네프론에서 방추형 낭종이 발생했습니다(SupplementaryMovies S11 및 S12). 가장 눈에 띄는 특징 중 하나는 방추형 낭포성 팽창이 동일한 네프론 분절을 따라 여러 위치에서 발생한다는 관찰이었습니다(보충 영화 S12 및 S13). 흥미롭게도 우리는 낭종이 PT와 HL내림차순 팔다리에서 결코 발생하지 않는다는 것을 관찰했습니다(그림 6a, 보충 영화 S12). 대조적으로, 그들은 CNT와 연속하여 HL 상승 다리, DCT, CNT 및 CD의 상부에서 주로 검출되었습니다(그림 6a, 보충 영화 S12). 특히, 우리는 DCT와 CNT 세그먼트가 각각의 더 먼 부분에서 낭종을 개발할 확률이 특별히 증가했음을 관찰했습니다(그림 6b). 3D 재구성 이미지의 정량적 형태 측정 분석은 네프론당 총 낭종 부피가 CNT에서 특히 높음을 보여주었습니다(그림 7a). 또한, 우리는 HL 및 DCT의 낭종 확대가 SNsand MN보다 JN에서 더 크다는 것을 관찰했습니다(그림 7a, 보충 영화 S12). 또한, 낭종 발생률은 JN에서 다른 유형보다 유의하게 높았습니다.네프론(그림 7b). 우리는 또한 평균 사구체 간 거리(가장 가까운 5개 사구체에서 계산됨)가 특히 더 표면적인 피질에서 특히 증가된 낭포성 마우스 경향이 있음을 관찰했습니다(보충 그림 S8).
그림 4|혈관은 네프론 모양을 결정합니다. (ㅏ)입체아치형 혈관에서 피질 방사 혈관까지 혈관 구조의 재구성. 바 ¼ 200mm. (b) "비제약"(상단 패널) 및 "제약"(하단 패널) 인접 근위 세뇨관의 대표적인 이미지. 바 ¼ 100mm. (c,d) "비제약" 및 "제약" 근위 세뇨관의 (c) 길이 및 (d) 직진도의 정량화. 데이터는 평균으로 표현됩니다.±SEM. Mann-Whitney 테스트: "제약된" 대 "비제약된":*P < 0.05,="" ***p=""><>

3D (입체) 수많은 낭종의 재구성은 모양과 부피가 극도로 다양하다는 것을 보여주었습니다(그림 6c, 보충 영화 S11 및 S13). HL 상행지에서 낭종은 직경이 작은 방추형을 가졌다. DCT에서 낭종은 다소 구형이고 더 큰 모양을 가졌으며 확장되지 않은 세뇨관 사이에 산재되어 있습니다. 흥미롭게도, DCT와 CNT 사이의 전환은 정상적인 비확장 구조로 체계적으로 특징지어졌습니다. 대조적으로, CNT에서 우리는 CD와 직접 접촉하는 인접한 확장된 낭포 구조를 체계적으로 관찰했습니다. 흥미롭게도 CD에서 이 구조는 점진적으로 정상적인 세뇨관 크기로 축소되었습니다. 더 이상 CD의 인접한 부분에서 더 이상의 낭종이 발견되지 않았습니다. 또 다른 일관된 특징은 HL 오름차순에서 낭종의 독특한 공간적 조직화였습니다. 사실, 낭종은 SN에서 더 깊고 루프에 더 가깝지만 JN에서 더 피상적이고 DCT에 더 가깝습니다(그림 6c). 다시 말하지만, 낭종은 MN에서 중간 위치를 차지했습니다(그림 6c).
그림 5|네프론 세관은 평평한 구조로 진화하는 경향이 있습니다. (a) 네프론 근위 세뇨관의 전형적인 경로. 이 경로는 평면에 누워 있는 경향을 보여줍니다. 경로 전개의 평면성은 관찰자의 관점과 적절하게 회전되고 정렬될 때 더 잘 볼 수 있습니다(왼쪽에서 다른 각도로 표시되는 동일한 관형 세그먼트의 오른쪽 표현 참조) . (b) 4개의 세그먼트로 구성된 관형 경로의 도식적 표현(예시로 표시된 주어진 관형 경로를 정의하는 5개 점 사이). 경로가 "평면을 벗어나는" 경향이 있는 정도는 여기에서 "베타"로 표시된 각도로 나타낼 수 있습니다. (계속되는)
그림 5|(계속) 이 각도는 평면(바로 앞의 점 p3, p2, p1으로 정의됨)을 기준으로 세그먼트 p{1}}p4 사이에서 측정되며 구성표에서 짙은 회색 직사각형으로 표시됩니다. 그런 다음 베타 각도의 계산은 관형 경로의 점 집합과 함께 재귀적으로 계산되었습니다. 이러한 베타 각도의 편향 정도를 평가하기 위해 각 관 경로(모든 연속 세그먼트 사이에서 측정)의 동일한 연속 알파 각도 세트를 사용하여 무작위 보행(Monte Carlosimulation[MCs])을 시뮬레이션했습니다. 이 무작위 걷기는 동일한 알파 각도 세트와 무작위 베타 각도 세트를 가진 경로를 생성했습니다. (c) 근위 세뇨관(PT), 헨레 루프의 가는 사지(TL), 헨레 루프의 두꺼운 오름차순(TAL), 원위 복잡한 세뇨관(DCT)의 MC 결과 및 베타 각도의 전역 분포에 대한 바이올린 플롯 ) 및 결합 세뇨관(CNT). MC, P <>

논의
전통적인 조직학적 방법은 전체적인 형태에 영향을 미치는 병리학적 변화를 감지하는 능력이 제한적입니다.네프론. 여기에서 우리는 문제 해결에 기반한 강력한 접근 방식을 제시합니다.신장정상 및 병리학 적 조건 하에서 전례없는 공간적 세부 사항을 가진 건축물. 우리의 결과는 기능적 특이성과 일치하는 위치, 모양 및 크기가 다른 3가지 유형의 네프론이 존재함을 확인했습니다. 또한, 우리는 nephronstend가 비행기에 누워 선박 공간 조직에 적응함을 보여주었습니다. 흥미롭게도 우리가 이 기술을 낭성 신장 질환 모델에 적용했을 때 우리는 낭종이 allnephron에서 발생하지만 특정 부분에서만 발생한다는 것을 관찰했습니다. 흥미롭게도 우리는 낭종의 모양이 네프론 분절에 따라 다르며 동일한 네프론을 따라 낭종이 정상적인 비확장 세뇨관과 삽입된다는 것을 보여주었습니다. 전체적으로 이러한 결과는 최초의 3D를 제공합니다. (입체)의 공간 배열의 특성화네프론및 혈관 및 중요하게는 낭형성과 같은 병리학적 과정을 이해하기 위한 기초를 제공합니다.
높은 수준의 자가형광 및 세포 밀도로 인해 신장 광학 청소가 어렵습니다. 서로 다른 제거 프로토콜을 비교하여 BABB에서 가장 깊은 부분에 위치한 구조의 시각화 및 재구성을 구현하기 위한 강력한 기술을 확인했습니다.신장, 즉 수질. 또한 BABB는 신속하고 확장 가능하며 일단 제거되면 샘플을 이미지 획득 전에 몇 달 동안 저장할 수 있습니다. 이 기술의 또 다른 주요 장점은 저렴한 비용입니다. 투명제는 구조를 축소하거나 확대할 수 있습니다.9-17 그러나 이러한 신장 크기 수정은 등방성이므로 상대 측정이 영향을 받거나 해석을 편향시키지 않을 것으로 예상됩니다. 가장 중요한 한계 중 하나는 시간이 많이 소요되는 구조의 주석입니다. 그럼에도 불구하고 이러한 한계를 빠르게 극복해야 하는 딥 러닝 기반 기술의 수가 증가하고 있습니다.
고전적 기술로 얻은 결과와 일치하게, 우리 연구는 네프론이 위치에 따라 모양과 길이가 다르다는 것을 보여주었습니다. 특히, 우리는 JN이 복잡한 PT와 더 큰 사구체를 가지고 있고 SN보다 2배 더 긴 것을 관찰했습니다. 증가된 길이는 모든 네프론 세그먼트에 비례적으로 영향을 미치기 때문에 조화로운 과정의 결과입니다. 우리는 또한 JN이 더 큰 HL을 가지고 있음을 관찰했습니다. 전체적으로, 이러한 데이터는 SN과 JN의 미세 해부학이 상당히 다르고 MN이 중간 기능을 표시한다는 것을 분명히 보여줍니다. 흥미롭게도 생리학적 연구에 따르면네프론또한 기능적으로도 다릅니다.2 이러한 차이점의 기초가 되는 형태 발생 이벤트는 아직 알려져 있지 않습니다. 따라서 JNs의 특정 구조가 기능의 특수성을 설명할 수 있다고 추측하고 싶은 유혹이 있습니다.
흥미롭게도 처음으로 3D를 제공함으로써 (입체)의 재건네프론그리고 그 주변 혈관에서 우리는 아치형 혈관과 네프론의 하위 그룹 사이의 공간적 제약을 발견했습니다. 따라서 혈관이 발달하는 동안 네프론이 길어지는 방식을 결정할 수 있다고 생각할 수 있습니다.34,35 계산 시뮬레이션과 결합된 네프론의 3D 모양 검사에서도 네프론이 절대 섞이지 않고 각 네프론이 평면에 놓이는 경향이 있음이 밝혀졌습니다. 이 관찰의 기능적 중요성은 아직 밝혀지지 않았습니다.
다낭성 중 낭종 발달신장질병은 여전히 흥미로운 과정입니다. 낭종 발달을 특징으로 하는 병리학적 상태인 NPHP는 소아 및 청소년에서 말기 신장 질환을 유발하는 가장 흔한 유전 질환입니다. 지금까지 20개의 NPHP 유전자가 확인되었습니다.36 그 중 NEK8은 섬모 기능과 세포 주기 진행에 중요한 역할을 하는 절대 inmitosis A 관련 키나제 계열의 구성원을 인코딩합니다.37 Nek8은 원래 jck 마우스에서 돌연변이된 유전자로 특성화되었습니다.32 특히, 동일한 단백질 도메인의 돌연변이가 인간에서 NPHP9로 이어지는 것으로 나타났습니다.{8}}D 연구에 따르면 낭종의 발달은 다양한 형태의 다낭성 신장 질환에 따라 크게 다릅니다.27,29 특히, NPHP에서는 낭종이 유도된 것으로 보입니다. CD와 DCT에서만 얻을 수 있습니다.31 유익한 정보이기는 하지만 이러한 면역조직화학적 연구는 특정 관상 표지자39의 손실이 이러한 관찰을 인위적으로 설명할 가능성에 대해 반박할 수 없습니다. 따라서 우리의 3D (입체) 연구는 낭종 발달이 특정 신장 분절만을 포함할 수 있는 과정이라는 첫 번째 명확한 증거를 제공합니다. 흥미롭게도 NIMA(Never In mitosisgene A)–Related Kinase 8(NEK8)은 모든 네프론 분절의 세포질에서 발현되지만 섬모에서의 발현은 DCT 및 CD로 제한됩니다. 이 부분들만이 낭종이 생기기 쉽기 때문에31 우리는 NEK8 모양체 기능의 붕괴가 낭종 형성에 중요한 사건이라고 가정할 수 있습니다. 흥미롭게도, 우리는 또한 방추형 낭포가 정상적인 비확장 세뇨관과 연속되어 있음을 관찰했습니다. 열성 생식계열 돌연변이가 세포의 일부에서만 병리학적 표현형을 초래한다는 사실은 상염색체 우성 다낭성 종양에 대해 제안된 바와 같이 두 번째 사건이 이러한 세포에서 낭종 발달을 유발할 수 있음을 시사합니다.신장질병.40,41
그림 6 |입체(3D) 네프론 재건은 낭종이 특정 네프론 세그먼트에서만 발생한다는 것을 보여줍니다. (a) 잭 마우스에서 사구체에서 표면 피질(파란색), 중간 피질(녹색) 및 골수 인접 영역(빨간색)의 수집 덕트까지 전체 네프론(왼쪽 패널)의 낭종 부피 렌더링이 있는 대표적인 3D 이미지. 3가지 유형의 네프론 분할(오른쪽 패널)네프론. 바{0}} mm. (b) 잭 마우스의 다른 네프론 분절에서 낭종이 발생할 확률. (계속되는)
그림 6|(계속) 수평 축은 50개의 빈에 해당하는 네프론의 정규화된 길이입니다(근위 세뇨관[PT], 청록색; Henleloop [HL], 흰색, 원위 세뇨관[DCT], 분홍색, 연결 세뇨관[CNT], 노란색). (c) HL(왼쪽 패널), DCT(중간 패널), CNT 및 피질 수집 덕트(CCD)(오른쪽 패널)의 오름차순 사지의 낭종 볼륨 렌더링이 있는 대표적인 3D 낭종 재구성 이미지(오른쪽 패널) 패널) 및 잭 마우스의 수질병합(하부 패널) 네프론. 바= 50 mm.

그림 7|네프론 전체에 걸친 포낭 분포 및 부피의 특성화. (a) 각 네프론 세그먼트(Henle loop [HL], 흰색, distal convoluted tubule [DCT], 분홍색, 연결 tubule [CNT], 노란색)에 대한 총 낭종 부피(네프론당 낭종의 합계)의 정량화 및 (b) jackmice에서 네프론의 각 유형(표면: 파란색, 중간: 녹색, juxtamedullary: 빨간색)에 대한 낭종이 차지하는 세뇨관의 길이. 데이터는 평균으로 표현됩니다.±SEM. Tukey-Kramer 테스트가 뒤따르는 분산 분석: juxtamedullary nephron[JN] 대 표면 nephron[SN]: #P < 0.05;="" jn="" 대="" 중간="" 네프론="" [mn]:="" *p="">< 0.05,="" **p=""><>
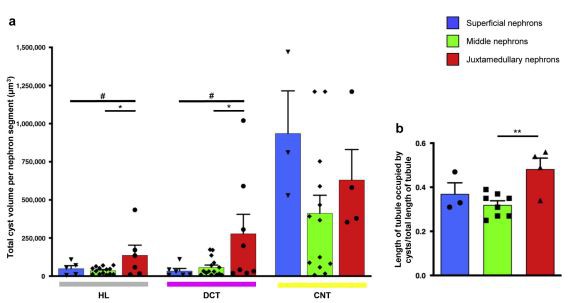
우리는 또한 적어도 PT와 CNT 사이에 위치한 낭종을 고려할 때 낭종 확대가 SN보다 JN에서 더 우세하다는 것을 관찰했습니다. 일관되게, 사구체 경화증의 맥락에서 사구체 병변은 inSN보다 JN에서 더 자주 발견되는 것으로 보고되었습니다.1,21,42 단일 네프론 사구체 여과율 및 수송/효소 활성 증가로 인한 과로가 JN의 감수성 증가를 설명하는지 여부 악화된다는 것은 더 조사할 가치가 있는 흥미로운 가설입니다.
요약하면 이미지를 만드는 새로운 기술을 설명합니다.신장3D로 (입체) 구체적으로 표지된 내부 구조(네프론, 혈관 및 낭종). 직접 정량화를 위한 편리함, 속도 및 능력을 감안할 때, 우리는 이 기술이 신장 병리 생리학을 이해하는 강력한 도구가 될 것으로 기대합니다.
행동 양식
동물
모든 동물 절차는 "Service Vétérinairesde la Préfecture de Police de Paris"와 Université Paris Descartes의 윤리 위원회의 승인을 받았습니다. 2개월 된 FVB/N 마우스(n=20)를 사용하여 실험 조건을 설정했습니다.신장그런 다음 이 연구는 2-주령 잭 수컷 쥐(n=4)와 대조군 한배새끼(n=3)에서 수행되었습니다.
신장 조직의 준비
죽이기 전에, 마우스는 25ml의 헤파린화 식염수(1000IU/l)에 이어 75ml의 인산완충식염수(PBS) 중 4% 파라포름알데히드로 심장내 카테터 삽입을 통해 관류했습니다. 실험은 자일라진(Rompun 2%, Bayer, Leverkusen, Germany, 6 mg/g 체중) 및 케타민(Clorketam 1000, Vetoquinol SA, Lure, France, 120 mg/g 체중) 마취하에 수행되었습니다.
청소 공부를 위해,신장4% 파라포름알데히드에 4시간 동안 고정하고 4% 아가로스 및 1.{4}}신장문을 둘러싸고 있는 mm 두께 섹션을 절단하고 4℃에서 PBS에 보관했습니다.도. 신장 섹션을 먼저 염색한 다음 제거했습니다.
얇은 절편에 대한 면역조직화학적 연구를 위해 신장을 4% 파라포름알데히드로 밤새 고정하고 파라핀 포매 및4-mm 절편을 절단했습니다.
더럽히는 것
과요오드산-쉬프 염색. 1.{1}}mm신장섹션은 투명하기 전에 실온에서 5분 동안 순수 또는 1:100 PBS로 희석된 과요오드산-Schiff에서 배양되었습니다.
얇은 파라핀이 포함된 섹션의 면역조직화학. 파라핀이 포함된 신장의 4마이크로미터 섹션을 항원 검색을 위해 가열하고 4℃에서 밤새 배양했습니다.4도세관을 추적하기 위해 형광색소 결합 렉틴(로다민 땅콩 응집소[RL{1}}] 및 로다민 밀 배아 응집소[RL{2}}], Vector Laboratories, Burlingame, CA, 1:200에서 희석) 및 세그먼트- 별개의 관형 세그먼트를 묘사하기 위한 특정 1차 항체(비오틴화된 Lotus tetragonolobus lectin[B{6}}], Vector Laboratories, 1:100으로 희석, 마우스 항-Calbindin D28K[D{11}}], Santa Cruz, Heidelberg, 독일, 1:200으로 희석, 염소 항-AQP2 [C{16}}], Santa Cruz, 1:200으로 희석). 다음날, 섹션을 실온에서 1시간 동안 이차 항체(Alexa Fluor 488 conjugate [S32354], Invitrogen; anti-goat Alexa Fluor 488 [A{24}}], Invitrogen; anti-mouse AlexaFluor 488 [A-21202], Invitrogen, Carlsbad, CA; 모두 1:500으로 희석한 후 40,{31}}디아미디노{32}}페닐인돌로 착색. 모든 이미지는 Nikon Eclipse E800 현미경(Champignysur Marne, France)으로 획득했으며 피지 소프트웨어(버전 1.50)를 사용하여 준비했습니다. 두꺼운 섹션에서 렉틴 염색. 1.{37}}mm 두께신장섹션은 4에서 인큐베이션되었습니다.4도Texas Red 또는 flfluorescein isothiocyanate 결합 렉틴에서 1개월 동안: 땅콩 응집소(RL{1}}) 및 밀 배아 응집소(RL{2}}), 1:1로 희석00 0.1% PBS 아지드 및 0.1% Triton-X에서. 그런 다음 섹션을 제거하기 전에 PBS로 2주 동안 매일 세척했습니다.

Cistanche-신장 기능
광학 클리어링
스케일 제거의 경우 1.{1}}mm신장섹션을 ScaleA2(4 M 요소, 0.1% Triton X-100, 10% 글리세롤) 또는 ScaleB4(8 Murea, 0.1% Triton X{10}} ) 2주, 최대 1년, 4시도.
BABB 제거를 위해 1.{1}}mm 신장 섹션을 실온에서 에탄올의 순차적 헹굼에서 탈수했습니다. 그런 다음 샘플을 4도에서 최소 2일 동안 1:2 비율로 BABB(Sigma-Aldrich, Saint Louis, MO)에서 인큐베이션했습니다.
2광자 현미경 이미지 획득
Mai Tai HP Titanium-Sapphire Laser(Spectra-Physics, Santa Clara, CA)가 장착된 역다광자현미경(LaVision BioTec)에서 수성 젤로 조직을 이미징했습니다(SupplementaryFigure S1A). 여기 파장은 8%의 전력에서 815 nm였습니다. 우리는 20X침수 대물렌즈(XLUMPLFL20XW,Olympus [일본 도쿄], 개구수, 0.95, 작동 거리, 2.0mm). 형광 획득을 위해 우리는 593/40 nm의 대역 통과 필터와 함께 80%에서 디스캔되지 않은 검출기를 사용했습니다.
첫 번째 단계는 최적이 아닌 획득 매개변수(400mm X400mm 및 1011X1011 픽셀, 10% 중첩 및 2에서 선형 평균)를 사용하여 중간 z 스택에서 2D 모자이크 이미지 획득으로 구성되어 가장 관련성이 높은 중앙 필드 선택을 안내합니다(보충 그림 S9A ). 관심 있는 XY 그리드와 z 필드가 정의되면 매개변수를 조정하여 고품질 이미지를 획득했습니다. 이러한 접근 방식은 관심 영역을 5로 줄였습니다.Xz 스택당 12개의 필드. 그런 다음, 우리는 850 z 스택/광학 슬라이스(1-mm 단계 크기)를 확보했습니다.신장부분.
이미지 스티칭, 처리 및 추적각 스택은 Preibischet al.43이 개발한 방법에 따라 타일링되었습니다. 이 방법은 피지 소프트웨어(HTTP://Fiji. sc/피지). 스티칭 후 2개의 인접한 이미지 사이의 중요한 이동을 관찰했기 때문에 Python으로 사용자 지정 일치 프로그램을 작성했습니다. 이 프로그램은 이미지 이동을 보정하여 이미지를 올바르게 정렬할 수 있습니다(보충 그림 S9B). 스티치 수정된 이미지는 Imaris 버전 8.4.2(Bitplane, Zurich, Switzerland)를 사용하여 분석되었습니다. Imaris의 필라멘트 추적기 패키지 수동 모드를 사용하여 세관과 혈관을 추적하고 MATLAB으로 개발한 Imaris Xtension(https://www.dropbox.com/s/sm9u5em3orjrpmc/Standalone{11}}Join{12}} 필라멘트{13}}Tool.zip?dl{14}})(보충 그림 S9C). 사구체 및 낭종은 Imaris 표면 패키지의 수동 모드를 사용하여 3D로 재구성되었습니다. 3D (입체) 사구체 공간 조직은 Imaris의 스팟 패키지의 수동 모드를 사용하여 표시되었습니다.
형태측정
Imaris의 필라멘트 트레이서 패키지를 사용하여 관형 세그먼트 길이, 네프론 길이 및 직진도를 결정했습니다. Imaris 소프트웨어에 따르면 직진도는 2점 사이의 거리와 네프론 세그먼트 경로의 길이 사이의 비율로 정량화되었습니다. 31명의 PT와 12명의 전체네프론3개의 야생형 마우스에서 재구성 및 측정된 반면 37개의 PT 및 17개의 전체 네프론은 4개의 잭 마우스에서 재구성 및 측정되었습니다. Imaris의 "표면 패키지"를 사용하여 낭종 및 사구체 부피를 결정했습니다. 야생형 andjack 마우스에서 각각 31개 및 34개 사구체가 측정되었습니다. 총 74개의 낭종이 측정되었습니다.
관형 회전의 "평면 밖" 각도("베타"로 표시)는 평면(3개의 연속 점으로 정의됨)과 공간 내 다음 연속 네 번째 점이 있는 방향 사이에서 측정되었습니다(그림 5b). 관찰된 편향의 통계적 유의성을 평가하기 위해 동일한 알파 각도 세트를 가진 동일한 세그먼트로 구성된 구조에서 베타 각도의 무작위 회전(몬테 카를로 시뮬레이션)으로 베타 각도 분포를 시뮬레이션했습니다.
네프론 분절과 함께 낭성 병변이 발생할 확률을 계산하기 위해 각 네프론을 공간의 점 집합으로 표시했습니다. 각 지점은 낭종의 존재 대 정상 구조 및 분절 유형과 관련하여 주석이 달렸습니다. 각 표준화된 길이(50개의 빈으로 설정)에서의 확률은 낭성 주석이 있는 포인트 수와 빈의 총 포인트 수 사이의 비율로 계산되었습니다.
평균 사구체 간 거리를 계산하기 위해 각 사구체에 대해 가장 가까운 5개 사구체에서 계산된 평균 사구체 간 거리를 고려했습니다.
데이터 분석 및 통계
데이터는 평균 ± SEM으로 표시됩니다. 실험 그룹 간의 차이는 Tukey-Kramer 테스트에 의해 유의미한 경우(P < {{0}}.05)="" 분산="" 분석을="" 사용하여="" 평가되었습니다.="" 두="" 그룹만="" 비교할="" 때는="" mann-whitney="" 테스트를="" 사용했습니다.="" 통계="" 분석은="" graph="" prism="" 소프트웨어(sandiego,="" ca,="" 버전="" 9.0.0)를="" 사용하여="">
폭로
모든 저자는 경쟁 이익을 선언하지 않았습니다.
감사의 말
기술 지원에 대한 Laboratoire 실험 Animale et Transgenese(LEAT), 구조 연방 deRecherche Necker의 조직학 및 이미징 플랫폼에 감사드립니다. 원고를 비판적으로 읽어준 Pierre Isard, Marie-Claire Gubler, Nicolas Kuperwasser에게 감사드립니다. 이 작업은 국립 드 라산테 et de la Recherche Médicale 국립 연구소, 파리 데카르트 대학, 공공 지원 – Hôpitaux de Paris, 에이전시 국립 드 라레쉐르, Whoami Laboratoire d' Excellence Who am I, RochePharma Research and Early Development(바젤, 스위스)의 지원을 받았습니다. , 및 Roche de Recherche et de Médecine Translationnelle 연구소(프랑스 파리).
저자 기여
TB, NG, MZ는 실험을 설계 및 수행하고 데이터를 분석했습니다. FB, LT, MGT 및 SG도 일부 실험을 수행하고 데이터를 분석했습니다. MB와 CN은 마우스 실험을 수행했습니다. TB와 MZ도 원고 작성에 기여했습니다.GF는 원고를 수정했습니다. FT와 MP는 개념적 틀을 제공하고 연구를 설계하고 프로젝트를 감독하고 논문을 작성했습니다.

Cistanche-네프론 신장의 3차원 구조
보충 자료
보충 파일(PDF)
그림 S1. 실험 설정, 획득 절차 및 이미지 처리.
그림 S2. XY 및 z 해상도에서 자가형광 신호의 한계.
그림 S3. 4-mm 파라핀이 매립된 PT와 TL 사이의 전환에 대한 2차원 이미지신장섹션.
그림 S4. 4-mm 파라핀 포매 신장 절편에서 TAL과 DCT 사이의 전환에 대한 2차원 이미지.
그림 S5. 4-mm 파라핀이 삽입된 신장 절편에서 DCT와 CNT 사이의 전환에 대한 2차원 이미지.
그림 S6. 3차원 재구성은 근위 세뇨관의 3가지 다른 모양을 보여줍니다.
그림 S7.입체재구성은 길이와 분할을 보여줍니다.네프론낭종의 영향을 받지 않습니다.
그림 S8. 통제 및 낭포성 사구체의 밀도신장.
그림 S9. 획득 절차 및 후처리 이미지 처리. 표 S1. 정리 방법 비교.보충 파일(동영상)
영화 S1. 렉틴 염색은 해상도와 신호 대 배경 비율을 현저하게 향상시킵니다.
영화 S2. 세뇨관 경로 추적.
영화 S3. Henle 루프의 근위 세뇨관과 얇은 다리 사이의 접합부를 보여주는 깨끗한 신장의 3차원 재구성.
영화 S4. Henleloop의 두꺼운 상행지와 원위 세뇨관 사이의 접합부를 보여주는 깨끗한 신장의 3차원 재구성.
영화 S5.입체클리어의 재건신장원위 세뇨관과 연결 세뇨관 사이의 접합부를 보여줍니다.
영화 S6. 근위세뇨관의 모양과 크기는 깊이에 따라 다릅니다.
영화 S7. controlmice에서 3차원 네프론 재구성.
영화 S8. 아치형 혈관에서 대동맥 방사 혈관까지의 혈관 경로 추적.
영화 S9. 아치형 혈관은 juxtamedullaryproximal tubules의 모양을 모델링합니다.
영화 S10.네프론비행기에 누워있는 경향이 있습니다.
영화 S11. 3차원 네프론 재건은 낭종 발달에 대한 특정 패턴을 보여줍니다.
영화 S12.입체네프론 분할은 낭포가 특정 네프론 세그먼트에서 발생함을 보여줍니다.
영화 S13. 공간배열과 상호관계네프론다낭성 혈관신장.
참조
1. 풍부한 AR. 지질성 신증에서 지금까지 설명되지 않은 골수 옆 사구체의 취약성. 불 존스 홉킨스 병원 1957;100:173–186.
2. Bankir L, Bouby N, Trinh-Trang-Tan MM. 신장 해부학의 이질성. 신장 Int 공급 1987;20:S25–S39.
3. Christensen EI, Grann B, Kristoffersen IB, et al.입체쥐 네프론의 재건. Am J Physiol Physiol. 2014;306:F664–F671.
4. Zhai XY, Birn H, Jensen KB 등 마우스 근위세뇨관의 디지털 3차원 재구성 및 미세구조. J Am Soc Nephrol.2003;14:611–619.
5. Zhai XY, Thomsen JS, Birn H, et al. 마우스 네프론의 3차원 재구성. J Am Soc Nephrol. 2006;17:77–88.
6. Puelles VG, Moeller MJ, Bertram JF. 우리는 이제 분명히 볼 수 있습니다: opticalclearing 및신장형태학. Curr Opin Nephrol Hypertens.2017;26:179–186.
7. Seo J, Choi M, Kim SY. 대규모 생물학적 조직에 대한 제거 및 라벨링 기술. 몰 세포. 2016;39:439–446.
8. Spalteholz W. Über das Durchsichtigmachen von menschlichen undtierischen Präparaten und seine theoretischen Bedingungen, nebst Anhang:Über Knochenfärbung. 독일 라이프치히: S. Hierzel; 1914.
9. Hama H, Kurokawa H, Kawano H, et al. 규모: 투명 마우스 뇌의 형광 이미징 및 재구성을 위한 화학적 접근. Nat Neurosci. 2011;14:1481–1488.
10. Ertürk A, Becker K, Jährling N, et al.입체3DISCO를 사용하여 용매가 제거된 장기의 영상화. 냇 프로토콜. 2012;7:1983–1995.
11. Kuwajima T, Sitko AA, Bhansali P, et al. ClearT: 신경 및 비신경 조직을 위한 세제 및 무용제 제거 방법.개발. 2013;140:1364–1368.
12. Ke MT, Imai T. SeeDB를 사용한 고정 뇌 샘플의 광학적 제거. CurrProtoc 신경과학. 2014;66:2.22.1–2.22.19.
13. Chung K, Deisseroth K. 신경계 매핑을 위한 CLARITY. NatMethods. 2013;10:508–513.
14. Tomer R, Ye L, Hsueh B, Deisseroth K. 손상되지 않은 조직의 빠른 고해상도 이미징을 위한 고급 CLARITY. 냇 프로토콜. 2014;9:1682–1697.
15. Yang B, Treweek JB, Kulkarni RP, et al. 전신 클리어링을 통해 투명한 온전한 조직 내의 단일 세포 표현형. 셀. 2014;158:945–958.
16. Susaki EA, Tainaka K, Perrin D, et al. 화학적 칵테일 및 컴퓨터 분석을 사용하는 단일 세포 분해능으로 전체 뇌 이미징. Cell.2014;157:726–739.
17. Alanentalo T, Asayesh A, Morrison H, et al. 성체 마우스 장기 내 단층 분자 영상화 및 3D 정량화. Nat Methods.2007;4:31–33.
18. Parra SG, Chia TH, Zinter JP, et al. Clearmouse 장기의 다광자 현미경. J Biomed Opt. 2010;15:036017.
19. Renier N, Wu Z, Simon DJ, et al. iDISCO: 부피 이미징을 위해 큰 조직 샘플을 면역 라벨링하는 간단하고 빠른 방법. 셀. 2014;159:896–910.
20. Lee H, Park JH, Seo I, et al. 뇌, 췌장, 간,신장, 폐 및 소장. BMC Dev Biol. 2014;14:1–7.
21. Iversen BM, Amann K, Kvam FI, et al. 증가된 사구체 모세혈관압과 크기는 SHR juxtamedullarycortex에서 사구체 경화증을 중재합니다. Am J Physiol Physiol. 1998;274:F365–F373.
22. Angelotti ML, Antonelli G, Conte C, Romagnani P. 신장 이미징: 빛에서 초고해상도 현미경으로. Nephrol 다이얼 이식.2021;36:19–28.
23. Puelles VG, van der Wolde JW, Schulze KE, et al. 전체 사구체에서 족세포를 계산하고 크기를 결정하는 3차원 방법의 검증. J Am Soc Nephrol. 2016;27:3093–3104.
24. Pannabecker TL, Dantzler WH, Layton HE, Layton AT. 의 역할입체therat 신장 내부 수질의 소변 농축 메커니즘의 아키텍처. Am J Physiol Physiol. 2008;295:F1271–F1285.
25. Saritas T, Puelles VG, Su XT, et al. 신장의 광학적 제거는 칼륨 매개 세뇨관 리모델링을 나타냅니다. 셀 담당자 2018;25:2668–2675.e3.
26. Schuh CD, Polesel M, Platonova E, et al. 신장의 결합된 구조적 및 기능적 영상은 근위 세뇨관 endocytosis에서 주요 축 차이를 나타냅니다. J Am Soc Nephrol. 2018;29:2696–2712.
27. Braun DA, Hildebrandt F. Ciliopathies. Cold Spring Harb Perspect Biol.2017;9:a028191.
28. Bergmann C, Guay-Woodford LM, Harris PC 등 다낭성신장질병. Nat Rev Dis Prim. 2018;4:50.
29. 윌슨 PD. 다낭성 신장 질환. N 영어 J Med. 2004;350:151–164.
30. Laitinen L, Virtanen I, Saxén L. lectinconjugates로 밝혀진 마우스 신장의 배아 발달 중 글리코실화 패턴의 변화. J Histochem Cytochem. 1987;35:55–65.
31. Smith LA, Bukanov NO, Husson H, et al. 어린 낭포성 신장 마우스에서 다낭성 신장 질환의 발달: 병인, 섬모 이상 및 인간 질병의 일반적인 특징에 대한 통찰력. J AmSoc Nephrol. 2006;17:2821–2831.
32. Liu S, Lu W, Obara T, et al. 새로운 Nek-패밀리 키나제의 결함은 마우스와 제브라피쉬에서 낭포성 신장 질환을 유발합니다. Development.2002;129:5839–5846.
33. Franke M, Baeßler B, Bechtel J, et al. 다낭성 신장 질환의 마우스 모델에서 낭형성 및 치료 반응의 조기 검출을 위한 자기 공명 T2 매핑 및 확산 강조 영상.신장국제 2017;92:1544–1554.
34. Barry DM, McMillan EA, Kunar B, et al. 네프론 혈관 전문화의 분자 결정 요인신장. 냇 커뮤. 2019;10:5705.
35. Perretta-Tejedor N, Jafree DJ, Long DA. 다낭성 내피-상피통신신장질병: 혈관 내피 성장 인자 신호의 역할. 세포 신호. 2020;72:109624.
36. Srivastava S, Molinari E, Raman S, Sayer JA. 많은 유전자 하나의 질병?신장염(NPHP) 및 NPHP 관련 장애의 유전학.Front Pediatr. 2017;5:287.
37. Fry AM, O'Regan L, Sabir SR, Bayliss R. 단백질 키나아제의 NEK패밀리에 의한 세포 주기 조절. J 세포 과학. 2012;125:4423–4433.
38. Otto EA, Trapp ML, Schultheiss UT, et al. NEK8 돌연변이는 모양체 및 중심체 국소화에 영향을 미치고 신장염을 유발할 수 있습니다. J Am SocNeprol. 2008;19:587–592.
39. 윌슨 PD. 다낭성 신장 질환 상피의 Apico-basal 극성. Biochim Biophys Acta. 2011;1812:1239–1248.
40. Happé H, Leonhard WN, van der Wal A, et al. Pkd{1}}결실 쥐의 신장에 있는 독성 세뇨관 손상은 조절되지 않은 평면 세포 극성 및 표준 Wnt 신호 전달 경로와 함께 방광 생성을 가속화합니다. 흠 몰 Genet. 2009;18:2532–2542.
41. Piontek K, Menezes LF, Garcia-Gonzalez MA, et al. 중요한 발달 스위치는 Pkd1 손실 후 신장 낭종 형성의 동역학을 정의합니다. 냇 메드. 2007;13:1490–1495.
42. Ikoma M, Yoshioka T, Ichikawa I, Fogo A. 성숙의 깊은 피질 사구체의 고유한 감수성의 메커니즘신장심한 국소 사구체 경화증에. 소아용 해상도 1990;28:270–276.
43. Preibisch S, Saalfeld S, Tomancak P. 타일링된 3D의 전역적으로 최적의 스티칭 (입체) 현미경 이미지 획득. 생물정보학. 2009;25:1463–1465.
