Beta Vulgaris Rubra L. (비트 뿌리) 껍질 메탄올 추출물은 H2O2 유도 산화 스트레스 인간 제대 정맥 내피 세포에서 VEGF 발현 증가를 통해 산화 스트레스를 감소시키고 세포 증식을 자극합니다
Feb 22, 2022
연락주세요oscar.xiao@wecistanche.com더 많은 것을 알기 위해
Laila Naif Al-Harbi 1,*, Subash-Babu Pandurangan 1, Alhanouf Mohammed Al-Dossari 1, Ghalia Shamlan 1, Ahmad Mohammad Salamatullah 1, Ali A Alshatwi 1 및 Amna Abdullah Alotiby 2
추상적인:폴리페놀의 항산화 능력과플라보노이드식이 요법제에 존재하는 활성 산소 종(ROS)의 발생을 억제하고 산화 스트레스/유도 괴사로부터 내피 평활근 세포를 보호하는 데 도움이 됩니다. 비트 뿌리(Beta vulgaris var. Rubra L., BVr)는 풍부한 공급원을 나타내는 일반적으로 소비되는 야채입니다.항산화제. 비트 뿌리 껍질의 생리 활성 화합물과 인간 제대 정맥 내피 세포(HUVEC)에서의 역할은 아직 연구되지 않고 있습니다. 본 연구에서는 비트 뿌리 껍질 메탄올 추출물(BPME)이 제조되었으며, 유도된 HUVEC에서 생체 효능, 핵 완전성, 미토콘드리아 막 전위, 혈관 세포 성장 및 면역 조절 관련 유전자 발현 수준에 미치는 영향산화스트레스를 분석했다. 가스 크로마토그래피-질량 분광법(GC-MS) 결과는 BPME가 5-하이드록시메틸푸르푸랄(32.6%), 메틸 피루베이트(15.13%), 푸르푸랄(9.98%) 및2,{10}}디하이드로{11} },{12}}디하이드록시{13}}메틸{14}}H-Pyran{16}}원(12.4%). BPM 추출물은 세포 증식을 효과적으로 향상시켰으며 MTT 분석에 의해 확인되었습니다. 핵 무결성은 요오드화 프로피듐(PI) 염색 분석에 의해 확인되었습니다. 미토콘드리아 막 전위(∆ψm)는 JC{19}}염색 분석으로 확인되었습니다. Annexin V 분석 결과 BPME 처리된 HUVEC는 99%의 생존 세포를 보여주지만 H2O2만 처리한 HUVEC에서는 39.8%의 생존율만 나타남을 확인했습니다. 또한 48시간 동안 HUVEC의 BPME 처리는 지질 과산화물(LPO)의 mRNA 발현을 감소시키고 NOS-3, Nrf{28}}, GSK{29}}, GPX, 내피 산화질소 합성효소(eNOS)를 증가시켰습니다. ), 및 혈관 세포 성장 인자(VEGF) mRNA 발현 수준. 우리는 BPME 치료가 전염증성(핵인자-κ(F-κ), 조직 괴사 인자-(TNF-), 톨유사 수용체-4(TLR{36}}), 인터루킨{37} } (IL-1 )) 및 혈관염증(세포내 부착 분자(ICAM), 혈관 세포 부착 분자(VCAM), EDN1, IL{1}}) 관련 mRNA 발현. 결론적으로, 근대 뿌리 껍질 처리는 혈관 평활 세포 성장 인자와 미세소관 발달을 효과적으로 증가시킨 반면, 혈관 염증 조절 인자를 감소시켰다. BPM은 혈관 평활 세포 재생, 조직 복구 및 노화 방지 잠재력에 유익할 수 있습니다.
키워드:비트 루트; 산화 스트레스; 미토콘드리아; 혈관신생; 염증

1. 소개
혈관신생은 신체의 기존 혈관구조로부터 혈관신생의 생리학적 과정이다[1]. 이는 배아의 발달과 번식뿐만 아니라 세포 주기와 조직 복구에도 필수적이다[2,3]. 그러나 이는 종양 성장, 류마티스 관절염 및 다양한 허혈성 및 염증성 질환과 같은 다양한 질병의 발병기전과 관련이 있다[3-5]. 혈관 내피는 혈관의 색조와 면역 및 염증 반응을 조절하여 혈관 지혈을 유지하는 데 중요한 역할을 합니다[6,7]. 내피 세포(EC)는 혈관의 모든 내부 표면을 감싸는 얇은 단세포 층으로 국부적으로 또는 먼 부위에서 작용하는 다양한 분자를 생성합니다[7]. 내피는 신체 항상성의 기본이며 내피 세포 반응의 변화는 죽상 동맥 경화증 및 고혈압과 같은 염증 및 혈관 질환 과정의 주요 사건으로 이어집니다 [6,8,9]. 이러한 질병은 산화 스트레스를 유발하여 EC 구조와 기능 무결성을 변경하고 내피 기능 장애를 유발합니다[9]. 인간 제대 정맥 EC(HUVEC)는 인간 혈관 내피 관련 연구의 모델로 널리 사용되었습니다. 또한, 내피 기능과 관련된 주요 생물학적 경로를 연구하는 데 유용한 모델을 나타냅니다[10]. 생리 활성 화합물과 식물 화학 물질은 과일, 채소, 녹색 허브 및 많은 식물에서 풍부하게 발견되며 항염, 항산화, 항암 및 혈관 생성과 같은 수많은 건강상의 이점을 나타냅니다[11-13]. 이와 관련하여 붉은 비트 뿌리(Beta vulgaris var. Rubra L.; BVr)는 Amaranthaceae 계통에 속하며 높은 수준의 항산화제의 가장 좋은 공급원 중 하나로 분류됩니다[14,15]. 특히, 여기에는 다음을 포함하여 생물학적으로 활성인 여러 파이토케미칼이 포함되어 있습니다.베타레인, 플라보노이드,폴리페놀, 치료 효소, 아스코르브산, 데히드로아스코르브산(DHAA) 및 무기 질산염(NO3) [16-18]. 또한 칼륨, 칼슘, 마그네슘, 나트륨, 철, 아연, 인, 구리 및 망간과 같은 귀중한 필수 영양소를 제공합니다[19]. 여러 연구에 따르면 붉은 비트 뿌리 추출물(뿌리)은 혈당 강하, 지질 저하, 항염증, 항고혈압 및 항증식 특성으로 인해 수많은 유익한 효과가 있다고 보고했습니다[20-22]. 이러한 유익한 특성은 모두 생리 활성 화합물의 자유 라디칼 소거 능력과 관련될 수 있습니다. 따라서 붉은 비트 뿌리의 섭취는 수많은 영양 및 건강상의 이점과 관련이 있습니다. 그 영양학적 가치 때문에 제2형 당뇨병, 심혈관 질환과 같은 만성 대사성 질환을 유발하는 산화 스트레스에 대한 기능성 식품 공급원으로 사용될 수 있다[23]. 문헌 검토에 따르면 Beta vulgaris는 강력한 항산화, 면역 조절 및 혈관 형성 특성을 가지고 있습니다. 아피게닌은 사탕무 잎에서 발견되었습니다. 간 및 장 세포에서 항증식 효과가 있으며 AMPK 활성화를 통해 고지방식이 유발 비만 동반질환을 개선할 수 있다[24,25]. De Silva et al., (2020) [26]은 Beta vulgaris가 이 식물에 존재하는 여러 생리 활성 화합물의 복합 효과로 인한 외부 유도 산화 스트레스로부터 혈관 EC를 보호한다는 것을 확인했습니다. 지금까지 베타 vulgaris 뿌리 껍질의 EC 증식 및 혈관 신생 효과에 대한 기계적 작용에 대한 연구는 미흡했습니다. 따라서 우리는 HUVEC에서 세포 형태 및 유전자 발현 분석을 사용하여 베타 vulgaris 뿌리 껍질과 관련된 혈관 세포 증식, 미세 소관 발달, 산화 스트레스 및 혈관 신생 능력을 조사하기 위해 본 연구를 수행하는 것을 목표로했습니다. 인간 혈관 EC에서 핵 완전성, 미세소관 발달, 미토콘드리아 효율 및 세포 주기 자극과 관련된 붉은 비트 뿌리 껍질 메탄올 추출물의 혈관신생 효과가 탐구됩니다.
2. 재료 및 방법
2.1. 비트 뿌리의 준비(Beta vulgaris rubra L.) 메탄올 추출물신선한 비트 뿌리(Beta vulgaris var. Rubra L.; BVr.)의 샘플은 처음에 사우디 아라비아 왕국(KSA)의 리야드에 있는 야채 가게에서 얻었습니다. 신선한 비트 뿌리는 줄기와 오염 물질을 제거하기 위해 증류수로 세척되었습니다. 겉 껍질을 벗겨서 제거하고 작은 조각으로 자릅니다. 샘플을 40의 열풍 오븐에서 건조시킨 다음 전자 블렌더를 사용하여 분말로 분쇄합니다. 그런 다음, 5{{10}}0g의 분말을 1L의 메탄올(Sigma, St. Louis, MO, USA)이 들어 있는 멸균 병에서 실온에서 24시간 동안 추출했습니다. 셰이커와 세 번 반복합니다. 이후 Whatmanfifilter(Whatman, Clifton, NJ, USA)를 사용하여 추출물을 여과하였다. 마지막으로 감압하여 용매를 추출물로부터 분리하고 메탄올을 증발시킨 후 고체 건조물로서 추출물을 수집하였다. 추출된 샘플은 추가 사용이 있을 때까지 4℃의 냉장고에 보관하였다. 2.2. 가스 크로마토그래피 및 질량 분광기 분석 비트 뿌리 껍질 메탄올 추출물(BPME)을 실리카 모세관 컬럼(30 m × {{60}}.25 mm ID × 0 0.25 µm 필름 두께) 화학 조성을 감지하기 위한 질량 선택 감지기가 있는 GC-MS 기기(Agilent 6890N/5973I, California, CA, USA). 기기의 온도는 초기 7{{90}} ◦C로 2분 유지하고 20 ◦C/min에서 305 ◦C까지 유지한 후 1분 동안 유지했습니다. 총 GC 실행 시간은 운반 가스로 헬륨 가스(99.999%)(일정한 동료 속도 1.2mL/min), 인젝터 온도로 250°C, 이온 소스로 230°C로 45분으로 설정되었습니다. 온도. GC-MS 스펙트럼을 기반으로 해당 성분의 상대 백분율을 계산하고 미지 성분의 질량 스펙트럼을 국립표준기술원에서 제공하는 알려진 62,{29}} 패턴과 비교하여 식별했습니다. 컴퓨터 라이브러리(NIST08). 2.3. 세포 배양 재료 및 화학물질 HUVEC는 American Type Culture Collection(ATCC, Manassas, VA, USA)에서 구입했습니다. Dulbecco's Modified Eagle Medium(DMEM), EDTA, 트립신 등과 같은 세포 배양 물질은 Gibco(Paisley, UK)로부터 입수하였다. 페니실린-스트렙토마이신(PS)과 태아 소 혈청(FBS)은 미국 Hyclone Laboratories에서 구입했습니다. 분자생물학 실험에 사용된 화학물질은 Sigma-Aldrich, 특히 MTT[3-(4,5-dimethylthiazol-2-yl)-2,5- diphenyltetrazolium bromide], PI 및 JC{40}} 염색. SYBR Green PCR Master Mix 및 cDNA 합성 키트는 Qiagen(Hilden, Germany)에서 구입했습니다. 2.4. HUVEC HUVEC를 DMEM에서 배양하고 1% PS 및 10% FBS 복합체로 보충했습니다. 세포를 37℃, 5% CO2의 가습 분위기에서 배양하고 대략 3일마다 계대 배양하였다. 2.5. MTT Assay에 의한 세포 생존율 및 세포 증식 HUVEC(1 × 104 cells/well)를 유지 배지로 배양하고 {{54}웰 배양 플레이트에서 밤새 부착되도록 했습니다. 그런 다음, 배지를 MTT assay plate map에 따라 증가하는 농도의 BPME(0, 0.05, 0.1, 0.2, 0.4, 0.8, 1.6, 3.2μg/mL)를 포함하는 새로운 배양 배지로 교체하고 24 및 48 동안 배양했습니다. 시간; 처리되지 않은 세포를 대조군으로 사용하였다. 배양 기간 후, 실험 세포를 20 μL/웰의 5 mg/mL의 MTT(3-[4,5-디메틸티아졸-2-일]-2, 5-디메틸 설폭사이드(DMSO)에 용해되고 37℃에서 4시간 동안 추가로 배양된 디페닐테트라졸륨 브로마이드. 그런 다음 배지를 버리고 생성된 보라색 포르마잔을 100% DMSO 100μL에 용해시켰다. 용액의 흡광도는 570 nm 파장에서 마이크로플레이트 리더(Thermo Scientific, Waltham, MA, USA)를 사용하여 측정하였다. 세포 증식의 백분율(%)은 다음 식에 의해 계산되었습니다: (샘플의 흡광도/대조군의 평균 흡광도) × 100. 2.6. 실험 설계 본 세포 증식 분석에 따르면, 시험된 더 낮은 농도의 BPME(0.1 및 0.2 μg/mL)는 독성 없이 증식하는 HUVEC 및 미세소관 형태를 나타냈다. 0.1 및 0.2 µg/mL 용량의 BPME를 선택하고 정상 HUVEC와 10mM의 H2O 유도 산화 스트레스 HUVEC로 48시간 동안 처리하여 세포 증식, 항염증, 혈관신생 및 세포자멸 잠재력을 결정했습니다. (그림 1). 차량 제어도 두 그룹에서 48시간 동안 유지되었습니다. 케르세틴(10 μM)은 두 실험 그룹 모두에서 참조 대조군으로 사용되었습니다. 배양 후 BDTM MitoScreen(JC{105}}) 키트를 사용하여 미처리 세포와 실험 세포를 세포 및 핵 형태와 미토콘드리아 막 전위에 대해 분석했습니다. 아폽토시스는 동료 세포 계측법에서 Annexin V/apoptosis 기반 세포 분류 방법에 의해 결정되었습니다. 산화 스트레스, 전염증 및 혈관 신생 관련 유전자 발현 수준을 조사했습니다.

2.7. 핵 손상에 대한 Propidium Iodide 염색 분석 HUVEC에서 0.1 및 0.2 µg/mL의 BPME(H2O2 포함 또는 제외)로 처리한 후 특징적인 핵 손상, pyknosis 또는 세포자멸사 형태 변화에 대한 세포 형태 Leite et al.에 의해 기술된 바와 같이 도립 형광 현미경 하에서 PI 염색 분석을 사용하여 결정되었다. [27].
2.8. JC-1 염료 염색에 의한 미토콘드리아 막 전위(Δψm) 분석 미토콘드리아 막의 전위(Δψm)는 JC-1 분석에 의해 결정되어 비히클 제어 및 {{4} }.1 및 0.2 µg/mL의 BPME 처리 HUVEC(H2O2 포함 및 제외). 간단히 말해서, JC{11}} 염색 용액을 유사한 부피의 배양 배지와 혼합한 다음 실험용 HUVEC에 첨가하고 37℃에서 20분 동안 암실에서 배양했습니다. 그런 다음, 결합되지 않은 JC{14}} 염료를 4 ºC에서 200 µL의 JC{16}} 염색 세척 완충액을 사용하여 부드럽게 두 번 세척했습니다. 이후, 형광현미경을 이용한 형광현미경으로 JC{19}} 염색에 대한 j-응집체의 축적을 관찰하고 영상을 촬영하였다. 또한 BDTM MitoScreen(JC{20}}) Kit를 사용하여 유세포 분석에서 미토콘드리아 막의 전위를 측정했습니다.
2.9. 유세포 분석을 사용한 Annexin V/apoptosis 분석 동료 세포 분석 기반 Annexin V/PI 검출 키트(Sigma Chemicals, USA) 방법을 사용하여 생존 세포, 세포 사멸 촉진, 조기 세포 사멸 및 괴사 세포를 정량화했습니다. 산화 스트레스 유발 HUVEC(1 × 105/웰)를 24-웰 플레이트에 플레이팅하고 BPME(0.1 및 0.2 µg/mL) 또는 비히클 대조군과 함께 배양했습니다. 48시간 인큐베이션 후 세포를 400μL의 5μL Annexin V-fluorescein isothiocyanate(FITC) 및 5μL의 PI 함유 결합 완충액에서 인큐베이션했습니다. 그 후, 세포를 암실에서 실온(RT)에서 15분 동안 유지하였다. 세포는 세포사멸(PI 음성 및 Annexin V 양성) 및 후기 세포사멸(PI 양성 및 Annexin V 양성) 세포를 식별하기 위해 동료 세포측정법(BD Biosciences, San Jose, CA, USA)으로 분석되었습니다[28].
2.10. 정량적 실시간 PCR 분석 Fastlane® Cell to cDNA 키트(Qiagen, Hilden, Germany)를 사용하여 반자동 정량 PCR(qPCR)을 사용하여 비히클 대조군, BPME 처리 HUVEC(H2O2 포함 및 미포함)에서 전체 RNA 및 합성 cDNA를 추출했습니다. 기기(Applied Biosystems, Foster City, CA, USA). (과산화지질, NOS{6}}), 항산화제(Nrf-2, GSK-3 및 GPx), 전염증성(핵인자-κ(NF-κ), 종양 괴사 인자-(TNF-), 인터루킨{13}}(IL{14}}), 혈관 세포 성장 인자(VEGF), 톨 유사 수용체{16}}(TLR{17}})) , 및 혈관 염증(세포내 부착 분자(ICAM), 혈관 세포 부착 분자(VCAM), EDN1 및 내피 산화질소 합성효소(eNOS)) 관련 유전자 및 참조 유전자인 -액틴을 HUVEC에서 분석하고 상기 방법으로 정량화하였다. Yuan et al. [29]. 증폭 값(∆Ct)은 Ct(처리)와 Ct(대조군)의 차이로 계산되었습니다. 유전자 발현은 2−∆∆Ct 값의 표현을 사용하여 플로팅되었습니다.
2.11. 통계 분석 모든 실험은 3중으로 진행되었으며 결과 데이터는 평균값 ± 표준편차(SD)로 표시되었습니다. 그룹 간의 차이에 대한 통계적 분석은 SPSS 소프트웨어(Version 28.5, SAS Institute Inc., Cary, NC, USA)를 사용하여 일원 분산 분석(ANOVA)에 의해 수행되었습니다. 그런 다음 유의한 차이가 발견되면 Tukey의 다중 비교 테스트를 수행했습니다. 모든 결과는 각 그룹에서 6회 반복에 대한 평균 ± SD로 표시되었습니다. p-값 < 0.05는="" 유의미한="" 것으로="">

면역력 향상을 위한 시탕슈
3. 결과
3.1. BPME의 생리활성 분자 GC-MS(Turbomass, PerkinElmer)를 이용하여 BPME의 화학적 성분을 확인하였다. 비트 뿌리 껍질 추출물의 화학적 조성은 NIST(National Institute of Standard and Technology) 스펙트럼 데이터베이스에서 사용할 수 있는 질량 스펙트럼을 비교하여 결정되었습니다. GC-MS 결과 BPME에는 하이드록시아세톤(8.18%), 5-하이드록시메틸푸르푸랄(32.6%), 메틸피루베이트(15.13%), 베타-d-알로피라노스(1.48%), 푸르푸랄(9.98%), 2-히드록시-감마-부티로락톤(1.32%) 및 2,{23}}디히드로-3,{25}}디히드록시- 6-메틸{27}}H-피란 -4-1(12.4%, 그림 2a, 표 1). 3.2. 세포 증식 HUVEC에 대한 BPME의 시험관 내 세포 증식 가능성은 그림 2b에 나와 있습니다. 비히클 대조군과 비교하여 실험군에서는 유의한 세포 성장 억제가 관찰되지 않았다. HUVEC로 처리한 BPME의 농도를 증가시키면 처리 24시간(1{51}}3%)과 비교하여 48시간(112%) 후에 세포 증식 및 생존율이 증가함을 본 연구를 통해 확인했습니다. 또한, 48시간 후 BPME 처리된 HUVEC의 광학 현미경 이미지는 부착 세포 형태의 균일한 모양을 갖는 정상 세포를 확인하고, 손상 없이 증식(복제) 세포의 수가 증가하는 것이 분명했습니다(그림 2c). 3.3. HUVEC에서 세포 및 핵 형태, 미세소관 형성 및 JC{46}} 염색 분석 그림 3은 FL 형광 현미경 이미지에서 미세소관 발달의 형태를 보여줍니다. H2O{49}}유도된 산화 스트레스 HUVEC는 대조군 HUVEC에 비해 불량한 증식 및 부착 세포의 불규칙한 형태를 보였다. 0.2 µg/mL의 BPME로 처리된 정상적인 HUVEC는 복제 또는 미세소관 형태의 신생을 통해 증식하는 세포를 보여주었습니다. 한편, 0.1 µg/mL 용량의 BPME 처리된 세포는 미세소관의 초기 단계를 가진 1{59}}0% 부착 세포를 보여주었습니다. 0.2μg/mL의 BPME로 처리된 산화 스트레스 HUVEC는 미세소관 형태와 감소된 산화 세포 손상을 가진 증식하는 새로운 세포를 확인했습니다. 또한 0.1 µg/mL의 BPME는 증식하는 세포와 함께 정상적인 혈관 세포 형태를 증가시켰습니다.

그림 4a는 대조군과 BPME(0.1 또는 0.2 µg/mL) 처리된 HUVEC에서 구형의 핵 구조의 정상적인 형태를 보여줍니다. 그림 4b는 H2O2에 의해 유도된 산화 스트레스가 있는 정상 및 HUVEC의 PI 염색 이미지를 보여줍니다. H2O{{1{12}}}}처리된 HUVEC는 불규칙한 모양의 핵을 보여 3{14}}분 후에 응축과 pyknosis를 나타냅니다. 그러나 산화 스트레스 하에 HUVEC에 대한 0.2 µg/mL의 BPME 처리는 정상적인 형태를 갖는 원형 핵을 보여주었습니다. 0.2 µg/mL의 BPME 추출물과 비교할 때 0.1 µg/mL의 BPME는 HUVEC에서 H2O{19}} 유도 산화 스트레스에 대한 보호 효과가 더 낮습니다.

그림 2. 비트 뿌리 껍질 메탄올 추출물(BPME)의 농도를 증가시켜 처리한 HUVEC에서 비트 뿌리 껍질 메탄올 추출물(a), 시험관 내 세포 증식(b) 및 세포 형태에 대한 광학 현미경 이미지(c)의 GC-MS 크로마토그램 결과 ) (빨간 화살촉으로 언급된 부착 및 증식 세포의 균일한 모양). 모든 값은 평균 ± SD(n=6)입니다. * p 차량 제어와 비교하여 0.05 이하.

그림 3. 비히클 대조군, 0.1 및 0.2 µg/mL 용량의 비트 뿌리 껍질 메탄올 추출물(BPME) 처리 정상 및 H2O{{6}에서 형광 현미경을 기반으로 한 미세관 형성 분석 } 48시간 후 산화 스트레스를 받은 HUVEC를 유도했습니다. 48시간 후, H2O{11}}유도 산화 스트레스 HUVEC는 차량 대조군과 비교할 때 변경된 형태를 보여주었습니다. 비트뿌리 껍질 메탄올 추출물(BPME) 처리된 HUVEC의 부피{13}}.1 및 0.2 µg/mL는 평활근 세포 행동의 일반적인 형태와 유사한 증식하는 세포가 있는 혈관 미세소관과 함께 정상적인 형태를 보여주었습니다.
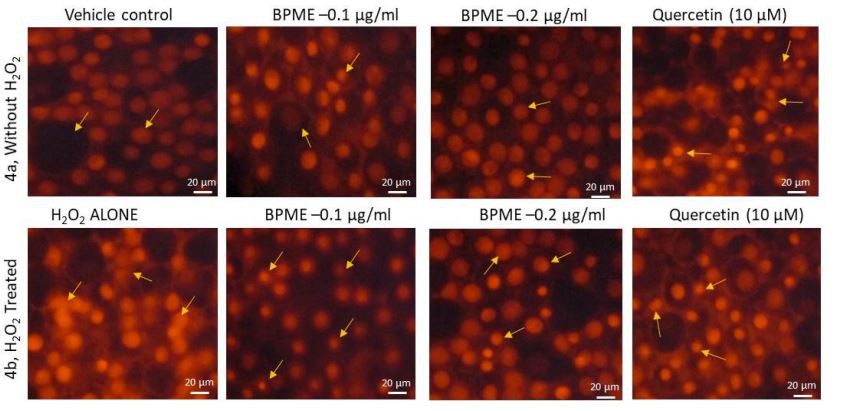
그림 4. 비트루트 껍질 메탄올 추출물(BPME) 처리된 정상(3a) 및 H2O2-는 48시간 후 산화 스트레스(3b) HUVEC를 유도했습니다. PIstaining에서, 비히클 대조군은 핵이 수축, pyknosis 또는 apoptotic 핵의 징후 없이 정상인 것으로 나타났습니다. H2O2 단독에서 처리된 세포는 48시간 후에 분극화된 핵막을 나타냈다. 0.2 µg/mL의 BPME 처리는 0.1 µg/mL BPME 또는 케르세틴 10 µM과 비교할 때 H2O 유도 핵막 분극을 정상화했습니다.
그림 5a는 대조군 및 BPME 처리된 세포를 포함한 HUVEC에 대한 JC{1}} 염색 결과를 보여줍니다. 그림은 미토콘드리아 외 친유성 양이온 JC-1(녹색) 및 미토콘드리아 내에서 적색으로 변환된 J-응집체의 음으로 하전된 미토콘드리아 흡수로 확인된 활성 미토콘드리아를 가진 건강한 세포를 보여줍니다. 그림 5b는 H2O2에 의해 유도된 산화 스트레스가 있는 HUVEC에 투여된 0.2 µg/mL의 BPME에 대한 JC-1 염색 결과를 보여줍니다. 결과는 0.1 µg/mL의 BPME(61.4%) 처리와 비교할 때 음으로 하전된 미토콘드리아의 거의 94%가 친유성 양이온 JC{13}}(녹색)를 적색 J-응집체로 전환했음을 확인했습니다. 또는 H2O{{20}}는 HUVEC에서 산화 스트레스를 유발합니다(2%). 미토콘드리아 막 전위(MMP)는 대조약인 케르세틴과 비교하여 BPME 처리 세포에서 더 높은 것으로 관찰되었습니다. 3.4. FACS 지원 미토콘드리아 막 전위(Δψm; BD MitoScan) 및 HUVEC의 Annexin V/아폽토시스 분석 그림 6은 정상 HUVEC의 0.2 µg/mL BPME 처리 후 BD MitoScan 분석의 미토콘드리아 막 전위 용량을 보여줍니다. 및 H2O2에 의해 유도된 산화 스트레스가 있는 HUVEC. 우리는 0.2 µg/mL의 BPME 처리가 H2O2만 처리한 HUVEC(27.9% ± 7.2%)와 비교할 때 MMP(Δψm)를 92.7% ± 3.7%로 증가시키는 것을 발견했습니다. 대조적으로, 케르세틴 처리된 세포는 BPME 및 H2O2 또는 H2O2 단독으로 처리된 HUVEC와 비교할 때 증가된 MMP(∆ψm)의 41.4% ± 1.6% 백분율을 나타내었습니다.

그림 5. 비히클 대조군에 대한 JC{1}} 염색을 사용한 미토콘드리아 막 전위 분석, 0.1 및 0.2 µg/mL의 비트 뿌리 껍질 메탄올 추출물(BPME) 처리 정상(a ) 및 H2O2- 유도 산화 스트레스 (b) 48시간 후 HUVEC. JC{1{16}}}}J-응집체 대 단량체 형태의 JC{11}}에 해당하는 염료의 빨강 및 녹색 신호 병합 이미지를 보여주는 JC{11}}형광 이미지. 우리는 HUVEC 단독으로 처리된 J-응집체 H2O2가 더 적음을 발견했습니다. 0.2 µg/mL BPME 처리 HUVEC에서 0.1 µg/mL의 BPME 또는 10 µM의 퀘르세틴과 비교하여 높은 미토콘드리아 막 전위를 직접 나타내는 높은 j-응집체(높은 MMP, Δψm)를 나타냅니다.
4. 토론
세포외 또는 세포내 스트레스 시 활성산소종(ROS) 생체이용률이 항산화 방어를 능가하고 산화 스트레스는 산화환원 신호 및 제어를 방해합니다[31]. 산화 스트레스의 발달은 퇴행성 신경 질환, 당뇨병 및 죽상 동맥 경화증과 같은 만성 질환의 발병 원인과 관련이 있습니다. 예를 들어, 산화 스트레스는 내피 기능 장애를 시작하고 전신 염증 및 대식세포 모집을 촉진합니다[32]. 활성화된 면역 세포는 혈관 구조로 이동하여 평활근 세포 혈관의 혈관 수축 및 리모델링 및 혈관 평활근 세포 및 혈관벽에 영향을 미치는 염증과 관련된 사이토카인 및 케모카인을 방출합니다[33]. 증가된 혈관 산화 스트레스는 혈관 손상, 평활근 세포 경직 및 구조적 엘라스틴 이상으로 끝납니다. 또한 혈관 산화 스트레스는 혈관주위 지방 조직에서 증가된 NADPH 산화효소(NOX{3}}) 활성으로 인해 내장 비만이나 죽상동맥경화증과 같은 다른 병리학적 상태에서 자극되었습니다[34]. 혈관 산화 스트레스는 노화 과정에서 발생하는 주요 후성 유전적 변화를 유발하며 조기 노화 과정으로 끝납니다[35]. 생물학적 시스템에서 ROS 생성 및 산화 스트레스의 발달은 NOX-2, 내피 xanthine oxidase, uncoupled eNOS 및 lipoxygenase 외에 미토콘드리아 기능 장애에 크게 의존합니다[36]. 식이제의 항산화 특성은 증가된 항산화 능력을 통해 ROS 생성을 중화할 수 있습니다[26]. 은행나무 추출물은 OxiLDL로 유발된 내피 기능 장애에서 ROS 생성과 리폭시게나제 활성을 감소시켜 죽상동맥경화증의 발병을 방지합니다[37]. 또한 다양한 페놀화합물과플라보노이드식용 식물과 곡물은 ROS와 지질 과산화를 제거하는 성질을 가지고 있습니다[38]. 비트 뿌리 껍질(Beta vulgaris) 메탄올 추출물은 고섬유질, 안토시아닌, 그리고 비텍신 및 베타닌과 같은 플라보노이드의 가용성으로 인해 항산화 가능성이 있습니다[39]. 현재 연구에서 BPME는 미토콘드리아 막 전위, LPO 소광 및 혈관 염증 관련 mRNA 발현 억제에 미치는 영향을 발견하기 위해 미토콘드리아 의존적 기계론적 접근을 확인하기 위해 선택되었습니다. MTT 분석은 0.2 µg/mL의 BPME를 테스트한 0.1 µg/mL에 비해 PI 염색에서 증가된 핵 무결성으로 확인된 바와 같이 BPME가 세포 증식을 유의하게 증가시켰음을 확인했습니다. 비피엠. 농도가 낮고 활성이 가장 높은 유효량을 확인하는 것은 생리학적으로 안전한 것으로 간주될 수 있습니다. 우리는 JC-1의 FL 형광 현미경 염색을 발견했으며 0.2 µg/mL의 BPME 후 미토콘드리아 막 전위가 정상 및 H2O{{1{12}}}유도 외부 자극 산화 스트레스 HUVEC 모두에서 회복되었습니다. 치료. 미토콘드리아 기능 장애는 글루타티온 퍼옥시다제에 의해 산소(O2·-) 라디칼을 H2O2 및 H2O로 변환하지 못하는 산화적 인산화를 변경합니다. 불충분한 ROS 해독 또는 통제되지 않은 ROS 생성으로 인해 증가된 미토콘드리아 산화 스트레스는 동맥경화증과 관련이 있습니다[40]. 비트 뿌리 껍질 추출물은 미토콘드리아 막 잠재력을 효과적으로 회복시켜 ROS 해독과 H2O2 생성을 성공적으로 증가시켰습니다. Annexin V/PI 염색 분석은 BPME 처리가 H2O2에 의해 유도된 산화 스트레스로 정상 HUVEC와 HUVEC 모두에서 생존 세포 비율을 유지하고 세포 증식 단계를 향상시키는 것을 확인했습니다. 이러한 맥락에서 Choo et al. [41] 허혈 부위에서 과도한 ROS 또는 외인성 H2O2가 생성된 후 이식된 중간엽 줄기세포(MSC)가 자가 증식 및 다계통 능력을 손상시킬 수 있음을 확인했다. 재생의학에서 혈관평활근세포는 동맥말초저항 유지, 혈압조절, 동맥수복 등을 통해 수축성 동맥의 주요 조절자이다[42]. 또한, EC의 연령 유도 표현형 조절은 세포 수축성 감소 및 세포 노화 증가와 관련이 있습니다. 지속적인 스트레스 또는 감소된 기계적 민감성 때문에 노화된 평활근 세포에서 미세 환경 신호의 감소된 적응이 확인됩니다[43]. 본 결과는 혈관신생 능력에 의해 입증된 바와 같이 BPME 처리가 생존 가능한 세포 집단을 유지함을 확인시켜 주었다. HUVEC에서 확인된 BPME의 증식 능력은 LPO 발현의 감소와 항산화 유전자 발현의 증가에 의해 뒷받침되었습니다. ROS와 LPO는 초기에 세포 증식 또는 분화 동안 미토콘드리아 복합체(I 및 III)와 NOX{31}}에서 생성됩니다[44]. 과도한 ROS는 생체 분자에 반응하고 손상을 일으키며, 특히 세포 증식과 기능에 중요한 게놈 DNA의 무결성을 변경합니다[45]. 그러나 에피갈로카테킨, 토코페롤과 같은 항산화 폴리페놀의식이 섭취는 산화 스트레스로부터 세포를 보호하고 증식 능력을 증가시키는 것으로 확인되었습니다 [46]. 우리 연구에서 H2O2에 의해 유도된 산화 스트레스가 있는 HUVEC에서 LPO의 mRNA 발현 수준이 감소했고 NOS-3, Nrf-2 및 eNOS가 2배 증가하는 것으로 밝혀졌습니다. eNOS는 NOS의 주된 동형이며, 평활근 세포와 혈관 조직에서 대부분의 NO·산물을 담당합니다. NO·는 모든 유형의 혈관을 확장하고 EC에서 혈소판 응집 및 백혈구 부착을 보호합니다[47]. 지금까지 심혈관 위험인자에 대한 상충되는 보고가 많았고, 내피 기능장애는 eNOS 발현의 감소 또는 증가와 관련이 있었다[48]. 혈관 질환에서 관찰된 eNOS의 증가된 발현은 H2O2의 과잉 생산의 결과일 가능성이 있습니다. 돌연변이 산물인 O2·-는 전사 및 전사 후 메커니즘을 통해 eNOS 발현을 증가시킬 수 있습니다[49]. 혈관 질환의 발병은 O2·-, 그리고 최종적으로 ONOO- 형태와 반응한 후 NO·의 분해가 가속화되어 eNOS 결합 해제 및 NOX 효소 기능 장애로 이어진다[50]. 산화 스트레스는 항산화 효소에 의해 억제되었으며 BPME 처리 후 GSK{49}} 및 GPX의 mRNA 수준이 증가했습니다. BPME는 베타레인, 플라보노이드, 폴리페놀, 치료 효소, 아스코르브산, 디히드로아스코르브산(DHAA) 및 무기 질산염(NO3)을 포함하여 생물학적으로 활성인 여러 파이토케미컬을 함유하고 있으며, 이들은 HUVEC의 항산화 능력 상향 조절에 관여할 수 있습니다. 이러한 맥락에서 Cha et al. (2014) [51]은 클로로겐산이 인간 각질형성세포에서 산화 스트레스로 인한 DNA 손상을 효과적으로 보호한다고 보고했습니다. 내피 유래 혈관수축제인 Endothelin-1(Edn{55}})은 평활근 세포 이동을 수행하고 산화질소 유도 스트레스가 있는 세포에서 항아폽토시스 인자로 작용합니다[52,53]. 혈관 리모델링, 이동, 증식 및 세포외 기질 축적 과정은 Edn{60}}과 NO[54,55] 모두에 의해 자극되었습니다. 산화 스트레스가 있는 HUVEC에서 BPME 처리 후 Edn{63}} 발현이 증가하는 것을 관찰했습니다. 산화 스트레스 또는 LPO 축적 시 혈관 염증의 초기 단계는 백혈구가 내피 평활근 세포에 부착되는 것이며, 이는 허혈 및 죽상 동맥 경화증의 중요한 사건에 두드러집니다[56]. VCAM 및 ICAM 발현에 의해 매개됩니다. 이는 NF-κB, IL{66}} 및 TNF- 발현과 같은 많은 케모카인 및 화학주성 제제에 의해 자극되었습니다[57]. IL{69}} 활성화의 억제에 이어 접착 분자 발현이 식이성 페놀 화합물 엘라그산에 의해 달성되었습니다[58]. 산화 스트레스로 외부 자극된 HUVEC에 BPME를 처리하면 VCAM, ICAM, NF-κB, IL{73}} 및 TNF-발현 수준과 같은 혈관 세포 특이적 전염증 인자가 유의하게 감소했습니다. 이와 관련하여 Crespo et al. [59] kaempferol과 quercetin은 각각 VCAM, ICAM, NF-κB 및 IL{78}} 발현과 같은 염증유발 유전자를 억제한다고 보고했습니다. 전반적으로, BPME의 산화 스트레스 및 혈관 염증 관련 유전자 발현 잠재력의 억제는 혈관 세포 성장 인자의 발현을 선호하고 잠재적으로 혈관 세포 증식 및 성장을 돕습니다.

5. 결론
본 연구 결과는 항산화 유전자의 증가된 발현이 산화 스트레스의 소멸과 연관되어 HUVEC 증식 및 혈관신생의 손상을 극복하는 데 도움이 된다는 것을 확인시켜줍니다. 하이드록시메틸푸르푸랄을 함유한 흑마늘은 HUVEC에 대한 TNF 유도 단핵구 세포 부착의 염증 효과를 억제하고 ROS 생성, VCAM{1}} 발현 및 NF-κB 활성화를 더욱 억제합니다[60]. 또한, He et al. [61]은 hydroxymethylfurfural이 저산소증으로부터 EC를 보호할 가능성이 있음을 확인했습니다. 비트 뿌리 껍질은 또한 플라보노이드, 푸란 및 5-하이드록시메틸푸르푸랄, 메틸 피루브산, 푸르푸랄 및 2,3-디하이드로-3,5-와 같은 항산화 성분을 포함하는 것으로 확인되었습니다. 디히드록시{10}}메틸{11}}H-피란{13}}온; 이러한 구성 요소는 향상된 항산화 능력과 전 염증성 혈관 평활근 세포 부착 분자의 억제를 담당합니다. 비트 뿌리 껍질은 과산화 세포 스트레스의 외부 자극 또는 내부 병리학적 자극을 억제하기 위한 항산화 풀의 자극제로 사용되었습니다. 우리의 연구 결과는 비트 뿌리 성분이 HUVEC에서 대사 스트레스와 염증을 줄이는 데 도움이 되며, 이는 혈관 세포 증식과 혈관 신생에 도움이 될 수 있음을 입증했습니다.
저자 기여:
개념화, LNA-H. 및 S.-BP; 방법론, LNA-H. 및 S.-BP; 소프트웨어, GS; 검증, LNA-H. 및 S.-BP; 공식 분석, S.-BP, AMA-D., AAA(Ali A Alshatwi) 및 GS; 조사, LNA-H., S.-BP 및 AMA-D.; 자원, LNA-H.; 데이터 큐레이션, S.-BP 및 LNA-H.; 쓰기 - 원본 초안 준비, LNA-H. 및 S.-BP; 쓰기 - 검토 및 편집, LNA-H., AMS, GS 및 AAA(Amna Abdullah Alotiby); 시각화, S.-BP 및 AAA(Ali A Alshatwi); 감독, LNA-H. 및 S.-BP; 프로젝트 관리, LNA-H.; 자금 조달, LNA-H. 모든 저자는 출판된 원고 버전을 읽고 동의했습니다. 자금 지원: 저자는 연구 그룹 no RG-1442-432를 통해 이 작업에 자금을 지원해 준 King Saud University의 과학 연구 학장에게 감사를 전합니다. : 이 연구에 제공된 데이터는 교신저자의 요청에 따라 제공됩니다. 이해의 충돌: 이 연구에는 이해의 충돌이 없습니다.
참고문헌
1. Abdolmaleki, Z.; 아랍, H.-A.; Amanpour, S.; Muhammadnejad, S. 활성 물질인 artemisinin과 비교한 Artemisia sieberi의 에탄올 추출물의 항혈관신생 효과. 브라스 목사. 파마코그. 2016, 26, 326–333. [교차 참조]
2. 유승준; 권, SM 혈관 신생 및 치료 기회. 중재. 염증. 2013, 2013, 127170. [교차참조] [PubMed]
3. Folkman, J. 암, 혈관, 류마티스 및 기타 질병의 혈관 신생. Nat. 메드. 1995, 1, 27–31. [교차 참조]
4. Hoeben, A.; Landuyt, B.; 하이리, MS; Wildiers, H.; 반 우스테롬, AT; De Bruijn, EA 혈관 내피 성장 인자 및 신생. 파마콜. 개정판 2004, 56, 549–580. [교차 참조]
5. 페라라, N.; Alitalo, K. 혈관신생 성장 인자 및 그 억제제의 임상 적용. Nat. 메드. 1999, 5, 1359-1364. [교차 참조]
6. 갤리, HF; Webster, NR 내피의 생리학. 브르. J. 아나에스. 2004, 93, 105–113. [교차 참조]
7. Onat, D.; Brillon, D.; 콜롬보, PC; Schmidt, AM 인간 혈관 내피 세포: 당뇨병 및 죽상 동맥 경화증의 혈관 염증 연구를 위한 모델 시스템. 커 당뇨병 대표 2011, 11, 193–202. [교차 참조] [PubMed]
8. 패커드, RR; Libby, P. 죽상동맥경화증의 염증: 혈관 생물학에서 바이오마커 발견 및 위험 예측까지. 클린. 화학 2008, 54, 24–38. [교차 참조]
9. 에스퍼, RJ; Nordby, RA; 빌라리뇨, 조; 파라가노, A.; 카카론, JL; Machado, RA 내피 기능 장애: 포괄적인 평가. 심장 박동 당뇨병. 2006, 5, 4. [교차참조]
10. Baudin, B.; 브루닐, A.; Bosselut, N.; Vaubourdolle, M. 인간 제대 정맥 내피 세포의 분리 및 배양을 위한 프로토콜. Nat. 프로토콜 2007, 2, 481–485. [교차 참조] [PubMed]
11. 차오, Y.; Cao, R. 차를 마시면 혈관 신생이 억제됩니다. Nature 1999, 398, 381. [CrossRef] [PubMed]
12. 엔, G.-C.; Duh, P.-D.; Tsai, H.-L. 아스코르브산과 갈산의 항산화 및 산화촉진 특성. 식품화학 2002, 79, 307–313. [교차 참조]
13. Dhalaria, R.; Verma, R.; Kumar, D.; 푸리, 에스.; Tapwal, A.; Kumar, V.; Nepovimova, E.; Kuca, K. 노화 방지 특성이 있는 식용 과일의 생리 활성 화합물: 인간의 수명을 연장하기 위한 포괄적인 검토. 항산화제 2020, 9, 1123. [CrossRef] [PubMed]
14. Baião, DdS; 다 실바, D.; 델 아길라, EM; Paschoalin, VMF 다양한 비트 뿌리 제형의 영양, 생리활성 및 물리화학적 특성. 음식 중독자. 2017, 6. [교차참조]
15. Lalonde, R.; Roitberg, B. 나무에서 짝짓기 행동의 진화: 포식 또는 날씨? 이다. Nat. 1992, 139, 6. [교차 참조]
16. 실바, D.; Baiao, DDS; 페레이라, VF; 다중 경로 산화 스트레스 및 염증 조절제로서의 Paschoalin, VMF Betanin: 심혈관 질환 발병기전에 보호 효과가 있는 비트 뿌리 색소. 크리. 식품 과학 목사. 뉴트르. 2020, 1–16. [교차 참조]
17. Baiao, DDS; 실바, D.; Paschoalin, VMF 주목할만한 야채: 건강에 도움이 되고 심혈관 질환 치료를 지원하기 위해 질산염과 식물화학물질 함량을 새로운 제형으로 조정할 수 있습니다. 항산화제 2020, 9, 960. [CrossRef] 18. Abd El-Ghaffar, EA; 헤가지, 뉴멕시코; 사드, HH; 솔리만, MM; 엘-레이, 매사추세츠; 셰하타, 에스엠; 바라캇, A.; Yasir, A.; Sobeh, M. 1형 당뇨병 쥐에서 사탕무(Beta vulgaris) 잎의 HPLC-ESI-MS/MS 분석 및 유익한 특성. 바이오메드. 약사. 2019, 120, 109541. [교차참조]
19. Singh, B.; Nathan, BS 비트 뿌리의 화학적 조성, 기능적 특성 및 가공-검토. 국제 J. Sci. 영어 해상도 2014, 5, 679.
20. Ninfali, P.; Angelino, D. Beta vulgaris cicla 및 rubra의 영양 및 기능적 잠재력. 피토테라피아 2013, 89, 188–199. [교차 참조]
