Cistanche Deserticola 다당류는 장내 미생물총-뇌 축을 복원하여 노화 모델 마우스의 인지 감소를 완화합니다
Mar 05, 2022
연락처: Audrey Hu Whatsapp/hp: 0086 13880143964 이메일:audrey.hu@wecistanche.com
Yuan Gao 1,*, Bing Li 1,*, Hong Liu 1, Yajuan Tian 2, Chao Gu 1, Xiaoli Du 1, Ren Bu 1, Jie Gao 1, Yang Liu 1, Gang Li 1
요약
최근 증거는 장내 미생물총-뇌 축의 변화가 노화에 따른 인지 장애를 유발할 수 있음을 시사합니다. 현재 연구에서 우리는 마우스에 D-갈락토스를 장기간 투여하면 인지 저하, 장내 미생물 불균형, 말초 염증 및 산화 스트레스를 유발한다는 것을 관찰했습니다. 이 연령 관련 인지 저하 모델에서,Cistanche Deserticola 다당류(CDPS)는 장내 미생물 항상성을 회복시켜 산화 스트레스와 말초 염증을 감소시켜 D-갈락토스 처리 마우스의 인지 기능을 개선했습니다. 이러한 노화 모델 마우스에서 CDPS의 유익한 효과는 항생제로 장내 미생물총을 제거하거나 사이클로포스파미드를 사용한 면역 억제를 통해 폐지되었습니다. 혈청 대사체 프로파일링은 크레아티닌, 발린, L-메티오닌, o-톨루이딘, N-에틸아닐린, 요산 및 프롤린의 수준이 노화 모델 마우스에서 모두 변경되었지만 CDPS에 의해 회복되었음을 보여주었습니다. 이러한 발견은 CDPS가 아미노산 불균형, 말초 염증 및 산화 스트레스를 완화시키는 장내 미생물총-뇌 축의 항상성을 회복함으로써 마우스의 D-갈락토스 유도 노화 모델에서 인지 기능을 향상시킨다는 것을 입증했습니다. 따라서 CDPS는 기억 및 학습 장애가 있는 환자, 특히 장내 미생물 불균형과 관련된 환자에게 치료 가능성을 보여줍니다.
시스탄체 데저티콜라다당류
소개
D-갈락토스(D-gal) 및 베릴륨염의 장기간 투여는 실험 동물 모델 및 시험관 내 1차 세포 배양에서 노화를 유도하고 자연 노화 과정의 기본 메커니즘을 확인하는 데 사용됩니다[1-4]. 이전 연구에서는 D-갈락토스 유도 노화 모델 마우스의 인지 저하가 뇌의 신경 성장 인자(NGF) 단백질 수준 감소 및 활성 산소종(ROS) 증가와 관련이 있음을 보여줍니다. 두 가지 모두 해마 뉴런의 퇴화를 유발하고 신경발생 [3, 4]. 최근 연구에 따르면 인간의 장내 미생물총의 구성과 수는 노화 과정에서 크게 변하는 것으로 나타났습니다[5].
시스탄체 데저티콜라중국 북서부 사막 지역에서 주로 자라는 약초로 한약재로 사용됩니다. 그것은 일반적으로 "사막의 인삼"으로 알려져 있습니다. Cistanche Deserticola 추출물에는 페닐에타노이드 배당체, 이리도이드, 리그노오스, 올리고당, 다당류 및 아미노산을 비롯한 여러 약리학적 활성 화합물이 포함되어 있습니다. 이러한 화합물은 항염, 항산화, 노화 방지, 신경 보호 및 면역 조절 특성과 관련이 있습니다[6, 7]. 예를 들어, Cistanche Deserticola에서 추출한 다당류는 한의학에서 대장암 치료에 사용되었습니다[8]. Chuanqiong polysaccharide, Ganoderma lucidum polysaccharide, Lycium barbarum polysaccharide [9-11]와 같은 여러 유기체에서 유용한 생체 활성을 가진 광범위한 약독성 다당류가 분리되었습니다. CDA-
0.05는 Cistanche Deserticola에서 분리된 갈락토글루칸으로, 여러 종의 Bacteroides 및 Lactobacillus를 포함하여 여러 유익한 장내 세균의 성장을 촉진합니다[12].
정상적인 노화 과정의 기본 메커니즘은 신경퇴행성 장애, 관상동맥 동맥경화증, 제2형 당뇨병(T2DM) 및 고혈압과 같은 여러 인간 질병과도 관련이 있습니다[13, 14]. 최근 연구에 따르면 장내 세균총의 변화가 인간의 노화에 중요한 역할을 한다는 것이 밝혀졌습니다[15]. 여러 연구에 따르면 실험용 쥐와 쥐에서 D-갈락토오스를 장기간 투여하면 정상적인 노화 과정을 모방하고 인지 저하와 같은 노화 관련 표현형을 연구하는 데 유용한 모델이 됩니다[16]. 또한, D-갈락토스 유도 노화 모델 마우스는 장내 미생물 구성의 변화를 보여줍니다[17]. 따라서 우리는 장내 미생물 구성의 변화가 D-갈락토스 유도 노화 모델 마우스에서 인지 저하를 유발할 수 있다는 가설을 세우고 Cistanche Deserticola polysaccharides(CDPS)가 장내 미생물 불균형을 복원하여 인지 저하를 완화할 수 있는지 조사했습니다.

시스탄체 데저티콜라
결과
D-갈락토스 유도 노화 모델 마우스는 인지 저하 및 장내 미생물 불균형을 보여줍니다
우리는 야생형(WT) 마우스와 새로운 개체 인식 및 Morris water maze(MWM) 테스트를 사용하여 2개월 동안(모델 또는 Mod) 체중 Kg당 150mg D-gal로 처리된 마우스의 행동 성능을 분석했습니다. 신규 물체 인식 테스트의 우선 지수 값은 WT 그룹 마우스에 비해 Mod 그룹 마우스에서 유의하게 감소했습니다(그림 1A, 1B). MWM 테스트 결과는 6일 후 탈출 대기 시간이 WT 그룹에 비해 Mod 그룹에서 유의하게 증가한 것으로 나타났습니다(그림 1C, 1D). 또한, 대상 플랫폼 횡단 및 대상 사분면 내 수영 시간은 WT 그룹에 비해 Mod 그룹에서 크게 감소했습니다(그림 1E, 1F). 이러한 결과는 D-gal-유도 노화 모델 마우스의 학습 및 기억 능력에서 상당한 감소를 보여주었다.
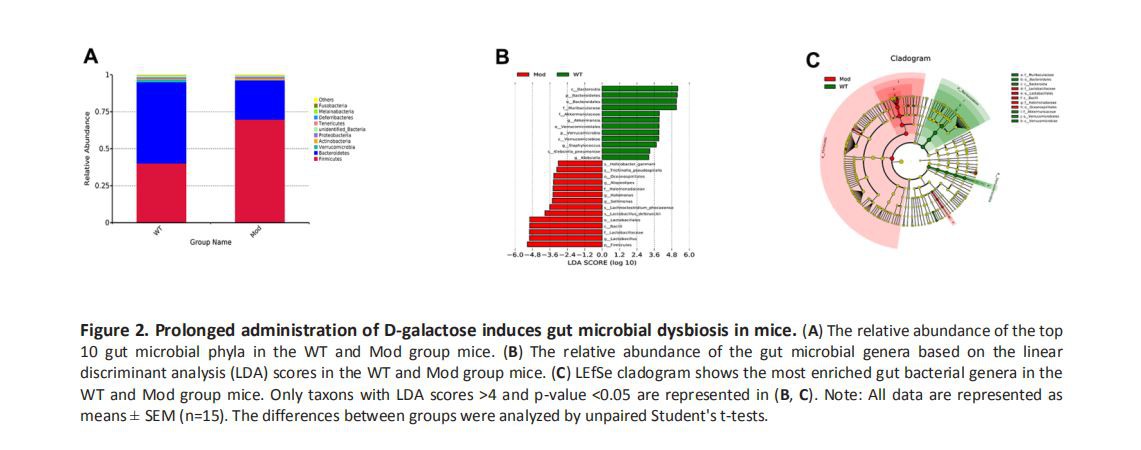
그런 다음 대변 샘플의 16S 리보솜 RNA(rRNA) 시퀀싱 데이터를 사용하여 마우스의 Mod 및 WT 그룹의 대변 샘플에서 장내 미생물 문, 속 및 종의 풍부함 및 구성의 차이를 분석했습니다. WT 및 Mod 그룹 마우스에서 우세한 장내 세균총은 Firmicutes 및 Bacteroides였습니다. 그러나 박테로이데스의 풍부함은 WT 그룹에 비해 Mod 그룹에서 크게 감소하고 Firmicutes의 풍부함이 크게 증가했습니다(그림 2A). 다음으로, 우리는 선형 판별 분석(LDA)을 수행하여 LDA 효과 크기(LEfSe) 점수를 결정한 다음 Kruskal-Wallis 및 Wilcoxon 테스트를 수행하여 WT 및 Mod 그룹 마우스에서 서로 다른 분류군의 상대적 풍부도를 평가했습니다. LDA 결과는 그림 2B에 나와 있습니다. 또한, 우리는 WT 및 모델 그룹에서 Bacteriodes 및 Firmicutes 문에 속하는 다양한 속 및 종의 차등 농축을 보여주는 분지도를 구성했습니다(그림 2C). 전반적으로, 우리의 결과는 D-갈락토스 유도 노화 모델 마우스에서 손상된 인지 능력과 장내 미생물 불균형을 보여주었습니다.
CDPS 처리는 D-gal 유도 노화 모델 마우스의 인지 능력을 향상시킵니다
우리는 CDPS 처리가 D-gal-유도 노화 모델 마우스의 인지 저하를 완화하는지 분석했습니다. 시
투여 2개월째, 격일로 체중을 측정하였다. 모델의 체중과 마우스의 CDPS 그룹은 유사했습니다(그림 3A). 마지막 복용 후 행동 실험을 수행합니다. 새로운 개체 인식 및 Morris 수중 미로 테스트 결과는 단기 기억이 마우스의 모델 그룹과 비교하여 마우스의 CDPS 그룹에서 유의하게 더 높음을 보여주었습니다. 마우스의 CDPS 그룹에서 장기 기억은 더 높았지만 마우스의 모델 그룹에 비해 통계적으로 유의하지 않았습니다(그림 3B, 3C). 이것은 CDPS 처리가 D-gal 처리된 마우스에서 단기 물체 인식 기억의 손실을 없앴다는 것을 시사했습니다.
이 마우스의 공간 학습 및 기억은 Morris 수중 미로 테스트에 의해 평가되었으며, 결과는 마우스의 CDPS 그룹의 탈출 잠복 시간이 WT 그룹의 마우스와 유사하고 Mod 그룹의 마우스보다 상당히 짧은 것으로 나타났습니다(그림 3D ). 또한, 탈출 대기 시간은 모델 그룹에 비해 CDPS 투여 후 6일째에 상당히 낮았습니다(그림 3E). 대상 사분면 내 수영 시간은 모델 그룹에 비해 CH 및 CM 그룹에서 유의하게 더 높았습니다. CL 그룹은 모델 그룹보다 높지만 통계적 유의성은 없습니다(그림 3F). 또한 플랫폼 횡단 횟수는 모델 그룹에 비해 CM 및 CL 그룹에서 유의하게 더 많았습니다. 그러나 CH 그룹은 모델 그룹보다 높으며 통계적 유의성은 없습니다(그림 3G). 이러한 결과는 CDPS 처리가 D-gal-유도 노화 모델 마우스에서 공간 학습 및 기억력을 개선함을 입증했습니다.

CDPS 처리는 D-갈락토스 노화 모델 마우스에서 장내 미생물 구성의 항상성을 회복합니다
단당류와 다당류는 박테리아의 성장에 필요한 필수 영양소입니다[18-21]. 또한 CDPS는 장내 미생물의 구성을 조절한다고 보고되었습니다[22]. 따라서 우리는 WT, 모델 및 CDPS 마우스 그룹의 대변 샘플의 16S rRNA 시퀀싱 데이터를 평가하여 CDPS 처리가 모델 그룹 마우스의 장내 미생물 불균형을 완화하는지 분석했습니다.
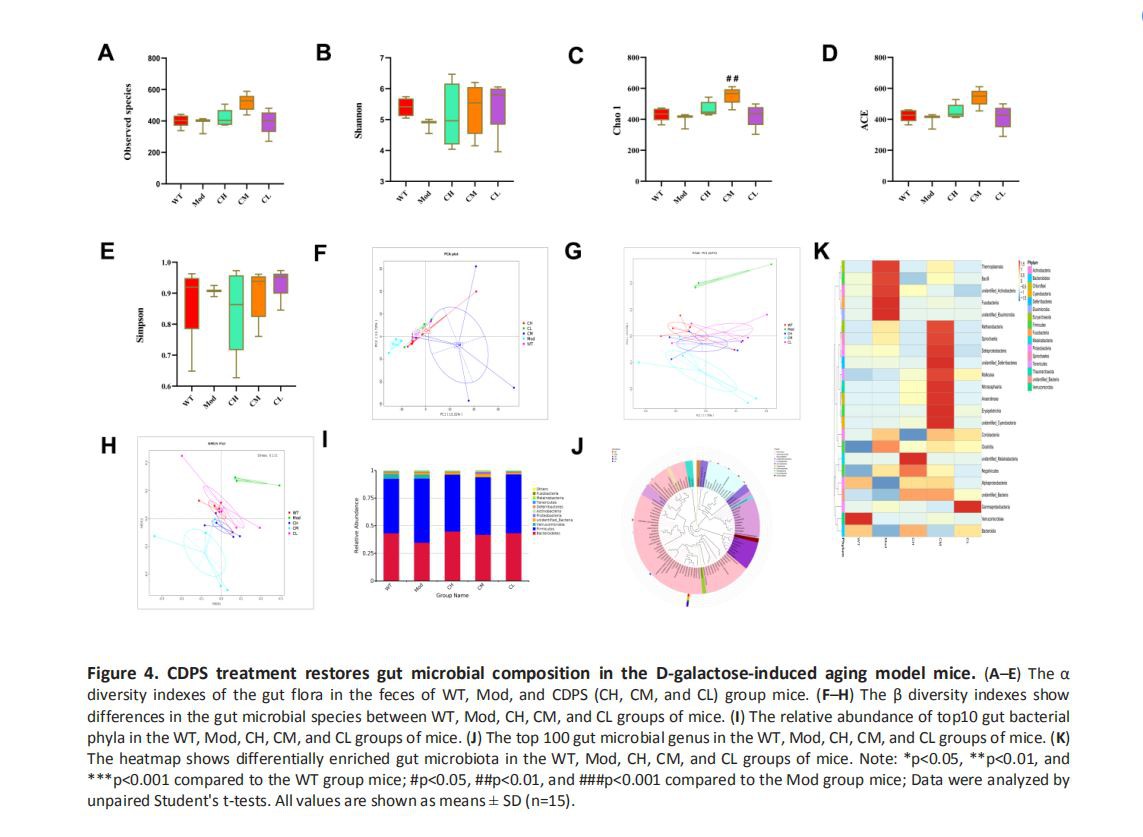
첫째, 우리는 알파 다양성 지수를 계산하여 이들 그룹 간의 전반적인 분변 미생물군 풍부도와 구조적 차이를 평가했습니다. 우리는 관찰된 종, Shannon, Chao 1, ACE 및 Simpson 지수 값과 같은 알파 다양성(-다양성) 지수를 분석하여 다른 쥐 그룹의 대변 샘플에서 다양한 박테리아 종의 구성 변화를 결정했습니다. -다양성(관찰종, Shannon, Chao 1, ACE 및 Simpson 지수) 지수는 WT 및 CDPS 마우스 그룹이 모델 그룹에 비해 높았으나 통계적 유의성은 CM 사이의 Chao 1 지수 값에서만 관찰되었습니다. 그룹 및 모드 그룹. CDPS를 사용한 투여는 미생물군유전체의 풍부함을 증가시키는 것으로 나타났습니다(그림 4A-4E). 다음으로 NMDS(Non-metric Multi-dimensional Scaling), PCoA(Principal Coordinates Analysis) 및 주성분 분석(Principal Component Analysis)을 사용하여 WT, 모델 및 CDPS 그룹 간의 장내 미생물 종의 차이를 식별하기 위해 다양성 지수를 분석했습니다. PCA). PCA는 치수 감소 및 패턴 및 추세의 유지를 포함하여 노화 과정 동안 모델 그룹 마우스의 장내 미생물 구성의 변화를 보여주었습니다(그림 4F). WT, 모델 및 CDPS 그룹 간의 대변 미생물군의 차이는 16S rRNA 유전자에 대한 비가중 UniFrac 거리의 PCoA를 기반으로 확인되었습니다(그림 4G). 클러스터링 분석은 모델 그룹과 WT 및 CDPS 그룹 간의 NMDS에서 상당한 차이를 보여주었습니다(그림 4H).
우리는 장내 미생물군의 상위 10개 문을 평가한 결과 Bacteroides 문이 모델 그룹에 비해 CH, CM 및 CL 그룹에서 유의하게 더 높다는 것을 발견했습니다(그림 4I). 이것은 CDPS가 D-gal 처리된 마우스에서 장내 미생물의 항상성을 회복했음을 시사했습니다. cladograms는 WT, 모델 및 CDPS 그룹에서 Bacteriodes 및 Firmicutes 문에 속하는 다양한 속 및 종의 차등 농축을 보여주었습니다(그림 4J). 히트맵에서 볼 수 있듯이 CDPS 처리는 온도플라스마타, 바실러스, 미확인 악티노박테리아, 푸소박테리아, 미확인 엘루시마이크로비아의 상대적 존재비를 감소시키고 메타노박테리아, 스피로케티아, 델타프로테오박테리아, 미확인{5}}데페리박테리아, 몰리오스파세균, 니트로세균의 상대적 존재비를 증가시켰습니다. , Erysipelotrichia 및 미확인 시아노박테리아_모델 그룹과 비교했습니다(그림 4K). 이러한 결과는 CDPS 처리가 D-gal-유도 노화 모델 마우스에서 장내 미생물의 항상성을 유의하게 회복시킴을 입증하였다.
CDPS 처리는 산화 스트레스를 감소시켜 D-gal-유도 노화 모델 마우스에서 신경 퇴행을 완화합니다
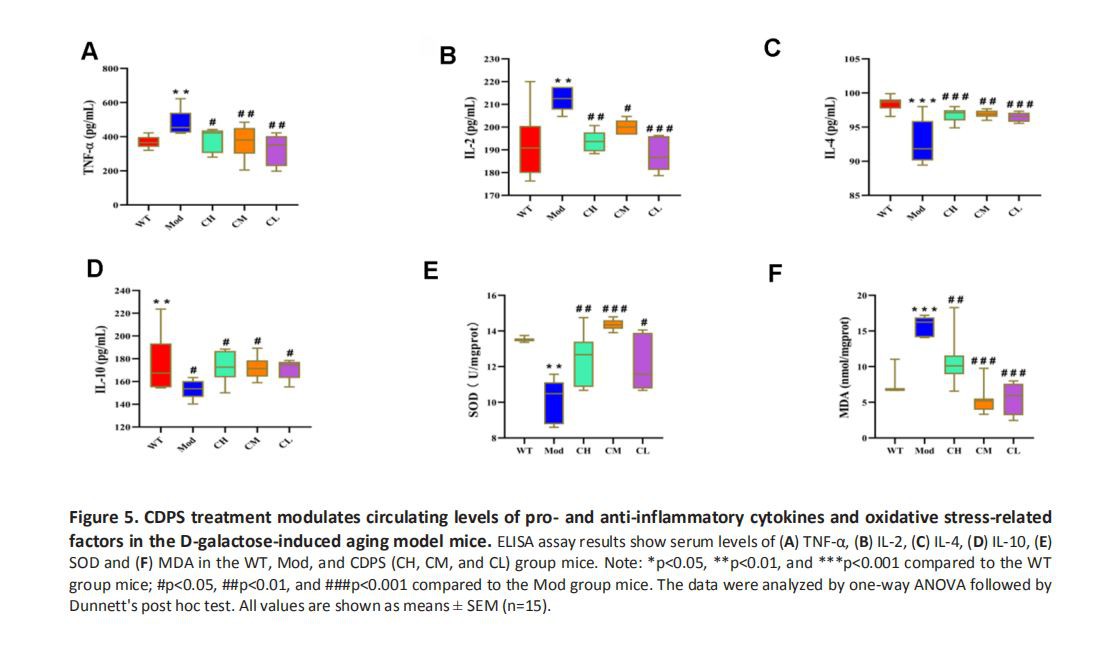
다음으로 우리는 전염증성 사이토카인(IL-2 및 TNF-)과 항염증성 사이토카인(IL-4 및 IL{5}})의 혈청 수준을 분석하여 염증에 대한 CDPS의 영향을 분석했습니다. ) 다른 그룹의 마우스에서. IL-2 및 TNF-의 혈청 수준은 모델에 비해 CH, CM 및 CL 그룹에서 유의하게 낮았고 IL-4 및 IL-10의 혈청 수준은 유의하게 높았습니다. 그룹. CDPS는 항염 효과가 있는 것으로 나타났습니다(그림 5A-5D).
산화 스트레스는 활성산소종(ROS)의 생성 증가로 인해 발생하며 노화를 촉진하는 주요 요인 중 하나입니다[23]. 따라서 우리는 항산화 효소인 SOD와 지질 과산화 생성물인 malondialdehyde(MDA)의 혈청 수준을 평가하여 D-gal에 의해 유도된 노화 마우스 모델에서 산화 스트레스에 대한 CDPS의 영향을 분석했습니다. MDA의 혈청 수준은 WT 그룹과 비교하여 Mod 그룹에서 유의하게 더 높았고 SOD의 혈청 수준은 유의하게 감소했지만 CDPS 처리는 이러한 효과를 역전시켰습니다(그림 5E, 5F). 이러한 결과는 D-gal-유도 노화 모델 마우스에서 산화 스트레스가 증가했지만 CDPS 처리에 의해 감소되었음을 입증했습니다.
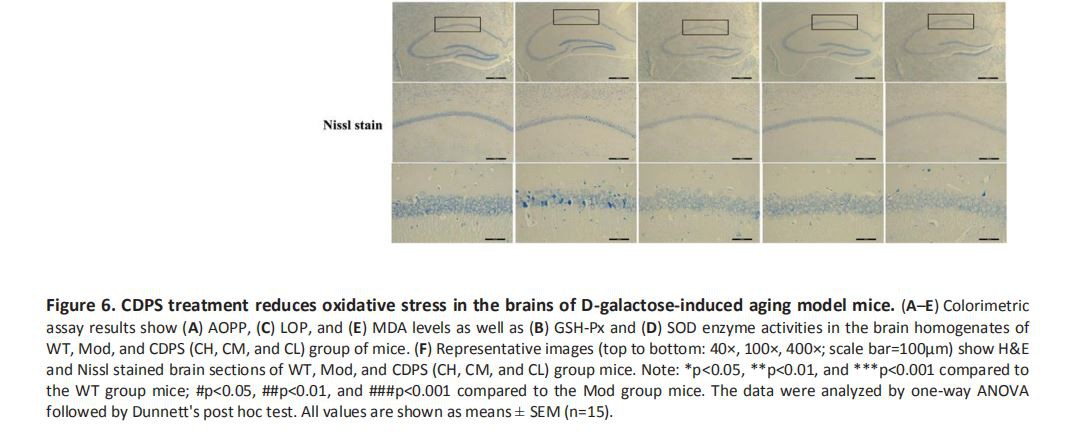
또한 AOPP(Advanced Oxided protein product), LPO(direct lipid peroxidation), MDA의 수준과 glutathione peroxidase(GSH-Px)와 같은 항산화 효소의 활성을 분석하여 뇌 조직의 산화 스트레스 수준을 평가했습니다. ) 및 뇌 조직의 과산화물 디스뮤타제(SOD)가 균질화됩니다. Mod 그룹 마우스의 뇌는 WT 그룹에 비해 SOD 및 GSH-PX의 활성이 유의하게 감소하고 AOPP, LPO 및 MDA의 수준이 크게 증가했지만 이러한 효과는 CH, CM 및 CL 그룹에서 역전되었습니다(그림 6A- 6E).
또한, 우리는 D-gal-유도 노화 모델 마우스의 뇌에 대한 CDPS의 보호 효과를 평가하기 위해 H&E 및 Nissl 염색으로 뇌 섹션의 조직학적 염색을 수행했습니다. Mod 그룹 마우스는 WT 그룹에 비해 신경 세포 수 및 부피의 유의한 감소, 신경 세포 간 간격 증가, 신경 세포의 불규칙한 배열 및 해마 CA1 영역의 핵 pyknosis를 나타내었지만 이러한 병리학적 변화는 CDPS 처리에 의해 유의하게 감소되었습니다( 그림 6F). 이러한 결과는 CDPS 처리가 D-gal-유도 노화 모델 마우스에서 산화 스트레스 및 뇌 병리를 유의하게 감소시킴을 입증하였다.
CDPS 치료는 D-gal 유도 모델 마우스에서 장내 미생물 항상성을 유지하여 말초 염증 및 산화 스트레스를 감소시킵니다
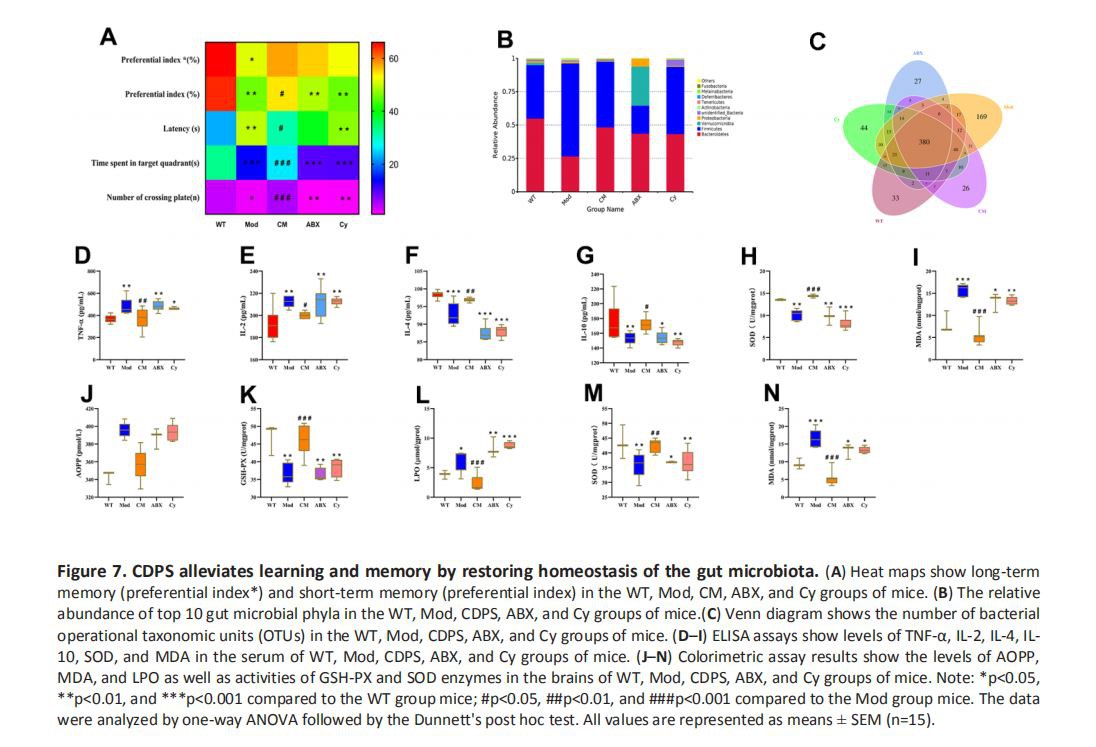
다음으로, 우리는 장내 미생물의 구성 변화가 노화 동안 증가된 말초 염증 및 산화 스트레스와 관련이 있는지 분석했습니다. 이를 위해 우리는 CDPS 처리 노화 모델 마우스에서 장내 미생물을 제거하거나 면역 억제를 유도하기 위해 삼중 항생제 칵테일(ABX 그룹) 또는 사이클로포스파미드(Cy 그룹; 또한 재료 및 방법 참조)를 사용했습니다. 항생제 치료는 노화 모델 마우스에서 CDPS 치료의 유익한 효과를 폐지했습니다. 우리는 CDPS 처리 그룹과 비교하여 ABX 그룹 마우스에서 손상된 학습 및 기억(그림 7A) 및 장내 미생물 구성의 변경(그림 7B, 7C)을 관찰했습니다. 위의 결과는 CDPS를 투여해도 장내 세균총을 변화시킨 후 마우스의 학습 및 기억 능력을 증가시킬 수 없음을 나타냅니다. 또한, 우리는 CDPS 그룹과 비교하여 ABX 그룹 마우스의 뇌와 혈청에서 염증성 사이토카인의 수준이 증가하는 것을 관찰했습니다(그림 7D-7N). ABX군과 CY군의 결과는 장내세균총과 면역기능이 파괴된 후 CDPS를 투여해도 쥐의 학습능력과 기억력을 향상시키지 못하는 것으로 나타났다. 이러한 결과는 CDPS 처리가 장내 세균 불균형을 예방함으로써 D-gal로 유도된 노화 모델 마우스에서 말초 염증, 산화 스트레스 및 인지 저하를 감소시킴을 시사한다.
그런 다음 면역억제제인 사이클로포스파미드[24]를 사용하여 CDPS의 유익한 효과에서 염증의 역할을 결정했습니다. Cyclophosphamide로 처리된 CDPS 마우스(Cy 그룹)는 학습 및 기억 능력 손상, 장내 미생물 구성의 변경, 야생형 및 CDPS 그룹 마우스와 비교하여 뇌와 혈청에서 염증성 및 항염증성 사이토카인의 비정상적인 수준을 보였습니다. 그러나 모델 및 ABX 그룹과 비교하면 의미가 없습니다. (그림 7A-7N). 이러한 데이터는 장내 미생물총 구성의 변경이 D-gal-유도 노화 모델 마우스에서 말초 염증을 증가시킨다는 것을 보여줍니다.
CDPS는 아미노산 대사를 조절하여 D-gal로 인한 노화를 방지합니다.
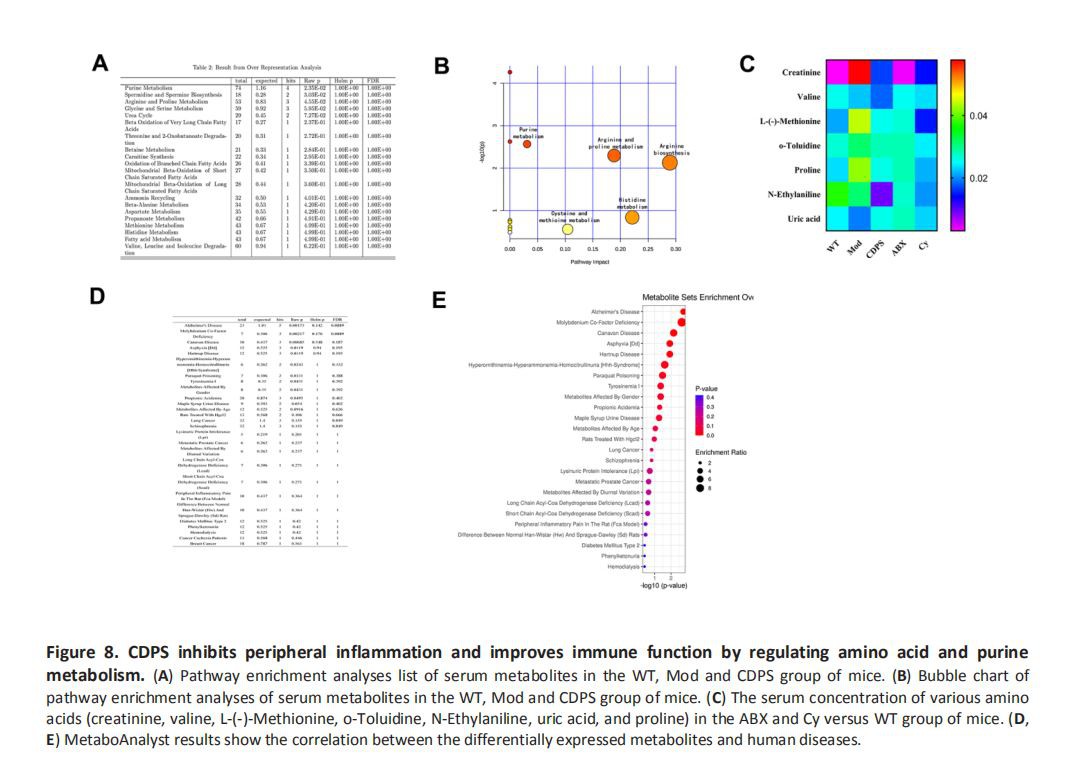
숙주의 면역 체계는 장내 미생물에 의해 생성되는 대사 산물의 영향을 받습니다[25]. 대변 대사 산물은 장내 미생물 대사 및 장내 미생물 구성의 기능적 판독을 나타냅니다[26]. 더욱이, 장내 미생물총의 대사산물은 혈액 순환으로 들어가 숙주의 신진대사와 건강에 영향을 미칩니다[26, 27]. fWT, Mod 및 CDPS 마우스의 혈청 샘플에서 총 1058개의 대사 산물이 확인되었습니다. 그런 다음 BioCyc, Kyoto Encyclopedia of Genes and Genomes(KEGG), Human Metabolome Database(HMDB)를 사용하여 이러한 대사 산물을 분석한 결과 65개의 대사 산물이 WT 그룹과 비교하여 Mod 그룹에서 다르게 발현되었음을 발견했습니다. 또한, 우리는 8가지 대사 산물(크레아티닌, 발린, L-(-)-메티오닌, o-톨루이딘, N-에틸아닐린, 요산, 프롤린 및 페닐알라닌)의 수준이 WT, Mod 및 CDPS 그룹 간에 유의하게 다르다는 것을 발견했습니다. . MetaboAnalyst[28, 29]를 사용한 이 8가지 대사 산물의 경로 농축 분석은 이러한 대사 산물이 아르기닌, 히스티딘, 아르기닌, 프롤린 및 퓨린 대사와 관련이 있음을 보여주었습니다(그림 8A, 8B). WT 그룹에서 MOD 그룹과 CDPS 그룹의 7가지 다른 대사 산물.
그런 다음 우리는 아미노산 대사의 변화가 장내 미생물 구성의 변화와 관련이 있는지 분석했습니다. 우리는 WT, Mod 및 CDPS 그룹의 7가지 다른 대사산물(크레아티닌, 발린, L-(-)-메티오닌, o-톨루이딘, N-에틸아닐린, 요산 및 프롤린)이 ABX, Cy, 및 WT 및 CDPS 그룹과 비교한 Mod 그룹. 또한 ABX와 Cy 그룹 사이에는 의미가 없습니다(그림 8C). 마지막으로, 차등 대사와 다른 노화 관련 질병 사이의 상관 관계를 조사하기 위해. MetaboAnalyst 데이터베이스를 사용하여 이 7가지 차등적으로 발현되는 대사 산물과 인간 질병 간의 상관 관계를 분석한 결과 이러한 대사 산물이 알츠하이머병과 관련이 있음을 발견했습니다(p{8}}.00173; 그림 8D, 8E). 전반적으로, 이러한 데이터는 CDPS가 아미노산 대사를 조절함으로써 D-gal 유도 노화로부터 보호한다는 것을 시사했습니다.


논의
인지 기능의 점진적인 감소는 노화의 특징입니다. 이전 연구에서는 CDPS 치료가 노화 모델 마우스의 학습과 기억을 유의하게 향상시키는 것으로 나타났습니다[30-33]. 이 연구에서 우리는 CDPS 처리가 D-gal-유도 노화 모델 마우스에서 장내 미생물 항상성의 회복을 통해 말초 염증 및 산화 스트레스를 억제함으로써 인지 기능을 개선함을 입증했습니다(그림 9). Cistanche 다당류를 먹인 Sprague-Dawley 쥐는 유익한 장내 세균의 성장이 증가하고 장내 미생물 다양성이 증가하는 것으로 나타났습니다[34]. Cistanche 중성 다당류인 CDA-0.05는 프로바이오틱 유산균의 성장을 향상시켰습니다[22]. 이러한 데이터는 Cistanche 다당류가 장내 세균의 항상성을 개선함을 시사했습니다.
이 연구에서 우리는 CDPS가 Bacteroidetes, Firmicutes 및 Proteobacteria와 같은 장내 세균 속의 풍부함을 조절함으로써 노화 모델 마우스의 인지 능력을 향상시키고 항염 효과가 있음을 입증했습니다. 따라서 CDP는 장내 미생물총의 구성을 재형성함으로써 노화 관련 질병에 치료적으로 유익할 수 있습니다[35, 36]. 또한, 이전 연구에서는 혈청 및 결장의 염증성 사이토카인 수준이 Bacteroidetes, Firmicutes 및 Proteobacteria와 같은 박테리아 속의 상대적 풍부함과 관련이 있음을 보여주었습니다[37, 38]. 또한, 장내 미생물 구성은 순환하는 여러 사이토카인 수준을 조절하여 뇌 기능을 조절합니다[39-43]. 우리의 결과는 CDPS 처리가 Thermoplasmata, Bacilli, 미확인 Actinobacteria, Fusobacteriia 및 미확인 Elusimicrobia의 상대적 존재비를 감소시키고 Methanobacteria, Spirochaetia, Deltaproteobacteria, 미확인{8}}Deferribacteres, Mollicutes, Nitrososphaeria, Erysipelotrichia 및 미확인_남세균.

장내 미생물 대사산물은 혈류로 방출되어 숙주의 건강과 신진대사를 조절합니다[26, 27]. 장내 미생물 대사산물은 장내 미생물 구성의 변화에 따라 변하는 대변 대사산물 구성을 평가함으로써 추정할 수 있다[44]. 최근 연구에 따르면 시트룰린, 프롤린, 아르기닌, 아스파라긴, 페닐알라닌 및 트레오닌의 혈장 수준이 알츠하이머병을 비롯한 신경퇴행성 질환과 관련이 있는 것으로 나타났습니다[45, 46]. 우리의 연구는 크레아티닌, 발린, L-메티오닌, o-톨루이딘, N-에틸아닐린, 요산 및 프롤린의 혈청 수준이 마우스의 D-gal 유도 노화와 관련이 있음을 보여주었습니다.
면역계의 선천성 및 적응성 팔은 장내강 표면에서 숙주-미생물 항상성을 유지하는 데 중요한 역할을 합니다[47]. 장내 미생물총은 또한 사이토카인과 대사산물을 혈류로 방출하여 중추신경계(CNS)와 면역을 조절하는 데 중요한 역할을 합니다[48, 49]. 전염증성 사이토카인은 여러 신경퇴행성 질환에서 중요한 역할을 합니다[50-52]. 예를 들어, 연령 관련 황반 변성(AMD) 및 녹내장은 망막 신경절 세포(RGC)에서 아밀로이드(A)의 세포외 축적 및 과인산화된 타우(p-tau) 및 철의 세포내 침착과 관련이 있습니다. 또한 염증은 녹내장과 관련된 발병기전에 중요한 역할을 합니다[53]. 시각 장애는 알츠하이머병(AD)의 초기 증상이며 인지 저하가 시작되기 전에 나타납니다[54]. 우리의 연구는 CDPS가 장내 미생물의 항상성을 유지함으로써 인지 기능 저하 및 말초 염증으로부터 보호한다는 것을 입증했습니다.
이 연구에는 몇 가지 제한 사항이 있습니다. 첫째, 아미노산 대사와 장내 미생물의 구성 사이의 관계는 잘 알려져 있지 않습니다. 둘째, CDPS의 조성과 분자구조는 알려져 있지 않다. 따라서 장내 미생물총-뇌 신호전달 축을 통해 알츠하이머병을 완화하는 데 있어 CDPS의 조절 역할을 더 탐구하기 위해서는 향후 연구가 필요합니다.
결론적으로, 우리 연구는 CDPS가 장내 미생물의 항상성을 회복시켜 아미노산 불균형, 말초 염증 및 산화 스트레스를 회복시켜 D-gal 유도 노화 모델 마우스의 인지 능력을 향상시킴을 입증했습니다. 이러한 발견은 CDPS가 학습 및 기억 장애가 있는 환자, 특히 장내 세균 불균형과 관련된 환자에게 잠재적인 치료제임을 시사합니다.
재료 및 방법
CDPS의 준비
약 1.{1}} 세척된 Cistanche Deserticola 1kg을 40℃의 오븐에서 자연 건조시킨 후 미분쇄하여 조분말로 만들었다. 분말을 뜨거운 에탄올에서 3시간 동안 추출하였다. 잔류물을 거즈를 통해 여과하여 여액을 제거한 다음 물(8X)로 희석하고 90℃에서 2시간, 1.5시간, 1시간 동안 순차적으로 환류하였다. 각 시점에서 용액을 원심분리하여 상등액을 분리하였다. 적갈색 여과액과 합하였다. 그 다음, 여액을 감압하에 농축하고, 실온으로 냉각시키고, 95% 에탄올(3X)에 천천히 첨가하고, 4℃에서 24시간 동안 방치하였다. 그 후, 용액을 4℃에서 6000 r/min으로 20분간 원심분리하였다. 물추출과 알코올 침전을 3회 반복하여 침전물을 모았다. 침전물을 물에 재구성하고, 단백질을 제거하고, 투석하고, 동결 건조하여 조 Cistanche Deserticola 다당류(CDP)를 얻었다. 다당류 함량은 자외선 분광광도법으로 평가했을 때 90% 이상이었습니다.
동물 그룹화 및 치료
8주령 수컷 Kunming 마우스(SCXK 라이선스 번호2019-0010)를 SPF Biotechnology Co. Ltd(Beijing, China)에서 구입하여 빛과 온도가 조절되는 방에 보관하고 음식과 물을 먹였습니다. 모든 동물 실험은 내몽골 의과 대학의 기관 동물 관리 및 사용 위원회에서 승인한 프로토콜에 따라 수행되었습니다. 실험은 국립보건원(NIH) 실험실 동물 관리 및 사용 지침에 따라 수행되었습니다.
새로운 환경에 적응한 지 1주일 후, 120마리의 마우스를 다음 7개 그룹으로 나누었습니다: (1) 야생형 대조군(WT); 모델 그룹(150 mg/Kg/일 D-gal; Mod); (3) CH: D-gal + 100 mg/kg CDPS; (4) CM: D-gal + 50 mg/kg CDPS; (5) CL: D-gal + 25 mg/kg CDPS; (6) ABX 그룹: 항생제 + D-gal + 50 mg/Kg CDPS; (7) Cy 기: 시클로포스파미드 + D-gal + 50mg/kg CDPS.
모델, ABX, Cy 및 CDPS 그룹의 마우스는 식염수를 피하 주사했습니다.
2개월 동안 매일 150mg/kg D-gal. WT 그룹은 동일한 부피의 식염수를 2개월 동안 피하 주사했습니다. 또한 CDPS 그룹 마우스는 2개월 동안 1{{1{15}}}}0 mg/kg, 5{19}} mg/Kg 또는 25 mg/Kg CDPS를 포함하는 위내 주사를 매일 투여했습니다. . ABX 그룹 마우스는 D-gal 및 CDPS 주사에 추가하여 2개월 동안 0.1 mg/mL 암피실린 및 0.5 mg/mL 스트렙토마이신이 함유된 식수를 받았습니다. D-gal을 투여하기 전에 ABX 그룹에서 마우스는 0.1 mg/mL 암피실린, 0.5 mg/mL 스트렙토마이신 및 0.1 mg/mL 콜리스틴을 함유하는 주사를 7일 동안 받았습니다. Cy 그룹 마우스는 D-gal 및 CDPS의 매일 주사에 추가하여 2개월 동안 격일로(qod) 20 mg/Kg 사이클로포스파미드의 복강내 주사를 받았다.
새로운 물체 인식 테스트
마지막 복용 후 행동 실험을 수행합니다. 객체 인식 테스트에는 친숙화, 교육 및 테스트 단계가 포함되었습니다. 친숙화 단계 동안, 마우스는 2일 동안 10분 동안 빈 시험실에 적응시켰다. 그런 다음, 3일차(훈련일)에는 크기, 모양, 색상이 같은 두 개의 물체(A1, A2)를 챔버의 반대쪽 끝에 배치했습니다. 그런 다음 모든 마우스에게 두 개의 유사한 개체를 탐색할 수 있는 10분이 주어졌습니다. 1-시간(세 번째 날) 및 24-시간(4일째) 학습-테스트 간격 후 유사한 객체(A1 또는 A2) 중 하나가 B 또는 C로 대체되었습니다. 테스트 당일 크기, 색상 및 모양이 다른 물체. 테스트 단계에서 각 마우스를 5분 동안 테스트하고 다음 공식을 사용하여 신규 개체(B 또는 C) 인식의 메모리를 결정하기 위해 우선 지수를 계산했습니다. 우선 지수{11}}객체 B 또는 C에서의 시간/( 물체 B 또는 C에 대한 시간 더하기 물체 A)에 대한 시간×100% .
모리스 물 미로 테스트
Morris 수중 미로 테스트는 깊이 45cm, 직경 90cm의 원형 수영장에서 수행되었습니다. Ruediger S, et al. (2011) [55] 및 Wood RA, et al. (2018) [56]이 여기에 고용되었습니다. 수영장의 수심은 30cm, 수온은 20±1℃였다. 플랫폼은 직경 6cm, 수중 1cm였다. 훈련 및 테스트 시간은 각각 60초였습니다. 훈련을 위해 우리는 연속 5일 동안 매일 숨겨진 플랫폼을 사용하여 각각 60초씩 4번의 시도를 수행했습니다. 60초 동안 마우스가 플랫폼을 발견하지 못하면 플랫폼으로 안내하고 5초 동안 플랫폼에 둡니다. 테스트 단계에서 교육 및 프로브 시험 세션에서 숨겨진 플랫폼에 도달하기까지의 대기 시간, 제거된 플랫폼 위치를 교차하는 횟수, 대상(플랫폼) 사분면에서 보낸 시간을 기록하고 분석했습니다.
ELISA 분석
Shanghai Yi에서 구입한 ELISA 키트를 사용하여 마우스 그룹별로 IL-2(), IL-4, IL{3}} 및 TNF-와 같은 전염증성 사이토카인의 혈청 수준을 분석했습니다. 제조업체의 지침에 따라 Li Biological Technology Co., Ltd.(중국 상하이). 난징 Jiancheng Bioengineering Institute (Nanjing, China)에서 구입한 분석 키트를 사용하여 마우스의 각 그룹의 혈청에서 항산화 효소인 슈퍼옥사이드 디스뮤타제(SOD)의 활성과 지질 과산화 생성물인 말론디알데히드(MDA)의 수준을 분석했습니다. . 뮤린 해마 샘플에서 고급 산화 단백질 제품(AOPP)의 수준은 제조업체의 지침에 따라 Shanghai Yi Li Biological Technology Co. Ltd.(Shanghai, China)의 ELISA 키트를 사용하여 추정되었습니다.
쥐 뇌의 산화 스트레스 추정
100mg 해마 조직을 0.9ml의 얼음으로 식힌 식염수로 균질화하고 균질액을 4℃에서 12000rpm에서 30분 동안 원심분리했습니다. 상등액의 단백질 함량은 BCA 단백질 분석 키트( Beyotime Biotechnology, 상하이, 중국). 지질 과산화(LPO) 및 말론디알데히드(MDA)의 수준, 해마 샘플에서 GSH-Px 및 SOD의 활성은 제조사의 지침에 따라 Nanjing Jiancheng Bioengineering Institute(Nanjing, China)의 키트를 사용하여 비색법으로 분석되었습니다.
장내 미생물 조성
모든 마우스로부터 대변 샘플을 수집하고 즉시 -80도 C에 보관했습니다. 16S rRNA 유전자의 V3 plus V4 영역은 Illumina MiSeq(Beijing Novogene Co. Ltd., Beijing, China)를 사용하여 시퀀싱하고 다음을 사용하여 분석했습니다. 장내 미생물군 프로파일을 결정하기 위한 QIIME 개방형 플랫폼.
혈청 대사 산물의 LC/MS 분석
혈청 샘플을 1:3의 비율로 미리 냉각된 메탄올과 함께 1분 동안 인큐베이션하여 단백질을 침전시켰습니다. 샘플을 4℃에서 15분 동안 12{14}00r/min으로 원심분리했습니다. 상층액을 Thermo Scientific Dionex UltiMate3000 Rapid Resolution Liquid Chromatography 및 QExactive 질량 스펙트럼으로 분석했습니다. 크로마토그래피 조건은 표 1에 나와 있습니다. 분석물은 이동상 A와 B로 0.1% 포름산과 아세토니트릴을 사용하여 XBridge BEH Amid 크로마토그래피 컬럼(2.1 x 100mm; Waters Co., Milford, MA, USA)에서 분리되었습니다. 각기. 유속은 0.4 ml/min, 주입 부피는 5 μl, 컬럼 온도는 25℃로 설정했습니다(표 1). 질량 스펙트럼 신호는 양이온 및 음이온 스캐닝 모드를 사용하여 얻었습니다. 이온 스프레이 전압 및 기타 특정 MS 매개변수는 표 2에 나와 있습니다.
통계 분석
Statistical analysis was performed using the SPSS 13.0 software (SPSS Inc., Chicago, Illinois, USA). The data plots were generated using GraphPad Prism 8.0.1 (GraphPad Software, La Jolla, California, USA). Partial least squares discriminant analysis (OPLS-DA) of SIMCA-P+13.0 (Umetrics, AB, Umeå, Sweden) and Principal Components Analysis (PCA) were used to assess normalized GC-MS spectral data. Variable Influence on Projection (VIP) values were used to identify significant variables with VIP values >1.0 및 피< 0.05.="" these="" significant="" variables="" were="" used="" to="" identify="" the="" spectral="" peaks.="" the="" student's="" t-test="" was="" used="" to="" analyze="" differences="" between="" two="" groups="" of="" data.="" the="" taxonomic="" rank="" differential="" between="" groups="" was="" determined="" using="" student's="" test="" (v3.1.2;="" r="" programming="" language).="" the="" correlation="" between="" genera="" abundance="" and="" mouse="" behavior="" was="" calculated="" using="" spearman="" correlation="" coefficients="" (r="" language).="" p="" <="" 0.05="" was="" considered="" statistically="" significant.="" the="" data="" are="" presented="" as="">

참조
1. Coates SS, Lehnert BE, Sharma S, Kindell SM, Gary RK. 베릴륨은 인간 섬유아세포에서 조기 노화를 유도합니다. J Pharmacol Exp Ther. 2007년; 322:70~79. https://doi.org/10.1124/jpet.106.118018 PMID:17395767
2. Shwe T, Pratayasakul W, Chattipakorn N, Chattipakorn SC. D-갈락토오스로 인한 뇌 노화의 역할과 치료적 중재에 사용되는 잠재력. 특급 게론톨. 2018년; 101:13~36. https://doi.org/10.1016/j.exger.2017.10.029 PMID:29129736
3. Ho SC, Liu JH, Wu RY. D-갈락토오스에 의한 쥐의 노화 모방 효과 확립. 생물노인학. 2003년; 4:15~18. https://doi.org/10.1023/a:1022417102206 PMID:12652185
4.Song X, Bao M, Li D, Li YM. D-갈락토스 유도 마우스 노화 모델의 고급 당화. 기계 노화 Dev. 1999년; 108:239~51.
https://doi.org/10.1016/s0047-6374(99)00022-6 PMID:10405984
5. Yamauchi T, Oi A, Kosakamoto H, Akuzawa-Tokita Y, Murakami T, Mori H, Miura M, Obata F. 장내 세균종은 초파리의 노화 동안 숙주 퓨린 대사 산물에 뚜렷하게 영향을 미칩니다. 아이사이언스. 2020년; 23:101477. https://doi.org/10.1016/j.isci.2020.101477 PMID:32916085
6. 중국약전위원회, 중화인민공화국 약전 Ver. 2015. China Medical Science and Technology Press, 베이징, 중국. 2015.
7. Wang N, Ji S, Zhang H, Mei S, Qiao L, Jin X.허바 시스탄체스: 노화 방지. 에이징 디. 2017년; 8:740~59. https://doi.org/10.14336/AD.2017.0720 PMID:29344414
8. Fu Z, Fan X, Wang X, Gao X.시스탄체스 허바: 화학, 약리학 및 약동학 속성의 개요. J Ethnopharmacol. 2018년; 219:233~47.
https://doi.org/10.1016/j.jep.2017.10.015 PMID:29054705
9. Zhong C, Liu Z, Zhang X, Pu Y, Yang Z, Bao Y. Ligusticum chuanxiong의 다당류의 물리화학적 특성 및 면역 조절을 통한 항종양 잠재력 분석. 식품 기능. 2021; 12:1719~31. https://doi.org/10.1039/d0fo02978e
PMID:33502414
10.Shi YJ, Zheng HX, Hong ZP, Wang HB, Wang Y, Li MY, Li ZH. 세포 및 제브라피시 기반 생물 검정에서 다양한 Ganoderma lucidum 포자 분말의 항종양 효과. J Integr Med. 2021년; 19:177~84. https://doi.org/10.1016/j.joim.2021.01.004 PMID:33495135
11. Zhang Z, Liu H, Yu B, Tao H, Li J, Wu Z, Liu G, Yuan C, Guo L, Cui B. Lycium barbarum polysaccharide는 내장을 조작하여 고지방식이식 마이크에서 심근 손상을 약화시킵니다. 마이크로바이옴과 대변 대사체. 식품 Res Int. 2020년; 138:109778. https://doi.org/10.1016/j.foodres.2020.109778 PMID:33288164
12. Newgard CB, Sharpless NE. 노화: 노화 및 치료 기회의 분자 동인. 제이클린 인베스트. 2013년; 123:946~50. https://doi.org/10.1172/JCI68833 PMID:23454756
13. Wang H, Dwyer-Lindgren L, Lofgren KT, Rajaratnam JK, Marcus JR, Levin-Rector A, Levitz CE, Lopez AD, Murray CJ. 187개국의 연령별 및 성별별 사망률, 1970-2010: 글로벌 질병 부담 연구 2010에 대한 체계적인 분석. Lancet. 2012년; 380:2071–94.
https://doi.org/10.1016/S0140-6736(12)61719-X PMID:23245603
14. Qabazard B, Stürzenbaum SR. H2S: 수명 연장 및 건강한 노화에 대한 새로운 접근 방식? Handb Exp Pharmacol. 2015년; 230:269–87. https://doi.org/10.1007/978-3-319-18144-8_14 PMID:26162840
15. Walrath T, Dyamenahalli KU, Hulsebus HJ, McCullough RL, Idrovo JP, Boe DM, McMahan RH, Kovacs EJ. 장 면역 및 마이크로바이옴의 연령 관련 변화. J Leukoc Biol. 2020. [인쇄를 앞둔 Epub]. https://doi.org/10.1002/JLB.3RI0620-405RR PMID:33020981
16. Mishra B, Manmode S, Walke G, Chakraborty S, Neralkar M, Hotha S. 클로로바이러스의 과분지형 코어 사당류 모티프의 합성. 조직 Biomol Chem. 2021; 19:1315~28. https://doi.org/10.1039/d0ob02176h PMID:33459320
17. Gao Y, Liu Y, Ma F, Sun M, Song Y, Xu D, Mu G, Tuo Y. Lactobacillus plantarum Y44는 피하 d-갈락토스가 있는 Balb/C 마우스에서 장내 미생물과 결장 장벽 기능을 조절하여 산화 스트레스를 완화합니다. 주입. 식품 기능. 2021; 12:373–86. https://doi.org/10.1039/d0fo02794d
PMID:33325942
18. Francisco ÉC, Franco TT, Wagner R, Jacob-Lopes E. 남조류 재배에서 외인성 탄소원으로서 다양한 탄수화물 평가. 바이오프로세스 바이오시스 엔지니어링 2014년; 37:1497~505. https://doi.org/10.1007/s00449-013-1121-1 PMID:24445336
19. Uhde A, Yun JW, Maeda T, Clermont L, Matano C, Krämer R, Wendisch VF, Seibold GM, Marin K. 아미노산 생성 Corynebacterium glutamicum의 탄소원으로서의 글루코사민. Appl Microbiol Biotechnol. 2013년; 97:1679–87. https://doi.org/10.1007/s00253-012-4313-8 PMID:22854894
1. Ladevèze S, Laville E, Despres J, Mosoni P, Potocki-Véronèse G. Mannoside 인식 및 박테리아에 의한 분해. Biol Rev Camb Philos Soc. 2017년; 92:1969–90.
https://doi.org/10.1111/brv.12316 PMID:27995767
2. 리몰리 DH, 존스 CJ, 워즈니악 DJ. 생물막 형성 및 기능에서의 세균성 세포외 다당류. 미생물 스펙트럼 2015년; 3:10.1128. https://doi.org/10.1128/microbiolspec.MB{7}} PMID:26185074
3. Zeng H, Huang L, Zhou L, Wang P, Chen X, Ding K. Cistanche Deserticola Y에서 분리된 갈락토글루칸.
씨.마. 및 장내 세균 균주에 대한 생체 활성. 탄수화물 폴리머. 2019년; 223:115038. https://doi.org/10.1016/j.carbpol.2019.115038 PMID:31426978
4. Subramanian V, Rodemoyer B, Shastri V, Rasmussen LJ, Desler C, Schmidt KH. 블룸 증후군 DNA 헬리카제 결핍은 산화 스트레스 및 미토콘드리아 네트워크 변화와 관련이 있습니다. 과학 대표 2021; 11:2157.
https://doi.org/10.1038/s41598-021-81075-0 PMID:33495511
5. Mashima K, Oh I, Fujiwara K, Izawa J, Takayama N, Nakano H, Kawasaki Y, Minakata D, Yamasaki R, Morita K, Ashizawa M, Yamamoto C, Hatano K, et al. 쥐 모델에서 이식편 대 숙주 질환 및 이식편 대 백혈병에 대한 알렘투주맙, 항흉선세포 글로불린 및 이식 후 사이클로포스파미드의 비교. 플로스원. 2021년; 16:e0245232. https://doi.org/10.1371/journal.pone.0245232 PMID:33428661
6. Rooks MG, Garrett WS. 장내 미생물, 대사 산물 및 숙주 면역. Nat Rev Immunol. 2016년; 16:341~52. https://doi.org/10.1038/nri.2016.42 PMID:27231050
7. Zierer J, Jackson MA, Kastenmüller G, Mangino M, Long T, Telenti A, Mohney RP, Small KS, Bell JT, Steves CJ, Valdes AM, Spector TD, Menni C. 장내 마이크로바이옴. 냇 제넷. 2018년; 50:790-95. https://doi.org/10.1038/s41588-018-0135-7 PMID:29808030
8. Wilmanski T, Rappaport N, Earls JC, Magis AT, Manor O, Lovejoy J, Omenn GS, Hood L, Gibbons SM, Price ND. 혈액 대사체는 인간의 장내 미생물군집 다양성을 예측합니다. Nat Biotechnol. 2019년; 37:1217~28.
https://doi.org/10.1038/s41587-019-0233-9 PMID:31477923
9. Chagoyen M, Pazos F. MBRole: 대사체 데이터의 농축 분석. 생물정보학. 2011년; 27:730~31. https://doi.org/10.1093/bioinformatics/btr001 PMID:21208985
10. Xia J, Wishart DS. 포괄적인 대사체학 데이터 분석을 위해 MetaboAnalyst 3.0 사용. Curr Protoc 생물정보학. 2016년; 55:14.10. https://doi.org/10.1002/cpbi.11 PMID:27603023
11. Miao X, Zhang H, Wu Y, Liu D, Zhang X, Li G. D-갈락토스 유도 PC12 신경 세포 손상에 대한 Cistanche verbascum 배당체의 보호 효과. 중국 약학 저널. 2017년; 52:2071~78.
12. Wu Y, Zhang H, Bu R, Ma H, Su M, Li G. D-갈락토오스에 의해 유도된 급성 노화 모델에 대한 Cistanche Deserticola 다당류의 보호 효과에 대한 연구. 중국 Pharmacol 게시판. 2017년; 33:927~33.
13. Yin R, Li G, Yu T, Ma H, Ma T, Guo M. 스코폴라민 유발 학습 및 기억 장애가 있는 마우스의 시냅스 가소성에 대한 Cistanche cistanche 다당류의 보호 효과. 중국 Pharmacol 게시판. 2014년; 30:801–07.
14. Ma H, Yin R, Guo M, Bao Y, Cui Z, Li G. Cistanche cistanche 다당류가 D-갈락토스 유도 노화 모델 마우스에서 CREB의 발현에 미치는 영향. 실험 전자 전통 중국 의학의 중국 저널. 2014년; 20:137~41.
15. Fu Z, Han L, Zhang P, Mao H, Zhang H, Wang Y, Gao X, Liu E. Cistanche 다당류는 생체 내에서 에키나코사이드 흡수를 향상시키고 장내 미생물에 영향을 미칩니다. Int J Biol Macromol. 2020년; 149:732 40.
https://doi.org/10.1016/j.ijbiomac.2020.01.216 PMID:31987946
16. Bajaj JS, Gillevet PM, Patel NR, Ahluwalia V, Ridlon JM, Kettenmann B, Schubert CM, Sikaroodi M, Heuman DM, Crossey MM, Bell DE, Hylemon PB, Fatouros PP, Taylor-Robinson SD. 간성 뇌병증에서 락툴로스 금단 현상에 대한 종단 시스템 생물학 분석. 메타브 브레인 디스. 2012년; 27:205~15. https://doi.org/10.1007/s11011-012-9303-0 PMID:22527995
17. Qian Y, Yang X, Xu S, Wu C, Song Y, Qin N, Chen SD, Xiao Q. 중국 파킨슨병 환자의 분변 미생물군 변화. 뇌 행동 면역. 2018년; 70:194~202. https://doi.org/10.1016/j.bbi.2018.02.016 PMID:29501802
18. Sjögren YM, Tomicic S, Lundberg A, Böttcher MF, Björkstén B, Sverremark-Ekström E, Jenmalm MC. 어린 시절 점막 및 전신 면역 반응의 성숙에 대한 초기 장내 미생물총의 영향. Clin Exp 알레르기. 2009년; 39:1842~51. https://doi.org/10.1111/j.1365-2222.2009.03326.x PMID:19735274
19. Uhde A, Yun JW, Maeda T, Clermont L, Matano C, Krämer R, Wendisch VF, Seibold GM, Marin K. 아미노산 생성 Corynebacterium glutamicum의 탄소원으로서의 글루코사민. Appl Microbiol Biotechnol. 2013년; 97:1679–87. https://doi.org/10.1007/s00253-012-4313-8 PMID:22854894
20.Ladevèze S, Laville E, Despres J, Mosoni P, Potocki-Véronèse G. Mannoside 인식 및 박테리아에 의한 분해. Biol Rev Camb Philos Soc. 2017년; 92:1969–90. https://doi.org/10.1111/brv.12316 PMID:27995767
21.리몰리 DH, 존스 CJ, 워즈니악 DJ. 생물막 형성 및 기능에서의 세균성 세포외 다당류. 미생물 스펙트럼 2015년; 3:10.1128. https://doi.org/10.1128/microbiolspec.MB{7}} PMID:26185074
22. Zeng H, Huang L, Zhou L, Wang P, Chen X, Ding K. Cistanche Deserticola YC Ma에서 분리된 갈락토글루칸. 및 장내 세균 균주에 대한 생체 활성. 탄수화물 폴리머. 2019년; 223:115038. https://doi.org/10.1016/j.carbpol.2019.115038 PMID:31426978
23.Subramanian V, Rodemoyer B, Shastri V, Rasmussen LJ, Desler C, Schmidt KH. 블룸 증후군 DNA 헬리카제 결핍은 산화 스트레스 및 미토콘드리아 네트워크 변화와 관련이 있습니다. 과학 대표 2021; 11:2157.
https://doi.org/10.1038/s41598-021-81075-0 PMID:33495511
24.Mashima K, Oh I, Fujiwara K, Izawa J, Takayama N, Nakano H, Kawasaki Y, Minakata D, Yamasaki R, Morita K, Ashizawa M, Yamamoto C, Hatano K, et al. 쥐 모델에서 이식편 대 숙주 질환 및 이식편 대 백혈병에 대한 알렘투주맙, 항흉선세포 글로불린 및 이식 후 사이클로포스파미드의 비교. 플로스원. 2021년; 16:e0245232. https://doi.org/10.1371/journal.pone.0245232 PMID:33428661
25. Rooks MG, Garrett WS. 장내 미생물, 대사 산물 및 숙주 면역. Nat Rev Immunol. 2016년; 16:341~52. https://doi.org/10.1038/nri.2016.42 PMID:27231050
26.Zierer J, Jackson MA, Kastenmüller G, Mangino M, Long T, Telenti A, Mohney RP, Small KS, Bell JT, Steves CJ, Valdes AM, Spector TD, Menni C. 장내 마이크로바이옴. 냇 제넷. 2018년; 50:790-95. https://doi.org/10.1038/s41588-018-0135-7 PMID:29808030
27. Wilmanski T, Rappaport N, Earls JC, Magis AT, Manor O, Lovejoy J, Omenn GS, Hood L, Gibbons SM, Price ND. 혈액 대사체는 인간의 장내 미생물군집 다양성을 예측합니다. Nat Biotechnol. 2019년; 37:1217~28.
https://doi.org/10.1038/s41587-019-0233-9 PMID:31477923
28. Chagoyen M, Pazos F. MBRole: 대사체 데이터의 농축 분석. 생물정보학. 2011년; 27:730~31. https://doi.org/10.1093/bioinformatics/btr001 PMID:21208985
29. Xia J, Wishart DS. 포괄적인 대사체학 데이터 분석을 위해 MetaboAnalyst 3.0 사용. Curr Protoc 생물정보학. 2016년; 55:14.10. https://doi.org/10.1002/cpbi.11 PMID:27603023
30. Miao X, Zhang H, Wu Y, Liu D, Zhang X, Li G. D-갈락토스 유도 PC12 신경 세포 손상에 대한 Cistanche verbascum 배당체의 보호 효과. 중국 약학 저널. 2017년; 52:2071~78.
31. Wu Y, Zhang H, Bu R, Ma H, Su M, Li G. D-갈락토스에 의해 유도된 급성 노화 모델에 대한 Cistanche Deserticola 다당류의 보호 효과에 대한 연구. 중국 Pharmacol 게시판. 2017년; 33:927~33.
32. Yin R, Li G, Yu T, Ma H, Ma T, Guo M. 스코폴라민 유발 학습 및 기억 장애가 있는 마우스의 시냅스 가소성에 대한 Cistanche cistanche 다당류의 보호 효과. 중국 Pharmacol 게시판. 2014년; 30:801–07.
33. Ma H, Yin R, Guo M, Bao Y, Cui Z, Li G. Cistanche cistanche 다당류가 D-갈락토스 유도 노화 모델 마우스에서 CREB의 발현에 미치는 영향. 실험 전자 전통 중국 의학의 중국 저널. 2014년; 20:137~41.
34. Fu Z, Han L, Zhang P, Mao H, Zhang H, Wang Y, Gao X, Liu E. Cistanche 다당류는 생체 내에서 에키나코사이드 흡수를 향상시키고 장내 미생물에 영향을 미칩니다. Int J Biol Macromol. 2020년; 149:732~40. https://doi.org/10.1016/j.ijbiomac.2020.01.216 PMID:31987946
35.Bajaj JS, Gillevet PM, Patel NR, Ahluwalia V, Ridlon JM, Kettenmann B, Schubert CM, Sikaroodi M, Heuman DM, Crossey MM, Bell DE, Hylemon PB, Fatouros PP, Taylor-Robinson SD. 간성 뇌병증에서 락툴로스 금단 현상에 대한 종단 시스템 생물학 분석. 메타브 브레인 디스. 2012년; 27:205~15. https://doi.org/10.1007/s11011-012-9303-0 PMID:22527995
36. Qian Y, Yang X, Xu S, Wu C, Song Y, Qin N, Chen SD, Xiao Q. 중국 파킨슨병 환자의 대변 미생물군 변화. 뇌 행동 면역. 2018년; 70:194~202. https://doi.org/10.1016/j.bbi.2018.02.016 PMID:29501802
37.Sjögren YM, Tomicic S, Lundberg A, Böttcher MF, Björkstén B, Sverremark-Ekström E, Jenmalm MC. 어린 시절 점막 및 전신 면역 반응의 성숙에 대한 초기 장내 미생물총의 영향. Clin Exp 알레르기. 2009년; 39:1842~51. https://doi.org/10.1111/j.1365-2222.2009.03326.x PMID:19735274
38.Rangel I, Ganda Mall JP, Willén R, Sjöberg F, Hultgren-Hörnquist E. 대장염의 정도는 G i{2}}결핍 마우스의 결장 및 맹장의 미생물 구성 및 사이토카인 반응과 상관관계가 있습니다. FEMS Microbiol Ecol. 2016년; 92:fiw098. https://doi.org/10.1093/femsec/fiw098 PMID:27162181
39. Larbi A, Pawelec G, Witkowski JM, Schipper HM, Derhovanessian E, Goldeck D, Fulop T. 경증 알츠하이머병에서 순환하는 CD4의 극적인 이동이지만 CD8 T 세포 하위 집합은 아닙니다. J 알츠하이머 Dis. 2009년; 17:91~103.
https://doi.org/10.3233/JAD-2009-1015 PMID:19494434
40.West CE, Rydén P, Lundin D, Engstrand L, Tulic MK, Prescott SL. IgE 관련 습진에서 장내 미생물군유전체 및 선천적 면역 반응 패턴. Clin Exp 알레르기. 2015년; 45:1419~29. https://doi.org/10.1111/cea.12566 PMID:25944283
41. Wong ML, Inserra A, Lewis MD, Mastronardi CA, Leong L, Choo J, Kentish S, Xie P, Morrison M, Wesselingh SL, Rogers GB, Licinio J. Inflammasome 신호는 불안 및 우울과 유사한 행동과 장에 영향을 미칩니다. 마이크로바이옴 구성. 몰 정신과. 2016년; 21:797–805.
https://doi.org/10.1038/mp.2016.46 PMID:27090302
42. Abildgaard A, Elfving B, Hokland M, Wegener G, Lund S. Probiotic 치료는식이 요법과 관계없이 쥐의 우울한 행동을 줄입니다. 정신신경내분비학. 2017년; 79:40~48. https://doi.org/10.1016/j.psyneuen.2017.02.014 PMID:28259042
43. Bercik P, Verdu EF, Foster JA, Macri J, Potter M, Huang X, Malinowski P, Jackson W, Blennerhassett P, Neufeld KA, Lu J, Khan WI, Corthesy-Theulaz I, et al. 만성 위장 염증은 불안과 유사한 행동을 유도하고 생쥐의 중추 신경계 생화학을 변경합니다. 위장병학. 2010년; 139:2102–2112.e1. https://doi.org/10.1053/j.gastro.2010.06.063 PMID:20600016
44.Yoshimoto S, Mitsuyama E, Yoshida K, Odamaki T, Xiao JZ. 노인 유형의 장내 미생물총이 있는 대상에서 잠재적으로 노화 관련 질병을 촉진하는 풍부한 대사 산물. 장내 미생물. 2021년; 13:1~11. https://doi.org/10.1080/19490976.2020.1865705 PMID:33430687
45. Chatterjee P, Chung YJ, Bhatnagar A, Goozee K, Wu Y, McKay M, Martins IJ, Lim WL, Pedrini S, Tegg M, Villemagne VL, Asih PR, Dave P, et al. 인지적으로 정상적인 노인에서 신경변성의 바이오마커 증거와 관련된 혈장 대사 산물. J Neurochem. 2020. [인쇄를 앞둔 Epub]. https://doi.org/10.1111/jnc.15128 PMID:32679614
46. Mahajan UV, Varma VR, Griswold ME, Blackshear CT, An Y, Oommen AM, Varma S, Troncoso JC, Pletnikova O, O'Brien R, Hohman TJ, Legido-Quigley C, Thaambisetty M. 다중 대사 네트워크의 조절 장애 알츠하이머병의 뇌 트랜스메틸화 및 폴리아민 경로 관련: 표적 대사체학 및 전사체 연구. 플로스메드. 2020년; 17:e1003012. https://doi.org/10.1371/journal.pmed.1003012 PMID:31978055
47. Duerkop BA, Vaishnava S, Hooper LV. 장 점막 표면의 미생물에 대한 면역 반응. 면역. 2009년; 31:368~76. https://doi.org/10.1016/j.immuni.2009.08.009 PMID:19766080
48. Forsythe P, Bienenstock J. 공생 및 프로바이오틱 박테리아에 의한 면역 조절. 이뮤놀 인베스트. 2010년; 39:429~48. https://doi.org/10.3109/08820131003667978 PMID:20450286
49. 스턴버그 EM. 타고난 면역의 신경 조절: 병원체에 대한 조정된 비특이적 숙주 반응. Nat Rev Immunol. 2006년; 6:318~28. https://doi.org/10.1038/nri1810 PMID:16557263
50.Colonna M, Butovsky O. 건강 및 신경 퇴행 중 중추 신경계의 Microglia 기능. Annu Rev Immunol. 2017년; 35:441~68. https://doi.org/10.1146/annurev-immunol-051116- 052358 PMID:28226226
51. El Khoury J. Neurodegeneration과 신경 면역 체계. 냇 메드. 2010년; 16:1369~70. https://doi.org/10.1038/nm1210-1369 PMID:21135838
52. Fu W, Vukojevic V, Patel A, Soudy R, MacTavish D, Westaway D, Kaur K, Goncharuk V, Jhamandas J. 베타 아밀로이드(A) 유도 염증 매개에서 미세아교 아밀린 수용체의 역할. J 신경염증. 2017년; 14:199. https://doi.org/10.1186/s12974-017-0972-9 PMID:28985759
53. Yang X, Zeng Q, Tezel G. 실험 녹내장에서 망막 신경절 세포와 성상교세포에서 고유한 caspase{1}} 기능의 조절. 뉴로바이올 디스. 2021년; 150:105258. https://doi.org/10.1016/j.nbd.2021.105258 PMID:33434617
54. Ashok A, Singh N, Chaudhary S, Bellamkonda V, Kritikos AE, Wise AS, Rana N, 맥도날드 D, Ayyagari R. 망막 변성 및 알츠하이머병: 진화하는 연결고리. Int J Mol Sci. 2020년; 21:7290. https://doi.org/10.3390/ijms21197290 PMID:33023198
55. Ruediger S, Vittori C, Bednarek E, Genoud C, Strata P, Sacchetti B, Caroni P. 메모리 정밀도에 필요한 학습 관련 피드포워드 억제 연결 성장. 자연. 2011년; 473:514–18. https://doi.org/10.1038/nature09946 PMID:21532590
56. Wood RA, Bauza M, Krupic J, Burton S, Delekate A, Chan D, O'Keefe J. 벌집 모양의 미로는 해마 종속 공간 탐색을 연구하기 위한 새로운 테스트를 제공합니다. 자연. 2018년; 554:102–05. https://doi.org/10.1038/nature25433


