Cyclopentanone은 B16F10 흑색종에서 항멜라닌 생성 및 항주름 활성을 나타냅니다
Mar 26, 2022
연락하다:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
정희진 1, 이아경 1,2, 박여진 1,2, 이상권 1,2, 강동완 1,2, 정영숙 1,2, 정해영 1,2, 문형룡 1, 2,*
추상적인:자외선(UV) 방사선 노출은 외부 피부 노화의 주요 원인이며, 이는 피부 과다 색소 침착 및 주름을 유발합니다. 이 연구에서 우리는 B16F10 흑색종에 대한 (2E,5E)-2,5-비스(3-히드록시{5}}메톡시벤질리덴)시클로펜타논(BHCP)의 미백 효과와 그 항염증 효과를 조사했습니다. Hs27 섬유아세포의 주름 활성 BHCP는 1.10μM 및 8.18μM 포르미코페놀레이트(L-티로신) 및 디페놀라제(L-DOPA)의 50% 억제 농도(IC50) 값으로 티로시나제를 강력하게 억제하는 것으로 밝혀졌으며 효소 동역학 연구는 BHCP가 경쟁형 티로시나제 억제제인 것으로 밝혀졌습니다. . 또한, BHCP는 멜라닌 함량과 세포성 티로시나제 활성을 유의하게 억제하고 소안구 관련 전사 인자(MITF), cAMP 반응 요소 결합(CREB) 단백질의 인산화된 수준 및 멜라닌 세포 자극 호르몬(-MSH) 유도 티로시나제 수준을 하향 조절했습니다. B16F10 흑색종 세포. 또한, BHCP는 Hs27 섬유아세포에서 p65의 인산화 및 기질 금속단백분해효소(MMP-1, MMP-9, MMP-12 및 MMP{31}})의 발현을 억제합니다. 따라서 우리의 결과는 BHCP가 과다색소침착 및 주름과 관련된 질병에 대한 치료제 개발을 위한 좋은 후보가 될 수 있음을 보여줍니다.
키워드: (2E,5E)-2,5-비스(3-하이드록시-4-메톡시벤질리덴)사이클로펜타논(BHCP); 티로시나제 억제제;항멜라닌 생성; 주름 방지

시스탄체는주름 방지.
1. 소개
피부 노화는 내적 요인과 외적 요인이 모두 관여하여 피부의 기능적, 미적 변화를 일으키는 복잡하고 점진적인 과정입니다[1]. 외인성 피부 노화는 자외선(UV), 스트레스, 흡연과 같은 환경적 요인에 의해 발생합니다. 그러나 주로 태양의 자외선에 반복적으로 노출되어 발생하며 이를 광노화라고 합니다. 피부 광노화는 거칠고 깊은 주름, 두께, 거칠기, 색소 침착 및 조직학적 변화를 특징으로 한다[2-4].
폴리페놀 산화효소(polyphenol oxidase)라고도 알려진 티로시나아제(EC 1.14.18.1)는 멜라닌 합성에 관여하는 다기능 구리 함유 효소 중 하나이며 자연계에서 널리 발견됩니다[5]. 티로시나아제는 일반적으로 대다수의 미생물, 식물, 그리고 동물. 식물에서 티로시나아제는 모노페놀을 디페놀로 산화(미코페놀레이트 활성)하여 작용하고 o-디페놀을 o-퀴논으로 산화(디페놀라제 활성)한 후 퀴논을 암갈색 안료로 산화시키는 데 관여합니다[6].
멜라닌 생성은 L-티로신이 3,{2}}디히드록시페닐알라닌(L-DOPA)으로 변환되는 과정이며, 여기서 L-DOPA는 DOPA 퀴닌으로 전환됩니다[7]. 따라서 tyrosinase는 멜라닌 세포에서 멜라닌 생성에 중요한 역할을 하며, tyrosinase의 억제는 색소침착 장애의 개선과 미백제의 개발을 위한 매력적인 표적이다[8,9]. 멜라닌 합성은 UV 및 이소부틸메틸크산틴(IBMX) 및 알파-멜라닌 세포 자극 호르몬(-MSH)을 포함한 화학 물질과 같은 여러 자극에 의해 유도됩니다. -MSH는 수용체 멜라노코르틴 1 수용체(MC1R)에 결합하여 세포질 순환 AMP(cAMP) 수준을 증가시킵니다. 증가된 cAMP 수준은 cAMP 반응 요소 결합 단백질(CREB)의 인산화를 통해 소안구증 관련 전사 인자(MITF)의 발현을 유도하는 단백질 키나제 A(PKA)를 활성화합니다. MITF는 tyrosinase, tyrosinase-related protein(TRP){18}}, TRP{19}}의 발현을 유도하여 최종적으로 멜라닌 합성을 증가시킵니다[10]. MITF는 멜라닌 생성의 핵심 전사 인자로 간주됩니다. 따라서 멜라닌 생성을 억제하기 위해 MITF의 발현을 조절하기 위한 많은 연구가 수행되었다[11].
주름 형성은 피부 세포외기질의 분해와 밀접한 관련이 있는 것으로 알려져 있으며, 자외선은 핵인자-κB(NF-κB)를 활성화시켜 콜라겐 단편화 및 MMP(matrix metalloproteinase) 생성을 증가시킨다[2]. MMP는 피부에서 세포외 기질 구조의 리모델링에 중요한 아연 의존성 엔도펩티다아제이다. 따라서 UV에 의해 유발된 MMP에 의한 콜라겐과 기질의 과도한 분해는 광손상 피부의 특징이며, MMP는 피부 염증뿐만 아니라 UV에 의한 광노화의 주요 표지자로 사용된다[12].
커큐민 유사 디아릴헵타노이드 골격 유도체는 항산화제, 보고된 항암제, 활성을 포함하고 있습니다. (2E,5E)-2,5-비스(3-히드록시{6}}메톡시벤질리덴)시클로펜타논을 포함한 스캐폴드 (BHCP) (그림 1),광범위한 항염증, 항멜라닌 생성, 특히 Leow et al. [19] Wnt/-cateninsignaling 경로의 조절을 통해 인간 골육종에 대한 보호 효과에 기여할 수 있는 생체 활성 및 anti-tyrosinase [13-18]dibenzylidene-cyclopentanone 2014에서 보고되었습니다. 그러나 BHCP의 멜라닌 생성 방지 및 주름 방지 효과는 아직 밝혀지지 않았으며 BHCP 활성의 기본 분자 메커니즘은 아직 명확하게 확립되지 않았습니다.

그림 1. (2E,5E)-비스(3-하이드록시-4-메톡시벤질리덴)사이클로펜타논(BHCP)의 구조.
현재 연구에서 우리는 BHCP의 항 멜라닌 생성 및 항 주름 잠재력을 조사하고, 특히 멜라닌 함량 및 세포 티로시나아제 활성과 관련하여 관련된 메커니즘을 확인하고자 했으며, 이는 티로시나아제 억제 분석 및 효소 동역학 분석을 사용하여 탐구되었습니다. 또한, 우리는 BHCP가 -MSH-유도 B16F10 마우스 흑색종 세포에서 CREB/MITF/티로시나제의 하향 조절 및 UV-유도 Hs27 인간 섬유아세포에서 p65의 인산화 및 MMP 발현 억제와 관련된 멜라닌 생성 및 주름에 억제 효과를 발휘함을 입증했습니다.

드래곤 허브 시스탄체
2. 결과 및 논의
2.1. (2E,5E)-2,5-비스(3-하이드록시-4-메톡시벤질리덴)사이클로펜타논(BHCP)의 합성
{{0}}히드록시-4-메톡시벤즈알데히드(100 mg, 0.66 mmol, 이소바닐린) 및 시클로펜타논(0.03 mL, 0.33)의 용액 mmol) 1 N HCl-아세트산 용액(0.02 mL)에 녹인 용액을 25℃에서 2시간 동안 교반하였다. 1일 동안 방치한 후, 반응 혼합물을 소량의 메탄올 존재하에 냉수로 처리하고, 여과하고, 냉수로 세척하여 BHCP(65.9 mg)를 56.9% 수율로 생성하였다. BHCP는 다음을 포함하는 분광법으로 확인하였다. 1H 및 13C-NMR 뿐만 아니라 공개된 스펙트럼 데이터 및 TLC(Thin Layer Chromatography) 분석과의 비교[19]. 구조는 그림 1에 나와 있습니다.
BHCP: 황색 무정형 분말(CHCl3); 1H-NMR(500 MHz, DMSO-d6) δ: 9.25(s, 2H, 2×OH), 7.28(s,2H,2×vinylicH), 7.14(d, 2H , J=2.0 Hz, 2 × 2-H), 7.11(dd, 2H, J=8.5, 2.0Hz, 2×6- H),7.01(d, 2H, J{33}}.5Hz, 2 × 5-H), 3.81(s, 6H, 2 × OMe), 3.01(s, 4H, 2 × CH2) ; 13C-NMR(100MHz,DMSO-d6) δ: 195.5, 149.9, 147.2, 136.0, 133.1, 129.1, 124.3, 117.5, 112.8, 56.3, 26.6; ESI-MS: m/z 351(M-H)-.
2.2. 버섯 티로시나제 활성에 대한 BHCP의 억제 효과
표 1에 나타난 바와 같이, BHCP는 1.10 ± 0.12 μMand 8.18 ± 0.44 μM의 IC5{4}} 값으로 티로시나제를 억제한 반면, kojic acid(양성 대조군)는 18.68 ± 1.40 μMand 33.89의 IC50 값을 가졌습니다. 모노페놀라제 및 디페놀라제 각각에 대한 μM. 티로시나아제의 합성 잠재력 억제제에 대한 이전 연구에서 우리는 분자 모델링 연구를 통해 벤질리덴의 3-하이드록시 및 4-메톡시 그룹이 티로시나아제 활성 부위에 대한 큰 결합 경향을 갖는 메커니즘을 발견했습니다[20]. 이 연구 결과로부터, 그것의 작용기(3-hydroxy 및 4-methoxy groups)가 tyrosinase 억제 활성의 유의한 증가와 관련이 있음을 보여주었습니다.

표 1. BHCP의 Tyrosinase 억제 활성 및 효소 동역학 분석.
또한, BHCP에 의한 티로시나제 억제를 담당하는 메커니즘은 본 연구에서 효소 동역학 분석에 의해 조사되었습니다(표 1 및 그림 2). Lineweaver-Burk 플롯은 동역학 연구에서 얻은 데이터를 사용하여 그리고 Dixon 플롯에서 억제 상수(Ki)를 얻었습니다. Lineweaver-Burk 이중 역수 플롯은 경쟁 유형 억제를 나타냅니다. 그림 2a-c에서 볼 수 있듯이 BHCP는 L-티로신과 L-DOPA의 경쟁 억제제로 작용했습니다. 또한 Dixon 플롯의 x축에 대한 절편은 일반적으로 효소-억제제 복합체[21,22]에 대한 효소 억제 상수(Ki)의 유형을 결정하는 데 사용되며, 여기서 x축 값은 -Ki 값을 나타냅니다. 그림 2b-d에 도시된 바와 같이, BHCP의 Ki 값은 L-티로신 및 L-DOPA에 대한 기질로서 각각 1.7μM 및 10.5μM이었습니다. Ki 값은 효소-억제제 복합체를 형성하는 데 필요한 농도를 나타내므로 Ki 값이 낮을수록 tyrosinase에 대한 억제가 더 효과적임을 나타냅니다.
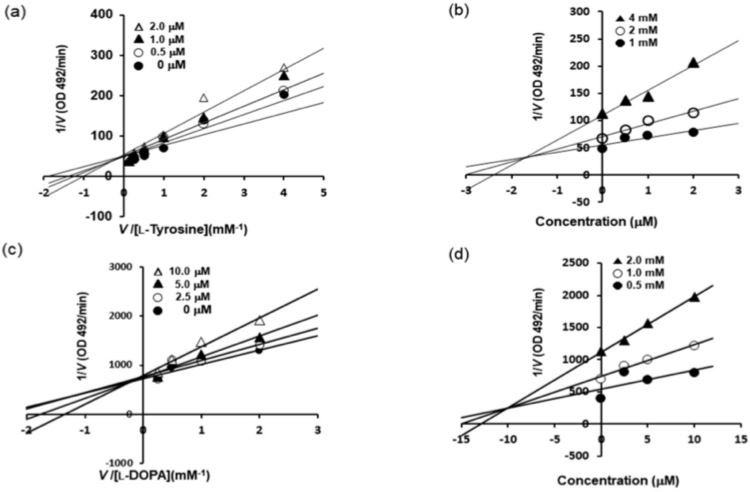
그림 2. BHCP에 의한 티로시나제 효소 억제에 대한 Lineweaver-Burk(a,c) 및 Dixon(b,d) 플롯.
2.3. B16F10 흑색종 및 Hs27 섬유아세포의 세포 생존력에 대한 BHCP의 효과
BHCP가 항 멜라닌 생성 및 항주름 활성을 나타내는지 여부를 결정하기 전에, 우리는 BHCP의 농도를 다른 시간 간격으로 처리하여 B16F10 세포 및 Hs27 세포에 대한 BHCP의 세포 독성을 조사하고 세포 생존율을 EZ-Cytox 분석으로 측정했습니다. 도 3a,b에 나타낸 바와 같이, 48시간 동안 최대 10μM의 BHCP는 B16F10 세포 또는 Hs27 세포의 생존을 감소시키지 않았다. 그 후, BHCP의 항멜라닌 생성 및 항주름 활성에 대한 추가 시험관 내 연구가 1, 5 및 10μM으로 수행되었습니다.

그림 3.B16F10 흑색종에 대한 BHCP의 세포 생존력(a) 및 Hs27 섬유아세포(b).
2.4. B16F10 흑색종 세포에서 멜라닌 함량 및 세포성 티로시나제 활성에 대한 BHCP의 억제
BHCP가 -MSH-유도된 B16F10 세포의 멜라닌 함량에 대한 억제 가능성을 발휘하는지 여부를 결정하기 위해, 세포를 표시된 다른 농도(1, 5 및 10μM)의 BHCP 또는 코직산(5mM)으로 24시간 동안 전처리한 다음 자극했습니다. 48시간 동안 -MSH와 함께. 도 4a에 나타난 바와 같이 -MSH 존재하에서 BHCP를 처리한 세포의 멜라닌 함량은 농도 의존적으로 감소하여 1μM에서 113%, 5μM에서 106%, 10μM에서 102%를 나타내었다. -MSH만 처리한 대조군(186%). 흥미롭게도 BHCP(1μM)는 코직산(5mM)보다 멜라닌 함량을 더 강력하게 억제했습니다. 또한, B16F10 세포에 대한 BHCP의 억제 효과를 측정하기 위해 세포성 티로시나제 활성 분석을 수행하였다. 그림 4b에서 볼 수 있듯이, BHCP는 -MSH만 처리한 대조군과 비교하여 1μM에서 120%, 5μM에서 116%, 10μM에서 105%까지 티로시나제 활성으로 농도 의존적으로 감소했습니다(181 퍼센트 ). BHCP의 억제 효과는 코직산의 억제 효과보다 훨씬 더 강력했습니다. 1μM에서 BHCP의 억제는 5mM에서 코직산(131%)의 억제보다 우수했습니다. 이러한 결과는 BHCP가 B16F10 멜라닌 세포에서 멜라닌 생합성 및 세포내 티로시나아제 합성을 억제하여 미백 효과가 있음을 시사한다.

그림 4. B16F10 흑색종 세포에 대한 BHCP의 멜라닌 함량(a) 및 세포성 티로시나아제 활성(b)의 억제.
2.5. B16F10 세포에서 MITF/Tyrosinase 및 인산화된 CREB의 발현에 대한 BHCP의 효과
특정 전사 인자인 MITF는 멜라닌 생합성의 속도 제한 단계인 TRP-1 및 TRP-2를 촉매하는 티로시나제를 비롯한 멜라닌 생성 유전자를 효과적으로 활성화하는 데 중추적인 역할을 합니다. MITF의 발현은 CREB의 인산화에 의해 증가된다[23]. CREB는 중요한 MITF 프로모터이며[24,25], 멜라닌 세포에서 CREB의 인산화는 멜라닌 세포에서 CREB(c-AMP response element-binding protein)에 결합하여 MITF 발현을 증가시킨다[26]. B16F10 세포에 대한 BHCP의 항멜라닌 생성 효과를 담당하는 분자 경로를 설명하기 위해 우리는 웨스턴 블롯 분석을 통해 멜라닌 생성에 중요한 역할을 하는 CREB 및 MITF를 포함한 주요 분자의 단백질 수준을 조사했습니다. 세포를 BHCP 또는 코직산으로 처리한 다음 -MSH로 48시간 동안 자극하였다. 측정을 위한 시간 간격은 이전 연구에서 설명한 방법론을 따랐습니다[27]. 도 5에서 보는 바와 같이 -MSH와 함께 티로시나아제와 MITF 수치가 증가했지만 BHCP는 이러한 단백질 수치를 감소시켰다. 더욱이, CREB의 인산화는 BHCP에 의해 유의하게 억제되었다. -MSH에 의해 유도된 CREB 인산화의 조절은 색소침착 조절에 잠재적으로 중요한 것으로 알려져 있다[28]. 이러한 결과는 BHCP의 항 멜라닌 생성 효과가 인산화된 CREB의 하향 조절을 통한 MITF 및 티로시나제의 하향 조절에서 비롯됨을 나타냅니다. 본 연구는 티로시나제 및 멜라닌 생성에 대한 BHCP의 억제 기전의 해명이 매우 중요하며 향후 추가 조사가 필요함을 시사한다. B16F10 흑색종 세포주가 일반적으로 시험관 내 신호 전달 기전을 조사하는 데 더 적합하지만 B16F10 세포주는 설치류 흑색종입니다. 따라서 인간 멜라닌 세포에 대한 추가 연구가 결과를 확인하는 데 필요할 것입니다.

그림 5.CREB, MITF 및 tyrosinasein의 인산화 발현 수준에 대한 BHCP의 효과 -MSH로 자극된 B16F10 흑색종 세포.
2.6. Hs27 세포에서 UV 유도 NF-κB p-p65 활성화에 대한 BHCP의 효과
우리는 다음으로 Hs27 섬유아세포를 사용하여 염증 매개체의 UV 유도 발현에 대한 BHCP의 효과를 조사했습니다. p65(Ser536)의 인산화는 유전자를 transactivate하는 능력에 필수적이라고 이전에 보고되었습니다[29]. 따라서, p-p65(Ser536) 및 p65의 단백질 수준은 웨스턴 블롯팅에 의해 핵 분획에서 조사되었다. 그림 6a, b에 표시된 바와 같이 Hs27세포에서 UV는 핵에서 p-p65(Ser536)의 단백질 수준을 증가시킨 반면 BHCP의 처리는 핵 p-p65(Ser536) 단백질 수준을 감소시켰습니다. 상응하게, p65의 총량은 UV에 의해 세포질에서 감소하고 BHCP에 의해 회복되었습니다(그림 6c,d). p65의 단백질 발현 수준은 UV 유도 후 세포질에서 감소하고 핵에서 증가했지만 BHCP 전처리는 이러한 경향을 용량 의존적으로 역전시켰다. 따라서, 이러한 결과는 BHCP에 의한 p-p65의 억제가 UV에 대한 피부 색소 침착 및 콜라겐 파괴에 대한 보호 효과에 기여할 수 있음을 시사한다.

그림 6. UV 유도 Hs27 인간섬유아세포에서 p-p65(Ser536)의 발현 수준에 대한 BHCP의 효과.
2.7. Hs27 세포에서 MMP의 발현에 대한 BHCP의 효과
MMP는 피부 노화에 중요한 역할을 합니다. UV 조사는 MMP의 발현을 상향 조절하여 피부의 결합 조직을 변경합니다[30,31]. MMP-1는 I형 프로콜라겐에서 합성된 콜라겐의 분해를 가속화하는 콜라겐 분해 효소입니다. MMP-9는 MMP-1에 의해 절단된 콜라겐 섬유를 분해하여 주름 생성과 탄력 손실을 증가시키는 젤라틴 분해 효소입니다. UV 유도에 대한 BHCP의 주름 개선 효과를 확인하기 위해 Western blotting으로 MMP-1 및 MMP{9}} 단백질의 수준을 측정했습니다. 또한 UV로 유도된 세포는 MMP{11}} 수치가 크게 증가했으며, 이는 MMP{12}} 대신 type I 및 III 콜라겐의 분해를 시작합니다. UV로 유도된 Hs27 세포를 1 및 10 μM에서 BHCP로 처리한 후 MMP(MMP1, MMP9, MMP12 및 MMP13)의 증가를 조사했습니다. 그림 7과 같이 UV 유도 후 MMP-1, MMP-9, MMP{25}}, MMP{26}} 발현 수준이 증가하였으나 BHCP 처리는 투여량에서 발현 감소 -의존적 방식. 우리의 결과는 BHCP가 UV 노출에 의해 유도된 MMP의 비정상적인 생성을 감소시켜 주름 형성 예방에 기여할 수 있음을 시사합니다. 이러한 결과는 BHCP가 Hs27섬유아세포에서 MMP 발현을 억제하여 콜라겐 분해를 방지하여 주름 생성을 방지함을 의미한다. 따라서 BHCP는 피부 관련 질병의 예방 및 치료 약물로 사용할 수 있는 가능성을 보여줍니다.
cistanche 줄기 이점
3. 재료 및 방법
3.1. 화학 및 계측
버섯 티로시나아제(EC 1.14.18.1), -MSH, L-티로신, 3,{7}디하이드록시페닐알라닌(L-DOPA), 디메틸 설폭사이드(DMSO) 및 코직산은 Sigma-Aldrich(St. Louis, 미주리주, 미국). 둘베코의 변형된 독수리 배지(DMEM), 소 태아 혈청, 스트렙토마이신 및 암포테리신은 Gibco Life Technologies Inc.(Carlsbad, CA, USA)에서 구입했습니다. MITF,CREB, p-CREB, p-p65(Ser536), p65, 티로시나제, MMP{15}}, MMP{16}}, MMP{17}}, MMP{18}}, TFIIB에 대한 항체 , 및 -액틴은 Santa Cruz Biotechnology(Santa Cruz, CA, USA)에서 구입했습니다. PVDF(Polyvinylidene difluoride) 멤브레인은 Millipore Corporation(Bedford, MA, USA)에서 구입했습니다. 조직 배양용 멸균 플라스틱 도자기는 SPL Labware(서울, 한국)에서 구입했습니다. UV 광원은 Crosslinker 800 시리즈(UVP, CA, USA) 6 램프 장치(8 watts/lamp)에서 제공했습니다. 박막 크로마토그래피 및 실리카겔 60(메시 230–400)은 실리카겔F{27} } Merck Millipore(Darmstadt, Germany)의 사전 코팅된 플레이트. NMR 스펙트럼은 Varian Unity INOVA 400(1H의 경우 400MHz, 13C의 경우 100MHz) 및 Varian Unity AS 500(1H의 경우 500MHz) 기기를 사용하여 기록했습니다. 화학적 이동 값(δ)은 각각의 잔류 용매 또는 중수소화 피크(DMSO의 경우 δH 2.50 및 δC 39.51)를 참조하여 보고됩니다. 저해상도 질량 분석 데이터는 Expression CMS 질량 분석기(Advion, Ithaca, NY, USA)로 얻었다.
3.2. 버섯 티로시나제 억제 분석
버섯 티로시나제 억제 활성은 Jung et al. [23]. 간단히 말해서, 190 μL의 티로시나제 효소(1mM L-티로신 및 L-DOPA 용액을 포함하는 버섯 티로시나제 완충제로 희석된 1000U)를 화합물의 존재 또는 부재(최종 농도 범위 1~20μM, 100% DMSO)를 웰 플레이트의 각 웰에 추가하여 200μL의 최종 부피를 제공합니다. 플레이트를 37℃에서 30분 동안 인큐베이션하였다. 티로시나아제 활성은 마이크로플레이트 리더(TECAN, Salzburg, Austria)를 사용하여 492 nm에서 흡광도를 측정하여 정량화하고 억제율(%)은 다음 식에서 구했습니다.
퍼센트 억제=(Ac − As)/Ac × 100 (1)
여기서 Ac는 대조군의 흡광도이고 As는 샘플의 흡광도입니다. IC50 값은 로그 선형 곡선과 해당 방정식에서 계산되었습니다. 세 가지 결정에 대한 평균 결과가 표시됩니다. 코직산을 양성 대조군으로 사용하였다.
3.3. Tyrosinase 억제의 동역학 분석
운동 메커니즘을 결정하기 위해 두 가지 운동 방법(Lineweaver-Burk 및 Dixon 플롯)이 보완적으로 사용되었습니다[21,22,33]. Lineweaver-Burk 이중 역수 플롯(1/효소 속도(1/V) 대 1/기질 농도(1/[S])의 플롯)의 경우 다양한 농도의 L-티로신(1, 2, 및 4mM) 및 L-DOPA({12}}.5, 1 및 2mM)를 다양한 농도의 BHCP 존재 하에 기질로 사용합니다. BHCP의 농도는 다음과 같았습니다:0, 0.5, 1.{{20}} 및 2.{24}} L-티로신의 경우 μM; 및 L-DOPA의 경우 0, 2.5, 5 및 1{37}} μM입니다. Dixon 플롯은 효소 억제 유형을 결정하기 위한 그래픽 방법(1/효소 속도(1/V) 대 억제제 농도(I)의 플롯)이며 효소-억제제 복합체의 해리 상수 또는 Ki를 결정하는 데 사용되었습니다. 억제의 Dixon 플롯(단일 역수 플롯)은 1, 2 및 4 mM 및 {{40}}, 0.5, 1에서 L-티로신 기질의 존재하에 얻어졌습니다.{ {47}} 및 2.{49}} BHCP의 경우 μM; 및 BHCP의 경우 {{50}}.5, 1.{56}} 및 2.0mM 및 0, 2.5, 5.0 및 10.0μM의 L-DOPA 기질.

시스탄체 식물티로시나제 억제제이다.
3.4. 세포주 및 세포 배양
Murine B16F10 흑색종 세포는 한국 세포주 은행에서 입수했습니다. 인간 피부 섬유 아세포 세포주 Hs27은 American Type Culture Collection (ATCC, Manassas, VA, USA)에서 구입했습니다. 이들 세포는 37℃의 가습된 5% CO2 배양기에서 10% 태아 소 혈청, 100U/mL 페니실린 및 100mg/mL 스트렙토마이신이 보충된 DMEM에서 유지되었습니다. 100mm 접시의 피부 섬유아세포를 BHCP로 처리하고 무혈청 DMEM(UV 광원, UVP)에서 50mJ/cm2UV에 노출시켰다. Hs27 세포를 직경 100mm 플레이트에서 70-80% 컨플루언스로 배양하고 계대 번호 5와 15 사이에 사용했습니다.
3.5. 세포 생존력 분석
세포의 생존력은 EZ-Cytox 키트 분석을 사용하여 평가되었습니다. 간단히 말해서, B16F1{10}} 세포와 Hs27섬유아세포를 96-웰 플레이트에 1 × 104 cells/well의 밀도로 파종하고 37℃에서 24시간 동안 배양했습니다. 세포에 다양한 농도(0, 1, 2, 5, 10μM)의 BHCP를 함유한 신선한 무혈청 DMEM을 공급하고 24시간 및 48시간 동안 배양했습니다. 이어서, 10 μL의 EZ-Cytox 용액을 각 웰에 로딩하고 세포를 2-4시간 동안 인큐베이션하였다. 어떠한 처리도 하지 않은 세포의 흡광도 측정은 100% 세포 생존으로 간주되었다. 각 처리는 세 번 수행되었으며 각 실험은 세 번 반복되었습니다.
3.6. 멜라닌 함량 분석의 측정
B16F10 세포에서 -MSH로 유도된 멜라닌 생성에 대한 BHCP의 효과는 약간 변형된 이전에 사용된 방법을 기반으로 합니다[34]. 간단히 말해서, 6-웰 플레이트의 B16F10 세포(5 × 104개 세포/웰)를 70~80% 합류로 성장하도록 허용했습니다. 그런 다음 세포를 다른 농도의 BHCP(1, 5, 10μM) 또는 코직산(5mM)으로 24시간 동안 처리한 다음 -MSH(5μM)로 48시간 동안 자극했습니다. 처리 후, 세포를 빙냉 PBS로 2회 세척하고 DMSO(5%)를 포함하는 90μL 1M NaOH 용액에 60℃에서 1시간 동안 용해시키고 마이크로플레이트 분광광도계(TECAN, Salzburg)를 사용하여 405nm에서 흡광도를 측정하였다. , 오스트리아). 실험에서 멜라닌의 양을 측정하기 위해, 세포 용해물의 상층액에 존재하는 단백질의 총량으로 보정된 합성 멜라닌의 알려진 농도의 흡광도로부터 처리군의 억제율을 계산하였다. 미처리 세포의 흡광도를 3회 측정하였다.
3.7. 세포성 티로시나제 활성 분석
세포내 티로시나아제 활성 분석은 L-DOPA의 산화율을 측정하여 수행하였다[35]. 5 × 104/세포 밀도의 B16F1{19}} 세포를 6-웰 디쉬에 넣고 밤새 배양했습니다. 그런 다음 세포를 다양한 농도의 BHCP(1, 5, 10μM) 또는 코직산(5mM)으로 24시간 동안 처리한 다음 -MSH(5μM)로 48시간 동안 자극했습니다. 세포를 PBS로 세척하고 100μL의 50mM 인산 완충액(pH 6.5), 0.1mM페닐메틸설포닐플루오라이드(PMSF) 및 1% Triton X{22}}를 포함하는 용액에 용해했습니다. 그런 다음 세포를 급속 냉동기(-80℃)에 30분 동안 넣었다. 세포를 해동한 후 세포 추출물을 4℃에서 12,{26}} rpm에서 30분 동안 원심분리하여 정제했습니다. 96-웰 플레이트에 총 80μL의 상등액과 20μL의 L-DOPA(2mg/mL)를 첨가하고 37º에서 1시간 동안 492nm 파장에서의 흡광도를 10분 간격으로 측정했습니다. C ELISA 플레이트 판독기(TECAN, 오스트리아 잘츠부르크).
3.8. Hs27 세포의 세포질 및 핵 추출물의 제조
Hs27 세포를 빙냉 PBS로 세척하고 수확하였다. 10mM Tris(pH 8.{9}}), 1.5mM MgCl2, 1mM DTT, 0.1% NP{11}} 및 프로테아제 억제제를 포함하는 완충액은 12,{13}} rpm에서 15분 동안 원심분리하고 10mM Tris, 50mM KCl, 100mM NaCl 및 프로테아제 억제제를 포함하는 완충액을 사용하여 펠릿에서 핵 분획을 추출하고 얼음 위에서 30분 동안 배양한 다음, 그런 다음 4 ºC에서 30분 동안 13,{21}}×g에서 원심분리하여 핵 분획을 얻었습니다.
3.9. 웨스턴 블로팅
용해물 샘플을 겔 로딩 완충액(125mM Tris-HCl, 4% 소듐도데실 설페이트(SDS), 10% 2-머캅토에탄올 및 0.2% 브로모페놀)에서 10분 동안 끓였습니다. 파란색, pH 6.8) 1:1의 부피비. 각 샘플의 총 단백질 당량은 Laemmli[36]에 의해 기술된 절차에 따라 아크릴아미드 겔을 사용하여 SDS-폴리아크릴아미드 겔전기영동(PAGE)에 의해 분리되었고 습식 전달 시스템을 사용하여 80V에서 2시간 동안 PVDF 막으로 전달되었습니다. 멤브레인을 즉시 10mM Tris, pH 7.5, 100mMNaCl 및 0.1% Tween{25}}의 차단 완충액(5% 무지방 우유)에 넣었습니다. 블롯은 25℃에서 2시간 동안 비특이적 결합을 방지하기 위해 차단되었습니다. 이어서, 막을 4℃에서 밤새 특이적 1차 항체와 함께 배양한 다음, 25℃에서 1시간 동안 양고추냉이 퍼옥시다제-결합 이차 항체로 배양했습니다. . 항체 표지는 제조자의 지시에 따라 강화된 화학발광에 의해 검출되었다. 단백질 정량은 Davinch-Chemi TM.Chemiluminescence Imaging System CAS{33}}SM(Core Bio, Seoul, Korea)을 사용하여 수행되었습니다. 분자량 측정을 위해 미리 염색된 단백질 마커를 사용했습니다.
3.10. 통계 분석
모든 데이터는 평균 ± SEM으로 표시됩니다. 데이터는 Bonferroni 사후 검정이 뒤따르는 처리 간의 차이에 대한 일원 분산 분석(ANOVA)으로 분석되었습니다. p < 0.05의="" 값은="" 통계적으로="" 유의한="" 것으로="">
4. 결론
요약하면, 본 연구의 결과는 BHCP가 -MSH로 유도된 B16F10 멜라닌 세포에서 멜라닌 생합성의 핵심 효소인 티로시나아제를 억제하여 피부 미백 효과가 있음을 보여주었다. 또한, BHCP는 UV 유도 섬유아세포에서 MMP 단백질 발현을 감소시켜 주름 개선 효과가 기대된다. 동물 및 임상 연구를 통해 BHCP의 미백 및 주름 개선 효과를 확인하기 위해서는 추가 연구가 필요합니다. 마지막으로 BHCP는 미백 및 주름 개선 효과가 모두 확인되어 과색소침착 및 주름과 관련된 질병 치료제 개발 가능성을 나타냅니다.

