신장 헵시딘/페로포틴 축은 철 재흡수를 제어하고 신장 및 전신 철 과부하의 크기를 결정합니다
Mar 02, 2022
연락처: emily.li@wecistanche.com
Goran Mohammad1, Athena Matakidou2, Peter A. Robbins1, Samira Lakhal-Littleton1
키워드:페로포틴; 혈색소 침착증; 헵시딘; 철; 철 과부하;신장세뇨관
Ferroportin(FPN)은 유일하게 알려진 포유류 철 수출 단백질입니다. 그것은 십이지장 장세포와 비장 세망내피 대식세포, 각각의 철 흡수 및 재활용 부위로부터 순환계로 철 방출을 매개합니다. 주로 간에서 생성되는 헵시딘은 FPN에 결합하고 FPN의 내재화를 유도하여 순환계로의 철 방출 및 말초 조직으로의 가용성을 제한합니다. 철 항상성.
신장은 철 재흡수 부위입니다. 트랜스페린에 결합되지 않은 철과 트랜스페린에 결합하지 않은 철은 모두 사구체 여과액으로 들어갈 수 있습니다.5 이 철의 대부분은 세뇨관 상피로 다시 흡수됩니다. 다중 리간드 메갈린-쿠빌린 수용체 복합체, 트랜스페린 수용체 1, 2가 금속 수송체 1, 아연 수송체 ZIP8 및 아연 수송체 ZIP14.5-10을 포함한 여러 수송체가 이 재흡수에 연루되어 있습니다.
일단신장상피, 철분은 순환계로 재흡수됩니다. FPN이 풍부하다.신장그리고 철 재흡수와 관련이 있습니다.11-14 그러나 신장 FPN이 정상적인 생리학적 조건에서 내인성 HAMP에 의해 조절되는지, 그리고 그렇다면 그러한 조절이 전신 및/또는 신장 철 항상성에 중요한지 여부는 알려지지 않았습니다.
이러한 질문을 해결하기 위해 우리는 유도 가능한 새로운 마우스 모델을 생성했습니다.신장세뇨관– HAMP 내성 FPNC326Y 단백질을 인코딩하는 fpnC326Y의 특정 녹인. 또한 이전에 보고된 철 재흡수에서 FPN의 역할을 확인하기 위해 유도성 마우스 모델도 생성했습니다.신장세뇨관– fpn 유전자의 특정 삭제. 우리의 결과는 내인성 HAMP가 FPN 매개 철 흡수를 직접 조절하고 이 조절이 두 가지 모두에 중요하다는 것을 보여줍니다.신장및 전신 철 항상성, 특히 과잉 철 가용성의 설정에서.
이 연구는 공식적으로 결정하기 위해 HAMP 반응성의 신장 특이적 손실을 지닌 마우스를 이용하는 최초의 연구입니다.중요성의신장HAMP/FPN 축. 그것은 혈색소 침착증의 설정에서 신장 및 신외 철 과부하의 정도를 결정하는 철 재흡수의 역할에 대한 새로운 통찰력을 제공합니다.

행동 양식
쥐
모든 동물 절차는 1986년 영국 가정 사무실 동물(과학적 절차)법을 준수했으며 옥스포드 대학 의료 과학 부서 윤리 검토 위원회의 승인을 받았습니다.
조건부 fpnflfl 및 fpnC326Yflfl 대립유전자는 이전에 설명한 대로 생성되었습니다.15,16
Pax8.CreERT2þ 이식유전자를 보유하고 있는 마우스는 케임브리지 대학교 암 연구 UK 케임브리지 연구소의 Athena Matakidou 박사의 선물이었습니다. 이 마우스는 이전에 설명한 대로 생성되었습니다.17 모든 마우스는 C57BL/6 배경에 있었습니다.
다이어트
달리 명시되지 않는 한, 동물에게 200ppm의 철을 함유한 표준 설치류 먹이가 제공되었습니다. 철분 조작 실험에서 쥐에게 철분이 풍부한 식단(5000-ppm iron; Teklad TD.140464) 또는 3일 동안 이유식부터 일치하는 대조군 식단(200- ppm iron; Teklad TD.08713)을 제공했습니다. 개월.
철 정량 및 철 지수
혈청 철 및 페리틴 수치는 ABXPentra 시스템(Horiba Medical)을 사용하여 결정되었습니다. 헤모글로빈 값은 HemoCue Hb 201 헤모글로빈 마이크로큐벳에 의해 결정되었습니다. 혈청 에리트로페론 수치는 효소 결합 면역흡착 분석법(Intrinsic Lifesciences)으로 측정했습니다. 조직 내 총 원소 철의 측정은 이전에 설명한 대로 유도 결합 플라즈마 질량 분석법으로 수행되었습니다.15,16,18 보정은 0 ng/g, 0.5 ng/ g, 1ng/g, 10ng/g, 20ng/g 및 100ng/g 철을 선택한 샘플의 복제물에 추가했습니다. 교정의 유효성을 확인하기 위해 외부 철 표준물질(고순도 표준물질 ICP-MS{13}}A 용액)을 희석하고 측정했습니다. 로듐은 또한 1ng/g의 농도에서 내부 표준으로서 각 블랭크, 표준 및 샘플에 스파이킹되었습니다. 소변 철 정량을 위해 24시간 동안 쥐로부터 소변을 수집하고 유도 결합 플라즈마 질량 분석기를 사용했습니다. 동일한 샘플의 크레아티닌 수준은 비색 크레아티닌 분석 키트(Abcam; ab65340)를 사용하여 측정되었고 철 값은 크레아티닌 농도로 정규화되었습니다.
면역조직화학
형광 면역염색은 1:100에서 FPN 항체(Novus Biologicals; NBP{2}}) 및 1:50에서 Pro-Hepcidin(AA 39-59) 항체를 사용하여 포르말린 고정, 파라핀 포매 조직 절편에서 수행되었습니다. (항체 온라인; ABIN350367). FPN 및 헵시딘 항체의 특이성은 Fpnflfl/flfl, Pax8.CreERT2þ 동물 및 Hamp–/– 동물을 각각 음성 대조군으로 사용하여 확인되었습니다(보충 그림 S1). 1:200에서 아쿠아포린 항체(Biotechne; NB{16}}), 1:200에서 아쿠아포린 항체(Biotechne, NBP{20}})를 사용하여 신장 분절 마커를 식별했습니다. 또는 1:100에서 칼빈딘 항체(Abcam; ab82812). 이차 항체는 항토끼 IgG Alexa Fluor{25}}(Abcam; ab150073), 항당나귀 IgG Cy3(Abcam; ab6949) 및 항마우스 IgG Alexa568(Abcam, ab175473)이었습니다. 슬라이드는 FV1000 Olympus 현미경을 사용하여 이미지화되었습니다.

웨스턴 블로팅
조직을 액체 질소에서 급속 동결하고 분쇄한 다음 제조업체의 지침에 따라 RIPA Lysis Buffer System(Santa Cruz; sc{0}})을 사용하여 용해했습니다. 조직 용해물을 4C에서 10분 동안 15 000g에서 원심분리하여 제거했습니다. 용해물의 단백질 농도를 BCA 단백질 분석(Pierce; 23225)으로 측정하고 각 배치에 대해 동일한 농도로 정규화했습니다. 그 다음, 용해물을 비환원성 Laemmli 나트륨 도데실 설페이트 샘플 완충액에서 희석하고 95℃에서 5분 동안 가열하였다. 단백질(30–50 mg)을 Mini-PROTEAN TGX 젤(Biorad, 4561096)에 로드했습니다. 전기영동 후, BioRad Translotter 시스템을 사용하여 단백질을 폴리비닐리덴 디플로오라이드 막으로 옮기고, 막을 5% 소 혈청 알부민을 함유하는 차단 완충액에서 1시간 동안 차단하였다. 그런 다음 멤브레인을 1:1000에서 토끼 다클론 항마우스 FPN 항체(NBP{14}}; Novus Biologicals) 또는 양고추냉이 퍼옥시다제 결합 항b-액틴 항체(Proteintech, HRP{18} }) 1시 50분. ECL 프라임 검출 키트(RPN2232; VWR International)를 사용하여 블롯을 개발했습니다. 신호 강도는 ImageJ로 정량화하고 FPN과 b-액틴 신호 사이의 비율을 계산하여 정규화된 강도를 생성했습니다.
Diaminobenzidine(DAB) 강화 Perls 염색
포르말린 고정, 파라핀 포매 조직 절편을 자일렌을 사용하여 파라핀 제거한 다음 에탄올에서 재수화했습니다. 그런 다음 슬라이드를 0.1 mol/L HCl 완충액 중 1% 칼륨 페리시안화물로 1시간 동안 염색했습니다. 내인성 퍼옥시다제 활성을 켄칭한 다음, 슬라이드를 DAB 크로모겐 기질로 염색하고 헤마톡실린으로 대조염색했습니다. 그들은 표준 명시야 현미경을 사용하여 시각화되었습니다.
정량적 중합효소 연쇄 반응
Hamp 및 하우스키핑 유전자 박틴(Life Technologies)에 대한 Applied Biosystems TaqMangene 발현 분석 프로브를 사용하여 유전자 발현을 측정했습니다. 먼저 관심 유전자에 대한 임계 사이클(CT) 값은 DCT 값을 얻기 위해 b-액틴에 대한 CT 값을 차감하여 정규화되었습니다. 테스트 샘플의 DCT 값은 DDCT 값을 얻기 위해 대조군 샘플에 대한 DCT 값의 평균으로 더 정규화되었습니다. 그런 다음 상대 유전자 발현 수준을 2-DDCT로 계산했습니다.
통계
값은 평균 SEM으로 표시됩니다. 쌍을 이루는 비교는 스튜던트 t 테스트를 사용하여 수행되었습니다. 분산 분석을 사용하여 다중 비교를 수행했습니다. 사후 테스트는 Bonferroni 보정을 사용했습니다.

그림 1|신장 세뇨관의 헵시딘/페로포틴(FPN) 축은 철 재흡수를 조절하고 신장 철 항상성에 중요합니다.암컷 쥐에서. (ㅏ)야생형 마우스의 신장에서 FPN, 아쿠아포린 1(AQP1), 아쿠아포린 2(AQP2) 및 칼빈딘(CalD)에 대한 면역형광 염색의 대표적인 이미지. 바=200mm, 원래 배율 10. 엔드 패널, 바=25mm, 원래 배율 60. (b) FPN에 대한 웨스턴 블롯신장타목시펜 처리 1주 후 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreER T2 þ 마우스 및 FpnC326Y flfl/flfl 대조군. 신호 강도의 정량화는 하단 패널에 표시됩니다. (c) 타목시펜 처리 1주 후 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 신장에서 FPN에 대한 웨스턴 블롯. 신호 강도의 정량화는 하단 패널에 표시됩니다. (d) 여성 및 남성 FpnC326Y의 신장 철 수치flfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군은 타목시펜 치료 후 1주, 1개월, 3개월 및 6개월에 대조군. (e) 타목시펜 유도 후 3개월에 해당 동물의 신장 피질 영역에서 디아미노벤지딘(DAB) 강화 Perls 철 염색의 대표적인 이미지. 막대 ¼ 200mm, 원래 배율 10. (f) 타목시펜 유도 후 1주, 1개월, 3개월 및 6개월에 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 신장 철 수치. (g) 타목시펜 유도 후 3개월에 해당 동물의 신장 피질 영역에서 DAB 강화 Perls 철 염색의 대표적인 이미지. (계속되는)
그림 1 |(계속) 막대 ¼ 200mm, 원래 배율 10. (h) 타목시펜 처리 후 1주, 1개월, 3개월 및 6개월에 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 혈청 철 수준. (i) 타목시펜 유도 후 1주, 1개월, 3개월 및 6개월에 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 혈청 철 수준. 값은 평균 SEM으로 표시됩니다. *P < 0.05,="" **p="">< 0.01,="" ****p="">< 0.0001.="" b-액트,="" b-액틴;="" 계속,="" 통제;="" dapi,="" 40,{25}}디아미디노{26}}페닐인돌;="" ppm,="" 백만분율.="" 이="" 이미지의="" 보기를="" 최적화하려면="" www.kidney-international.org에서="" 이="" 기사의="" 온라인="" 버전을="">
결과
신장 세뇨관의 헵시딘/FPN 축은 철 재흡수를 조절하고 암컷 마우스의 신장 철 항상성에 중요합니다
우리는 먼저 FPN 발현의 정확한 위치를 설정하려고 했습니다.신장. 이를 위해 우리는 FPN 및 분절 특이적 마커인 아쿠아포린 1(헨리의 근위 세뇨관 및 가는 하행의 마커), 아쿠아포린 2(집합관 및 연결 세관의 마커) 및 칼빈딘(마커 원위 복잡한 세뇨관과 피질 연결 및 수집 덕트). 우리는 FPN이 피질에서 강하게 발현되어 aquaporin 1과 근위의 복잡한 세뇨관에 공존한다는 것을 발견했습니다. 내부 수질에 약간의 FPN이 있었고 아쿠아포린 2와 함께 수질 집합관에 공동화되었습니다. calbindin과 FPN의 colocalization은 없었습니다(그림 1a, 보충 그림 S2에 표시된 더 큰 패널). 이러한 결과는 FPN이 근위 세뇨관 내의 피질 영역에서 가장 풍부하다는 것을 확인시켜줍니다.
신장 FPN이 HAMP에 의해 조절되는지 여부를 결정하기 위해 우리는 근위 및 원위 세뇨관에서 쌍을 이루는 상자 유전자 8 pax8 프로모터의 제어 하에 Cre 재조합효소의 타목시펜 유도성 발현을 유도하는 Pax8.CreERT2þ 노크인 트랜스진을 보유하는 마우스를 사용했습니다. 덕트 수집 또한, 이전에 보고된 철 재흡수에서 신장 FPN의 역할을 확인하기 위해 우리는 Pax8.CreERT2þ 마우스를 Fpnflfl/flfl 대립유전자를 보유하는 마우스와 교배했습니다. Pax8.CreERT2 이식유전자를 유도하기 위한 타목시펜 치료 후 1주일, FpnC326Yflfl/flfl 대조군에 비해 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스에서 신장 FPN 수준이 증가하여(그림 1b), 신장 FPN이 정상적인 생리적 조건에서 내인성 HAMP를 제거하고 Pax8.CreERT2þ 이식유전자의 효율성을 확인합니다. 반대로, Fpnflfl/flfl 대조군에 비해 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스에서 신장 FPN 수준이 감소하여 Pax8.CreERT2þ 이식유전자의 효율성을 추가로 확인했습니다(그림 1c). 이 Pax8.CreERT2þ 이식유전자의 특이성은 또한 결실 대립유전자(DFpn)의 존재에 의해 확인되었습니다.신장그러나 Fpnflfl/flfl ,Pax8.CreERT2þ 마우스의 간이나 비장에는 없습니다(보충 그림 S2A).
다음으로 우리는 신장 HAMP/FPN 축이 철 재흡수를 조절하는지 여부를 결정하기 시작했습니다. 이를 위해 타목시펜 치료 후 1주, 1개월, 3개월, 6개월에 신장 및 혈청 철 수치를 측정하였다. 우리는 신장 철
함량은 FpnC326Yflfl/flfl, Pax8.CreERT2þ 암컷에서 FpnC326Yflfl/flfl 대조군 암컷보다 모든 시점에서 낮았습니다(그림 1d). 남성의 신장 철 함량은 유전자형에 따라 다르지 않았습니다(그림 1d). DAB 강화 Perl의 철 얼룩은 또한 FpnC326Yflfl/flfl, Pax8.CreERT2þ 암컷의 근위 세뇨관 내 철 수준의 감소를 확인했습니다(그림 1e, 보충 그림 S2에 표시된 더 큰 패널). 반대로, 우리는 1개월 이후부터 Fpnflfl/flfl, Pax8.CreERT2þ 암컷에서 Fpnflfl/flfl 대조군 암컷보다 신장 철 함량이 더 높다는 것을 발견했습니다(그림 1f). 남성의 신장 철 함량은 유전자형에 따라 다르지 않았습니다(그림 1f). DAB 강화 Perls 철 얼룩은 또한 Fpnflfl/flfl, Pax8.CreERT2þ 암컷의 근위 세뇨관 내에서 철 축적을 확인했습니다(그림 1g, 보충 그림 S2에 표시된 더 큰 패널).
혈청 철 수치는 1-개월 시점에서 FpnC326Yflfl/flfl 대조군에 비해 수컷 및 암컷 FpnC326Yflfl/flfl ,Pax8.CreERT2þ 마우스 모두에서 일시적으로 증가했습니다(그림 1h). 반대로, 혈청 철 수치는 1-개월 시점에서 Fpnflfl/flfl 대조군 암컷에 비해 Fpnflfl/flfl, Pax8.CreERT2þ 암컷에서 감소한 반면, 모든 시점에서 다른 유전자형의 수컷에서는 비슷한 수준으로 유지되었습니다(그림 1i ). 3개월령에 대조군 동물에서 관찰된 혈청 철 수준의 회복은 정상적인 신장 FPN 수준의 회복에 기인할 수 없습니다. 실제로, 신장 FPN 수준의 Pax8.CreERT2þ 유도 변화는 타목시펜 치료 후 3개월 후에도 여전히 유지되었습니다(보충 그림 S2B 및 C). FpnC326Yflfl/flfl,Pax8.CreERT2þ 암컷에서 신장 철 함량 감소 및 혈청 철 수준 증가는 근위 세뇨관에서 FPN 의존성 철 재흡수가 정상적인 생리적 조건에서 HAMP에 의해 조절된다는 것을 보여줍니다. Fpnflfl/flfl ,Pax8.CreERT2þ 암컷의 신장 철 함량 증가 및 혈청 철 수치 감소는 신장 FPN이 철 재흡수에 기여한다는 이전 연구 결과를 확인시켜줍니다. 또한, 정상적인 생리학적 조건에서 신장 HAMP/FPN 축에 의한 철 재흡수 조절은 적어도 C57BL/6 계통에서 남성보다 여성에서 더 중요한 것으로 보입니다.

Cistanche는 신장 기능을 향상시킬 수 있습니다
신장 HAMP/FPN 축은 정상적인 철분 가용성 조건에서 정상적인 전신 철분 항상성에 기여하지만 필수적인 것은 아닙니다.
다음으로, 우리는 전신 철 항상성에 대한 신장 HAMP/FPN 축의 기여도를 결정하기 시작했습니다. 우리는 FpnC326Yflfl/flfl,Pax8.CreERT2þ 암컷이 1-개월 시점에서 혈청 페리틴(그림 2a), 간 철 함량(그림 2b) 및 비장 철 함량(그림 2c)이 일시적으로 증가한다는 것을 발견했습니다. FpnC326Yflfl/flfl 대조군 암컷과 비교. 그들의 헤모글로빈 수준은 모든 시점에서 대조군의 수준과 유사하게 유지되었습니다(그림 2d). 이러한 매개변수는 FpnC326Yflfl/flfl, Pax8.CreERT2þ 수컷과 FpnC326Yflfl/flfl 컨트롤 간에 다르지 않았습니다(그림 2a–d). Erythroferrone 수준은 유전자형에 따라 다르지 않았습니다(보충 그림 3A). 반대로 Fpnflfl/flfl ,Pax8.CreERT2þ 암컷은 1- 및 3-개월 시점(그림 2e)에서 혈청 페리틴 수치가 낮고 3- 및 6-월 시점(그림 2f) 및 Fpnflfl/flfl 대조군 암컷과 비교할 때 1- 및 3-월 시점(그림 2g)에서 더 낮은 비장 철분 함량. 그들은 또한 3-개월 시점에서 일시적이고 가벼운 헤모글로빈 수치 감소를 보였습니다(그림 2h). Fpnflfl/flfl , Pax8.CreERT2þ 남성과 Fpnflfl/flfl 컨트롤 간에 이러한 매개변수 중 어떤 것도 다르지 않았습니다(그림 2e–h). Erythroferrone 수준도 유전자형에 따라 변경되지 않았습니다(보충 그림 3B). 함께, 이러한 데이터는 정상적인 생리학적 조건에서 신장 HAMP/FPN 축이 전신 철분 수준에 기여하지만 그 자체가 정상적인 전신 철분 항상성의 유지에 필수적인 것은 아님을 보여줍니다.

그림 2|신장 헵시딘 항균성 펩타이드/페로포틴(FPN) 축은 정상적인 전신의정상적인 철분 가용성 조건에서 철분 항상성. (기원 후)타목시펜 치료 후 1주, 1개월, 3개월 및 6개월 후 암컷 및 수컷 FpnC326Yflfl/flfl,Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 전신 철 지수((a) 혈청 페리틴, (b) 간 철 함량 포함) , (c) 비장 철분 함량, (d) 헤모글로빈. (e–h) 타목시펜 유도 후 1주, 1개월, 3개월 및 6개월 후 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 전신 철 지수 (e) 혈청 페리틴, ( f) 간 철분 함량, (g) 비장 철분 함량, (h) 헤모글로빈. 값은 평균 SEM으로 표시됩니다. *P < 0.05,="" **p="">< 0.01="" 및="" ***p="">< 0.001.="" ppm,="">

그림 3|신장 헵시딘 항미생물 펩티드(HAP)/페로포틴(FPN) 축은 과잉 철 가용성 조건에서 신장 및 전신 철 과부하의 크기를 결정합니다. (a-f)암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 신장 외 철 지수는 3개월 동안 대조군 식단(200ppm) 또는 철분 함유 식단(5000ppm)을 제공했습니다. (계속되는)
그림 3 |(계속) 지수에는 (a) 혈청 철, (b) 혈청 페리틴, (c) 비장 철 함량, (d) 심장 철 함량, (e) 폐 철 함량 및 (f) 간 철 함량이 포함됩니다. (g) 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 신장 철 함량은 대조군 식단(200ppm) 또는철이 들어있는3개월 동안 다이어트(5000 ppm). (h,i) 디아미노벤지딘(DAB)의 대표적인 이미지 - 간 및 해당 동물의 신장 임계 영역에서 강화된 Perls 철 얼룩. 막대 ¼ 200mm, 원래 배율 10. (j) 해당 동물의 간에서 hamp 유전자의 상대적 발현. 값은 평균 SEM으로 표시됩니다. *P < 0.05,="" **p="">< 0.01,="" ***p="">< 0.001,="" ****p="">< 0.0001,="" *****p="">< 0.00001="" 및="" ******p="">< 0.000001.="" 이="" 이미지의="" 보기를="" 최적화하려면="" www.kidney-international.org에서="" 이="" 기사의="" 온라인="" 버전을="">
신장 HAMP/FPN 축은 과잉 철 가용성 조건에서 신장 및 전신 철 과부하의 크기를 결정합니다.
다음으로, 우리는 철 과부하 설정에서 신장 HAMP/FPN 축의 역할을 결정하기 시작했습니다. 이를 위해 FpnC326Yflfl/flfl, Pax8.CreERT2þ 동물 및 FpnC326Yflfl/flfl 대조군을 타목시펜으로 유도한 다음 3개월 동안 200ppm 철분을 함유한 대조군 차우 식이 또는 5000ppm 철분을 함유한 철분 함유 식이를 제공했습니다. . 우리는 철분이 풍부한 식단의 제공이 두 유전자형의 남성과 여성에서 혈청 철, 혈청 페리틴 및 조직 철 함량을 증가시키는 것을 발견했습니다. 그러나 FpnC326Yflfl/flfl,Pax8.CreERT2þ 동물은 혈청 철(그림 3a), 혈청 페리틴(그림 3b) 및 비장(그림 3c), 심장(그림 3d), 폐(그림 3e)의 철 함량이 더 크게 증가했습니다. , FpnC326Yflfl/flfl 대조군보다 간(그림 3f). 대조적으로, 그들은 신장 철 함량의 증가가 더 낮았습니다(그림 3g). 근위 세뇨관 및 간에서의 철 부하 정도의 유전자형 간의 차이는 DAB 강화 Perls 철 염색에서도 분명했습니다(그림 3h 및 i, 보충 그림 S4에 표시된 더 큰 패널). 더 큰 전신 철 과부하에 따라 FpnC326Yflfl/flfl , Pax8.CreERT2þ 동물도 FpnC326Yflfl/flfl 대조군과 비교하여 간 햄프 유전자 발현이 더 크게 증가했습니다(그림 3j). 헤모글로 빈 수준은식이 요법이나 유전자형에 영향을받지 않았으며 이와 일치하여 혈청 에리트로 페론 수치도 변하지 않았습니다 (보충 그림 4A 및 B). 이러한 발견은 과도한 철 가용성 조건 하에서 신장 HAMP/FPN 축에 의한 철 재흡수의 제어가 신장 철 과부하를 증가시키면서 전신 철 과부하를 감소시킨다는 것을 입증합니다.
신장 HAMP/FPN 축은 혈색소 침착증에서 조직 철 과부하의 패턴을 결정합니다
다음으로, 우리는 헵시딘 생산 또는 헵시딘 반응성의 결함으로 인한 철 과부하의 유전적 조건인 유전성 혈색소증의 맥락에서 신장 HAMP/FPN 축의 역할을 탐구하기 시작했습니다. fpnC326Y 대립유전자(Fpnwt/C326Y)의 이형접합 유비쿼터스 노크인을 보유하는 집. 우리는 이전에 이 마우스가 유전성 혈색소증의 특징인 철 과부하 표현형을 발달시킨다는 것을 입증했습니다.15,18 우리는 조직의 패턴을 비교했습니다.철 과부하3개월 동안 이유식으로부터 철분이 풍부한 식단을 먹인 야생형 마우스에서 볼 수 있는 이 마우스에서. Fpnwt/C326Y마우스와 철이 풍부한 식단을 먹인 야생형 마우스 모두
각각의 대조군과 비교하여 간, 심장 및 폐의 철분 함량이 증가했습니다(그림 4a 및 b). Fpnwt/C326Ymice의 신장 철 함량은 3개월령에 정상이었고(그림 4a) 6개월령의 대조군에 비해 32%만 증가했습니다(보충 그림 5A). 대조적으로, 철분이 풍부한 식이를 제공한 야생형 동물은 정상 식이를 제공한 동물에 비해 신장의 철분 함량이 260% 증가했습니다(그림 4b). 두 모델 간의 신장 및 간 철 과부하의 상대적인 차이는 DABenhanced Perls 철 염색에서도 분명했습니다(그림 4c 및 d, 보충 그림 S5에 표시된 더 큰 패널). 신장 과부하의 크기는 2개 모델 간에 비슷했지만, 신장 과부하의 크기는 Fpnwt/C326Y 마우스보다 철분이 풍부한 식단을 제공한 야생형 동물에서 상당히 더 높았습니다(그림 4e). FPN은 Fpnwt/C326Y 마우스와 철이 풍부한 식단을 제공한 야생형 마우스 모두의 피질에서 증가했습니다(그림 4f 및 g, 더 큰 패널은 보충 그림 S5에 표시됨). 근위 세뇨관에서 FPN 발현 부위를 자세히 조사한 결과 Fpnwt/C326Y 마우스에서 기저외측 막뿐만 아니라 세포내로 국소화되는 것으로 나타났습니다. 대조적으로, FPN은 주로 세포질, 정점 막에 국한되는 것으로 나타났으며 놀랍게도 마우스의 핵은 철분이 풍부한 식단을 제공했습니다(그림 4f 및 g, 하단 패널). 철분이 풍부한 식단의 제공으로 인해 발생하는 FPN 국소화 패턴은 Fpnflfl/flfl, Pax8.CreERT2þ Fpnflfl/flfl, Pax8.CreERT2þ 동물을 음성 대조군으로 사용하여 추가로 확인되었습니다(보충 그림 S5B). 이러한 관찰은 FpnC326Yflfl/flfl,Pax8.CreERT2þ 동물이철이 들어있는식이 요법에서 신장 FPN에 대한 HAMP 작용의 손실이신장유전성 혈색소 침착증에서 철 부하로 인한 것.
논의
현재 연구의 가장 중요한 발견은 내인성 HAMP가 FPN 매개 철 재흡수를 조절한다는 것입니다. 이전 연구에서는 배양된 신장 세포에서 외인성 HAMP에 의한 FPN의 조절과 신장 세포에서 HAMP와 FPN 수준 사이의 역 관계가 보고되었습니다.신장일측성 요관 폐쇄 후 발생합니다.12,13 그러나 이것은 이러한 조절이 정상적인 생리적 조건에서 생체 내에서 그리고 신장 및 전신 철 항상성에 영향을 미치는 방식으로 작동한다는 첫 번째 증명입니다. 이 연구의 특별한 강점은 HAMP 반응성의 신장 관련 손실을 숨기기 위해 사내에서 생성된 새로운 마우스를 사용한다는 것입니다. 이 접근 방식을 사용하면 유비쿼터스 동물 모델에서 볼 수 있는 변경된 전신 철 항상성의 교란 효과 없이 신장 HAMP/FPN 축을 연구할 수 있습니다.
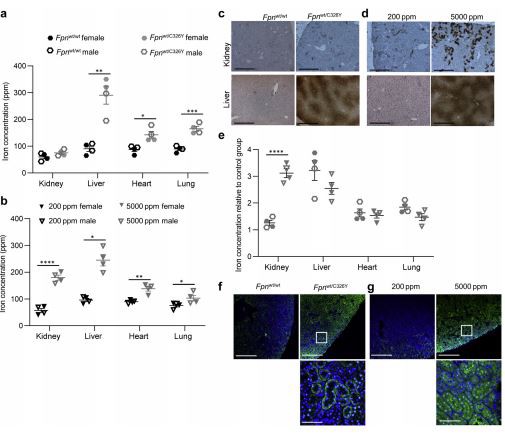
그림 4|신장 헵시딘 항균 펩티드/페로포틴(FPN)은 혈색소 침착증에서 조직 철 과부하의 패턴을 결정합니다. (ㅏ)3개월령의 Fpnwt/C326Y 동물 및 Fpnwt/wt 대조군의 신장, 간, 심장 및 폐의 철 수치. (b) 철분 수치신장, 야생형 동물의 간, 심장 및 폐는 대조군 식단(200ppm[ppm]) 또는 철분이 풍부한 식단(5{{4{{ 42}}}00 ppm) 이유부터 3개월 동안. (c) 3개월령의 Fpnwt/C326Y 동물 및 Fpnwt/wt 대조군의 신장 피질 및 간에서 디아미노벤지딘(DAB) 강화 Perls 철 염색의 대표적인 이미지. 바=200mm, 원래 배율10. (d) 야생형 동물의 신장 피질과 간에서 DAB 강화 Perls 철 염색의 대표적인 이미지는 3개월 동안 이유식으로부터 대조군 사료(200ppm) 또는 철이 풍부한 식단(5000ppm)을 제공했습니다. Bar=200 mm, 원래 배율 10. (e) Fpnwt/C326Y 동물과 철이 풍부한 식단을 섭취한 야생형 동물 사이의 조직 철 부하 정도 비교. 각 동물에 대해 표시된 값은 각 대조군의 평균으로 정규화되었습니다. (f) 3개월령의 Fpnwt/C326Y 동물 및 Fpnwt/wt 대조군의 신장 피질에서 FPN 면역형광 염색의 대표적인 이미지. 상단 패널, 막대=200mm, 원래 배율 10. 하단 패널, 막대=25mm, 원래 배율 60. (g) 야생형 동물의 신장 피질에서 FPN 면역형광 염색의 대표적인 이미지는 대조군 식단(200 ppm) 또는 이유식부터 3개월 동안 철분이 풍부한 식단(5000ppm). 상단 패널, 막대=200mm, 원래 배율 10. 하단 패널, 막대=25mm, 원래 배율 60. 값은 평균 SEM으로 표시됩니다. *P < 0.05,="" **p="">< 0.01,="" ***p="">< 0.001,="" ****p="">< 0.0001.="" 이="" 이미지의="" 보기를="" 최적화하려면="" www.kidney-international.org에서="" 이="" 기사의="" 온라인="" 버전을="">
본 연구의 두 번째 중요한 발견은 신장 HAMP/FPN이 신장 및 전신 철 과부하의 크기를 결정한다는 것입니다(그림 5). 실제로, 신장 세뇨관에서 HAMP 반응성의 손실은 간, 비장, 심장 및 폐 철 과부하의 크기를 증가시키는 반면 철이 풍부한 식단 제공 후 신장 철 과부하의 크기를 감소시켰습니다. 이와 일치하게, 혈색소증 쥐(신장 HAMP/FPN 축이 또한 중단) (그래픽 초록). 이 발견은 다음과 같은 임상적 관찰을 설명할 수 있습니다.신장유전성 혈색소 침착증이 있는 환자에서는 일반적으로 영향을 받지 않습니다.19

그림 5|철분 과부하 설정에서 신장 헵시딘 항균 펩티드(HAMP)/페로포틴(FPN) 축의 역할.철분이 풍부한 식단의 제공은 사구체 여과액의 혈청 철분 가용성과 철분 수준을 증가시키고 간에서 헵시딘(HAMP) 생산 및 방출을 증가시킵니다. 증가된 혈청 HAMP는 신세뇨관에서 FPN을 차단하여 철 재흡수를 억제합니다. 철 재흡수의 억제는 신장 철 저류를 유발하는 반면 전신 철 가용성을 감소시키고 결과적으로 간 철 과부하를 감소시킵니다. FpnC3326Yflfl/flfl,Pax8.CreERT2þ 마우스에서 신장 세뇨관에서 HAMP 반응성의 손실은 조절되지 않은 철 재흡수를 유발합니다. 이것은 차례로 신장의 철분 저류를 방지하는 동시에 전신 철분 가용성을 증가시키고 결과적으로 간 철분 과부하를 증가시킵니다.
혈색소침착증과 식이 철 과부하가 신세뇨관에서 FPN을 증가시켰지만, 이들은 정점, 세포내 또는 기저외측 구획에 대해 상이한 패턴의 국소화를 초래하는 것으로 나타났습니다. 쥐 십이지장에서도 유사한 관찰이 이루어졌는데, 철 위관 영양법이 십이지장 장세포에서 이들 구획 사이의 FPN의 상대적 분포를 변경하는 것으로 밝혀졌습니다. 이러한 결과에 대한 한 가지 해석은 식이 철 과부하 설정에서 FPN 번역이 증가한다는 것입니다(매개 철 조절 단백질)은 신세뇨관 세포에서 높은 전체 FPN 생산을 유지하는 역할을 하는 반면, 증가된 혈청 HAMP는 기저외측막에 국한될 수 있는 FPN의 비율을 감소시킬 것입니다. 이 해석에서 근위 세뇨관에서 FPN의 위치에 대한 이전 보고서 사이의 차이는 다른 연구에서 사용된 동물 모델 간의 세뇨관 철 함량과 혈청 헵시딘 수준의 차이를 반영할 수 있습니다.5,11-14,21 이러한 차이는 현재 연구에서 사용된 것을 포함하여 상업용 FPN 항체와 관련하여 이전에 보고된 비특이적 반응성의 정도를 반영할 수 있습니다. 철 부하 마우스의 소변 철 배설에서 (보충 그림 5C). 또 다른 흥미로운 관찰은 일부 FPN이 철-부하된 마우스의 신장 세뇨관에서 핵에 국한된 것으로 나타났다는 것입니다. 철이 풍부한 대식세포와 쥐의 간에서도 유사한 관찰이 이루어졌습니다. 후자의 연구는 핵 FPN이 급성기 반응의 일부로 핵 철 보유에 관여한다는 것을 발견했습니다. 신장에서 FPN.
신장 HAMP의 조절과 기능도 완전히 이해되지 않았습니다. 우리는 철분이 풍부한식이 요법 (보충 그림 5E)을 제공 한 후 야생형 동물에서 신장에서 햄프 유전자의 발현이 증가했지만 혈색소 침착 마우스 (보충 그림 5D)와 신세뇨관이있는 쥐에서는 변경되지 않은 채로 있음을 발견했습니다. FPN 또는 신세뇨관의 특정 손실 - HAMP 반응성의 특정 손실(보충 그림 S5F 및 G). 이러한 결과는 신장 햄프 유전자 발현이 신장 철 수준에 의해 국소적으로 조절된다는 개념을 뒷받침하지 않습니다. 신장 HAMP의 기능 측면에서, 일측성 요관 폐쇄 모델에 대한 이전 연구에서는 신장 FPN 조절에 관여한다고 제안했습니다. 우리는 신장 HAMP(pro-HAMP 펩티드에 대한 항체를 사용하여 검출됨)가 칼빈딘(원위 복잡한 세뇨관 및 피질 집합관 및 연결 덕트의 마커)과 공동 국소화됨을 발견했습니다(보충 그림 S5H). 반면에 FPN 발현은 HAMP 반응성의 신장 특이적 손실을 지닌 마우스에서도 칼빈딘과 함께 국소화되지 않습니다(그림 1a 및 보충 그림 S5I). 이러한 결과는 신장 FPN 조절에서 신장 HAMP의 자가분비 역할과 일치하지 않습니다. 그럼에도 불구하고, 신장 HAMP는 신장 FPN의 측분비 조절에 관여할 수 있습니다. 미래에는 신장 HAMP의 측분비 기능을 연구하고 철 재흡수 조절에 대한 신장 및 간 HAMP의 상대적 기여도를 정량화하는 것이 흥미로울 것입니다.
본 연구의 또 다른 흥미로운 관찰은 정상적인 철분 가용성 조건에서 신장 HAMP/FPN 축이 정상적인 전신 철분 항상성의 유지에 필수적이지 않고 대신 적어도 다음의 암컷 마우스에서 신장 철분 수준을 조절하는 데 더 중요하다는 것입니다. C57BL/6 균주. 실제로, 신장 세뇨관에서 FPN 또는 HAMP 반응성의 손실로 인한 신장 철 수준의 관찰된 변화가 지속되었지만 전신 철 지수의 변화는 본질적으로 일시적이었습니다. 전신 효과의 일시적인 특성은 관여 보상 메커니즘을 암시합니다. 한 가지 가능한 보상 메커니즘은 간 HAMP에 의한 식이 철분 흡수의 조절입니다. 실제로, 본 발명자들은 HAMP 반응성의 신장 특이적 손실을 지닌 마우스에서 1-개월 시점에서 혈청 철 수준의 증가에 따라 간 햄프 유전자 발현이 증가하고 이후 시점에서 증가된 상태를 유지한다는 것을 발견했습니다. 반대로, hepatic hamp 유전자 발현은 1-개월 시점에서 혈청 철 수치가 감소한 후 FPN의 신장 특이적 손실이 있는 마우스에서 억제되었고 이후 시점에서 억제된 상태를 유지했습니다(보충 그림 S6A 및 B). 또한, 첫 번째 설정에서 증가된 간 햄프 유전자 발현은 감소된 장 FPN 수준을 동반한 반면, 두 번째 설정에서 감소된 간 햄프 유전자 발현은 더 높은 장 FPN을 동반했습니다(보충 그림 S6C 및 D). 이러한 결과는 식이 철 흡수에 대한 간 HAMP의 작용이 교란된 신장 철 재흡수에 직면하여 정상적인 전신 철 항상성을 유지하는 것과 관련된 활성 보상 메커니즘임을 나타냅니다.
Cistanche는 신장 기능을 복구할 수 있습니다
참고로, 정상적인 철 가용성 조건에서 신장 HAMP/FPN 축은 적어도 C57BL/6 계통에서 수컷 마우스보다 암컷 마우스에서 더 중요한 것으로 보입니다. 이 관찰은 Pax8.CreERT2þ 이식유전자의 활성에서 남성과 여성 간의 차이에 기인할 수 없습니다. 네프론을 따라 있는 수송체의 수준과 패턴의 성적 이형성은 이전에 이 마우스 계통에서 보고된 바 있습니다.24 이와 일치하여 우리는신장남성 한배의 신장보다 여성의 비율이 높습니다(보충 그림 S2D). 구성적으로 활성인 Nestin 프로모터에 의해 구동되어 전체 네프론에서 fpn을 삭제하는 다른 Cre 재조합효소 이식유전자를 사용한 이전 연구에서도 신장 철 수치가 증가하고 혈청 철 및 간 철 저장량이 감소했다고 보고했습니다. 그러나 해당 연구는 다른 마우스 계통(129/SvEvTac)에서 수행되었으며 성별 또는 시간 경과에 따른 표현형을 분석하지 않았습니다.14
혈색소 침착증 및 기타 철 장애.
폭로
모든 저자는 경쟁 이익을 선언하지 않았습니다.
감사의 말
SL-L은 British Heart Foundation Intermediate Basic Science Postdoctoral Fellowship(FS/12/63/29895)의 수혜자였습니다. GM은Kidney Research UK 프로젝트SL-L에 부여된 교부금(RP_020_20160303).
저자 기여
SL-L은 연구를 잉태했습니다. SL-L과 GM은 실험을 수행했습니다. SL-L은 결과를 분석하고 해석했습니다. SL-L이 원고를 작성했습니다. AM이 자료를 제공했습니다. PAR은 원고에 대해 논평했습니다.
보충 자료
보충 파일(PDF)
그림 S1. FPN 및 HAMP 항체 특이성 확인. (A) 3개월령의 Fpnflfl/flfl, Pax8.CreERT2þ 동물 및 Fpnflfl/flfl 대조군의 신장 피질에서 FPN 면역형광 염색의 대표적인 이미지. 상단 패널, 막대=200mm, 원래 배율 10. 하단 패널, 막대=25mm, 원래 배율 60. (B) 3에서 Hamp–/– 동물 및 야생형 대조군의 신장 피질에서 HAMP 면역형광 염색의 대표적인 이미지 몇 개월. 상단 패널, 막대=200mm, 원래 배율 10. 하단 패널, 막대=25mm, 원래 배율 60.
그림 S2. Pax8.CreERT2þ 활동 및 특정성 확인. (A) Fpnflfl/flfl 및 Fpnflfl/flfl, Pax8.CreERT2þ 마우스의 간, 비장 및신장타목시펜 유도 1주일 후. (B) FPN에 대한 웨스턴 블롯신장타목시펜 치료 3개월 후 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Y 대조군. 하단 패널에 표시된 신호 강도의 정량화. (C) 타목시펜 처리 후 3개월에 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 신장에서 FPN에 대한 웨스턴 블롯. 하단 패널에 표시된 신호 강도의 정량화. (D) 3개월령에 야생형 암컷 및 수컷 한배 새끼의 신장에서 FPN에 대한 웨스턴 블롯. 하단 패널에 표시된 신호 강도의 정량화. (E–G) 각각 그림 1a, g 및 e의 더 큰 버전의 패널입니다. 값은 평균 SEM으로 표시됩니다. *P < 0.{13}}5,="" ***p=""><>
그림 S3. 혈청 에리트로페론 수치는 FpnC326Yflfl/flfl Pax8.CreERT2þ 및 Fpnflfl/flfl, Pax8.CreERT2 마우스에서 변경되지 않습니다. (A) 타목시펜 처리 후 1주, 1개월, 3개월 및 6개월 후 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 혈청 에리트로페론 수준. (B) 타목시펜 유도 후 1주, 1개월, 3개월 및 6개월에 암컷 및 수컷 Fpnflfl/flfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 혈청 에리트로페론 수준. 값은 평균 SEM으로 표시됩니다.
그림 S4. FpnC326Yflfl/flfl ,Pax8.CreERT2þ 철분이 풍부한 식단에서 헤모글로빈 및 혈청 에리트로페론 수치는 변경되지 않습니다. (A) 암컷 및 수컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 헤모글로빈 수치는 3개월 동안 이유식으로부터 대조군 식단(철분 200ppm 함유) 또는 철분 함유 식단(철분 5000ppm 함유)을 먹였습니다. . (B) 대조군 식단(200ppm 철 함유) 또는철분이 많은 식단(철분 5000ppm 함유) 이유기부터 3개월. 값은 평균 SEM으로 표시됩니다. (C,D) 각각 그림 3h 및 i의 더 큰 버전의 패널입니다.
그림 S5. 다른 마우스 모델에서 신장 철 처리 및 신장 햄프 발현. (A) 6개월령의 Fpnwt/C326Y 동물 및 Fpnwt/wt 대조군의 신장 철 수치. (B) Fpnflfl/flfl, Pax8.CreERT2þ 동물 및 Fpnflfl/flfl 대조군의 신장 피질에서 FPN 및 AQP1 면역형광 염색의 대표적인 이미지는 3개월 동안 이유식에서 5{47}}00ppm이 함유된 철분이 풍부한 식단을 먹였습니다. Bar=25mm, 원래 배율 60. (C) 5000ppm 철분을 함유한 철분이 풍부한 식단 또는 3개월 동안 이유식을 통해 200ppm 철분을 함유한 대조군 식단을 섭취한 야생형 동물의 소변 철 수치(뇨 크레아티닌으로 정상화됨). (D) 3개월령의 Fpnwt/C326Y 동물 및 Fpnwt/wt 대조군에서 신장 햄프 유전자 발현. (E) 5000ppm 철을 함유한 철이 풍부한 식이 또는 3개월 동안 이유식으로부터 200ppm 철을 함유하는 대조군 식이를 공급한 야생형 동물에서 신장 햄프 유전자 발현. (F) 타목시펜 처리 후 1주, 1개월, 3개월 및 6개월 후 암컷 및 수컷 FpnC326Yflflflfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflflflfl 대조군에서 신장 햄프 유전자 발현. (G) 타목시펜 유도 후 1주, 1개월, 3개월 및 6개월에 암컷 및 수컷 Fpnflflflfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군에서 신장 햄프 유전자 발현. (H) 3개월령에 야생형 동물의 신장 피질에서 HAMP 및 CalD 면역형광 염색의 대표적인 이미지. 막대=25mm, 원래 배율 60. (I) 1개월령의 FpnC326Yflfl/flfl, Pax8.CreERT2þ 동물의 신장 피질에서 FPN 및 CalD 면역형광 염색의 대표적인 이미지. 막대=25mm, 원래 배율 60. (J–M) 각각 그림 4c, d, f 및 g에서 패널의 더 큰 버전. 값은 평균 SEM으로 표시됩니다. *P <>
그림 S6. 간 햄프 유전자 발현과 장내 FPN 수준은 신세뇨관-특정 fpn 녹아웃이 있는 마우스와 신세관-특정 fpnC326Y 녹인이 있는 마우스에서 변경됩니다. (A) 타목시펜 처리 후 1주, 1개월, 3개월 및 6개월 후 암컷 FpnC326Yflfl/flfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 간에서 hamp mRNA의 상대적 발현. (B) 타목시펜 처리 후 1주, 1개월, 3개월 및 6개월에 암컷 Fpnflflfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 간에서 hamp mRNA의 상대적 발현. (C) 타목시펜 처리 1개월 후 암컷 FpnC326Y flflflfl, Pax8.CreERT2þ 마우스 및 FpnC326Yflfl/flfl 대조군의 내장에서 FPN 면역염색의 대표적인 이미지. 막대 ¼ 200 mm, 원래 배율10. (D) 타목시펜 처리 1개월 후 암컷 Fpnflflflfl, Pax8.CreERT2þ 마우스 및 Fpnflfl/flfl 대조군의 내장에서 FPN 면역염색의 대표적인 이미지. 바=200mm, 원래 배율 10. 값은 평균 SEM으로 표시됩니다. *P < 0.05,="" **p="">< 0.01="" 및=""><>

Cistanche는 신장 감염을 완화할 수 있습니다
참조
1. Donovan A, Lima CA, Pinkus JL, et al. 철 수출업자 ferroportin/slc40a1은 철 항상성에 필수적입니다. 세포 대사. 2005;1:191–200.
2. Ganz T. 세포성 철분: 페로포틴이 유일한 탈출구입니다. 세포 대사. 2005;1:155–157.
3. Nemeth E, Tuttle MS, Powelson J, et al. Hepcidin은 ferroportin에 결합하여 내재화를 유도하여 세포의 철 유출을 조절합니다. 과학. 2004;306:2090–2093.
4. Qiao B, Sugianto P, Fung E, et al. ferroportin의 Hepcidin에 의한 endocytosis는 ferroportin ubiquitination에 의존합니다. 세포 대사. 2012;15:918–924.
5. Wareing M, Ferguson CJ, Green R 등 마취된 쥐에서 신장 철 수송의 생체 내 특성화. J Physiol. 2000;524:581–586.
6. Christensen I, Birn H, Storm T, et al. 신장 근위 세뇨관의 세포내 수용체. 생리학. 2012;27:223–236.
7. Zhang D, Meyron-Holtz E, Rouault T. 신장 철 대사: 트랜스페린 철 전달 및 철 조절 단백질의 역할. J Am Soc Nephrol. 2007;18:401–406.
8. Canonne-Hergaux F, Gruenheid S, Ponka P, Gros P. 장의 브러시 경계에서 Nramp2 철 수송체의 세포 및 세포 내 국소화 및식이 철에 의한 조절. 피. 1999;93: 4406–4417.
9. Wang C, Jenkitkasemwong S, Duarte S, et al. ZIP8은 세포 표면 발현이 세포 철 로딩에 의해 상향 조절되는 철 및 아연 수송체입니다. J Biol Chem. 2012;287:34032–34043.
10. Martines A, Masereeuw R, Tjalsma H, et al. 철 유발성 신장 손상의 발병기전에서 철 대사. Nat Rev Nephrol. 2013;9:385–398.
11. Wolff N, Liu W, Fenton R, et al. Ferroportin 1은 쥐의 신장 근위 세뇨관 세포에서 기저외측으로 발현되고 철분 과잉은 막 이동을 증가시킵니다. J Cell Mol Med. 2011;15:209–219.
12. Pan S, Qian ZM, Cui S, et al. 국소 헵시딘은 신장에서 페로포틴의 분해를 통해 세포내 철 과부하를 증가시켰습니다. Biochem Biophys Res Commun. 2020;522:322–327.
13. Mooulouel B, Houamel D, Delaby C, et al. 헵시딘은 원위 네프론에서 신장 내 철 처리를 조절합니다. 신장 국제 2013;84:756–766.
14. Wang X, Zheng X, Zhang J, et al. 신장 철 재활용 및 허혈성 급성 신장 손상의 조절에서 ferroportin의 생리 기능. Am J Physiol 신장 Physiol. 2018;315:F1042–F1057.
15. Lakhal-Littleton S, Wolna M, Chung YJ, et al. 심장 철 항상성에서 헵시딘의 필수적인 세포 자율적 역할. 엘라이프. 2016;5: e19804.
16. Lakhal-Littleton S, Wolna M, Carr CA, et al. 심장 페로포틴은 세포 철 항상성을 조절하며 심장 기능에 중요합니다. Proc Natl Acad Sci US A. 2015;112:3164–3169.
17. Espana-Agusti J, Zou X, Wong K, et al. 신세뇨관 상피 세포의 유도 및 특이적 유전자 조작을 위한 Pax8-CreERT2 유전자 변형 계통 및 Slc22a6-CreERT2 녹인 계통의 생성 및 특성화. 플로스원. 2016;11:e0148055.
18. Lakhal-Littleton S, Crosby A, Frize M, et al. 폐동맥 평활근 세포의 세포 내 철 결핍은 생쥐에서 폐동맥 고혈압을 유발합니다. Proc Natl Acad Sci US A. 2019;116:13122–13130.
19. Camaschella C. 혈색소 침착증 및 관련 장애의 유전자 분석을 통한 철 항상성의 이해. 피. 2005;106: 3710–3717.
20. Núñez MT, Tapia V, Rojas A, et al. 철 공급은 장내 철 수송체 DMT1 및 ferroportin 1의 정단/기저측 막 분포를 결정합니다. Am J Physiol Cell Physiol. 2010;298:C477–C485.
21. Veuthey T, D'Anna MC, Roque ME. 철 항상성에서 신장의 역할: 빈혈 마우스에서 prohepcdin, ferroportin 및 DMT1의 신장 발현. Am J Physiol 신장 Physiol. 2008;295:F1213–F1221.
22. Naz N, Malik I, Sheikh N, et al. Ferroportin-1은 쥐 간의 "핵" 음성 급성기 단백질로, 다른 철 수송 단백질과 비교됩니다. 연구소 투자. 2012;92:842–856.
23. Aydemir F, Jenkitkasemwong S, Gulec S, Knutson MD. 철 로딩은 뮤린 J774 대식세포에서 페로포틴 이종 핵 RNA 및 mRNA 수준을 증가시킵니다. J Nutr. 2009;139:434–438.
24. Veiras LC, Girardi ACC, Curry J, et al. 신장 수송체와 전해질 항상성의 성적 이형 패턴. J Am Soc Nephrol. 2017;28: 3504–3517.
